Менопауза. Перименопаузальный период. Постменопаузальный период. Пременопаузальный период. Патологии и развитие астенического синдрома. Коррекция.
Шишкова В.Н., Калашникова М.Ф.
По данным Всемирной организации здравоохранения (ВОЗ), в настоящее время сохраняется общемировая тенденция увеличения в популяции численности лиц старшей возрастной группы. Также экспертами рассчитано, что доля женщин старше 45 лет к 2015 г. составит около 46% [1]. Это объясняет большой интерес врачей различных специальностей к изучению изменений, происходящих в организме женщины в этот период, и поиску рациональных путей оптимальной коррекции всех возникающих нарушений с целью улучшения качества жизни.
Продолжительность активного периода жизни женщин, вне зависимости от возраста и статуса менопаузы, в значительной степени зависит от образа жизни, социально-экономических условий проживания, характера питания, наличия и выраженности сопутствующих соматических заболеваний и, что особенно важно, – от психологического благополучия [2]. Наиболее высокая средняя продолжительность активной жизни наблюдается в Японии, где она составляет 74,5 года, а самая низкая – в странах Африки – около 30 лет. В России в настоящее время данный показатель у женщин превышает 60 лет, а средний возраст жизни женщин – 76,5 года [3]. Таким образом, почти 1/3 своей жизни современная женщина проводит в периоде постменопаузы, развитию которой предшествуют определенные события.
Менопауза является естественным переходом к нерепродуктивному периоду жизни женщины, однако накопленные к этому времени соматические и психологические проблемы, выражающиеся в гормональных и метаболических изменениях, у 48% женщин приводят к развитию климактерического синдрома (КС) разной степени выраженности [4–6]. Процесс постепенного снижения фертильной функции – наступления менопаузы делят на следующие периоды [5]:
– Пременопаузальный период – от начала снижения функции яичников до наступления менопаузы. Эндокринологически он характеризуется снижением гормональной функции яичников, биологически – снижением фертильности. Продолжительность пременопаузы варьирует от 1 до 2 лет.
– Перименопаузальный период – охватывает весь период пременопаузы и 2 года после последней самостоятельной менструации.
– Менопауза – последняя самостоятельная менструация. Возраст менопаузы устанавливается ретроспективно – через 12 мес. отсутствия менструаций.
– Постменопаузальный период – длится от менопаузы до почти полного выключения функции яичников. Различают раннюю (3–5 лет) и позднюю (более 5 лет) постменопаузу.
При физиологическом течении пременопаузального периода происходит постепенное угасание функции яичников, которое клинически характеризуется наступлением менопаузы. Нередко менопауза не оказывает никакого отрицательного влияния на жизнедеятельность и все функции женского организма. К факторам, определяющим физиологическое течение климактерического периода (КП), относятся неотягощенная наследственность, нормальное течение беременностей и родов, постоянная профилактика ожирения, физическая активность, отсутствие профессиональных вредностей, рациональная организация труда и отдыха, вовремя выявленные и полностью контролируемые соматические заболевания [5].
Нередко КП приобретает патологическое течение – развивается КС. КС – симптомокомплекс, появляющийся у части женщин в период угасания функции репродуктивной системы на фоне общей возрастной инволюции организма. Его наличие осложняет физиологическое течение КП. КС характеризуется вазомоторными, эндокринно-обменными и нервно-психическими нарушениями [4–6].
Клинические проявления КС нередко взаимосвязаны и могут быть обусловлены существующими к моменту менопаузы различными заболеваниями. Классическими проявлениями КС являются вазомоторные («приливы» и гипергидроз) и нервно-психические (утомляемость, слабость, снижение работоспособности и нарушения сна). Общая частота КС варьирует от 40 до 80%. Клинические симптомы могут проявляться по отношению ко времени прекращения менструаций с различной частотой: в пременопаузальном периоде – у 35–40% женщин, сразу с наступлением менопаузы – у 39–85%, в течение 1 года после менопаузы – у 26%, через 2–5 лет после менопаузы – у 3% [4–6]. В зависимости от степени тяжести течения КС различают легкую, средней степени тяжести и тяжелую формы.
При легкой форме отмечается до 10 «приливов» в течение 1 сут при ненарушенном общем состоянии и работоспособности женщины. Для КС средней тяжести характерны 10–20 «приливов» в течение 1 сут, выраженные многообразные симптомы заболевания (общая слабость, сонливость, утомляемость, головокружение, головная боль, нарушение сна, памяти и др.), ухудшающие общее состояние женщины и снижающие ее работоспособность. Тяжелая форма сопровождается полной или почти полной потерей работоспособности. Следует учесть, что климактерические расстройства, которые развиваются у части женщин в период угасания функции яичников, представляют собой не что иное, как синдром дезинтеграции – нарушение целостной деятельности лимбико-ретикулярной системы в составе ЦНС. Следует подчеркнуть, что вазомоторные симптомы в перименопаузе являются не следствием эстрогенного дефицита как такового, а проявлением своеобразной «абстиненции» эстрогенчувствительных нейрональных систем, которые длительное время находились в условиях высокого содержания половых гормонов. Это косвенно объясняет, в частности, почему у пациенток с различными формами первичной аменореи в молодом возрасте, несмотря на крайне низкое содержание эстрогенов, никогда не бывает «приливов» и они появляются только после назначения и внезапной отмены гормональной терапии [5].
Почти у половины женщин с развившимся КС отмечается его тяжелое течение (51%), у каждой третьей (33%) его проявления носят умеренный характер и только в 16% случаев КС сопровождается легкими проявлениями [4–6]. Следует также учитывать продолжительность проявлений КС. Только у 18% женщин яркие проявления КС исчезают в течение первого года. Продолжительность симптомов до 5 лет наблюдается у 35–56% женщин, затяжное течение КС – у 26%. Наибольшая частота и интенсивность типичных проявлений КС отмечаются в течение первых 2–3 лет постменопаузы [4, 5].
Особенно длительное и тяжелое течение приобретает КС, который развился при преждевременном наступлении менопаузы в возрасте 38–43 лет. Возникающие при этом нейровегетативные, обменно-эндокринные, психоэмоциональные нарушения нередко приводят к потере трудоспособности и нарушениям психосоциальной адаптации в профессиональной, интеллектуальной и семейной сферах жизни [4–6].
Женщины с КС нуждаются в комплексном обследовании и ведении врачами ряда специальностей. Основным является обследование у гинеколога, которое обязательно проводится для уточнения гормональной активности яичников, определения уровня эстрогенных влияний и выявления связи между появлением «приливов» жара и климактерическими изменениями менструальной функции.
Однако с учетом характера и выраженности изменений каждая женщина с КС нуждается в терапевтическом, а также, что немаловажно, и в психоневрологическом обследовании, поскольку значительное влияние на состояние и поведение женщины оказывает психологическое восприятие ею КП как признака старения и окончания важной биологической функции женского организма [5, 6].
У 30% женщин в этот период наблюдается астеническая депрессия, которая является одним из наиболее тяжелых и с трудом поддающихся лечению симптомов. По данным современных исследователей, изучавших клинические проявления КП у женщин в возрасте 45–54 лет с продолжительностью заболевания в пределах 5 лет, расстройства психоэмоциональной сферы выявляются в 78,4% случаев [4, 5]. Часто женщины в этот период предъявляют жалобы астенического характера: слабость, повышенная утомляемость, эмоциональная лабильность, гиперстезия, нарушения сна.
Развитие астенического синдрома, как и возникновение «приливов», обусловлено нарушением функции ретикулярной активирующей системы – плотной нейрональной сети, ответственной за управление энергетическими ресурсами организма. Она вовлечена в контроль координации произвольных движений, автономную и эндокринную регуляцию, сенсорное восприятие, запоминание, активацию коры головного мозга [4, 5]. В клинической картине КС, помимо усталости, отсутствия мотивации, отмечаются расстройства сна, сексуальной функции, а также снижение памяти, внимания, физической выносливости, аппетита, что свидетельствует о выраженности астенических проявлений в этот период жизни женщины [6, 7].
В структуру астенического синдрома в период менопаузы входят:
- Повышенная утомляемость, истощаемость, отсутствие внутренней готовности к выполнению той или иной деятельности, снижение концентрации внимания, ухудшение памяти, появляются ошибки при выполнении сложных заданий, снижается уровень общего самочувствия, что отражается на настроении, восприятии окружающего.
- Повышенная раздражительность, возбудимость, количественная выраженность неадекватности в реакциях на окружающую действительность, вследствие чего развивается своеобразная функциональная дезадаптация.
- Наличие соматовегетативных расстройств разнообразного характера.
Выделяют 2 варианта астенического синдрома: гипостенический и гиперстенический. Если в клинической картине преобладают утомление, истощаемость над раздражительностью, возбудимостью, это говорит о гипостеническом варианте астенического синдрома, если раздражительность, возбудимость преобладают над истощаемостью, – о гиперстеническом варианте. Оба варианта течения астенического синдрома могут претерпевать определенную динамику и переходить друг в друга, к ним могут присоединяться другие невротические расстройства [6, 7].
Важными факторами развития психоэмоциональных нарушений у пациенток во время КП являются психологические травмы, стрессы, особенности социального статуса (семейное положение, материальная обеспеченность, наличие работы, взаимоотношения с детьми, мужем, друзьями), самоуважение, удовлетворенность жизнью, качество сексуальных отношений (наличие партнера, нарушения в половой сфере), психические расстройства в анамнезе и хронические соматические заболевания (сахарный диабет (СД), артериальная гипертензия (АГ) и т. д.). При этом и социальные, и соматические факторы могут либо способствовать адаптации женщины в переходный жизненный период, либо, наоборот, сильно затруднять ее [5–7].
Таким образом, к моменту наступления менопаузы большинство женщин, к сожалению, имеют развившиеся соматические заболевания. Кроме того, определенные психосоциальные факторы влияют на психологическую и интеллектуальную сферы здоровья женщин и ухудшают течение КП.
В настоящее время методом выбора при лечении пациенток с КС является назначение заместительной гормональной терапии (ЗГТ) с использованием натуральных эстрогенов в комбинации с прогестинами. Считается эффективным влияние эстроген-прогестагенной терапии на предотвращение возникновения «приливов» и гипергидроза, однако психоэмоциональные нарушения у женщин в КП могут быть вызваны совсем не гормональными причинами. Поэтому при коррекции психоэмоциональных нарушений при КС следует помнить, что терапия некоторыми прогестинами может вызывать или усиливать имеющуюся депрессию, а астенические проявления полностью не купируются на фоне традиционной ЗГТ [5, 6].
К альтернативным вариантам терапии психоэмоциональных расстройств, в частности наиболее часто встречающихся астенических проявлений, возникающих в КП, относят применение психотропных препаратов, психотерапию и пропаганду здорового образа жизни [5–8, 11]. Фармакотерапевтические средства должны обладать высокой эффективностью и безопасностью. Однако на сегодняшний день имеется мало информации об эффективном использовании антиастенических препаратов в терапии КС. Одним из перспективных в данном отношении средств является препарат Нооклерин® (производитель – ООО «ПИК-ФАРМА», Россия).
Нооклерин® – ноотропный препарат с антиастенической активностью. По химической структуре он близок к естественным метаболитам головного мозга (γ–аминомасляная, глутаминовая кислоты). Нооклерин® оказывает положительное терапевтическое действие на астенические (вялость, слабость, истощаемость, рассеянность, забывчивость) и адинамические расстройства, повышая умственную и физическую активность, улучшая общий тонус и настроение. Вызывает быструю редукцию астенических нарушений, при этом он лишен отрицательных свойств психостимуляторов и обладает позитивным влиянием на психофизиологические показатели когнитивной деятельности пациентов.
Целью настоящего исследования являлось изучение эффективности и безопасности применения препарата Нооклерин® в терапии астенического синдрома у женщин в период пре-, пери- и постменопаузы.
Материалы и методы
В открытом контролируемом рандомизированном исследовании приняли участие 60 женщин в период пре-, пери- и постменопаузы (медиана возраста – 52 года (45; 58)).
Критерии включения пациенток в исследование:
– возраст 40–60 лет;
– наличие астенических жалоб (быстрая утомляемость, сниженная умственная и физическая работоспособность, снижение настроения, астенодепрессивная симптоматика);
– изменения менструального цикла в возрасте от 40 лет, не связанные с заболеваниями, что подтверждено осмотром врача-гинеколога (аменорея или нерегулярные менструации в период пре-, пери- и постменопаузы).
Критерии исключения из данного исследования:
– склонность к аллергическим реакциям, в т. ч. гиперчувствительность к компонентам препарата Нооклерин® в анамнезе;
– получение ЗГТ половыми стероидами или применение психотропных препаратов, таких как: ноотропы, анксиолитики, антидепрессанты (в т. ч. растительного происхождения), антиконвульсанты, нейролептики (типичные и атипичные), адаптогены (в т. ч. растительного происхождения);
– зависимость от психоактивных веществ;
– состояния, угрожающие жизни пациента.
Проведен опрос всех женщин по специально разработанной карте, включающей блоки медико-социального анамнеза, а также вопросы о наследственности, статусе курения, потреблении алкоголя, диете, течении сопутствующих соматических и гинекологических заболеваний, контрацептивный анамнез; оценку КС проводили по шкале модифицированного менопаузального индекса Купермана (ММИК) в модификации Е.В. Уваровой (1982), в основу которого положено определение нейровегетативного, обменно-эндокринного и психоэмоционального симптомокомплексов. Клинико-лабораторное исследование включало оценку соматического и неврологического статуса. Всем женщинам проводились: измерение роста, веса, окружности талии (ОТ), окружности бедер (ОБ); расчет индекса массы тела и соотношения ОТ/ОБ; измерение систолического и диатолического АД, частоты сердечных сокращений в покое; ЭКГ в 12 отведениях в покое в положении лежа; осмотр молочных желез, по показаниям – маммография; электрокардиография; по показаниям – УЗИ щитовидной железы; лабораторные исследования: клинический анализ крови и мочи, биохимический анализ (глюкоза крови, липидограмма – общий холестерин, триглицериды, аланинаминотрансфераза (АЛТ), аспартатаминотрансфераза (АСТ), билирубин). Оценку выраженности астенических проявлений выполняли по шкале астении MFI-20. Исследование когнитивного статуса пациенток проводили по стандартным нейропсихологическим методикам (Мини-Ког, Мока-тест, MMSE).
Исследование выполнено в соответствии с Хельсинкской декларацией, принятой в июне 1964 г. и пересмотренной в октябре 2000 г. (Эдинбург, Шотландия). От каждой пациентки получено информированное согласие.
Статистическая обработка полученных результатов осуществлялась с применением пакета анализа Microsoft Excel, а также при помощи пакета программ Statistica 6.0. Распределения количественных данных, отличные от нормального, описывались с указанием медианы и интерквартильного размаха в виде 25 и 75% процентилей. Достоверность различий оценивалась по методу вариационной статистики с использованием критериев Манна – Уитни, Крускала – Уоллиса и Данна для независимых выборок и критерия Уилкоксона для парных случаев непараметрических распределений. Различия считались достоверными при значениях p<0,05.
Результаты и обсуждение
Все пациентки, включенные в исследование, прошли первичное клинико-лабораторное обследование. После обследования 60 женщин были рандомизированы методом конвертов в 2 группы.
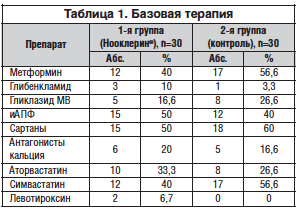
В 1-й группе (n=30) пациенткам к базовой терапии (антигипертензивной, гиполипидемической, антиагрегантной, сахароснижающей и т. д.) (табл. 1) был добавлен препарат Нооклерин® в суточной дозе на весь период исследования – 2 г/сут (2 мерные ложки). Суточный прием распределялся следующим образом: разовая доза составляла 1 г (1 мерная ложка), 1-й прием – утром, 2–й – днем, но не позднее 16:00 и не ранее чем за 4 ч до сна, с учетом показателей переносимости препарата.
Во 2-й группе (n=30) была оставлена прежняя терапия (антигипертензивная, гиполипидемическая, антиагрегантная, сахароснижающая и т. д.) и/или стандартизованные поливитаминные комплексы, в т. ч. биологически активные добавки (с кальцием, витаминами А, В, D, С и содержащие фитоэстрогены и т. д.).
Продолжительность терапии в обеих группах составила 6 нед. Оценка состояния пациенток с использованием всех методик проводилась на этапе включения в исследование, далее на 14-й, 28-й дни и в конце терапии.
После рандомизации всем пациентам были даны рекомендации по коррекции имеющихся у них метаболических нарушений. Рекомендации касались изменения образа жизни: отказ от курения, ограничения потребления животных жиров, рафинированных углеводов и соли в пище, увеличение физической активности за счет аэробных нагрузок (пешеходные прогулки на свежем воздухе по 30–45 мин ежедневно).
Предшествующая базовая (антигипертензивная и сахароснижающая) терапия в обеих группах на протяжении всего исследования не изменялась. Перед началом исследования всем пациенткам были розданы дневники самочувствия и учета побочных действий проводимой терапии.
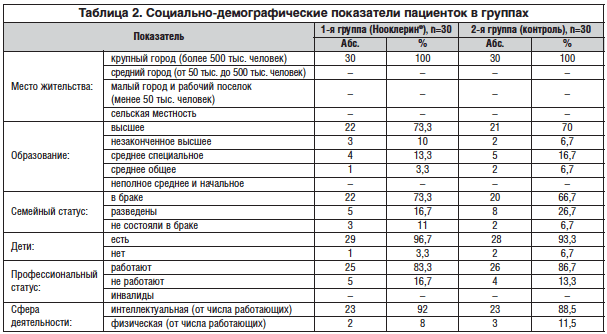
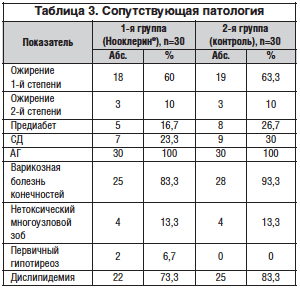
Социально-демографические показатели в обеих группах приведены в таблице 2. Выявленная сопутствующая патология представлена в таблице 3. Следует отметить, что практически у всех женщин, включенных в исследование, была выявлена АГ 1–2 степени и назначена антигипертензивная терапия. Также высокой оказалась распространенность дислипидемии и нарушений жирового обмена – до 80% среди всех включенных в исследование (табл. 3). Эти данные свидетельствуют о высокой распространенности невыявленной сопутствующей сердечно-сосудистой патологии у женщин в КП, значимо ухудшающей течение КС.
Средний возраст наступления естественной менопаузы у женщин, включенных в исследование, был практически одинаковым в обеих группах и составил в 1-й группе 48 (42–54), во 2-й – 49 (42–52) лет (р>0,05).
Для оценки степени выраженности клинических проявлений КС использовался ММИК в модификации Е.В. Уваровой (1982). Проводился анализ нейровегетативных, обменно-эндокринных и психоэмоциональных нарушений путем оценки количества баллов в каждой группе симптомов, а также распределения степеней тяжести данных нарушений.
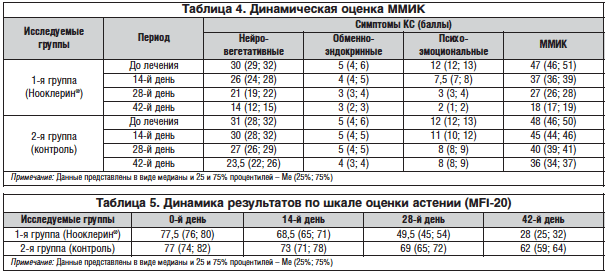
Показатели нейровегетативных, обменно-эндокринных и психоэмоциональных проявлений КС у женщин на этапе включения в исследование представлены в таблице 3, из которой видно, что исходная тяжесть проявлений КС в обеих группах была сопоставимой (р>0,05). Следует отметить исходную более высокую степень тяжести КС по блокам нейровегетативных и психоэмоциональных нарушений в обеих группах. Все изменения ММИК, произошедшие в группах за время наблюдения, отражены в таблице 4.
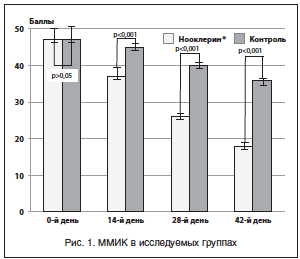
Из полученных данных видно, что в обеих группах произошло снижение степени тяжести проявлений КС, имеющее достоверный характер (р<0,001). Однако необходимо подчеркнуть, что в 1-й группе изменения носили более ярко выраженный характер: через 6 нед. ММИК в 1-й группе в виде медианы составил 18 (17; 19), в то время как во 2-й группе – 36 (34; 37). При сравнении результатов между группами с использованием критерия Манна – Уитни получили достоверное различие р<0,001. У пациенток в 1-й группе через 6 нед. лечения отмечено снижение проявлений КС до легкой степени (рис. 1).
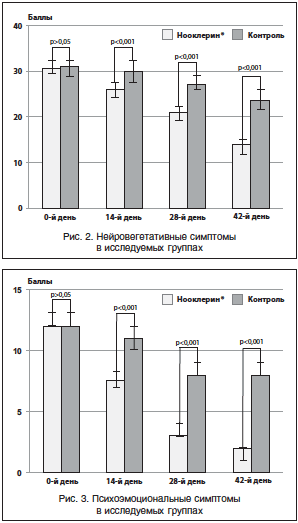
На рисунках 2 и 3 наглядно показано, что изменение степени течения КС в обеих группах женщин в основном произошло вследствие снижения выраженности нейровегетативных и психоэмоциональных проявлений, в то время как значимых изменений обменно-эндокринных симптомов отмечено не было.
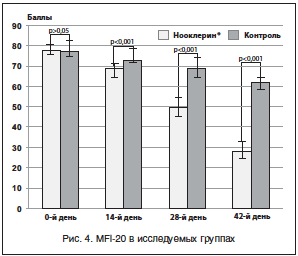
С учетом того, что все включенные в исследование женщины имели жалобы и проявления астенического характера, была проведена оценка выраженности астении по шкале астении MFI-20 в обеих группах до и после терапии. Полученные результаты представлены в таблице 5 и показаны на рисунке 4. Как видно из представленных данных, исходно выраженность астенических проявлений у женщин в 1-й и 2-й группах достоверно не различалась (р>0,05).
На фоне 6-недельной терапии препаратом Нооклерин® в 1-й группе отмечено ярко выраженное улучшение состояния женщин: повышение общего тонуса, работоспособности, улучшение настроения, которое носило достоверный характер при сравнении с исходными показателями в 1-й группе (р<0,001) и с группой контроля (р<0,001), что подтверждает высокую эффективность данной терапии.
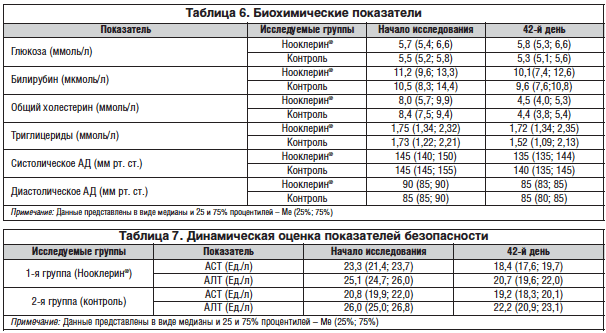
Также необходимо отметить хорошую переносимость препарата Нооклерин®. За все время наблюдения ни одна из пациенток 1-й группы не выбыла из исследования, не было случаев непереносимости или отказа от терапии препаратом Нооклерин®. Побочных эффектов или аллергических реакций у женщин из 1-й группы также зарегистрировано не было. В таблице 6 представлены основные биохимические и гемодинамические показатели за время наблюдения, можно сделать вывод об отсутствии негативного влияния препарата Нооклерин® на данные показатели. В таблице 7 представлены динамические данные оценки концентрации ферментов печени в течение всего исследования, свидетельствующие об отсутствии отрицательного влияния данной терапии на показатели функции печени.
Таким образом, в процессе терапии препаратом Нооклерин® в 1-й группе у женщин в пре-, пери- и постменопаузе отмечалось выраженное улучшение состояния, что проявлялось в значимой редукции симптомов КС и астенической симптоматики.
Заключение
Из представленных результатов можно сделать следующие практические выводы:
- Распространенность соматической патологии у женщин в пре-, пери- и постменопаузе, имеющих астенические жалобы, достаточно высока, наиболее часто встречаются АГ (имеющая дополнительное влияние на развитие когнитивных нарушений) и нарушения жирового и липидного обменов (ожирение и дислипидемия), что делает эту проблему актуальной для широкого круга врачей – от акушеров-гинекологов до терапевтов и кардиологов.
- Терапия препаратом Нооклерин® в изучаемой дозе у пациенток в пре-, пери- и постменопаузе с астеническим синдромом показала себя весьма эффективной. Отмечено значимое улучшение показателей в блоке нейровегетативных и психоэмоциональных нарушений, что в конечном итоге повлияло на степень выраженности проявлений КС у данной категории женщин. У большинства пациенток степень тяжести нарушений изменилась – от тяжелой к умеренной и легкой.
- Терапия препаратом Нооклерин® в течение 6 нед. привела к практически полной редукции астенической симптоматики у женщин с исходно высокими баллами по шкале астении. У женщин повысились умственная и физическая работоспособность, повседневная активность, улучшилось настроение. Можно отметить мягкость активирующего действия препарата и относительно быстрое наступление эффекта – достоверные изменения отмечались уже на 2-й нед. и сохранялись до конца исследования.
- Изучение переносимости и безопасности 6-недельного курса терапии препаратом Нооклерин® в суточной дозе 2 г показало отсутствие негативного влияния на состояние основных биохимических и гемодинамических показателей у испытуемых. Также не было выявлено негативного лекарственного взаимодействия и непереносимости данной терапии.
Таким образом, следует подчеркнуть важность того факта, что при наличии у женщин астенического синдрома в период пре-, пери- и постменопаузы нейровегетативные и психоэмоциональные симптомы КС обычно появляются раньше, чем у женщин без астенических нарушений, выявляются уже в пременопаузальном периоде и усиливаются сразу с наступлением менопаузы, а также отличаются более выраженными расстройствами [5, 9–11]. Следовательно, женщины с астеническим синдромом входят в группу высокого риска развития ранних тяжелых проявлений КС, с одной стороны, и имеют абсолютные противопоказания к назначению традиционной ЗГТ, с другой стороны (неконтролируемая АГ, субклинический атеросклероз и т. д.). Применение ноотропной терапии с антиастеническим эффектом может быть единственным патогенетическим вариантом лечения и профилактики климактерических расстройств у таких пациенток. Прием препарата Нооклерин® в дозе 2 г/сут в течение 6 нед. продемонстрировал высокую эффективность и безопасность у пациенток с астеническим синдромом в период пре-, пери- и постменопаузы, что дает возможность рекомендовать данную терапию.
Литература
- Балан В.Е. Эпидемиология климактерического периода в условиях большого города // Акушерство и гинекология. 1997. № 3. С. 13–16.
- Величковский Б.Т. Социальный стресс, трудовая мотивация и здоровье // Бюл. сиб. медицины. 2005. Т. 4. № 3. С. 5–17.
- Сафарова Г.Л. Демографические аспекты старения населения России // Успехи геронтологии. 1997. № 1. С. 20–25.
- Сметник В.П., Тумилович Л.Г. Неоперативная гинекология: Руководство для врачей. СПб., 1995. 224 с.
- Медицина климактерия / под ред. В.П. Сметник. М.: Литтерра, 2009. С. 847.
- Шишкова В.Н. Проблемы старения и заместительная гормональная терапия у женщин в постменопаузе // Российский вестник акушера-гинеколога. 2013. № 2. С. 42–47.
- Воробьева О. В. Многогранность феномена астении // РМЖ. 2012. № 5. С. 248–252.
- Дюкова Г.М. Лечение астении // Лечение нервных болезней. 2002. № 3 (2(7)). С. 4–9.
- Чичановская Л.В. Гипертоническая энцефалопатия у женщин менопаузального периода: Автореф. дисс. … д.м.н. М., 2009. 51 с.
- Синельникова М.Н. Цереброваскулярная патология в климактерическом периоде: Автореф. дисс. … к.м.н. Иркутск, 2004. 24 с.
- Практические рекомендации. Ведение женщин в пери- и постменопаузе / под ред. В.П. Сметник, Л.М. Ильина. Ярославль: ИПК «Литера», 2010. С. 222.








Комментировать