Оценка влияния слезозаместительной и корнеопротекторной терапии на состояние глазной поверхности при синдроме «сухого глаза», индуцированного длительным ношением контактных линз и применением препаратов, содержащих консерванты. Контроль эффективности медикаментозной терапии методами биомикроскопии, пробы Норна, пробы Ширмера, импрессионной цитологии, конфокальной микроскопии, тиаскопии.
Егорова Г.Б., Федоров А.А., Митичкина Т.С., Шамсудинова А.Р., Сафонова Т.Н.
Резюме
Цель: оценить влияние слезозаместительной и корнеопротекторной терапии на состояние глазной поверхности при синдроме «сухого глаза»; (ССГ), индуцированного длительным ношением контактных линз (КЛ) и применением препаратов, содержащих консерванты.
Методы: все пациенты были разделены на 2 группы: в 1-й группе – пациенты с миопией, миопическим астигматизмом и кератоконусом I–IV стадии, которые были обследованы на фоне длительного ношения мягких и жестких КЛ, во 2-й группе – пациенты с глаукомой, длительно применяющие антиглаукоматозные препараты, содержащие консерванты.
Для купирования признаков ССГ были использованы слезозаменители, осмопротекторы, корнеопротекторы, режим назначался индивидуально, длительность курса лечения составляла от 1 (носители КЛ) до 3 мес. (больные с глаукомой). Я бы заказал курсовую на Студланс.ру . Как правило проблем с авторами студенческих работ не возникает.
Для контроля эффективности медикаментозной терапии применялись следующие методы исследования: биомикроскопия, проба Норна, проба Ширмера, импрессионная цитология, конфокальная микроскопия, тиаскопия.
Результаты: под наблюдением находилось 37 пациентов (74 глаза): в 1-й группе – 27 пациентов, во 2-й – 10. На фоне проводимого лечения наблюдалась положительная динамика исследуемых показателей в виде повышения переносимости КЛ, уменьшения дискомфорта при закапывании антиглаукоматозных препаратов. На фоне инстилляции слезозаменителей в течение 1 мес. в 1-й группе отмечено увеличение времени разрыва прекорнеальной слезной пленки на 62,8%. Во 2-й группе пациентов было выявлено отсутствие тенденции к дальнейшему снижению стабильности слезной пленки. После курса слезозаместительной терапии в течение 1 мес. отмечено повышение среднего уровня суммарной слезопродукции в 1-й группе на 22,7%, через 3 мес. во 2-й группе – на 35%. По данным конфокальной микроскопии через 1–3 мес. выявлено восстановление структуры клеток поверхностного и базального слоев эпителия роговицы, с помощью импрессионной цитологии отмечено появление бокаловидных клеток. По данным тиаскопии через 1–3 мес. после назначения слезозаменителей выявлено перераспределение толщины липидного слоя слезной пленки в сторону увеличения зоны с наибольшей толщиной и уменьшения зоны неопределенности и зоны ее наименьших значений.
Заключение: при ССГ на фоне длительного ношения КЛ и применения препаратов, содержащих консерванты, назначение слезозаместительной и корнеопротекторной терапии позволяет улучшить состояние эпителия роговицы и конъюнктивы.
Ключевые слова: контактные линзы, глазная поверхность, слезная пленка, слезозаменители, антиглаукоматозные препараты, корнеопротекторы, консерванты.
Глазная поверхность представлена передним эпителием роговицы, в области лимба переходящим в эпителий бульбарной и тарзальной конъюнктивы. Эпителий, покрывающий поверхность роговицы, представлен 5–6 слоями клеток неороговевающего эпителия. Клетки базального слоя мигрируют из лимбальной ростковой зоны к центру, продолжая делиться. В процессе дифференцировки они перемещаются кнаружи, образуя слои крыловидных и плоских клеток. Свободная поверхность плоских клеток содержит микроворсинки для удержания муцинового слоя прекорнеальной слезной пленки. По мере отмирания эти клетки десквамируются и уносятся с током слезы.
Бульбарная конъюнктива покрыта многослойным плоским неороговевающим эпителием с включениями из бокаловидных клеток, секретирующих муцин. Вблизи лимба роговицы эпителий конъюнктивы без резкой границы переходит в передний эпителий роговицы.
Конъюнктива переходной складки покрыта 5–6-слойным цилиндрическим эпителием с большим количеством бокаловидных клеток. Тарзальная конъюнктива покрыта двуслойным цилиндрическим эпителием и содержит у края век бокаловидные клетки, а у дистального конца хряща – крипты Генле, которые также секретируют муцин [1].
Слезная пленка, покрывающая поверхность роговицы, носит название прероговичной слезной пленки, выполняет защитную функцию и способствует транспорту кислорода и питательных веществ к эпителиальным слоям роговицы и конъюнктивы, а также удалению отмерших эпителиальных клеток.
Толщина слезной пленки у здоровых людей колеблется от 7 до 40 мкм. Она формирует переднюю поверхность главной преломляющей среды оптической системы глаза. Для осуществления данных функций и обеспечения условий для нормального функционирования эпителия роговицы и конъюнктивы слезная пленка должна иметь определенный состав, структуру и обладать достаточной стабильностью [2, 3].
Слезная пленка представляет собой водно-муциновый гель, содержащий растворенные мукопротеиды, концентрация которых возрастает по направлению к эпителиальной мембране. Бокаловидные клетки конъюнктивы секретируют гель-формирующий муцин 5, который представлен гетерогенной комбинацией высокомолекулярных гликопротеинов. Секрет бокаловидных клеток, взаимодействуя с молекулами воды, образует водно-муциновый слой слезной пленки с максимальной концентрацией мукопротеидов у поверхности эпителиальных клеток [4].
Клетки эпителия конъюнктивы и роговицы синтезируют трансмембранные муцины 1, 2 и 4 типа, которые образуют гликокаликс и удерживают муцины на гидрофобной поверхности клеток эпителия. Муцин придает слезной пленке вязкость и стабилизирует ее при мигательных движениях век [5].
Водная составляющая водно-муцинового слоя (98% его состава) является продуктом добавочных и основной слезных желез, имеет толщину 7 мкм и содержит растворимые в воде электролиты и органические низко- и высокомолекулярные вещества.
Наружный слой представлен тонкой липидной пленкой, состоящей из 2 слоев. По водно-липидной границе располагается слой полярных липидов (фосфолипиды, сфингомиелины и др.), воздушно-липидную границу формирует слой неполярных липидов (свободные жирные кислоты, холестерол, триглицериды). Составляющие липидного слоя продуцируются голокриновыми мейбомиевыми железами, расположенными в тарзальной пластинке век, и железистыми клетками конъюнктивы Цейса и Моля. Секрет мейбомиевых желез выделяется и распределяется на поверхности глазного яблока во время мигательных движений [6].
Липидная часть слезной пленки обладает защитными свойствами, участвует в теплоотдаче с поверхности эпителия роговицы и конъюнктивы, а также препятствует чрезмерному испарению водного слоя слезной пленки, что влияет на ее стабильность. Толщина липидного слоя варьирует от 1 до 100 нм [7].
Структура и стабильность слезной пленки нарушаются при возникновении ССГ. Провоцирующими факторами могут быть длительное ношение КЛ, инстилляции препаратов, содержащих консерванты [8–10]. Снижение стабильности слезной пленки сопровождается возникновением эпителиопатии, нарушением структуры эпителиального слоя, что также дестабилизирует слезную пленку.
Цель работы: оценить влияние слезозаместительной и корнеопротекторной терапии на состояние глазной поверхности при ССГ, индуцированного длительным ношением КЛ и применением препаратов, содержащих консерванты.
Методы
Под наблюдением находилось 37 пациентов (74 глаза). Пациенты были разделены на 2 группы: в 1-й группе – 27 пациентов с миопией, миопическим астигматизмом и кератоконусом I–IV стадии, которые были обследованы на фоне длительного ношения мягких и жестких КЛ, во 2-й группе – 10 пациентов с глаукомой, длительно применяющие антиглаукоматозные препараты, содержащие консерванты.
У всех пациентов были жалобы на чувство сухости глаз, покраснение глаз к концу дня, дискомфорт при длительной работе с компьютером, ощущение «отсутствия слезы», ухудшение переносимости КЛ, нестабильность и снижение остроты зрения в течение дня.
Все пациенты были обследованы с применением методов биомикроскопии, пробы Ширмера, пробы Норна.
Для оценки толщины липидного слоя прекорнеальной слезной пленки был использован метод тиаскопии, разработанный в ФГБНУ «НИИГБ», основанный на фоторегистрации цветового феномена интерференции [11]. Липидный слой слезной пленки является единственным из ее составляющих, визуализация которого возможна только с помощью данного метода [12, 13].
В результате взаимодействия световых волн, отраженных от двух поверхностей, наблюдается характерное пространственное распределение интенсивности света (интерференционная картина). Цвет интерференционной картины в каждой точке определяется длиной волны луча света, проходящего через липидный слой и отражающегося от его внутренней поверхности. А толщина липидного слоя может быть вычислена исходя из цвета интерференции в каждой точке исследуемой зоны [14, 15].
Цифровые изображения интерференционной картины липидного слоя прекорнеальной слезной пленки получают с помощью фотощелевой лампы со специальным осветителем. С целью объективизации результатов исследования и получения более подробной информации нами была разработана компьютерная программа «Lacrima», позволяющая на основе анализа цифрового изображения интерференционной картины получать данные о толщине липидного слоя, оценивать площадь исследуемой зоны с определенной толщиной липидного слоя (в %), а также судить о равномерности распределения липидов. В алгоритм программы введен коэффициент распределения липидов (регистрационный номер программы «Lacrima» 2010613451). Компьютерный анализ изображений может быть представлен в виде диаграммы и компьютерной модели слезной пленки.
Для оценки изменений эпителия глазной поверхности были использованы методы конфокальной микроскопии и импрессионной цитологии. Обследование было проведено для определения исходного состояния эпителия глазной поверхности и состояния слезной пленки и после курса лечения.
Для купирования признаков ССГ были использованы слезозаменители, препараты на основе гиалуроновой кислоты (Оксиал, Хило-Комод, Хилозар-Комод), Систейн баланс, осмопротекторы (Оптив), корнеопротекторы (Корнерегель, Солкосерил). Режим назначался индивидуально, длительность курса лечения составляла от 1 (носители КЛ) до 3 мес. (больные с глаукомой).
Результаты
При биомикроскопии наиболее типичными были изменения конъюнктивы в виде гиперемии, отека переходных складок, «шероховатости», фолликулеза различной степени выраженности. Эпителиопатию роговицы регистрировали в виде точечных дефектов поверхностного слоя эпителия.
После курса слезозаместительной терапии уменьшилось чувство дискомфорта при ношении КЛ, закапывании антиглаукомных препаратов. При биомикроскопии было отмечено уменьшение гиперемии и отека переходных складок. Признаки эпителиопатии в 1-й группе отсутствовали в 60% случаев, во 2-й группе – в 33% случаев, в остальных случаях отмечено уменьшение степени выраженности эпителиопатии.
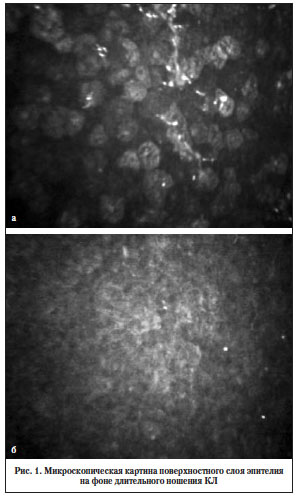
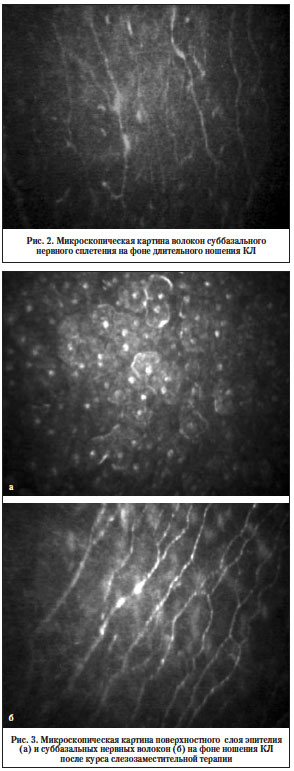
При исследовании исходного состояния роговичной поверхности с помощью конфокальной микроскопии были выявлены признаки отека эпителиоцитов с изменением их формы и нарушением адгезии (рис. 1а), нечеткость границ клеток поверхностного слоя эпителия, в большинстве случаев ядра клеток не визуализировались (рис. 1б). В базальном слое имелись точечные участки бесклеточных зон, контур нервных волокон суббазального нервного сплетения был неравномерным и нечетким, правильность хода волокон нарушена (рис. 2).
Через 1 мес. применения слезозаменителей была выявлена положительная динамика с восстановлением четкости границ эпителиоцитов и их ядер (рис. 3а), отмечено улучшение состояния базального слоя. Нервные волокна в суббазальном слое хорошо визуализировались с четкой структурой и правильной ориентацией, что свидетельствовало о положительной динамике состояния передних слоев стромы роговицы (рис. 3б).
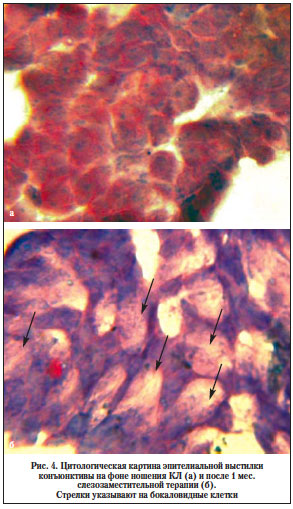
Методом импрессионной цитологии при первичном обследовании пациентов было подтверждено наличие признаков сквамозной метаплазии эпителия конъюнктивы. Выявлены изменения в виде нарушения клеточных контактов, полиморфизма клеток, выраженной кератинизации, десквамации поверхностного эпителиального пласта, уменьшения количества бокаловидных клеток или их отсутствия (рис. 4а).
После курса слезозаместительной терапии в течение 1 мес. цитологическая картина характеризовалась восстановлением архитектоники эпителиального пласта, плотными равномерными межклеточными контактами, а также появлением бокаловидных клеток (рис. 4б).
При исследовании суммарной слезопродукции с помощью пробы Ширмера выявлено ее снижение в обеих группах. Среднее значение суммарной слезопродукции в 1-й группе составило 7,8±2,3 мм, во 2-й группе – 7,3±7,0 мм. После курса слезозаместительной терапии в течение 1 мес. была отмечена четкая тенденция к повышению среднего уровня суммарной слезопродукции в 1-й группе на 22,7%, через 3 мес. во 2-й группе – на 35%.
При длительном ношении КЛ выявлено уменьшение времени разрыва прекорнеальной слезной пленки в среднем до 5,3±1,2 сек. На фоне инстилляции слезозаменителей в течение 1 мес. отмечено его увеличение на 62,8%. Во 2-й группе пациентов на фоне длительного использования препаратов, содержащих консерванты, время разрыва прекорнеальной слезной пленки в среднем составило 8,5±1,6 сек. После дополнения основного режима инстилляциями слезозаменителей и корнеопротекторов (режим назначался индивидуально) было отмечено отсутствие тенденции к дальнейшему снижению стабильности слезной пленки.
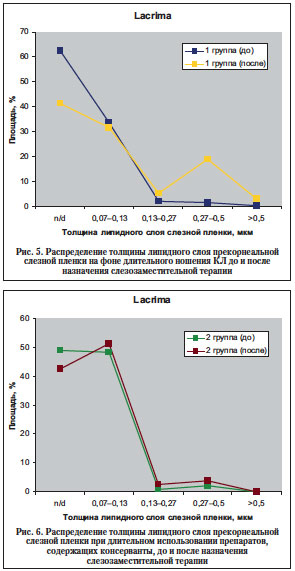
С помощью метода тиаскопии была определена толщина липидного слоя слезной пленки. В обеих группах наблюдали преобладание относительной площади зоны неопределенности (n/d) и зоны с наименьшими значениями толщины липидного слоя слезной пленки (0,07–0,13 мкм), а также минимальные значения относительной площади зоны с наибольшей толщиной липидного слоя (0,27–0,5 мкм). После курса слезозаменителей мы наблюдали перераспределение толщины липидного слоя слезной пленки в сторону увеличения зоны с наибольшей толщиной и уменьшения зоны неопределенности и зоны ее наименьших значений. Данная тенденция была выражена в большей степени у пациентов 1-й группы (рис. 5). У пациентов 2-й группы (рис. 6) на фоне слезозаместительной терапии не было выявлено отрицательной динамики в состоянии липидного слоя слезной пленки.
Клинический пример
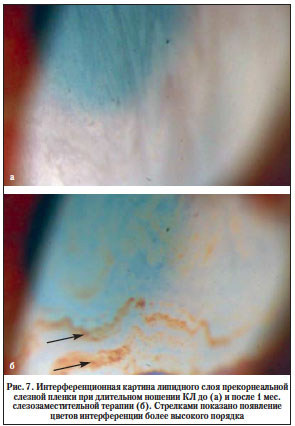
Данные исследования толщины липидного слоя слезной пленки методом тиаскопии на фоне многолетнего ношения КЛ до и после проведения курса слезозаместительной и корнепротекторной терапии представлены на рисунке 7. После проведенного курса в структуре слезной пленки было зарегистрировано появление цветов интерференции более высокого порядка.
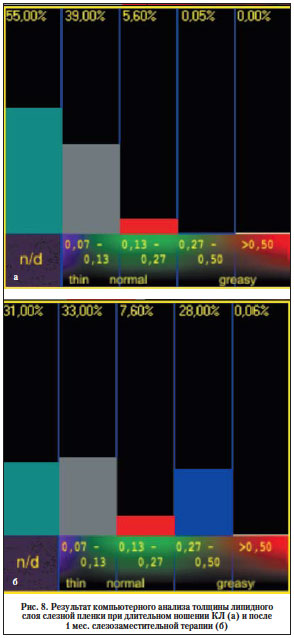
Данные компьютерного анализа представлены в виде диаграмм и компьютерной модели слезной пленки (рис. 8). После курса слезозаместительной терапии отмечается перераспределение относительной площади липидного слоя слезной пленки в сторону ее наибольших значений (0,27–0,5 мкм).
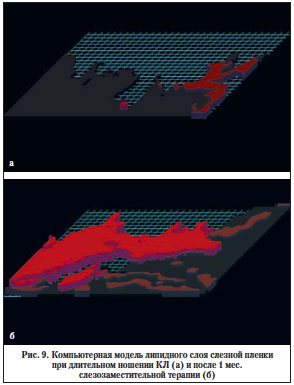
Коэффициент распределения липидов увеличился от 0,87 до 2,0, что указывает на более равномерное распределение липидов слезной пленки (рис. 9).
Заключение
Таким образом, результаты проведенных исследований свидетельствуют о возможности получения достоверных данных о состоянии глазной поверхности с помощью современных методов, таких как конфокальная микроскопия, импрессионная цитология, тиаскопия с компьютерным анализом интерференционной картины липидного слоя слезной пленки. Данные методы позволяют оценить степень изменений глазной поверхности и эффективность лечебных мероприятий.
При ССГ, индуцированном длительным использованием КЛ и применением препаратов, содержащим консерванты, назначение слезозаместительной и корнеопротекторной терапии позволяет улучшить состояние эпителия роговицы и конъюнктивы с восстановлением дифференцировки бокаловидных клеток.
На фоне длительного ношения КЛ применение слезозаменителей позволяет предотвратить дальнейшее снижение стабильности слезной пленки и добиться увеличения времени ее разрыва при ношении КЛ на 62,8%. Отмечена также положительная динамика в восстановлении липидного слоя.
При длительном использовании антиглаукомных препаратов, содержащих консерванты, и дополнительном применении слезозаменителей и корнеопротекторов в течение 3 мес. не было выявлено тенденции к дальнейшему снижению стабильности слезной пленки и отрицательной динамики состояния липидного слоя.
Литература
- Сомов Е.Е. Клиническая анатомия органа зрения человека (издание второе, переработанное и дополненное). СПб.: Ольга, 1997. 144 с.
- Бржеский В.В., Сомов Е.Е. Синдром «сухого глаза» // СПб.: Аполлон, 1998. С. 96.
- Prydal J.I., Artal P., Woon H., Cambell F.W. Study of human precorneal tear film thickness and structure using laser interferometry and confocal microscopy // Invest Ophthalmol Vis Sci. 1992. Vol. 33. Р. 2006–2011.
- Gipson I.K. Distribution of mucins at the ocular surface // Exp Eye Res. 2004. Vol. 78. Р. 379–388.
5.Tiffany J.M. The viscosity of human tears // Int Ophthalmol. 1991. Vol. 15. Р. 371–376.
- Tiffany J.M. The role of meibomian secretion in the tears // Trans. Ophthal. Soc. U.K. 1985. Vol. 104. Р. 396–401.
- Bron A.J., Tiffany J.M., Gouveia S.M., Yokoi N., Voon L.W. Functional aspects of the tear film lipid layer // Exp Eye Res. 2004. Vol. 78. Р. 347–360.
- Егорова Г.Б., Митичкина Т.С., Шамсудинова А.Р. Корнеопротекция при применении контактных линз // Вестник офтальмологии. 2014. № 130 (2). С. 59–67.
- Петров С.Ю., Сафонова Д.М. Консерванты в офтальмологических препаратах: от бензалкония хлорида к поликватерию // Глаукома. 2013. № 4. С. 82–96.
- Лещенко И.А. Проблемы сухости глаз при ношении контактных линз и их решение // Современная оптометрия. 2010. № 1 (31). С. 18–20.
- Егорова Г.Б., Новиков И.А., Митичкина Т.С. Совершенствование и оценка возможностей метода тиаскопии // Вестник офтальмологии. 2011. № 127 (6). С. 35–39.
- Bron A.J., Tiffany J.M., Gouveia S.M., Yokoi N., Voon L.W. Functional aspects of the tear film lipid layer // Exp Eye Res. 2004. Vol. 78. Р. 347–360.
- Norn M.S. Semiquantitative interference study of fatty layer of precorneal film // Acta Ophthalmol. 1979. Vol. 57. Р. 766–774.
- Ландсберг Г.С. Оптика. М.: Физматлит, 2006. С. 848.
- King-Smith P.E., Fink B.A., Fogt N. Three interferometric methods for measuring the thickness of layers of the tear film // Optom Vis Sci. 1999. Vol. 76. Р. 19–32.






Комментировать