Витамин D и его необходимость в организме человека. Витамин D и патофизиология сахарного диабета. Результаты эпидемиологических исследований, подтверждающие связь между недостаточным потреблением витамина D и риском развития сахарного диабета и его осложнений.
Калинченко С.Ю., Гусакова Д.А., Тюзиков И.А., Тишова Ю.А., Ворслов Л.О., Кафедра эндокринологии ФПК МР РУДН (Москва); НИИ Урологии им. Н.А. Лопаткина – филиал ФГБУ «НМИРЦ» Минздрава России (Москва); Клиника профессора Калинченко (Москва).
Введение
Витамин D синтезируется в организме человека самостоятельно под действием ультрафиолетовых (УФ) лучей солнечного света, или поступает в организм с некоторыми продуктами питания, такими как рыбий жир, масло, яйца, молоко.
ВитаминD относится к группе жирорастворимых витаминов, однако не является собственно витамином в классическом смысле этого термина, поскольку оказывает многообразные биологические эффекты за счет взаимодействия со специфическими рецепторами, локализованными в клетках многих тканей и органов. В этом отношении активный метаболит витамина D ведет себя как истинный гормон, именно поэтому он получил второе название D-гормон. Витамин D, получаемый из продуктов питания и в виде пищевых добавок, а также образующийся при пребывании на солнце, биологически инертен. Для активации и превращения в активную форму D-гормона [1,25(ОН)2D] в организме должны пройти два процесса гидроксилирования. Таким образом, под термином «витамин D» мы понимаем целую группу биологически-активных веществ, куда входят инертный витамин D, получаемый из пищи и синтезированный в коже, промежуточная (транспортная или депо) форма и активный метаболит витамина D (Таблица 1).
Таблица 1. Формы витамина D
| 1 | D2 (эргокальциферол) | Поступает в организм с продуктами растительного происхождения |
| 2 | D3 (холекальциферол) | Образуется в коже под влиянием солнечного излучения или поступает в организм с продуктами животного происхождения |
| 3 | 25(ОН)D3 (25-гидрокси-холекальциферол), кальцидол | Печеночный метаболит витамина D3, основной показатель обеспеченности организма витамином D |
| 4 | 1,25(ОН)2D3 (25-дигидро-холекальциферол), кальцитриол | Почечный метаболит витамина D3, обеспечивающий основные биологические эффекты витамина D |
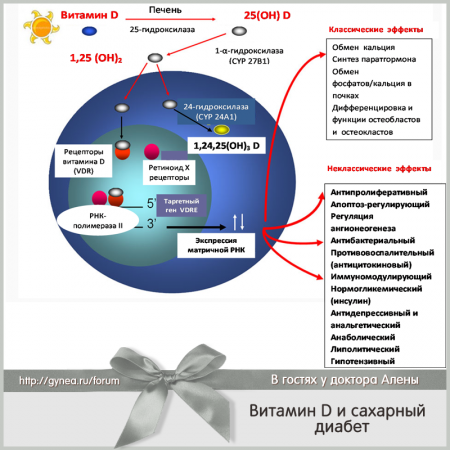
Наши традиционные представления о витамине D связаны, прежде всего, с его важной ролью в кальциево-фосфорном гомеостазе и влиянии на минеральную плотность костной ткани [1]. Однако, этим не ограничиваются биологические эффекты витамина D. Он также влияет и на другие физиологические процессы в организме, включающие модуляцию клеточного роста, нервно-мышечную проводимость, иммунитет и воспаление [12, 13]. В последнее время накоплен значительный материал о взаимосвязи дефицита витамина D с ожирением [14], инсулинрезистентностью [15], неблагоприятным влиянием на секрецию инсулина и толерантность к глюкозе [16]. Влияние витамина D на метаболизм костной тканиназывают «классическими» эффектами,а влияние на другие функции – «неклассическими» эффектами (Рисунок 1).
Следуя исторической традиции, в научной литературе витамин D до сих пор называют «витамином», несмотря на то, что в отличие от всех других витаминов, он не проявляет ни одного витаминоподобного свойства, так как, во-первых, не участвует подобно истинным витаминам как ко-фермент ни в одном биохимическом процессе; во-вторых, биологически не активен, и только за счет двухступенчатого метаболизма в организме превращается в активную гормональную форму; в–третьих, в организме к его активной форме [1,25(ОН)2D] экспрессируются специализированные рецепторы, которых не имеет ни один из известных витаминов. Активированная витамином D молекула рецептора (VDR) взаимодействует с активаторами и репрессорами этого рецептора, оказывая комплексное воздействие на процессы транскрипции генома. Таким образом, VDR представляет собой «классический» стероидный рецептор, а активная форма витаминаD [1,25(ОН)2D] – мощный стероидный гормон с уникальным спектром «неклассических» системных метаболических эффектов, который регулирует около 3% генома человека (несколько десятков тысяч генов) (Рисунок 1) [2].
Рисунок 1. «Классические» и «неклассические» эффекты гормона D в организме [2].
Витамин D и патофизиология сахарного диабета
Согласно данным современных исследований, все больше доказательств появляется в пользу того что витамин D влияет на метаболизм глюкозы и инсулина, а дефицит витамина D является фактором риска для развития инсулинорезистентности, нарушения толерантности к глюкозе и, как следствие, сахарного диабета 2 типа (СД2).
Проводимые в течение последних десятилетий эпидемиологические исследования предоставили неоспоримые свидетельства ассоциации между недостаточным потреблением витамина D и риском развития сахарного диабета и его осложнений. Важным результатом этих исследований является подтверждение низкого уровня витамина D [25(OH)D] в плазме как независимого фактора риска СД2. Например, в крупномасштабном исследовании «National Health and Nutrition Examination Survey» (NHANES) было показано, что недостаточное потребление витамина Dсвязано с повышенным риском такогосерьёзного осложнения СД2 как периферическая нейропатия (ОР 2,12; 95% ДИ=1.17-3.85). Достоверность ассоциации сохранялась после поправок на демографические факторы, ожирение и сопутствующие заболевания, в том числе СД2 [17].
В рамках крупномасштабного «Исследования Здоровья Медсестер» («Nurses’ Health Study», США), было проведено сравнение группы из 608 женщин с впервые выявленным СД2 и контрольной группы из 559 женщин без диабета. После корректировки на другие факторы риска, более высокие уровни 25(OH)D в плазме крови были ассоциированы с более низким риском СД2. При сравнении подгруппы с самыми высокими уровнями 25(OH)D (более 33 нг/мл) с подгруппой с самыми низкими уровнями 25(OH)D (менее 14 нг/мл), риск СД2 снижался почти в 2 раза (ОР 0.52; 95% ДИ=0.33-0.83) [18].
В популяционной когорте 2465 европейцев уровни 25(OH)D в сыворотке были низкими (<50 нмоль/л) у 29% и очень низкими (<37 нмоль/л) у 11% обследованных. После внесения поправок на пол, возраст, географический регион проживания, уровень образования, курение, индекс массы тела (ИМТ), физическую активность, общую калорийность питания, риск сахарного диабета был значимо связан с более низкими уровнями 25(OH)D в плазме крови. Участники с уровнями 25(OH)D более 80 нмоль/л в два раза реже страдали сахарным диабетом (ОР 0.5; 95% ДИ=0.3-0.9) по сравнению с участниками, имевшими низкие уровни 25(OH)D (менее 37 нмоль/л) [19].
Накопленный объем исследований приемлемого качества настолько высок, что позволил провести ряд мета-анализов ассоциации между дефицитом витамина D в организме и риском метаболических нарушений (к которым относятся метаболический синдром и сахарный диабет 2-го типа). Мета-анализ 28 исследований (n=99745) показал, что среди участников в квартиле с самыми высокими уровнями 25(OH)D в сыворотке отмечено снижение риска кардиометаболических расстройств (СД2 и метаболического синдрома) на 43% (ОР 0.57; 95% ДИ=0.48-0.68) [20]. Мета-анализ 11 наблюдательных исследований (3612 случаев СД2, всего 59325 участников) показал, что уровни 25(ОН)D в самом высоком квартиле соответствовали снижению риска СД2 на 41% (ОР 0.59; 95% ДИ=0.52-0.67) [21]. Мета-анализ 16 кросс-секционных исследований показал, что при увеличении уровней 25(OH)D в сыворотке крови на каждые 25 нмоль/л риск метаболического синдрома снижался на 13% (ОР 0.87; 95% ДИ=0.83-0.92, p <0.001) [22].
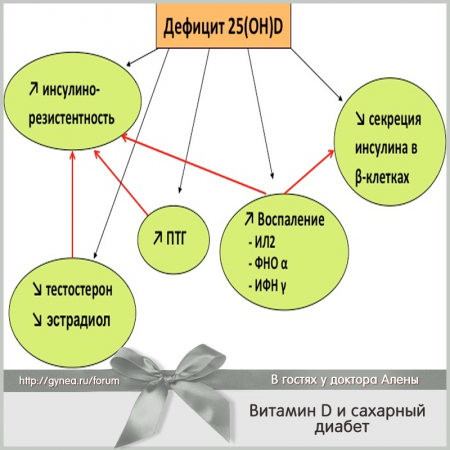
Изучение роли дефицита витамина D в патогенезе СД2 началось с открытия рецептора витамина D (VDR) в бета-клетках поджелудочной железы. В настоящее время можно выделить несколько возможных механизмов влияния витамина D на патогенез СД2 (Рисунок 2).
Рисунок 2. Механизмы влияния дефицита витамина D на патогенез СД2
Влияние витамина D на бета-клетки и секрецию инсулина
Витамин D может воздействовать на бета-клетку поджелудочной железы двумя возможными путями: либо непосредственно индуцирует секрецию инсулина бета-клетками, за счет увеличения внутриклеточного уровня кальция с помощью неселективных потенциал-зависимых кальциевых каналов, или опосредованно активирует кальций-зависимую эндопептидазу бета-клеток, которая преобразует проинсулин в активный инсулин [23]. Кроме того, витамин D участвует в механизмах промоции гена инсулина человека и обеспечивает активацию его транскрипции [8,9].
Влияние витамина D на чувствительность тканей к инсулину (инсулинорезистентность)
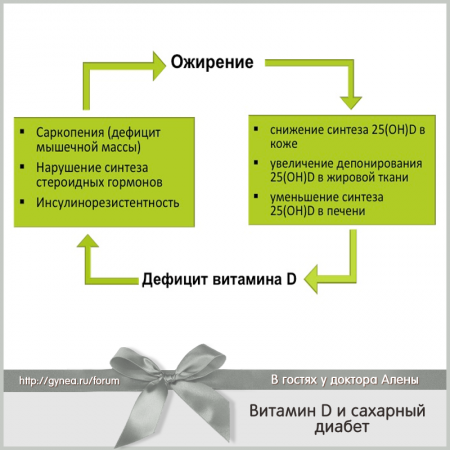
Инсулинорезистентность является признанным фактором в патогенезе СД2. Витамин D может влиять на чувствительность тканей к инсулину либо непосредственно, стимулируя экспрессию рецепторов инсулина в клетках [24], как было показано в исследовании in-vitro c культурой промоноцитов человека, подвергающихся воздействию активного метаболита витамина D, что приводило к повышенной экспрессии мРНК инсулиновых рецепторов и увеличению транспорта глюкозы в клетку в 1,3 раза по сравнению с контрольной культурой клеток [25], либо косвенно, за счет увеличения внеклеточного кальция и, таким образом, повышения притока кальция внутрь клетки в инсулин-зависимых тканях, который необходим для инсулин-опосредованных внутриклеточных процессов [7, 24]. С другой стороны, витамин Dнаходится в тесной взаимосвязи с половыми стероидами, которые также влияют на экспрессию генов инсулинового рецептора и его чувствительность [26]. Половые гормоны являются важнейшими активаторами гена инсулинового рецептора, а тестостерон у обоих полов обеспечивает метаболизм мышечной ткани — основного места утилизации глюкозы в организме. Существует точка зрения, что дефицит витамина D, приводя к дефициту половых гормонов, способствует нарушению соотношения жирозапасающих (пролактин, инсулин, кортизол) и жиросжигающих (гормон роста, катехоламины, половые гормоны, тиреоидные гормоны) факторов, а возникшее и прогрессирующее ожирение уменьшает уровень циркулирующего в крови 25(ОН)D за счет повышенного захвата жировой тканью и снижения скорости гидроксилирования в печени за счет жирового гепатоза, что формирует своеобразный «порочный круг патогенеза», характерный для СД 2 типа (Рисунок 3) [3]. При этом пациенты с ожирением часто избегают солнечного света, который необходим для синтеза витамина D в коже, так как страдают соматическими заболеваниями (прежде всего, сердечно-сосудистыми), не позволяющими им долго находиться под прямыми лучами Солнца [4]. И сегодня существуют доказательства того, что низкий уровень витамина D может рассматриваться как независимый предиктор формирования и прогрессирования ожирения, ведущего к инсулинорезистентности и СД 2 типа, который ранее правильнее назывался «диабетом тучных» [5,6].
Рисунок 3. Дефицит витамина D и ожирение «порочный круг»
Влияние витамина D на секрецию паратгормона
В связи с увеличением распространенности нарушенной толерантности к глюкозе и СД2 у больных с первичным гиперпаратиреозом [27], было высказано предположение, что, может быть, дефицит витамина D, путем индукции вторичного гиперпаратиреоза, может способствовать развитию и прогрессированию СД 2 типа. При дефиците витамина D повышается сывороточная концентрация паратгормона (ПТГ), который, в свою очередь, может подавлять чувствительность инсулинового рецептора и увеличивать риск развития метаболического синдрома и СД2, что было показано в перекрестном исследовании 2007 года в мужской когорте пациентов [28].
Дефицит витамина D и воспаление
Одна из существующих гипотез патогенеза СД2 основана на воспалительных факторах, способствующих нарушению секреции инсулина за счет повреждения и преждевременного апоптоза бета-клеток с одной стороны и развития инсулинорезистентности с другой. Помимо рецепторов к 1,25(ОН)2D (VDR)в бета-клетках поджелудочной железы был также обнаружен Са-связывающий белок кальбиндин (один из эффекторов витамина D), посредник транспорта кальция, одновременно играющий важную роль и в защите клеток различных тканей от патологического апоптоза (программируемой клеточной смерти) [29]. В частности, кальбиндин способствует защите бета-клеток поджелудочной железы, что подтверждается экспериментальными исследованиями на линях мышей с делециями гена кальбиндина [30]. Витамин D также оказывает существенное влияние на синтез некоторых воспалительных цитокинов, препятствуя транскрипции ряда генов цитокинов или подавляя факторы транскрипции, участвующие в генерации цитокинов [31]. Таким образом, витамин Dоказывает мощное модулирующее действие на иммунную систему, а дефицит витамина D может вызывать системный воспалительный ответ, который способен индуцировать инсулинорезистентность [10,11].
Распространенность дефицита витамина D. Целевые значения витамина D: что считать нормой, а что – патологией?
По оценкам ряда исследователей из разных стран, более половины населения мира имеет дефицит витамина D [32]. Один из значимых для современной медицины вопросов, касающихся витамина D, заключается в том, как правильно этот дефицит определять.
Сывороточная концентрация 25(OH)D является лучшим показателем статуса витамина D, поскольку отражает суммарное количество витамина D, производимого в коже и получаемого из пищевых продуктов и пищевых добавок, и имеет довольно продолжительный период полураспада в крови — порядка 15 дней [33]. Существуют некоторые разногласия среди экспертов относительно «нормы» 25(OH)D достаточной для поддержания здоровья человека. В некоторых случаях для оценки референсного интервала используется анализ уровней витамина D в заведомо здоровой популяции с расчетом 95-го перцентиля. Однако, ввиду высокой распространенности дефицита витамина D даже в «здоровой» популяции, этот метод не является оправданным.
Дефицит витамина D, включая мнение экспертов Международного эндокринологического общества [34], определяется как уровни 25(OH)D в сыворотке крови менее 20 нг/мл. Многие эксперты считают, что уровни между 20-30 нг/мл должны расцениваться как «недостаточность» витамина D, а оптимальный уровень — более 30 нг/мл [35, 36, 37]. Однако, уже сейчас существует целый ряд исследований, демонстрирующих значительные преимущества в отношении здоровья и качества жизни при достижении более высоких уровней 25(OH)D [37, 38]. Согласно рекомендациям «The Vitamin D Society», канадского общества экспертов по изучению витамина D, оптимальным уровнем 25(OH)D в сыворотке крови можно считать 100 – 150 нмоль/л (40 – 60 нг/мл). Только достижение такой концентрации 25(OH)D позволит снизить риск возраст-ассоциированных заболеваний, таких как остеопороз, СД 2 типа, различные виды онкологических заболеваний и увеличить продолжительность жизни.
На фармацевтическом рынке в настоящее время имеется несколько препаратов витамина D. Одним из наиболее интересных считается МИНИСАН® — оригинальный препарат финской компании Verman. Удобны в применении жевательные таблетки препарата, содержащие по 400 МЕ натурального жирорастворимого витамина D3. Таблетки разрешены к применению у детей от 3 лет и взрослых. А для детей более раннего возраста МИНИСАН® выпускается в каплях.
В настоящее время дефицит витамина D представляет собой пандемию, затрагивающую большую часть общей популяции. В группе риска по развитию дефицита витамина D находятся дети, беременные женщины, пожилые люди, люди с ограниченным пребыванием на солнце (менее 2-х часов в день), люди с ожирением, с заболеваниями, сопровождающимися нарушением всасывания жиров, а также население стран, расположенных выше 35 градуса северной щироты (вся территория России), когда из-за более острого угла падения солнечных лучей и их рассеивания в атмосфере в период с ноября по март кожа практически не вырабатывает витамин D, вне зависимости от времени, которое проводится человеком на солнце [39]. Низкое содержание витамина D в большинстве продуктов питания, само по себе, представляет риск дефицита данного витамина, развитие которого становится еще более вероятным при аллергии на молочный белок, непереносимости лактозы и вегетарианстве [40].
Таким образом, восполнение дефицита витамина D с помощью препаратов витамина D в настоящее время является практически необходимым условием достижения и поддержания нормальной концентрации 25(OH)D в сыворотке крови. Согласно рекомендациям международных экспертов, для профилактики и лечения дефицита витамина D применяется колекальциферол, или витамин D3, реже используются препараты эргокальциферола, витамина D2 [34]. Подбор оптимальной дозы витамина D проводится в зависимости от исходной концентрации 25(OH)D в сыворотке крови, измерение которой является обязательным компонентом подбора начальной дозы и исследования достаточности компенсации дефицита на фоне проводимой терапии.
В различных странах, рекомендуемое суточное потребление витамина D составляет 400-600 МЕ/сут для взрослых. В настоящее время ведется активное обсуждение необходимости повышения суточной дозировки витамина D до 2000-4000 МЕ/сут, а для терапии ожирения и СД 2 типа могут потребоваться дозы порядка 6000 – 10 000 МЕ/сут [34, 41]. В некоторых источниках литературы вместо Международных единиц предлагаются микрограммы. Для этого применяется формула: 1 МЕ = 0,025 мкг, или 1 мкг = 40 МЕ.
Заключение
В целом, следует отметить, что в настоящее время проблеме дефицита/недостаточности витамина D с точки зрения патогенетических взаимоотношений с СД уделяется недостаточное внимание, хотя обе метаболические проблемы сегодня идут рука об руку и между ними не может не быть связи.
Распространенность сахарного диабета и ожирения продолжает расти во всем мире, захватывает все более молодой возраст, а современные методы терапии СД не приносят соответствующих результатов в отношении продолжительности и качества жизни больных СД.
Согласно результатам современных эпидемиологических исследований, нет основания сомневаться в наличии взаимосвязи столь высокой распространенности СД и дефицита витамина D в популяции. ВитаминDхарактеризуется широким спектром воздействия на молекулярную физиологию клеток и тканей. Приведенные нами данные экспериментальных и клинических исследований, указывают на многочисленные свидетельства из различных смежных областей современных биологии и медицины, подтверждающие целесообразность использования витамина D для терапии и в профилактики сахарного диабета.













Комментировать