Результаты статистики. Профилактико-лечебные меропрития.
Чувиров Д.Г., Маркова Т.П.
Ежегодно в России регистрируется 27,3–41,2 млн случаев острых респираторных заболеваний (ОРЗ), при этом доля вируса гриппа как возбудителя ОРЗ составляла в первом 10-летии XXI в. около 6,2–12,6%. Расходы на лечение гриппа и его осложнений в мире ежегодно составляют около 14,6 млрд долларов. В России экономические потери от гриппа в год оцениваются в 10 млрд руб. [1]. ОРЗ являются причиной смерти в 19% случаев у детей младше 5 лет, особенно в странах Африки, Латинской Америки. 20% медицинских консультаций у детей связаны с ОРЗ, в 30% случаев ОРЗ является причиной нетрудоспособности [10].
Среди взрослых заболевает 5–10% населения, среди детей – 20–30%. При последней пандемии «свиного» гриппа в 2009 г. грипп был зарегистрирован в 214 странах, число летальных исходов составило 18 тыс. 90% заболевших были в возрасте до 65 лет, у умерших отмечалось быстрое поражение легких с развитием респираторного дистресс-синдрома. У 26–38% умерших определена вирусно-бактериальная микст-инфекция. За октябрь – декабрь 2009 г. в России гриппом переболели 13,26 млн человек, в 44% случаев это были лица 18–39 лет. По данным Департамента здравоохранения г. Екатеринбурга, среди заболевших 91,8% составили непривитые, а среди умерших в 2009 г. было 100% непривитых против сезонного гриппа [2].
При вирусно-бактериальных микст-инфекциях респираторного тракта чаще высеваются Streptococcus (S.) pneumoniae, Staphylococcus (Staph.) aureus, Haemophilus (H.) influenzae, Moraxella (М.) catarrhalis или Neisseria catarrhalis [3, 4].
Природным резервуаром S. pneumoniae является носоглотка человека, возбудитель передается воздушно-капельным путем. Каждый ребенок инфицирован одним или несколькими штаммами S. pneumoniae и может быть переносчиком инфекции, особенно в первые годы жизни, в промышленно развитых странах – и в возрасте 6 мес. Чаще всего инфицирование не приводит к развитию клинических проявлений, а проходит бессимптомно. Клинические проявления начинаются при распространении инфекции из носоглотки в другие органы. Большинство инфекционных заболеваний возникает не после длительного носительства, а после инфицирования новыми серотипами, чувствительность организма зависит от состояния иммунной системы и вирулентности штамма возбудителя. Высокий уровень пневмококковых инфекций наблюдается у детей и пожилых людей, относящихся к группе риска по развитию иммунодефицита. Пневмококковая инфекция, по данным ВОЗ, приводит к смертельным исходам у 1,6 млн человек в год, при этом около 50% случаев составляют дети в возрасте от 0 до 5 лет. У 76% взрослых (0,5 млн случаев в год) и у 90% детей (70 тыс. случаев) пневмония вызывается пневмококковой инфекцией [2]. Особой тяжестью отличается пневмококковый менингит, частота которого составляет 8 на 100 тыс. детей до 5 лет. 30–40% острых средних отитов у детей вызывается пневмококком [2].
Большинство штаммов H. influenzae являются условно-патогенными микроорганизмами. У новорожденных и маленьких детей H. influenzae типа В (Hib-инфекция) вызывает бактериемию, пневмонию и острый бактериальный менингит. В ряде случаев развиваются воспаление подкожной клетчатки, остеомиелит, инфекционный артрит.
- catarrhalis (или Neisseria catarrhalis) – грамотрицательная бактерия, вызывает инфекционные заболевания респираторного тракта, среднего уха, глаз, центральной нервной системы и суставов. M. catarrhalis относится к условно-патогенным микроорганизмам, представляет угрозу для человека и персистирует в респираторном тракте. M. catarrhalis в 15–20% случаев вызывает острый средний отит у детей.
Термин «часто болеющие дети» (ЧБД) введен в литературу В.Ю. Альбицким, А.А. Барановым (1986). — ЧБД [6]:– до 1-го года – 4 и более эпизодов ОРЗ в год;– до 3-х лет – 6 и более эпизодов ОРЗ в год;
– 4–5 лет – 5 и более эпизодов ОРЗ в год;
– старше 5 лет – 4 и более эпизодов ОРЗ в год.
Нами среди ЧБД выделена группа ЧБД с хроническими заболеваниями (ЧБД-ХЗ) [3].
ЧБД-ХЗ:
– с заболеваниями рото- и носоглотки;
– с заболеваниями верхних дыхательных путей;
– с заболеваниями нижних дыхательных путей.
По данным Ю.О. Хлыниной, у ЧБД на слизистых происходит вытеснение сапрофитной флоры условно-патогенными микроорганизмами, включая S. pneumoniae, Staph. аureus, H. influenzae. В контрольной группе в основном из носо- и ротоглотки высевались S. viridens – у 26%, S. mutans – у 23,3%, S. salivaricus – у 20% детей. У ЧБД эти возбудители высевались в 15,3; 16,6; 9,7% случаев. Доминирующими микроорганизмами являются Staph. aureus – 52,7%; S. pyogenes – 23,6%; Candida albicans – до 50% ЧБД. Повышается плотность заселения слизистых микроорганизмами: S. pneumoniaе – lg=3,5±0,97 КОЕ; H. influenzaе – lg=2,4±0,48 КОЕ; Staph. aureus – lg=3,5±0,87 КОЕ. Лишь 36,5% штаммов M. catarrhalis чувствительны к ампициллину. H. influenzaе была резистентна к ампициллину в 36,5% случаев. Разница представленных показателей была статистически достоверна. Смена сапрофитной флоры на условно-патогенную, высевание Candida albicans, резистентность флоры к антибактериальной терапии затрудняют лечение и реабилитацию ЧБД [4, 5].
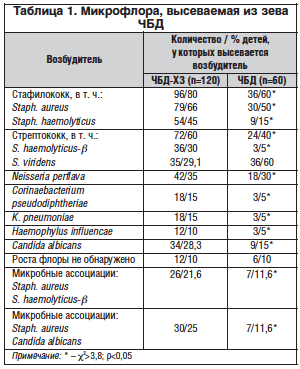
Микрофлора, высеваемая из зева ЧБД, представлена в таблице 1.
Обследовано и отобрано 60 ЧБД, согласно классификации В.Ю. Альбицкого, А.А. Баранова (1986) на основании частоты ОРЗ [13], и 120 ЧБД-ХЗ с частотой ОРЗ 6 и более раз в год и хроническими заболеваниями носо- и ротоглотки. Было проведено сравнение персистенции флоры у ЧБД и ЧБД-ХЗ. В мазках из зева монокультура выделена у 40% ЧБД-ХЗ, 2 и более возбудителя – у 46,6%, Candida albicans – у 28,3%, сочетанная бактериальная и грибковая флора – у 25%. Количество возбудителей колебалось от 105хКОЕ до 108хКОЕ/мл. С уменьшением числа эпизодов ОРЗ уменьшаются частота и спектр высеваемых микроорганизмов. Сравнение частоты высеваемости Staph. haemolyticus и Staph. aureus, S. haemolyticus-β, Neisseria perflava в группах статистически достоверно (χ2>3,8; p<0,05). У ЧБД-ХЗ по сравнению с ЧБД выше частота микробных ассоциаций Candida albicans и Staph. aureus или S. haemolyticus-β и Staph. aureus (χ2>3,8; p<0,05). Количество возбудителей у ЧБД колебалось от 103хКОЕ до 105хКОЕ/мл [3].
Проведенные нами многочисленные исследования показывают, что у ЧБД в дополнение к частым респираторным вирусным инфекциям (ОРВИ) наблюдается персистенция бактериальной флоры, которая может активироваться на фоне задержки развития иммунной системы и частых ОРВИ [3]. У ЧБД происходит замена сапрофитной флоры на условно-патогенную флору, резистентную к антибактериальной терапии [4, 5].
Полноценный местный иммунитет (дефенсины, лизоцим, иммуноглобулины (Ig) класса A, s-IgA) у детей формируется к 5–7-летнему возрасту [11]. У детей наблюдается снижение экспрессии толл-подобных рецепторов (TLR) 2, TLR4-рецепторов на эпителиальных клетках, концентрации дефенсинов в слизи, что способствует развитию респираторных инфекций [12]. По нашим данным, у ЧБД-ХЗ наблюдается задержка развития иммунной системы, наиболее выражено снижение уровня IgA и s-IgA, интерферона (ИФН)-γ в слюне, синтеза ИФН-α [3].
Представленные результаты подтверждают целесообразность назначения бактериальных лизатов и специфических вакцин в профилактике и лечении ОРЗ и профилактике осложнений у ЧБД.
При формировании иммунного ответа взаимодействие бактериальных антигенов с TLR-рецепторами на поверхности дендритных клеток приводит к их созреванию, активации и миграции в лимфатические узлы. Дендритные клетки презентируют антигены Т- и В-клеткам, что сопровождается синтезом цитокинов, дифференцировкой Т–хелперов (Th). В дальнейшем происходит пролиферация В-клеток в плазматические клетки, синтезирующие специфические Ig, особенно IgA и s-IgA, возвращающихся и защищающих слизистые. Фагоциты и естественные киллеры (Nk-клетки) уничтожают патогены.
Образовавшиеся антитела (АТ) обеспечивают процесс опсонизации поступающих в организм или имеющихся в нем патогенных микроорганизмов, что делает возможным поглощение и уничтожение патогенных микроорганизмов фагоцитами. Данный механизм действия позволяет снизить частоту, продолжительность и тяжесть инфекционных заболеваний респираторного тракта. При опсонизации происходит распознавание специфических мембранных АТ, покрывающих патоген. Фагоциты имеют специфические рецепторы для IgG и IgA АТ, что позволяет фагоцитировать патогены, покрытые АТ, и уничтожить их с помощью ферментов фагосом. Специфические IgM АТ, синтезируемые на раннем этапе иммунного ответа, в комплексе с патогеном активируют компоненты комплемента С3b и C4b, усиливающие опсонизацию. Фагоциты имеют рецепторы для этих компонентов комплемента, кроме того, компонент С5 способен активировать и усиливать фагоцитоз, приводящий к уничтожению патогена [7].
К сожалению, резистентность к пневмококку в различных странах составляет 30–40% [2]. В нашем арсенале имеются 2 вакцины против S. pneumoniaе: конъюгированная для вакцинации детей до 5 лет и полисахаридная для вакцинации детей и взрослых. При вакцинации конъюгированной вакциной (Превенар, США) вырабатываются АТ против 13 серотипов, входящих в ее состав (1, 3, 4, 5, 6А, 6В, 7F, 9V, 14, 18C, 19А, 19F, 23F) и конъюгированных с белком-носителем (дифтерийным анатоксином), длительность эффекта вакцинации – до 5 лет. Вакцина Синфлорикс (Бельгия) содержит полисахариды 10 серотипов (1, 4, 5, 6B, 7F, 9V, 14, 18C, 19F, 23F), конъюгированных с протеином D бескапсульной H. influenzaе. В вакцину включены полисахариды 1 и 5 серотипов пневмококка. Считается, что 1 серотип вызывает в России 25% пневмоний, осложненных плевритом. Cеротип 7F вызывает наибольшую летальность. Синфлорикс также вызывает синтез АТ к родственным серотипам 6А и 19А [2].
Вакцинацию детей Превенаром и Синфлориксом проводят в возрасте 2–60 мес. (2 дозы по 0,5 мл в/м в возрасте 2–6 мес. с интервалом 2 мес.; 3-я инъекция – в возрасте 15 мес., через 6 мес. после 2-й). При начале вакцинации в:
– 7 мес. – 2 дозы с интервалом 2 мес., 3-я доза на 2-м году жизни;
– 12–23 мес. – 2 дозы с интервалом 2 мес.;
– 2–5 лет – 1 доза Превенар-13 однократно.
Вакцина для детей и взрослых Пневмо-23 (Франция) содержит 23 серотипа пневмококка (1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F); вакцина производства США также содержит 23 серотипа (1, 2, 3, 4, 5, 6B, 7F, 8, 9N, 9V, 10A, 11A, 12F, 14, 15B, 17F, 18C, 19F, 19A, 20, 22F, 23F, 33F). Препарат вводят с возраста 2 года – 1 дозу (0,5 мл) подкожно или в/м. Перенесенная пневмококковая инфекция не является противопоказанием. Вакцинация Пневмо-23 проводится в группах высокого риска однократно. Вакцина может вводиться вместе с другими вакцинами (грипп, БЦЖ) в разные места тела. Эффективность сохраняется 5–8 лет. При иммунодефицитах вакцинацию можно повторять через 3 года. При вакцинации Превенаром могут развиться местные и редко системные реакции (лимфаденопатия, анафилактоидные, коллаптоидные реакции, многоформная эритема, дерматит, зуд). На введение Пневмо-23 могут быть местные и системные реакции по типу феномена Артюса, чаще после перенесенной стрептококковой инфекции [2].
Возможно сочетанное применение вакцин против пневмококка. Например, детей 2–5 лет из группы риска, вакцинированных ранее Превенаром или Синфлориксом, можно вакцинировать Пневмо-23 для расширения спектра серотипов возбудителя. Группа риска включает детей и пожилых старше 60 лет, пациентов с ожирением, диабетом, сопутствующими, хроническими заболеваниями легких и сердечно-сосудистой системы, беременных. В группе риска инфекции чаще сопровождаются осложнениями и смертельными исходами. У пожилых пациентов с внебольничной пневмонией риск смертельного исхода в 3–4 раза выше, чем у более молодых [2].
Вакцинация в группе риска осенью Инфлюваком и Превенаром у детей 18–72 мес. привела к снижению фебрильных респираторных инфекций на 25% по сравнению с контрольной группой. Частота случаев гриппа снизилась на 51 и 52% в обеих группах соответственно [2].
Эффективность вакцины Превенар была проверена в 9 контролируемых исследованиях у 18 925 детей в 2006–2008 гг. В США массовая вакцинация детей снизила частоту пневмококковых инфекций в 45 раз, включая пневмококковый менингит. По данным ВОЗ, вакцинация детей в 72 развивающихся странах может предотвратить смерть 500 тыс. человек [2].
К сожалению, проведение вакцинации не всегда возможно, приходится использовать другие методы лечения и профилактики. Препараты, содержащие лизаты бактерий, привлекают интерес многих специалистов, их часто назначают для профилактики и лечения инфекций респираторного тракта. Первые препараты появились в 1970-х гг. (ОМ-86). Длительное изучение их свойств и механизма действия подтверждает их иммунотропный эффект и указывает на отсутствие формирования стойкого протективного иммунитета, поэтому более правильно называть эти лекарственные средства бактериальными иммуномодуляторами. Изучение особенностей механизма действия позволило разделить бактериальные лизаты на группы (табл. 2).
Такие препараты, как продигиозан, пирогенал, сальмозан в настоящее время не применяются.
Клинический эффект бактериальных иммуномодуляторов направлен на снижение числа и тяжести обострений респираторных инфекций. Механизм действия связан, с одной стороны, с выработкой специфического IgA и фиксацией его на слизистых, а с другой стороны, – с активацией иммунной системы (Т-, В-клетки, макрофаги, дендритные клетки).
Активация макрофагального звена, цитотоксических Т-лимфоцитов способствует уничтожению инфицированных клеток и инфекционных агентов. Специфические и неспецифические механизмы действия бактериальных иммуномодуляторов определяют их эффект не только против бактерий, лизаты которых входят в состав препаратов, но и против других возбудителей респираторных инфекций, что можно проследить по частоте ОРВИ в группе ЧБД [8, 9].
C позиций доказательной медицины были проанализированы 35 статей. Показан положительный статистически достоверный эффект бактериальных лизатов (ОМ-86) на частоту респираторных инфекций. Не отмечено побочных эффектов в группах, получавших бактериальные лизаты, в сравнении с группами контроля, получавшими плацебо. Авторы отмечают необходимость проведения исследований с позиций доказательной медицины для подтверждения эффективности иммунотропных препаратов в профилактике ОРЗ [10].
Хорошо изучена эффективность Рибомунила – бактериального иммуномодулятора системного действия. В его состав входят рибосомы микроорганизмов S. pneumoniaе, S. pyogenes, Klebsiella (К.) pneumoniaе, H. influenzaе и протеогликаны K. pneumoniaе. Рибосомы являются клеточными органоидами, участвующими в синтезе белка и процессе считывания РНК. В состав рибосом входят детерминанты, общие с детерминантами поверхности клетки, что определяет высокую иммунологическую активность препарата. В Рибомуниле не присутствуют живые ослабленные микроорганизмы, что исключает возможность инфицирования и заболевания.
Показания к назначению Рибомунила – профилактика рецидивирующих инфекций ЛОР-органов. Препарат разрешен у детей с 2-х лет и у взрослых, доза не зависит от возраста. Применяется утром, натощак по 1 таблетке (0,75 мг) или 1 пакетику с гранулами (0,75 мг, предварительно развести кипяченой водой) в первый месяц – 4 дня/нед., 3 нед., последующие 2–5 мес. – по 4 дня/мес. На 2–3 день приема препарата может быть транзиторное повышение температуры тела, что не требует отмены препарата.
Противопоказания: индивидуальная гиперчувствительность, аутоиммунные заболевания, острая кишечная инфекция.
Механизм действия: протеогликаны K. pneumoniaе стимулируют фагоцитарную активность макрофагов и нейтрофильных лейкоцитов. Отмечается повышение функциональной активности Т- и В-лимфоцитов, продукции сывороточных Ig, включая секреторный IgA, интерлейкина (ИЛ) –1, ИФН-α и ИФН-γ.
Согласно данным фармаконадзора, зарегистрировано более 30 млн назначений препарата Рибомунил. Компания-производитель («Пьер Фабр», Франция) имеет партнеров в 60 странах мира, где препарат распространяется под разными названиями, но его состав остается идентичным. Во Франции препарат был зарегистрирован в виде спрея в 1976 г., таблеток – в 1984 г., гранул – в 1989 г.
С 1976 по 2005 г. было зафиксировано только 304 сообщения о побочных эффектах после применения препарата. С 2000 по 2006 г. были описаны побочные эффекты средней тяжести у 27 и тяжелые – у 7 пациентов (астения, мультиформная эритема, гипертермия, кожные высыпания, экзема, желудочно-кишечные расстройства). Показано, что препарат не должен назначаться при стрептококковом гломерулонефрите, тяжелых иммунодефицитах, аутоиммунных заболеваниях (ревматоидный артрит, аутоиммунный тиреоидит, системная красная волчанка, миастения), хроническом гепатите, инсулин-зависимом диабете, тяжелых вирусных инфекциях. Рибомунил может назначаться при аллергических заболеваниях, наблюдается снижение синтеза IgE. У беременных клинических исследований не проводили. Многочисленные исследования подтверждают высокий профиль безопасности Рибомунила [14].
По данным А.Л. Заплатникова и соавт., триггерными факторами обострения бронхиальной астмы (БА) у детей в 75% случаев являются ОРЗ. Комбинированная иммунопрофилактика с использованием противогриппозной вакцины и Рибомунила позволила в 68% случаев достичь контроля БА при применении более низких доз базисной терапии. В исследовании участвовали 128 детей 9–17 лет с БА легкой и средней степени тяжести. Дети вакцинированы против гриппа (вакцина агриппал) и получали Рибомунил по стандартной схеме в течение 6 мес.
Не отмечалось обострения БА по сравнению с контрольной группой детей с БА, вакцинированных только противогриппозной вакциной, и группой детей с БА без вакцинации. Защитные титры АТ к вирусу гриппа сохранялись в течение всего эпидемиологического периода. Заболеваемость гриппом и ОРЗ у детей с БА (агриппал + Рибомунил) снизилась на 20%, но разница не была статистически достоверной. Достоверно сократилась длительность ОРЗ (с 9,54±0,63 до 7,46±0,62 дня), уменьшилась тяжесть эпизодов. Достоверно снизилась частота обострений БА – на 61,2% [13].
60 детей в возрасте 6–14 лет с рецидивирующими аденоидитами (не менее 4 эпизодов за 6 мес.) наблюдались c сентября 2006 г. по декабрь 2007 г. и были рандомизированно разделены на 2 группы. 30 детей 7–14 лет получали Рибомунил, 30 детей 6–13 лет не получали Рибомунил. Эффективность лечения оценивали по количеству эпизодов аденоидита, необходимости назначения антибиотиков, результатам тимпанометрии, иммунологического обследования (уровень сывороточных IgG, IgM, IgE, IgA). По окончании наблюдения уровень IgE был достоверно ниже в группе, получавшей Рибомунил, уровни сывороточных IgG и IgA были достоверно выше (р<0,05), результаты были положительными в течение 6 мес. наблюдения. Динамика сывороточного IgM не была достоверной. Улучшались показатели тимпанометрии и передней риноманометрии. За период наблюдения эпизоды обострения аденоидита наблюдали у 2 из 30 детей, получавших Рибомунил, и у 18 из 30 детей, его не получавших (разница статистически достоверна).
При формировании микроорганизмами биопленок на слизистых проникновение под них антибиотиков затруднено, что способствует созданию очагов резистентной инфекции. Бактериальная флора при аденоидитах включает H. influenzaе, М. catharralis, S. pneumoniaе, Staph. aureus, K. pneumoniaе. В лимфоидной ткани аденоидов могут синтезироваться все классы Ig, что чаще наблюдается в возрасте 4–10 лет. При аденоидитах формируется воспаление, происходит экспрессия молекул адгезии ICAM, которые могут быть рецепторами для риновирусов, что облегчает инфицирование. Рибомунил повышает синтез ИЛ-12, который активирует Th1-тип иммунного ответа, наивные CD4+-клетки, синтез трансформирующего ростового фактора-β, под действием которого происходит переключение синтеза с IgM на IgA [15].
При среднем отите S. pneumoniaе при посеве выделений из уха высевается в 60–70% случаев. Этиологическое значение S. pneumoniaе при внебольничной пневмонии колеблется от 35 до 76%. У детей отмечается высокая восприимчивость к данному возбудителю, а способность вырабатывать полноценные АТ к полисахаридам S. pneumoniaе у ребенка формируется к 5-летнему возрасту [16].
С 1985 по 1999 г. в Германии, Франции, России в 19 двойных слепых плацебо-контролируемых исследованиях с участием 14 тыс. пациентов (взрослых и детей) была продемонстрирована эффективность Рибомунила при рецидивирующих бронхолегочных заболеваниях [17]. У детей с аденоидитами, получавших Рибомунил, отмечены более низкий уровень IgE и более высокий уровень IgA, чем в контрольной группе [15]. При респираторных инфекциях среди детей младше 5 лет, получавших Рибомунил, эпизоды ОРЗ не наблюдали у 20,4%, а в группе, получавшей плацебо, – у 4,4% детей [18]. У детей с БА при назначении Рибомунила не отмечалось повышения уровня IgE, снижались частота приступов затрудненного дыхания и гиперреактивность бронхов [19]. У детей с БА наблюдали положительный эффект Рибомунила через 3 и 6 мес. Отмечено повышение уровня ИЛ-2, ИФН-γ, снижение уровней фактора некроза опухоли-α, ИЛ-4, лейкотриена В4, CD4+-, CD25+-, CD23+-клеток, повышение содержания CD3+-, CD8+-клеток [20].
В исследованиях 2010–2011 гг. Рибомунил получали 55 детей с обструктивным бронхитом, 44 – с БА, 32 – с повторными отитами. ОРЗ не были зарегистрированы у 17, 18,3 и 22% детей соответственно. У остальных детей отмечали снижение частоты ОРЗ на 30%. У 5 детей отметили повышение температуры тела до 38°С во время приема препарата [17].
В исследованиях у детей и взрослых показан высокий профиль безопасности Рибомунила при респираторных заболеваниях [14].
Профилактика и лечение вирусно-бактериальных ОРЗ – актуальная проблема современной медицины. Вакцинация против пневмококковой инфекции, бактериальные лизаты по праву занимают достойное место в лечении и профилактике респираторных инфекций.

Литература
- Зайцев А.А., Синопальников А.И. Грипп: диагностика и лечение // РМЖ. 2008. Т. 16. № 22. С. 1494–1502.
- Таточенко В.К., Озерецковский Н.А., Федоров А.М. Иммунопрофилактика – 2014. М.: ПедиатрЪ, 2014. 199 с.
- Маркова Т.П. Применение изопринозина для профилактики повторных респираторных инфекций у часто болеющих детей // Фарматека. 2009. № 6. С. 46–50.
- Хлынина Ю.О. Часто болеющие дети: микроэкологическое обоснование подходов к лечению и реабилитации: Автореф. дисс. … канд. мед. наук. Волгоград, 2012. 25 с.
- Хлынина Ю.О. Резидентное стафилококковое бактерионосительство в популяции человека, живущего в крупных промышленных городах // Вестник новых медицинских технологий. 2009. № 1. С. 43–45.
- Альбицкий В.Ю., Баранов А.А. Часто болеющие дети. Клинико-социальные аспекты, пути оздоровления. Саратов: Медицина, 1986.
- Mellioli J. Deciders in pulmonology (Принятие решений в пульмонологии) // Giorn. It. Mal. tor. 2002. Vol. 56 (4). Р. 245–268.
- Маркова Т. П., Чувиров Д. Г., Гаращенко Т.И. Механизм действия и эффективность бронхо-мунала в группе длительно и часто болеющих детей // Иммунология. 1999. № 6. С. 49–52.
- Maul J. Stimulation of immunoprotective mechanisms by OM-85 BV // Respiration. 1994. Vol. 61 (Suppl. 1). Р. 15.
- Del-Rio Navarro B.E., Espinosa-Rosales F.J., Flenady V., Sienra-Monge J.J.L. Immunostimulants for preventing respiratory tract infection in children (Review) // The Cochrane Collaboration. The Cochrane Library. 2011. Issue 6.
- Evans S.E., Tuvin M.J., Dickey B.F. Induciblе innate resistance of lung epithelium to infection // Ann. Rev. Physiol. 2010. Vol. 72. P. 413–435.
- Levy O. Innate immunity of the newborn: basic mechanisms and clinical correlates // Nat. Rev. Immunol. 2007. Vol. 7. P. 379–390.
- Заплатников А.Л., Гирина А.А., Бурцева Е.И. и соавт. Иммунопрофилактика гриппа и других острых респираторных вирусных инфекций в достижении контроля над течением бронхиальной астмы у детей // Педиатрия. 2013. Т. 92. № 1. С. 51–56.
- Olivieri D., Fiocchi A., Pregliasco F. et al. Safety and tolerability of ribosome-component immune modulator in adults and children // Allergy Asthma Proc. 2009. Vol. 30. Р. 33–36. doi: 10.2500/aap.2009.30.3247.
15. Mora R., Dellepiane M., Crippa B. et al. Ribosomal therapy in the treatment acute adenoiditis // Eur.Arch.Otorhinolaryngol. 2010. Vol. 267. P. 1313–1318. - Akikusa J.D., Kemps A.S. Clinical correlates of response to pneumococcal immunization // J.Paediatr. Child Health. 2001. Vol. 37 (4). Р. 382.
- Геппе Н.А. Рибосомальный комплекс в профилактике частых респираторных заболеваний у детей // Фарматека. 2013. № 1. С. 65–70.
- Fiocchi A., Omboni S., Mora R. et al. Efficacy and safety of ribosome-component immune modulator for preventing of recurrent respiratory infections in socialized children // Allergy Asthma Proc. 2012. Vol. 33 (2). P. 197–204.
- Сорока Н.Д. Особенности иммунотерапии затяжных и рецидивирующих болезней у детей // Педиатр. фармакология. 2008. Т. 5. № 5. С. 38–41.
- Алексеева А.А., Намазова-Баранова Л.С., Торшхоева Р.М. Рибосомальный комплекс в профилактике и лечении острых респираторных инфекций у детей // Вопр. совр. педиатрии. 2010. Т. 9. № 6. С. 127–130.






Комментировать