Л.А. Матыцина, М.Ю. Сергиенко, В.Ю. Яцеико
Воспалительные заболевания половой сферы являются одними из доминирующих в структуре гинекологической патологии девочек, влияют на состояние здоровья будущей женщины, ее детородную функцию. На фоне снижения социально-экономического уровня жизни населения, увеличения общей и гинекологической заболеваемости у девочек, снижения рождаемости, ухудшения демографической ситуации проблема воспалительных заболеваний половых органов, особенно вызванных УГИ, приобретает особую значимость. Актуальность проблемы обусловлена высокой частотой патологии, склонностью к хронизации патологического процесса, что ведет к серьезным нарушениям репродуктивного здоровья.
Наиболее часто детские гинекологи сталкиваются с воспалением наружных половых органов — вульвовагинитом. Вульвовагинит составляет от 56,2 до 84,8% гинекологической патологии, выявляемой у девочек во время профилактических медицинских осмотров. Пик заболевания приходится на возраст 3-8 лет, что обусловлено многими предрасполагающими факторами.
В нейтральном периоде развития девочки и в фазу раннего пубертата вследствие физиологической гипоэстрогении эпителий влагалища тонок, имеет 5-8 слоев, защитные механизмы слущивания и цитолиза поверхностных клеток отсутствуют. Клетки эпителия не ороговевают, не содержат гликогена, следовательно, во влагалище девочки нет условий для развития палочки Додерлейна, среда влагалища щелочная. Основной механизм защиты — фагоцитоз полиморфно-ядерными лейкоцитами. В то же время автономные механизмы защиты (секреторный иммуноглобулин А, лизоцим, которые продуцируются эндоцервиксом шейки матки, система фагоцитоза у девочек) в этом периоде находятся в стадии становления, их защитная роль минимальная (И.Б. Вовк, 2004).
Для детского возраста характерно несовершенство общего иммунитета. Любое снижение реактивности организма, которое чаще всего возникает после какого-нибудь острого или хронического заболевания, приводит к нарушению равновесия микрофлоры влагалища, развитию воспалительного процесса. В таких условиях условно-патогенная микрофлора может приобретать патогенные свойства.
Развитию вульвовагинитов могут способствовать также эндогенные факторы: анемия, сахарный диабет, экссудативный диатез, инфекции мочевыводящих путей, энтеробиоз. Важную роль в развитии воспалительного процесса играет нарушение микрофлоры кишечника.
Вульвовагинит всегда сочетается с воспалительными заболеваниями слизистых оболочек других органов и систем, особенно респираторного, желудочно-кишечного тракта, мочевыделительной системы. Развитию и поддержанию воспалительного процесса способствуют некоторые индивидуальные анатомические особенности: отсутствие задней спайки, низкое расположение уретры, синехии малых половых губ, аномалии наружных гениталий.
Важную роль в развитии вульвовагинита играют нарушения гигиены, термические (перегревание, переохлаждение), химические (ношение синтетического белья, средства для подмывания), механические (мастурбация) факторы.
Остановимся подробнее на характеристике микрофлоры влагалища в разные периоды полового развития.
Микробный пейзаж организма человека условно делится на две группы:
- постоянно живущие полезные агенты;
- постоянно живущие потенциально опасные или условно-патогенные микроорганизмы, при снижении иммунологической резистентности организма они становятся патогенными (Ю.А. Гуркин, 1999).
Микрофлора половых органов девочек по видовому составу соответствует тому же делению, но с одним существенным различием — постоянная вегетация лактофлоры в половом канале отсутствует. Это обусловлено низкой эндокринной функцией яичников. В период «полового покоя», в среднем до 10 лет, реакция влагалищной среды щелочная или нейтральная. Слизистая преддверия и стенок влагалища розового цвета, нежная, без макроскопически видимого секрета. В мазках определяются эпителиальные клетки в скудном количестве, мало лейкоцитов, флора кокковая в минимальном или умеренном количестве. Лактобациллы в описываемом периоде отсутствуют.
В препубертатном периоде, с повышением секреции половых гормонов, влагалище заселяется лактобактериями, количество которых значительно увеличивается в пубертатном периоде. Реакция влагалищной среды становится кислой, усиливаются физиологические пубертатные бели.
В состав лактофлоры влагалища входит 11 штаммов лактобацилл, которые составляют грамположительную палочковую флору полового канала. Доминирующим штаммом (42,9%) являются палочки Додерлейна. Роль лактофлоры многогранна. Она обеспечивает колонизационную резистентность полового канала и проявляет ферментативную функцию, обусловливающую кислую среду влагалища, пагубно действующую на патогенную флору. Часть лактобацилл является индукторами местного иммунитета.
Кокковая флора, вегетирующая в половом канале девочек, относится к условно-патогенной флоре, вместе с тем часть штаммов кокков входит в состав нормальной микрофлоры кожи, слизистых оболочек дыхательных путей, пищеварительного тракта и половых органов. Из рода стафилококков в половом канале чаще всего вегетируют золотистый стафилококк, эпидермальный стафилококк и микрококк (сапрофитный стафилококк). Из рода стрептококков: зеленящий, гемолитический стрептококк, энтерококк (фекальный стрептококк), пневмококк (стрептококк пневмонии), имеющий форму диплококка. Экологическая ниша пептострептококков (анаэробные кокки) — ротовая полость, кишечник, половые органы. Биологическая особенность кокков в том, что молодые кокки интенсивно окрашиваются по Граму, а при старении они становятся грамотрицательными.
Условно-патогенная палочковая флора также вегетирует в половом канале. Она представлена дифтероидами, грамположительными палочками (род Corynebacterium). Некоторые виды дифтероидов являются представителями нормальной флоры дыхательный путей, слизистых оболочек кожи, половых путей.
Enterobactriaceae — грамотрицательные палочки: кишечная палочка, протей, энтеробактер (синегнойная палочка), клебсиелла. Они составляют значительную часть нормальной флоры кишечника, участвуют в обеспечении его нормального функционирования. Проникая за пределы своей экологической ниши, они становятся патогенной флорой.
Гарднереллы- (представители рода Gardnerella, вида Gardnerella vaginalis) — мелкие грамотрицательные палочки (могут быть в форме коккобацилл), являющиеся факультативными анаэробами. Гарднереллы обнаруживают у практически здоровых женщин с частотой от 47 до 68% , а также у девочек в возрасте от 2-х месяцев до 15 лет, не имеющих каких-либо клинических проявлений вульвовагинита. В силу подобного феномена гарднереллы рассматривают как комменсалы (сожители) полового канала. Вопрос о патогенності! гарднерелл до настоящего времени остается открытым.
Leptotrix — грамвариабельные палочки, могут иметь форму коккобацил, являются факультативными анаэробами и вегетируют в половых путях человека. В природе являются постоянными обитателями медленно текущих вод, загрязненных стоками бумажной или молочной промышленности.
Acinetobacter — аэробные, грамотрицательные толстые короткие палочки, имеют форму диплококков, сходны в мазках с гонококками и менингококками. Среда их обитания в организме человека — кожа, слизистые оболочки, дыхательные пути, мочеполовые пути. При иммунодефицитах у детей в ассоциации с другими микроорганизмами могут вызвать сепсис.
Представление о биоценозе влагалища позволяет более точно понять основные механизмы возникновения воспалительных процессов гениталий девочек и девочек-подростков (табл. 17.1). Для изучения микроэкологии влагалища желательна комплексная оценка результатов культуральной диагностики и микроскопии мазков вагинального отделяемого. С этой целью мы предлагаем классификацию, в которой выделяются три типа влагалищного мазка: нормоциноз (I тип), промежуточный (II тип), выраженный вульвовагинит (III тип).
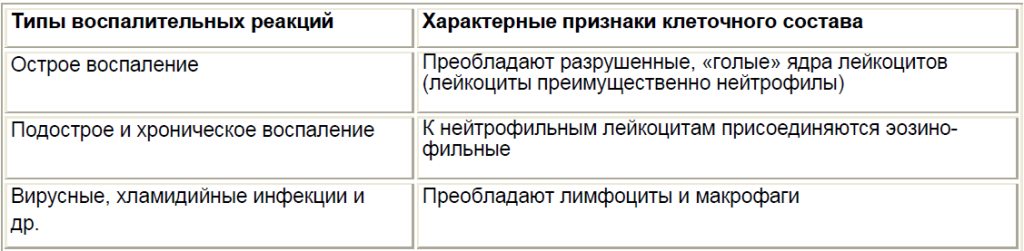
Воспаление проявляется экссудативными, дегенеративными, репаративными, защитными изменениями клеточного состава (табл. 17.2).
Таким образом, при изучении вагинального микроценоза у девочек и девочек-подростков диагностика должна быть клинико-микробиологической, а среди лабораторных методов приоритет должен быть отдан цитологической диагностике.
Наиболее распространенным воспалительным заболеванием гениталий в детском возрасте является неспецифический вульвовагинит. В качестве инфекционных причинных факторов выявляются: стафилококки — эпидермальный, сапрофитный, золотистый; стрептококки — пиогенный, энтерококк, зеленящий; протей — вульгарный, мирабилис; кишечная палочка; клебсиелла;. синегнойная палочка; микрококки.
Диагноз вульвовагинита ставится на основании анамнеза, осмотра наружных половых органов, вагиноскопии, микроскопического и бактериологического исследования отделяемого влагалища. В анамнезе необходимо обратить внимание на начало и течение данного заболевания, связь с патологическими состояниями других органов и систем, возможное наличие глистной инвазии.
Лечение вульвовагинита всегда комплексное. Основа терапии — устранение этиологического фактора: при первично не инфекционных вульвовагинитах — инородного тела, глистной инвазии, повышение реактивности организма и т. д.; в случае инфекционных вульвовагинитов — местная или общая антимикробная терапия.
Особо необходимо остановиться на специфических вульвовагинитах у детей, вызванных инфекциями, передающимися половым путем.
Урогенитальные воспалительные заболевания на современном этапе во многих случаях утратили специфичность клинических особенностей, как утратил свою значимость постулат Р. Коха: «Один микроб — одна болезнь».
Пути передачи специфической урогенитальной инфекции различны. В подростковом возрасте, среди девушек, имеющих опыт половой жизни, возможен половой путь заражения. В более ранние возрастные периоды доминирует бытовой способ передачи инфекции (предметы обихода, места общего пользования, нарушение правил гигиены).
В России и в Украине за последние 10 лет количество больных заболеваниями, передающимися половым путем (ЗПШТ), увеличилось в 10 раз. Среди молодых людей в возрасте до 19 лет заболеваемость возросла более чем в 35 раз (И.И. Гребешева, 1997). По данным ВОЗ, но уровню заболеваемости ЗППП на первом месте — группа 20-24-летних, на втором — лица в возрасте 15-19 лет.
Анализ структуры гинекологической заболеваемости у девочек Донецкого региона показал неуклонный рост гинекологической патологии за последние годы. В настоящее время ее выявляют у каждой третьей девочки-подростка.

Примечание. * — дегенеративно и реактивно измененные клетки.
Таблица 17.2.
Тенденция к росту гинекологической заболеваемости, в том числе УГИ, отмечается повсеместно,
В структуре гинекологической заболеваемости среди девочек и девочек-подростков воспалительные заболевания наружных и внутренних гениталий занимают первое место (50,5%). На фоне тотальной бесконтрольной антибиотикотерапии они зачастую имеют стертую клиническую картину и рецидивирующее течение. Заметное место в этиологии воспаления стали занимать хламидии, микоплазмы, уреаплазмы, гарднереллы, вирусы.
Анализ структуры гинекологической патологии девочек и девочек-подростков, находившихся на лечении в отделении детской подростковой гинекологии ДРЦОМД, показал, что за период с 1999 по 2003 год в отделении пролечено 4610 пациенток, из них с воспалительными заболеваниями гениталий (ВЗГ) — 2082 (45%). Удельный вес этой патологии имеет устойчивую тенденцию к росту, за последние 10 лет зарегистрировано ее увеличение более чем в 2 раза (табл. 17.3),
Самым распространенным ЗППП в настоящее время является хламидиоз. И тут мы сразу сталкиваемся с противоречием: в главе, посвященной детям, говорим о половом пути передачи инфекции. Возможно, поэтому длительное время опровергалось существование «детского хламидиоза». Однако в печати одно за другим стали появляться сообщения о том, что у девочек с хроническим вульвовагинитом при использовании высокочувствительной и специфической ПЦР во влагалище и цервикальном канале обнаружены инфекционные агенты, вызывающие ЗППП. По данным О.В. Ромащенко (1998), мочеполовой хламидиоз выявляют у 32,7% девочек в возрасте от 13 до 18 лет.
Таблица 17.3.
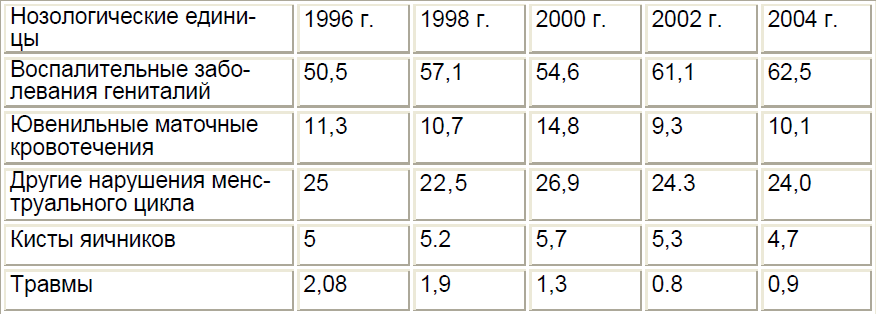
В структуре гинекологической заболеваемости девочек, находившихся на лечении в отделении детской подростковой гинекологии ДРЦОМД с 1999 по 2003 год, удельный вес воспалительных заболеваний гениталий хламидийной этиологии составил 14,5% (301 случай). В 51% случаев хламидиоз встречался как моноинфекция, в остальных — выявлены микробные ассоциации. Смешанная инфекция была обусловлена сочетанием: хламидки + уреаплазма; хламидии + гарднереллы; хламидии + кишечная палочка; хламидии + стафилококк; хламидии + гарднереллы + уреаплазма; хламидии + гарднереллы + кандида; хламидии + гарднерелла + стафилококк. Наличие микробных ассоциаций способствует не только лучшей адаптации хламидии к внутриклеточному паразитированию, но и усиливает патогенные свойства каждого из сочленов этой ассоциации, что приводит к усилению сопротивляемости микроорганизмов к внешним вредным воздействиям, в том числе к антибиотикам.
В наших наблюдениях частота возникновения хламидийной инфекции увеличивалась с возрастом пациенток и чаще диагностировалась у девочек старше 13 лет. В процентном соотношении выявляемость урогенитального хламидиоза распределялась следующим образом: от 13 до 15 лет — наиболее часто (в 70%), а в возрасте менее 13 и старше 15 лет — значительно реже (11% и 18% соответственно). Пик заболеваемости приходился на возраст 15 лет.
Хламидийная инфекция приводила к различным осложнениям со стороны внутренних гениталий. В наших наблюдениях в 83% случаев хламидиоз носил осложненный характер: хронические заболевания внутренних гениталий, ретенционные кисты яичников, нарушения менструального цикла, в том числе пубертатные маточные кровотечения.
Хламидии — это облигатные внутриклеточные паразиты с уникальным циклом развития. Основой цикла развития хламидии является закономерная смена вегетативных репродуцирующих неинфекционных клеток (ретикулярных телец — РТ) спороподобными инфекционными клетками (элементарными тельцами — ЭТ). Промежуточные формы, выделяемые в цикле развития, определяются как промежуточные тельца (ПТ), они образуются на двух стадиях цикла развития хламидии: на ранней, при преобразовании ЭТ в РТ, и на поздней, при реорганизации РТ в ЭТ.
Антибиотики практически не действуют на инфекционные ЭТ, в то время как РТ высокочувствительны к ним. При неблагоприятных условиях на этапе функционирования РТ могут образоваться так называемые L-формы. Такая трансформация возникает при использовании малых доз и непродолжительных курсов антибактериальных препаратов с антихламидийной активностью, инертных в отношении к хламидиям антибиотиков (пенициллина) и сульфаниламидов, при дисбактериозе кишечника и снижении иммунитета. Это может явиться основой персистенции хламидийной инфекции. Все изложенное необходимо учитывать при диагностике и лечении урогенитального хламидиоза.
Среди нескольких видов хламидий в основном Ch1. trachomatis вызывает развитие урогенитальной патологии. Существуют следующие пути заражения урогенитальным хламидиозом: трансплацентарный, контактный и половой.
Инфицирование новорожденных зависит от длительности безводного периода и способа родоразрешения, при аспирации околоплодных вод и длительном контакте слизистых оболочек с инфицированной средой. Инфицирование хламидиями может происходить антенатально и во время родов и зависит от локализации и выраженности хламидийного воспалительного процесса у женщины. При его локализации в области шейки матки заражение плода происходит интранатально, а при поражении труб, эндометрия, децидуальной оболочки — антенатально в результате аспирации или попадания возбудителя на слизистые оболочки, в том числе вульвы, уретры.
Примерно у 50-75% детей, рожденных от инфицированных матерей, развивается поражение одного или нескольких органов. Как правило, развитие хламидиоза у новорожденных во влагалище и прямой кишке протекает бессимптомно, у 15% детей, рожденных от инфицированных матерей, обнаруживают субклинически протекающую инфекцию. Мы часто сталкиваемся с тем, что на консультацию к детскому гинекологу направляют девочек в возрасте до 3-4-х лет, получавших или получающих лечение по поводу инфекции мочевыводящих путей. Иногда к моменту обращения они уже прошли не один курс антибиотикотерапии, в том числе препаратами пенициллинового ряда, которые способствуют образованию L-форм хламидий. У таких пациенток не всегда имеется клиническая картина вульвовагинита, но при сборе анамнеза можно найти подтверждение наличия хронического воспалительного процесса влагалища и вульвы (периодическую гиперемию, высыпания, дискомфорт при мочеиспускании, выделения на белье; при этом мамы лечили детей самостоятельно, не обращаясь к гинекологу). Помня о том, что хламидии поражают урогенитальный тракт, рекомендуем пройти обследование. У каждой 4-5-й девочки подтверждается наличие хламидийной инфекции.
Вторым путем заражения хламидиозом является бытовой (при использовании общих предметов туалета, постели и т. п). При обследовании родителей девочек с урогенитальным хламидиозом в 75% инфекция обнаруживается у отцов и в 90% — у матерей (Э.Б. Яковлева, 1995). Около 30-35% детей в семьях, где родители больны урогенитальным хламидиозом, переносят хламидийную инфекцию. В настоящее время введен термин «семейный хламидиоз», поскольку обследование семьи позволяет выявить инфицирование не только детей и их родителей, но и родственников двух-трех поколений.
Инфицированность хламидиями увеличивается с возрастом ребенка, что может быть связано с расширением бытовых контактов, а также нейроэндокринной перестройкой у подростков. В нашей практике были случаи обращения девочек младшего школьного возраста с энурезом. Все они неоднократно получали лечение у разных специалистов без особого эффекта. После обследования было установлено, что причиной энуреза являлся хламидиоз.
Третьей группой риска в отношении хламидийной инфекции являются сексуально активные подростки. Этому способствуют изменения в сексуальном поведении, наблюдаемые в последнее время: ранний половой дебют, частая смена половых партнеров, незнание и пренебрежительное отношение к барьерным средствам контрацепции и т.д. Если у virgo хламидиоз констатирован в 12% от общего количества вульвовагинитов (Л.А. Матыцина, 1996), то с началом половой жизни этот показатель возрастает до 33% (О.В. Ромащенко, 1998), т. е. увеличивается почти в 3 раза. Дебют заболевания у сексуально-активных подростков связан, как правило, с началом половой жизни, сменой полового партнера. Удельный вес хламидиоза среди девочек-подростков, страдающих воспалительными заболеваниями, достигает 80%. Причем 30-40% девочек-подростков переносят скрытую хламидийную инфекцию в течение 2-5 лет после заражения.
Исследования, проведенные в Англии, США, Канаде, Австрии, России, показали, что около 25-35% девушек имели сексуальные контакты до 16 лет, а в возрасте 16-19 лет — от 40 до 70%. При этом подросткам свойствены случайный характер половых связей, безграмотность в вопросах контрацепции, профилактики ЗППП. Около 80% девочек-подростков Украины одобряют половые отношения до брака, около 1/3 из них уже имели сексуальные контакты, не имея достаточного представления о способах предупреждения беременности и ЗППП.
Сотрудниками отделения «Молодежная клиника» ДРЦОМД совместно с городским центром «Здоровье» было проведено анкетирование 286 подростков в возрасте 14-18 лет, учащихся общеобразовательных школ, ПТУ, техникумов г. Донецка. В анкетировании приняли участие 78 (27,3%) юношей и 208 (71,7%) девушек. Целью программы было изучение уровня знаний подростков г. Донецк, связанных с вопросами сексуального здоровья.
3,1% респондентов считают, что половую жизнь следует начинать с 12-13 лет; 11,9% -с 14-15 лет; 49,7% — с 15-17 лет; 35% — старше 18 лет. Вместе с тем наличие опыта половой жизни признали 119 (41,6%) опрошенных (по данным профилактических осмотров эта цифра значительно ниже — до 20%).
Наши исследования показали, что 86% подростков знают о существовании гормональных контрацептивов, 92,3% — о презервативах, 62,9% — о ВМС, 19,2% — о химических средствах контрацепции. Большинство подростков (81,5%) признали, что в целях предохранения от беременности используют презерватив, КОК — 9,2%, вагинальные свечи — 0,8%, прерванный половой акт — 1,0%; 5,9% респондентов не применяют контрацепцию. 60,8% опрошенных утверждают, что используют презерватив в целях контрацепции постоянно, среди причин отказа от этого способа 64,9% ответили «не хочу», 10,8% — «не получаю удовольствия», 21,6% — не всегда есть в наличии, 2,7% — хочу иметь ребенка.
При незащищенном половом контакте инфицирование хламидиозом происходит в 30-40% случаев. Поскольку хламидии не входят в состав нормальной микрофлоры, их обнаружение всегда указывает на наличие инфекционного процесса, а отсутствие клинических симптомов заболевания свидетельствует о временном равновесии между паразитом и организмом человека в условиях, ограничивающих размножение патогенного микроорганизма, но не препятствующих ему. Хламидии выключают важнейший защитный механизм клетки хозяина — фагоцитоз, обеспечивая себе возможность дальнейшего размножения в цитоплазматическом включении клеток макроорганизма.
Патогенез и клинические проявления хламидийной инфекции определяются повреждением тканей в результате внутриклеточной репликации хламидии, а также воспалительной реакцией в ответ на Ch1. trachomatis и разрушенные в процессе ее размножения собственные клетки. В основе повреждающего действия могут быть иммунные реакции, которые возникают при хронической или персистирующей хламидийной инфекции.
Возможны как острая, так и хроническая формы заболевания, рецидивирование или носительство инфекции, причем в 80% случаев она протекает бессимптомно. При нарушении иммунологических функций заболевание может переходить в глубокие системные поражения многих органов и тканей, а также провоцировать аутоиммунные процессы.
Для «детского хламидиоза» характерно разнообразие клинических проявлений, стертая картина заболевания и осложненное течение.
Длительная персистенция хламидий в организме способствует переходу заболевания в преимущественно субклинические формы, имеющие незначительное количество клинических симптомов или их отсутствие. Затяжному и рецидивирующему течению воспалительного процесса способствует тот факт, что в окружении ребенка, как правило, имеются носители хламидиоза, что создает условия для реинфицирования, а формирующаяся у детей иммуносупрессия способствует развитию различных хронических заболеваний.
Клиническая картина
Выделяют хламидийное поражение нижнего отдела урогенитального тракта и восходящую инфекцию. К поражениям нижнего отдела урогенитального тракта следует относить хламидийный уретрит, парауретрит, бартолинит, цервицит. Цервициты наблюдаются как первичное и наиболее частое проявление хламидийной инфекции. При обследовании 125 девочек-подростков, проведенном в США (R. Morris et al., 1993), у 17 (13,6%) выявили С.Trachomatis: у 4 — только в уретре (24%.), у о — только в цервикальном канале (31%), у 8 — в обоих местах (45%).
Наличие клинических проявлений вульвовагинита хламидийной этиологии (гиперемия слизистой наружных гениталий, слизисто-гнойные выделения) наблюдаются у 31% девочек. Появление гнойных выделений свидетельствует о сочетанном поражении или присоединении вторичной инфекции.
Уретриты не имеют специфических проявлений, и больные редко предъявляют жалобы на болезненное мочеиспускание. В отдельных случаях может встречаться экссудативное воспаление протоков и бартолиниевых желез. Первичные хламидийные кольпиты встречаются редко, поскольку хламидий не способны размножаться в многослойном плоском эпителии. Вне клеток они высокочувствительны к кислой среде влагалища. Первичные кольпиты возможны только при патологическом изменении гормонального фона у пожилых женщин, беременных и девочек.
Получить более полную информацию о клинической картине хламидиоза у девочек возможно при проведении вагиноскопии.
Вагиноскопия — это эндоскопический метод диагностики заболеваний нижних отделов половых путей с помощью специального прибора — вагиноскопа. При проведении вагиноскопии оцениваются состояние слизистой оболочки влагалища (цвет, складчатость, наличие разрастаний или дефектов слизистой), растяжимость, длина влагалища, состояние сводов, характер выделений (молочные, творожистые, крошковидные, пенистые, слизистые, кровянистые); состояние шейки матки (гипоплазия, гипертрофия, гиперемия слизистой оболочки); наличие цервицита, эктопий эпителия, псевдоэрозий; состояние наружного зева шейки матки (щелевидный, точечный, наличие полипов цервикального канала, отделяемого из зева).
О высокой информативности вагиноскопии свидетельствует тот факт, что воспалительные изменения влагалища и шейки матки выявлены у 651 (74,6%) из 873 пациенток, которые находились на лечении в отделении детской и подростковой гинекологии с различными диагнозами, такими как задержка полового созревания, первичная и вторичная аменорея, хронический сальпингоофорит, и предъявляли жалобы на периодические выделения из половых путей. У 280 девочек при проведении вагиноскопии произведен забор материала (соскоб эпителия из цервикального канала) для определения урогенитальной инфекции.
С биологической точки зрения шейка матки у физически зрелой женщины создает механизм, предупреждающий восходящую инфекцию и последующие заболевания тазовых органов. У подростков риск таких осложнений высок, поскольку цервикальная слизь и гуморальный иммунитет до появления овуляции отсутствуют. Таким образом, выявление воспалительных изменений шейки матки у девочек является показанием для обследования на УГИ, в первую очередь — хламидиоз, что способствует своевременному назначению адекватной терапии, профилактике развития патологического процесса внутренних гениталий.
Инкубационный период заболевания составляет 7-30 дней. Клинические симптомы генитального хламидиоза в основном не отличаются от клиники неспецифического вульвовагинита. В наших наблюдениях пациентки обращались с жалобами на выделения из половых путей длительностью свыше 6 месяцев и неэффективность проводимой терапии по поводу неспецифического вульвовагинита.
Генитальный хламидиоз у девочек, по-видимому, может длительные сроки протекать стерто или бессимптомно, активизируясь под влиянием различных неблагоприятных факторов и других патогенных агентов.
Восходящая хламидийная инфекция развивается следующими путями:
- каналикулярно — через цервикальный канал, полость матки, маточные трубы на брюшину и органы брюшной полости;
- лимфогенно — по лимфатическим капиллярам;
- гематогенно, вызывая экстрагенитальные поражения (глотка, суставные сумки);
- при половом контакте посредством сперматозоидов;
- при использовании внутриматочных средств, медицинских манипуляциях, абортах.
При восходящей хламидийной инфекции поражаются слизистая оболочка матки, труб, яичники, околоматочные связки, брюшина. Хламидийный сальпингит и сальпингоофорит — наиболее частые проявления этой инфекции. Девочкам с хламидийной инфекцией часто ставят диагноз «неспецифического» воспаления. При отсутствии своевременной терапии заболевание принимает хронический характер. Длительно и вяло текущая инфекция приводит к непроходимости маточных труб, внематочной беременности, трубно-перитонеальному бесплодию, спаечному процессу в малом тазу, невынашиванию беременности. Основная жалоба пациенток — непостоянные боли внизу живота без четкой локализации, усиление белей перед менструацией (неспецифическое проявление хронического воспалительного процесса). В таких ситуациях помогает использование дополнительных методов исследования — УЗИ внутренних гениталий. Наличие в эхокартине участка ограниченной жидкости позволяет предположить существование воспаления в маточной трубе, назначить обследование на хламидиоз.
Распознавание хламидиоза и других урогенитальных инфекций на основании жалоб, осмотра, результатов бактериоскопии затруднительно. Стертая клиническая картина, отсутствие симптомов, специфичных для этих инфекций, тяжесть осложнений при отсутствии адекватного лечения определяют важность диагностики ЗППП и правильной трактовки результатов обследования. Достаточно высокая его стоимость, возможность выполнения только в крупных специализированных лабораториях делают невозможным скрининговое обследование. Поэтому нам кажется важным выделение группы риска, нуждающейся в обследовании на ЗППП и в первую очередь — на хламидиоз. Это:
- девочки с хроническим вульвовагинитом и инфекцией мочевыводящих путей;
- девочки с хроническими, часто рецидивирующими воспалительными заболеваниями наружных и внутренних гениталий, которые не поддаются традиционной терапии;
- девочки с гинекологической патологией, у которых при УЗИ выявлены признаки воспалительного процесса в области маточных труб;
- сексуально активные подростки;
- девочки-подростки, у которых диагностирована эктопия шейки матки.
Диагностика основана на выявлении возбудителя и обнаружении хламидийных антител в сыворотке крови больного.
Одним из самых ответственных этапов диагностики хламидиоза является забор материала. У девочек дошкольного возраста для исследования используется первая порция утренней мочи в количестве 15 мл. У более старших пациенток взятие материала для исследования производится из уретры, парауретральных ходов (при их выраженности), слизистой преддверия влагалища, а в отдельных случаях — из цервикального канала при вагиноскопии.
Принципы иммунологической диагностики у детей не отличаются от таковых у взрослых. Следует особо отметить, что у новорожденных гораздо чаще обнаруживают IgG (материнские антитела), уровень которых, как правило, быстро снижается к 4-5-месячному возрасту, если ребенок не инфицировался.
Лечение
Лечение хламидийной инфекции у детей представляет значительную проблему, т. к. необходимо учитывать возрастные особенности, из-за которых сужается спектр используемых препаратов. Ни в коем случае нельзя превышать разовые и суточные дозы для достижения излеченности у детей. Больным урогенитальным хламидиозом назначают этиотропную, патогенетическую и симптоматическую терапию.
Принципы лечения основаны на двухфазном цикле развития хламидий, чувствительности к антибиотикам внутриклеточных форм и нечувствительности внеклеточных форм хламидий.
Основные принципы комплексной терапии сводятся к следующему:
- применение антибиотиков, обладающих высокой антихламидийной активностью и способностью проникать внутрь клетки, обеспечивая в ней бактерицидную концентрацию;
- курс лечения должен перекрывать не менее 3-х циклов развития хламидий (10-14 дней);
- использование препаратов, повышающих эффективность антибиотиков (индукторы интерферона, ферменты);
- восстановление системы перекисного окисления липидов и антиоксидантной защиты организма (ПОЛАОВ);
- снятие побочного действия антибиотиков (витамины Е, С, В, эубиотики, антимикотики).
Учитывая хламидиостатическую активность пенициллина, его полусинтетических аналогов и производных, а также цефалоспоринов, мы рекомендуем при любых проявлениях вульвовагинитов у девочек не применять пенициллин и его производные до получения результатов полного обследования.
К числу наиболее активных препаратов относятся макролиды/азалиды, тетрациклины, фторхинолоны, клиндамицин.
Из перечисленных групп антибиотиков рекомендуем определенные препараты с учетом возраста.
- Макролиды:
— рокситромицин (рулид) дважды в сутки 10-14 дней; дети весом: 10-24 кг — 100 мг/сут; 24-40 кг — 200 мг/сут; более 40 кг — по 150 мг 2 раза в сутки;
—спирамицин (ровамицин): дети — 1,5 млн/МЕ на 10 кг массы тела в сутки, 2-3 р/день, 10-14 дней ;
— эрик (эритромицин в виде микрокапсулированного основания) — 30-50 мг/кг в сутки в 3-4 приема, 10-14 дней;
— кларитромицин (клацид, клабакс) — 7,5 мг/кг в сутки 10-14 дней;
- Тетрациклины:
— доксициклин (вибрамицин, юнидокс, доксибене, тетрадокс): дети старше 8 лет — 2-4 мг/кг сутки; с массой тела более 50 кг — дозы как для взрослых, 10-14 дней.
- Азалиды (препараты, у которых макроциклическое лактонное кольцо (макролиды) расширено в результате введения азаметильной группы):
— азитромицин (сумамед) — назначают детям старше 12 месяцев: 1 день — 10 мг на кг в сутки, остальные дни — 5 мг на кг сутки.
По массе тела:
1 день со 2 дня
10-14 кг — 100 мг 50 мг
15-24 кг— 200 мг 100 мг
свыше 25 кг— 250 мг 125 мг
- Фторхинолоны (не назначаются детям в возрасте до 14-15 лет).
Эти препараты обладают широким спектром действия, что важно при лечении хламидиоза с микробными ассоциациями, а также способны в высоких концентрациях накапливаться в тканях половых органов и проникать внутрь клетки.
При наличии трихомонад за 3 дня до лечения этиотропными препаратами необходимо назначить метронидазол в возрастной дозировке курсом 5-7 дней.
Всем больным рекомендован пероральный и/или местный прием противогрибковых препаратов, эубиотиков.
Лечение хламидиоза без коррекции иммунных нарушений малоэффективно, поэтому терапию антибиотиками дополняют иммуномодулирующими препаратами интерферонового ряда (циклоферон), иммунотропным препаратом многоцелевого воздействия при внутриклеточных патогенах (протефлазид), иммуноглобулинами. Иммуноглобулин антихламидийный (ЗАО «Биофарма») назначается по схеме: по 1,5 мл (1 доза) в/м один раз на 1, 4, 7, 10, 13, 16, 19, 21-й день лечения.
Детям с 4-летнего возраста циклоферон назначают по 6-10 мг/кг массы тела в сутки внутримышечно один раз в день в 1, 2, 4, 6, 8, 11,14, 17,20, 23-й день. Этиотропную терапию антибиотиками начинали в день второй инъекции циклоферона.
Протефлазид применяется по стандартной схеме: первая неделя — по 5 капель; вторая, третья — 10 капель; четвертая — 8 капель три раза в день. Детям в возрасте 3-4-х лет назначается 1/4, 7-8 лет — 1/2 взрослой дозы; с 14 лет девочкам назначается полная доза препарата.
Немаловажную роль в лечении урогенитального хламидиоза играют протеолитические ферменты (трипсин, химотрипсин) и энзимы (вобэнзим), способствующие разжижению гнойных очагов и проникновению антибиотиков вглубь очага и клетки тканей. Энзимы оказывают мягкое иммуностимулирующее действие (стимулируют и регулируют уровень функциональной активности интерферонов, моноцитов-макрофагов — естественных киллерных клеток).
Детям не рекомендуется назначение пирогенала и продигиозана. Направленные на определенные звенья патогенетической цепи, они могут вызвать противоположные эффекты: восходящую инфекцию, угнетение клеточного иммунитета, гиперстимуляцию в-клеток и опухоленекротизирующего фактора, аллергические реакции и даже развитие септического шока.
Местное лечение проводится с целью ликвидации явлений вульвовагинита, повышения эффективности действия антибиотиков. Для санации влагалища мы используем раствор бетадина в разведении 1:10, 1%-ный спиртовой раствор хлорофиллипта (5 мл на 100 мл теплой воды). При отсутствии положительной динамики, наличии цервицита практикуем введение во влагалище мазей, содержащих антибиотик, обладающий антихламидийной активностью.
При наличии осложнений (сальпингиты, сальпингоофориты) традиционно назначаются нестероидные противовоспалительные препараты внутрь после еды или в ректальных свечах.
После окончания антибактериальной терапии по показаниям местно применяются препараты для восстановления нормального биоценоза влагалища.
Важной составной частью комплексной терапии воспалительных заболеваний мочеполовых органов, вызванных хламидиями, является физиотерапия (электрофорез, ультразвук, УВЧ, бальнеотерапия, лазеротерапия). Мы назначаем физиотерапию после окончания антибактериальной терапии, курсом на 10 дней. В период стойкой ремиссии воспалительного процесса проводим реабилитацию пациентов в санатории «Донбасс» (г. Славянск).
По нашим наблюдениям, именно такая тактика ведения больных с урогенитальным хламидиозом позволяет значительно повысить этиологическую излеченность и снизить риск возникновения бесплодия в дальнейшем. Наша задача — свести к минимуму количество курсов противохламидийной терапии.
Предложенная нами схема не является универсальной, так как для лечения хламидийной инфекции у детей, как и у взрослых, требуется индивидуальный подход со всеми «за» и «против».
Необходимо помнить, что мы лечим не болезнь, а пациента.
Критерии излеченности
После окончания курса антибактериальной терапии контрольное обследование проводится трижды:
- первое обследование — не ранее чем через 3-4 недели (за это время происходит элиминация возбудителя из клеток эпителия);
- второе обследование — через месяц после первого;
- третье обследование — через месяц после второго.
Наиболее информативными являются методы ПЦР и прямой иммунофлюоресценции (ПИФ). Однако трактовать их нужно с осторожностью. Положительные результаты свидетельствуют как о реинфекции, так и неэффективности лечения, или о том, что не произошла полная элиминация антигена, хотя метод лечения был достаточно эффективен.
При серодиагностике необходимо помнить, что снижение титра антител происходит в сроки до 4-12 месяцев после окончания этиологического излечения. Определение в этот срок даже низких титров антител указывает на латентное течение или реинфекцию.
Наиболее высокой информативностью обладает метод определения хламидий в культуре клеток (McCoy) в течение первых 2-х недель после окончания лечения. Он дает возможность обнаружить в организме пациента жизнеспособные формы хламидий.
Итак, здоровыми считаются те пациенты, у которых клиническая излеченность сочетается с этиологической.
Несколько реже, чем с хламидийной инфекцией, при воспалительных заболеваниях наружных и внутренних гениталий детские гинекологи встречаются с урогенитальным микоплазмозом. В наших исследованиях он был выявлен и пролечен в 230 (11%) случаях. Из них в 59% наблюдалась моноинфекция, в 41% случаев — микоплазмы в ассоциации с другими патогенными агентами. В 73,7% случаев инфекция носила осложненный характер: в 37% случаев был диагностирован аднексит; в 42,1% — гидросальпинкс; в 15,8% — ретенционные кисты яичников.
Урогенитальный микоплазмоз — условное наименование воспалительного процесса в мочеполовых органах в случае, когда при лабораторном обследовании выявлен один (или несколько) из возбудителей: M.hominis, M.genitalium, U. urealyticuni. Мочеполовой микоплазмоз — довольно распространенное заболевание. Его возбудители часто (60-80%) входят в состав смешанной инфекции при различных острых и хронических воспалительных заболеваниях органов малого таза, у больных с пиелонефритом, гломерулонефритом и циститом. Возбудитель заболевания широко распространен в природе, нередко обнаруживается у здоровых женщин. Адсорбируясь на мембране клеток, микробы длительное время могут вызывать латентное бессимптомное течение заболевания. Обострение часто возникает при присоединении другой инфекции.
Пути передачи микоплазмоза и хламидиоза идентичны. Инфекции передаются контактно-бытовым, в т. ч. половым путем, при этом последний наиболее распространен. Возможен и вертикальный путь передачи, который может осуществляться в результате восходящей инфекции из влагалища и цервикального канала. Внутриутробно плод инфицируется при наличии инфекции в околоплодных водах через пищеварительный тракт, кожу, глаза, урогенитальный тракт.
Инкубационный период составляет в среднем 2-3 недели, однако это имеет значение только при половом пути передачи инфекции. В своей практике мы очень редко встречаемся со свежими случаями микоплазмоза с бытовым и внутриутробным путем передачи. Чаще всего отмечаются латентные бессимптомные формы микоплазменной инфекции, которые могут обостряться при переохлаждении, стрессовых ситуациях, эндо- и экзогенных провоцирующих факторах, а кроме того, стать причиной воспалительных процессов мочеполовых органов.
Микоплазменная бессимптомная инфекция чаще протекает без субъективных ощущений и симптомов, с незначительной клиникой воспалительного процесса, имеет рецидивирующее течение, отличается большой частотой осложнений и устойчивостью к проводимой терапии.
Микоплазмы вызывают воспалительные процессы урогенитального тракта: вульвовагиниты, цервициты, сальпингиты,сальпингоофориты, эндометриты. Клиническая картина обычно не отличается от воспалительных процессов другой этиологии, этиологический фактор выявляется только при лабораторном обследовании.
Данное состояние расценивается как носительство — наличие микроорганизма в мочеполовой системе и отсутствие признаков патологического воспалительного процесса. Отсутствие жалоб со стороны обследуемого не является признаком носительства, о нем можно говорить только в том случае, когда при клиническом, лабораторном и инструментальном методах обследования не выявлено патологии со стороны мочеполовых органов. Поэтому при обнаружении генитальных микоплазм необходимо провести следующие исследования:
- осмотр преддверия влагалища, стенок влагалища и шейки матки;
- бимануальное исследование матки и придатков;
- микроскопическое исследование мазков из уретры, влагалища и цервикального канала;
- микроскопическое исследование осадка мочи (5-10 мл первой порции мочи) — рекомендовано для детей младшего возраста;
- ультразвуковое исследование матки и придатков.
Только отсутствие патологических изменений при вышеприведенных методах обследования позволит судить о наличии клинического здоровья у пациентки.
Носительство микоплазм надо расценивать как «состояние риска». В любой момент развитие инфекционного процесса может быть спровоцировано различными факторами: сопутствующей инфекцией, изменением гормонального фона в связи с фазой естественного цикла созревания яйцеклетки, состоянием беременности и другими нарушениями физиологического и иммунного статуса организма.
Клиническая картина урогенитального микоплазмоза у девочек периода полового покоя, препубертата и пубертата малоспецифична. Вульвовагинит микоплазменной природы встречается у девочек несколько чаще, чем это принято считать. Характерными симптомами для младшего возраста являются стойкая гиперемия слизистой преддверия влагалища и незначительные дизурические расстройства: частые позывы к мочеиспусканию, сопровождающиеся чувством жжения. Обычно пациентки направляются к детскому гинекологу по поводу недержания мочи после обследования мочевыделительной системы, которое не выявляет патологических изменений. В этом возрасте для лечения микоплазмоза используют макролиды. Трудности терапии заключаются в том, что маленькие пациентки зачастую уже получали препараты этого ряда короткими курсами и в меньшей дозировке, что способствовало формированию устойчивости микоплазм к антибиотикотерапии.
В поздней фазе препубертата и в пубертатном периоде превалируют жалобы на зуд, ощущение раздражения в области уретры и вестибулярного отдела вульвы при учащенном мочеиспускании. У некоторых пациенток эти симптомы вызывают мучительное состояние, нередко с появлением невротических расстройств. Инфекция проявляется скудными серозными или клейстерообразными белями (гнойные выделения не характерны), периодическим дискомфортом в области наружных половых органов. Объективно отмечается умеренно выраженная гиперемия, пастозность в области уретры и девственной плевы.
При вагиноскопии обнаруживают пастозность и диффузную гиперемию насыщенного розового цвета слизистых оболочек стенок влагалища; наличие эндоцервицита — относительно редкое явление. У девочек, в отличие от женщин, реже наблюдается бессимптомное течение заболевания. Вероятно, это обусловлено особенностями организма девочек в данные периоды развития.
Очень часто (до 75-80% случаев) отмечается совместное выявление уреаплазм, микоплазм и анаэробной микрофлоры (гарднерелла, мобилункус). Оптимальное значение рН для размножения микоплазм — 6,5-8. Во влагалище в норме рН составляет 3,8-4,4. Кислую реакцию поддерживает молочная кислота, образуемая лактобациллами из гликогена клеток слизистой генитального тракта: в норме 90-95% микроорганизмов составляют лактобациллы, на долю других приходится соответственно 5-10% (дифтероиды, стрептококки, стафилококки, кишечная палочка, гарднерелла). В результате различных неблагоприятных воздействий (применение антибиотиков, гормонотерапия, радиоактивное облучение, ухудшение условий жизни и развитие иммунодефицита), а также психических стрессов возникает состояние дисбиоза и возрастает количество условно-патогенной микрофлоры. G.vaginalis образует янтарную кислоту, которая используется другими условно-патогенными микроорганизмами. Их рост сопровождается изменением рН от 3,8-4,4 до 6,8-8,5. Таким образом, создаются благоприятные условия для колонизации генитального тракта микоплазмами, и происходит их активное размножение. В свою очередь уреаплазмы и микоплазмы активно используют для своей жизнедеятельности кислород, что ведет к усиленному размножению анаэробных бактерий.
Для обнаружения микоплазм используются методы ПЦР, ПИФ, ИФА. Предпочтение следует отдавать культуральному исследованию с выделением микоплазм в клиническом материале (предпочтительно с количественной оценкой).
Лечение
Принципы терапии урогенитального микоплазмоза те же, что и при хламидиозе: назначаются антибиотики, иммуномодулирующие препараты, энзимы, эубиотики, витамины, антимикотики. Микоплазмы чувствительны к тетрациклинам, макролидам и ряду других препаратов. Механизм действия тетрациклинов и макролидов связан с подавлением в микробной стенке синтеза белка. Отдельно на схемах антибиотикотерапии мы останавливаться не будем, они изложены в разделе, посвященном хламидиозу у детей.
Местная терапия включает спринцевание растворами бетадина, хлорофиллипта, применение эритромициновой или тетрациклиновой мази на область преддверия или непосредственно во влагалище.
Установление клинико-микробиологических критериев излеченности уреаплазменной инфекции проводится через 3-4 недели после окончания лечения (дальнейшие исследования по показаниям).
Обсуждая вопросы урогенитальных инфекций у девочек, нельзя не остановиться на проблеме вульвовагинального кандидоза (ВК). Поскольку клиническая картина хламидиоза и микоплазмоза не отличается особой специфичностью, зачастую именно рецидивирующий кандидоз является поводом для обследования пациенток на УГИ, при которых дрожжеподобные грибы могут встречаться в микробных ассоциациях.
Различают 3 варианта течения вагинального кандидоза:
- «бессимптомное носительство» — 13,7%;
- «истинный» вагинальный кандидоз — 68%;
- сочетание вагинального кандидоза и бактериального вагиноза— 18,3%.
На базе отделения детской и подростковой гинекологии ДРЦОМД проводилось исследование, целью которого явилось изучение структуры сомато-гинекологической патологии у девочек с вульвовагинальным кандидозом, разработка рекомендаций по ведению пациенток с ВК и оценка эффективности проводимой ан-тимикотической терапии. Под наблюдением находилось 122 пациентки в возрасте от 1 года до 17 лет с диагнозом вульвовагинальный кандидоз.
Распределение больных по возрастам было следующим: девочек — 38 (32,8%), девочек-подростков — 84 (67,2%). Это согласуется с данными Ю.А. Гуркина (2000), что кандидозный вульвовагинит у девочек периода полового покоя встречается редко, а частота развития ВК повышается, начиная с поздней фазы препубертата, и увеличивается в пубертатном и юношеском периодах.
У 90 пациенток диагноз вульвовагинального кандидоза сочетался с наличием НМЦ, патологией внутренних гениталий (хронический сальпингоофорит, ретенционные кисты яичников). В 92-х случаях кандидоз был диагностирован как моноинфекция, в 30 (27,5%) — в сочетании с другой патогенной микрофлорой: хламидиями — 10 (33,3%), гарднереллами — 15 (50%), микоплазмами — 5 (16,7%).
Анализ частоты заболеваний, связанных с нарушением баланса половых стероидных гормонов, показал довольно широкий спектр этих состояний у девочек-подростков с вульвовагинальным кандидозом (СПКЯ — 4,6% , воспалительные заболевания — 9,2%, олигоменорея — 4,5%). Существует взаимосвязь между нарушением баланса половых стероидных гормонов и развитием кандидозного вульвовагинита, поскольку половые гормоны играют основную роль в регуляции пролиферации и дифференциации эпителия влагалища, что говорит о необходимости более тщательного обследования этих больных, включая в план обследования исследование гормонального статуса.
Сопутствующая экстрагенитальная патология выявлена у 108 (81,8%) больных: заболевания органов дыхания — в 30 (27,5%) случаях, патология желудочно-кишечного тракта — 45 (41,3%), мочевыводящих путей — 10 (9,2%), железодефицитная анемия — 5 (4,6%). У 41-й (37,6%) пациентки наблюдались частые (до 5 раз в год) заболевания ОРВИ. Вульвовагинальный кандидоз чаще развивался на фоне заболеваний ЖКТ (41,3%), что еще раз подтверждает роль состояния микробиоценоза ЖКТ в патогенезе вульвовагинального кандидоза. Тот факт, что у 36,3% больных ВК развивался на спровоцированном частыми ОРВИ преморбидном фоне, свидетельствует о нарушении иммунного гомеостаза у этой группы больных, что подтверждается достаточно высокой цифрой среднего инфекционного индекса — 3 и говорит о необходимости своевременного проведения иммунологической диагностики с последующей коррекцией.
Все обследованные предъявляли жалобы на обильные творожисто-белые выделения из половых путей, зуд в области наружных гениталий отмечался лишь у 41 (36,3%) больной.
Пациенткам проводились бактериоскопическое и бактериологическое исследования. В 30 (27,5%) случаях в анализе выделений отмечалось наличие лейкоцитов более 10 в поле зрения, грибы рода Candida были представлены дрожжевыми клетками, псевдомицелием, а доминирующей флорой были Lactobacilus, что в совокупности с клинической картиной и жалобами, а также результатами культурального исследования (высевались грибы рода Candida 1 х 106-1 х 107/ мл), соответствовало острому генитальному кандидозу. В 81-м (74,3%) случае в анализе выделений лейкоциты составляли 1/2 или все поле зрения, флора — смешанная, грибы рода Candida были представлены вегетирующими формами, в результатах культурального исследования — грибы рода Candida 1 х 107/мл и более, что в совокупности с клиническими показателями и данными анамнеза (рецидивы) соответствовало хроническому (рецидивирующему) вульвовагинальному кандидозу. У 72,7% больных наблюдалось хроническое (рецидивирующее) течение заболевания, что указывает на склонность ВК к рецидивам.
В ходе культурального исследования в 100% случаев выделены грибы рода Candida albicans. Необходимо различать несколько вариантов миконосительства: мобильное, т. е. неуклонно нарастающее (или убывающее); стабильное, т. е. сохраняющееся на одном уровне с незначительными колебаниями (монотонная форма) или с выраженными размахами (ундулирующая форма), с увеличением количества грибков в выделениях из влагалища за 5-7 дней до очередной менструации и уменьшением по ее окончании. Таким образом, обнаружение гриба в исследуемом материале не всегда имеет абсолютное значение. Необходима оценка по количественным и качественным показателям (степень обсемененности, морфологические и биохимические признаки). Идентификация полученных культур дрожжеподобных грибов должна основываться на изучении морфологических признаков бактериальных клеток и внешнего вида выросших колоний. Учитывая то, что оптимальный рН для роста гриба равен 5,8-6,5, необходимо обязательно определение рН влагалища.
Лечение вульвовагинального кандидоза проводилось по общепринятой схеме. Использовались витаминотерапия, десенсибилизирующая терапия, осуществлялась коррекция неспецифического иммунитета, в т. ч. адаптогенами, назначались препараты для восстановления микрофлоры кишечника и влагалища, физиотерапия (61-й (56%) больной проведено светолечение линейно-поляризованным светом, 51-й (46,8%) — УФО наружных гениталий). Воздействие на этиологический фактор осуществлялось с помощью антимикотических средств: пимафуцина, флуконазола внутрь, вагинально проводилось введение пимафуцина, полижинакса, клотримазола.
Положительная динамика, отсутствие рецидивов наблюдались у 86 (78,9%) больных, 76 (88,4%) из них получали комбинированное лечение специфическими противогрибковыми препаратами.
Наше исследование показало необходимость комплексного подхода к терапии кандидоза, включающего общеукрепляющие, иммуномодулирующие препараты, коррекцию гормонального баланса, восстановление микробиоценоза кишечника, лечение сопутствующей соматической патологии.
Одной из основных задач подростковой контрацепции является профилактика ЗППП у девочек-подростков. Результаты нашего анкетирования показали, что 63,9% респондентов хотели бы получить информацию по вопросам контрацепции от врача-гинеколога.
Подростковая контрацепция должна отвечать следующим требованиям: безопасность для здоровья, высокая эффективность; удобство применения, доступность приобретения. Поэтому среди существующих методов контрацепции следует назвать: барьерные (механические — презерватив; химические — спермициды) и гормональные. Барьерные методы решают проблему предохранения от нежелательной беременности, защищают от ИППП. Однако, несмотря на доступность эффективной барьерной контрацепции и знания о презервативах, многие молодые люди подвергают себя риску нежелательных последствий сексуальной активности.
Одним из наиболее используемых местных контрацептивов является фарматекс производства французской фармацевтической компании «Иннотек Интернасиональ». Этот препарат единственный в Украине, который выпускается в разнообразных формах: гинекологических таблетках, свечах, креме, тампонах, что позволяет каждой женщине выбрать удобную форму. Разные формы фарматекса по-разному увлажняют влагалище при половом контакте: крем обладает выраженным увлажняющим эффектом, свечи — умеренным, а вагинальные таблетки — не увлажняют вообще. Применение тампона «Фарматекс» возможно женщинам с различным типом секреции, так как он может оказывать как увлажняющее действие, так и сорбировать избыток секрета. Контрацептивный эффект фарматекса осуществляется за счет хлорида бензалкония, который, в отличие от других веществ (например, от ноноксинола-9), не проникает в кровь, материнское молоко, не влияет на нормальную микрофлору, не повреждает слизистую влагалища.
Контрацептивный эффект препарата реализуется благодаря следующим механизмам: обездвиживание сперматозоида вследствие отрыва жгутика; разрушение мембраны сперматозоида в результате изменения ее поверхностного натяжения; максимальный контакт препарата со сперматозоидами благодаря обволакивающему эффекту; коагуляция цервикальной слизи препятствует проникновению сперматозоидов в матку.
Препарат оказывает антисептическое и противовоспалительное действие, не изменяя микрофлору влагалища, активен в отношении гонококков, хламидий, трихомонад, микоплазм, гарднерелл, ЦМВ, ВИЧ, что существенно снижает риск ЗППП. Контрацептивный эффект фарматекса сопоставим с эффектом КОК, презерватива. По данным разных исследований, процент контрацептивных неудач варьировал от 0 до 5%. Результаты нашего анкетирования показали, что 63,9% респондентов хотели бы получить информацию по вопросам контрацепции от врача-гинеколога. Профессиональная и своевременная информация о фарматексе позволила бы вытеснить из способов контрацепции прерванный половой акт, «народные» средства, уменьшить количество абортов, нежелательных беременностей, ЗППП у подростков.
Выводы
- Воспалительные заболевания наружных и внутренних гениталий являются одними из доминирующих в структуре гинекологической патологии девочек, влияют на состояние здоровья будущей женщины, ее детородную функцию. Заметное место в этиологии воспаления занимают хламидии и микоплазмы.
- Актуальность проблемы обусловлена высокой частотой патологии, склонностью к хронизации патологического процесса, что ведет к серьезным нарушениям репродуктивного здоровья.
- Пути передачи специфической урогенитальной инфекции различны. В подростковом возрасте, среди девушек, имеющих опыт половой жизни, возможен половой путь заражения. В более ранние возрастные периоды доминирует бытовой способ передачи инфекции.
- Для «детских» урогенитальных инфекций характерны разнообразие клинических проявлений, стертая картина заболевания и осложненное течение.
- Своевременно диагностировать патологию и уменьшить частоту осложнений поможет выделение группы риска, нуждающейся в обследовании на ЗППП.
- В условиях стационара пациенткам с подозрением на наличие урогенитальной инфекции широко использовать вагиноскопию для получения более полной информации о клинической картине заболевания и забора материала для исследования.
- Учитывая частое сочетание воспалительных заболеваний с нарушениями менструального цикла, необходимы более полное обследование и коррекция гормонального статуса больных,
- Одной из основных задач подростковой контрацепции является профилактика ЗППП.
ЛИТЕРАТУРА
- АнкирскаяА.С, Муравьева В.В, Микробиологическая характеристика инфекции влагалища, вызванной грибами рода Candida // ЗППП, — 1998. — №2. —С. 12-14.
- Богданова ЕЛ. Гинекология детей и подростков. — М.: Медицинское информационное агентство, 2000. — С. 96-97.
- Вовк І.Б., Білоченко A.M. Вульвовагініт у дітей: сучасний погляд на проблему /,/ ПАГ. — 2004. — № 4. — С. 94-97.
- Гуркин ЮА. Гинекология подростков: Руководство для врачей. — СПб.: ИКФ «Фолиант», 2000. — С. 321-328.
- Гуркин ЮА. «Новые» заболевания, передающиеся половым путем, у девушек: Пособие для врачей. — СПб., 1999. — 64 с.
- Диагностика, лечение и профилактика заболеваний, передаваемых половым путем: Методические материалы. —1998 (Ассоциация САНАМ).
- Золотухин Н.С., Друпп Ю.Г., Смоляк Л.Л., Князева Н.В., Мацынин А.Н. Лечение кандидоза в гинекологической практике // Медико-социальные проблемы семьи. — 1999. — Т. 4, № 2. — С. 90-95.
- Коколина В.Ф. Детская гинекология: Руководство для врачей. — М.: ООО «Медицинское информационное агентство», 2001. — 368 с.
- Кузнецова Я.И., Желтоноженко Л.В. Роль бактериоскопического исследования в диагностике воспалительных заболеваний гениталий у девочек и девочек-подростков / Тези доповідей міжрегіональної науково-практичної конференції «Актуальні проблеми реабілітації репродуктивного здоров’я». — 2004. — С. 115-117.
- Матыцина ЛА., Соркин AM. Иммунологические аспекты воспалительных заболеваний гениталий у девочек и девочек-подростков // Медико-социальные проблемы семьи. — 1999. — Т. 4, № 1. — С. 39-43.
- Ромащенко О.В. Генитальный хламидиоз у юных женщин // ПАГ. — 1998. — № 2. — 32 с.
- Слюсарев АА., Матыцина Л А., Ракша-Слюсарева ЕА., Аяексеенко АА. Перспективы клеточной трансплантологии в восстановлении репродуктивной функции женского организма с подросткового возраста // Основы репродуктивной медицины / Под ред. проф. В.К. Чайки. — Донецк: ООО «Атьматео», 2001. — С. 515-523.
- Суколин Г.И. Кандидоз гениталий: болезнь, передаваемая половым путем? // Вестник дерматологии и венерологии. —1997. — № 3. — С. 39-41,
- Чайка В.К., Матыцина Л А., ОнипкоА.Н. Профилактика, диагностика и лечение урогенитальных инфекций у детей и подростков // Диагностика и коррекция нарушений репродуктивной системы у детей и подростков / Под ред. проф. В.К. Чайки, Л.А. Матыциной. — Донецк: ООО «Лебедь», 2000.— С. 106-116.
- Чайка В.К., Матыцина Л А, Онипко АЛ. Распространенность урогенитальных инфекций (УГИ) у девочек и девочек-подростков // Вісник асоціації акушерів-гінекологів України. — 1999, — № 1. — С. 47-49.
- Чеботарева Ю.Ю.. Яценко ТА. Гинекология детского и подросткового возраста / Под ред. проф. В.П. Юровской. — Ростов-на-Дону: Феникс, 2003. — 384 с.
- Юлиш Е.И., Волосовец АЛ, Врожденные и приобретенные TORCH-инфекции у детей. — Донецк, 2005, — 216 с.
- Carpenter S.E.K.,Rock J A. Pediatric and Adolescent Gynecology. — 2nd Ed. — 2000. — P. 322-324.
- Emans S.J., Laufer M.R., Goldstein D.P. Pediatric and Adolescent Gynecology. — 4th Ed. — 1998.
- Diagnosis and Management of Sexually Transmitted Diseases 2001 (Royal Adelaide Hospital).
- Sexually Transmitted Diseases Treatment Guidelines 2002 (Centers for Disease Control and Prevention ).









Комментировать