Использование Бэби-Кард. Результаты проведенных исследований.
Лахно И. В.,* Шульгин В. И., Печенин А. В., Федотенко В. В., Наседкин К. В., Задерихин А. К., Токарев А. В.
Харьковская медицинская академия последипломного образования*, Национальный аэрокосмический уни- верситет им. Н. Е. Жуковского, «Харьковский авиационный институт», НТЦ «ХАИ-МЕДИКА»
Представления о плоде как пациенте обосновывают необходимость антенатального наблюдения за его состоянием. Проблема мониторинга биофизической активности плода экстраполирует свое влияние на особенности клинической интерпретации полученной информации, что при наличии субъективизма или низ- кой точности выбранной методики зачастую повышает уровень необоснованных интервенций. В современной перинатологии существует целый ряд заболеваний, требующих динамической оценки процессов жизнедеятельности плода. Среди них: синдром задержки роста плода (СЗРП), дистресс плода, врожденные ано- малии сердца, гемолитическая болезнь, фетопатии. В некоторых случаях, когда срок гестации не позволяет надеяться на рождение жизнеспособного новорожденного, качественный непрерывный мониторинг являет- ся основой для применения методов фетальной хирургии или традиционных терапевтических подходов [1, 8,11].
Осуществление высокоинформативного фетального мониторинга представляет собой комплексную проблему, теоретически и практически релевантную к уровню адаптационно-приспособительных реакций в рамках единой системы «мать-плацента-плод». Роль «посредника» в обеспечении взаимосвязи регулятор- ных механизмов матери и плода выполняют волновые процессы в маточно-плацентарном контуре гемоди- намики. Именно медленные колебательные процессы сосудистой системы матери, распространяющие свое влияние через плацентарный барьер, принимают непоредственное участие в создании оптимальных усло- вий для развития плода. Колебания (вариабельность) сердечного ритма (ВСР) являются наиболее удобным в практическом отношении и теоретически релевантным объектом изучения межсистемных взаимодействий в организме, которые порождают эти колебания [8, 9]. Известно, что дисфункция плаценты и СЗРП сопро- вождаются отсутствием гестационного «ресеттинга» автономной нервной регуляции матери с патологичес- ким преобладанием симпато-адреналовых влияний [5, 8, 9]. Это может служить основой для развития гене- рализованного сосудистого спазма и преэклампсии. В рутинной практике акушеров-гинекологов использует- ся метод ультразвуковой допплеровской кардиотокографии (КТГ), основанный на графическом отображении ВСР плода. Интерпретацию результата КТГ проводят на основании учета мгновенной («удар к удару») вариабельности и более длительных изменений ритма (акцелераций и децелераций) [11, 15]. Физической основой метода является механическая регистрация длительности кардиоинтервалов, связанная с изменением длины отраженной от клапанного аппарата сердца ультразвуковой волны. Отсутствие учета первичных электрофизиологических процессов в синусовом узле снижает точность результата. Ультразвук нельзя считать абсолютно нейтральным для плода [14]. Помимо этого к недостаткам КТГ можно отнести следующее. Ульт- расонографическая локация сердца может быть применена только с 28 недель. Использование механичес- кого кардиоинтервала и усреднение данных ритмограммы не обеспечивает точность оценки мгновенной ЧСС[1]. Альтернативой является изучение ВСР по данным неинвазивной электрокардиографии (ЭКГ) плода.
Антенатальная неинвазивная ЭКГ плода основана на регистрации в абдоминальном отведении общего сигнала, состоящего из ЭКГ матери, миографических и прочих составляющих, и последующей фильтрации отдельных компонентов. Решение этой задачи соответствует «слепому разделению источников» на ос- новании анализа независимых компонентов [6, 7, 13]. В этом направлении работают многочисленные научные группы и отдельные исследователи [13, 15, 16]. При этом единственным в мире примером практической реализации неинвазивной ЭКГ плода является появление экспертного фетального монитора Monica (Monica Healthcare Ltd, Великобритания). Коллектив исследователей НТЦ «ХАИ-МЕДИКА» под руководством профессора Шульгина В. И. за последнее десятилетие осуществил разработку первого в Украине фетального ЭКГ монитора Бэби-Кард [2, 6, 7, 10]. Фетальный монитор Бэби-Кард, по сути дела, представляет собой пор- тативный электрокардиограф с функцией регистрации и анализа электрокардиограммы плода и матери. Си- стема состоит из миниатюрного регистратора с автономным питанием и беспроводной передачей данных по Bluetooth, персонального компьютера (настольного ПК, ноутбука или планшетного ПК) с установленной на нем программой, и цветного принтера. При этом система может комплектоваться как одним, так и несколь- кими регистраторами для одновременного наблюдения за рядом пациенток. Использование Бэби-Кард дает возможность одновременного мониторинга ВСР матери и плода, что особенно важно для беременных с сердечно-сосудистой патологией и преэклампсией.
Полученные результаты позволяют обозначить возможные преимущества созданного комплекса Бэби-Кард по сравнению с данными КТГ [2, 3, 4, 5]. Использование Бэби-Кард позволяет с 20-23 недель гестации непосредственно регистрировать ЭКГ плода с последующим морфологическим и временным анализом параметров сердечного цикла: PR- и PQ-интервалы, ширину QRS-комплекса, изменения Р- и Т-волн, а также ST-сегмента. В результате возможно получение дополнительной информации об оксигенации плода [12, 15,16]. В отличие от традиционной КТГ, такая запись сердечного ритма характеризуется высокой степенью точ- ности, так как она получена на основе анализа QRS-комплексов плода, а не является восстановленной из ультразвукового допплеровского сигнала [11, 15, 16]. Последнее дает возможность непосредственно прово- дить поцикловый анализ различных видов «быстрых» неритмичностей и аритмий у плода. Это особенно важ- но, когда аритмия не сопровождается дистрессом плода и не требует экстренного родоразрешения. Более того, данный метод позволяет осуществлять многократное и долговременное мониторирование сердечногоритма (фетальный холтер), что вообще невозможно при использовании УЗ-методов наблюдения [14, 16].
Метод абсолютно безвреден для плода и матери, поскольку он выполняет свои функции в пассивном режиме без каких либо излучений.
Фетальный монитор Бэби-Кард является устройством для мониторинга и неинвазивного измерения следующих параметров сердечной деятельности плода и матери:
— частоты сердечных сокращений плода (ЧССП), базальной ЧСС плода;
— частоты сердечных сокращений матери (ЧССМ);
— двигательной активности матери (MMov);
— количества и параметров акцелераций и децелераций ЧССП;
— эпизодов высокой и низкой вариабельности;
-показателя степени тяжести антенатального дистресса плода;
— параметров вариабельности сердечного ритма (ВСР) плода и матери по истинным RR интервалам “от удара к удару”;
— параметров морфологии электрокардиограммы плода (длительность интервалов PQ, QRS, QT, амп- литуд пиков R, S и T, смещения ST и т.д.).
Ключевые особенности и преимущества системы Бэби-Кард:
— неинвазивное и пассивное (без использования ультразвукового излучения) определение параметров сердечной деятельности плода и матери;
— отсутствие ограничения по количеству исследований и по их продолжительности;
— возможность проведение ЭКГ исследования непрерывно в течение до 24 часов (суточный или ноч- ной мониторинг у пациенток находящихся в группе риска);
— нет необходимости в контроле за ходом мониторинга и переориентации датчиков во время сеанса наблюдения;
— миниатюрный, легкий, незаметный на теле матери, беспроводной монитор (размером с мобильный телефон), отсутствие пояса для крепления КТГ датчиков;
— высокая точность измерения ЧСCП и ЧСCМ (“от удара к удару”), а также набора параметров ВСР матери и плода на протяжении II половины беременности;
— автоматический анализ КТГ (базальный ритм, акцелерации, децелерации и т.д.) в масштабе реаль- ного времени с 20-ти недель беременности и в первом периоде родов с оценкой функционального состояния плода.
— отображение результатов мониторинга производится в стандартном для современных кардиотоког- рафов виде (что очень важно для опытного врача) и формате на обычной бумаге;
— дистанционное получение результатов КТГ исследований (через сеть интернет);
— простота в работе с прибором.
Сердечный ритм плода имеет мультифрактальную природу, во многом связанную с его биофизичес- кой активностью. То есть проявлением ответа механизмов нейрофизологического управления во время эпи- зодов двигательной активности плода является возрастание общей мощности (Total Power, TP) ВСР. КТГ не позволяет представить фрактальную структуру ритма плода, а также инициальные механизмы изменчивости сердечных циклов [2, 3]. Построение фазовых портретов ВСР плода позволяет глубже понять природу ос- цилляторов в их проекциях на синусовый узел сердца, порождающих волновые процессы гемодинамики. В процессе жизнедеятельности плода принято выделять два стационарных состояния: период двигательной активности («бодрствования») и период «сна-отдыха». Безусловно, эти два режима отличаются по характеру регуляции. По данным КТГ регистрации в покое плод демонстрирует запрограммированную ареактивность сердечной деятельности, что может быть расценено как признак патологии [3, 4, 5 ]. Необходим поиск похо- дов к оценке показателей ВСР плода без учета его активности, то есть позволяющих оценивать базовое сос- тояние нейрофизиологической регуляции. В качестве доступного математического аппарата оценки ВСР ис- пользуются быстрые преобразования Фурье, нашедшие реализацию в программном обеспечении Бэби-Кард. Сущность метода состоит в подобии трехгранной призме, преломляющей ритмограмму на три элементарные составляющие, что аналогично декомпозиции волн оптического диапазона на три цвета. У плода спектр сос- тоит из высокочастотного компонента (High Frequency, HF), связанного с вагальными реакциями на измене- ния внутриамниотического давления и дыхательными движениями передней брюшной стенки матери. Низ- кочастотная (Low Frequency, LF) часть спектра отражает активность подкорковых симпатических центров и характеризует колебания собственного осциллятора в системе регуляции давления. Очень низкочастотная (Very Low Frequency, VLF) область связана с центральной метаболо-гуморальной регуляцией. Внутриутробный период жизни характеризуется доминированием метаболического звена регуляции, достаточно выраженным симпатическим влиянием на стабилизацию сердечного ритма и практически слабой активностью вагального тонуса [3].
Целью работы было проведение сравнительного изучения биофизического профиля плода и показателей ВСР плода по данным неивазивной компьютерной ЭКГ.
Материалы и методы. Под наблюдением находилось 146 беременных в сроках гестации 37-41 не- деля, которые были поделены на несколько клинических групп. К I (контрольной) группе было отнесено 52 пациентки с физиологическим течением беременности. Во II группе было 54 беременные с преэклампсией (ПЭ) легкой степени, а III группу составили 40 женщин с ПЭ средней и тяжелой степени. Пациентки III группы получали гипотензивную терапию в соответствии с клиническим протоколом № 676 Министерства Здравоохранения Украины.
Всем обследованным пациенткам проводили изучение ВСР плода путем неинвазивной ЭКГ плода на 10-минутных записях с помощью компьютерно-диагностической системы Кардиолаб Бэби-Кард НТЦ “ХАИ-Медика” (Харьков, Украина). У плода оценивали значение общей мощности спектра автономной нерв- ной регуляции (TP) и мощности трех спектральных компонентов: очень низкочастотного (VLF), низкоча- стотного (LF) и высокочастотного (HF). Изучали следующие временные характеристики ВСР плода: SDNN, RMSSD, pNN5O, АМо и ИН. Регистрацию ЭКГ плода проводили в периоды двигательной активности плода и «покоя-сна». Всем представленным в работе пациенткам проводили изучение биофизического профиля плода (БФП), в состав которого входил и нестрессовый тест (НСТ) по данным КТГ.
Полученные результаты обработаны статистически методами параметрической статистики (среднее – M, ошибка – m) с помощью пакета программ Excel, адаптированных для медико-биологических исследований.
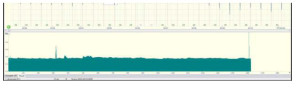
Результаты и обсуждение. Изучение показателей ВСР плодов обследованных пациенток позволило установить значительные различия (табл. 1). У пациенток I группы было отмечена максимальная TP с пре- обладанием VLF. На фоне состояния «покоя-сна» отмечалось пропорциональное уменьшение фрактальных компонентов ВСР и уменьшение TP. При этом открывались некоторые закономерности. В периоды шевеле- ний TP ВСР значительно возрастала, что влекло увеличение мощности всех частотных областей спектра при незначительном вкладе со стороны HF. Уровень линейных показателей вагального звена регуляции RMSSD и pNN5O был невысоким. Обращало на себя внимание снижение значения ИН и АМо, характеризовавших центральный симпатический контур регуляции, по мере роста TP (табл. 1). Следовательно, шеве- ления не были связаны с симпатической барорефлекторной активностью. По-видимому, основа регулятор- ных изменений во время движений плода находилась в метаболо-гуморальной (VLF) части спектра ВСР, ко- торая зависела от уровня различных вазоактивных веществ, в том числе и катехоламинов. Принимая во внимание, что метаболо-гуморальное звено регуляции является доминирующим у плода при любых значе- ниях ВСР можно предположить, что торможение центральных симпатических влияний принимает участие в обеспечении наиболее эргономичного режима движений плода. То есть шевеления плода не были взаимосвязаны с формированием стрессорных реакций. В покое возрастание показателей симпатического звена регуляции ИН и АМо демонстрировало относительную стабильность ритма, что на КТГ проявляло себя как «немой» или монотонный тип. С этим были связаны 7 случаев (13, 7 %) ложноареактивного НСТ по данным КТГ в I группе. Оценка БФП составила 8,1±0,6 балла. В I группе независимо от биофизической активности плода значения ИН были менее 350 усл. ед., а АМо – менее 45,0 %. Таким образом, компьютерная неинва- зивная ЭКГ плода дает возможность изучения спектральных составляющих ритма плода и учитывать «по- правку» на «сон». Полученный результат наводит на мысль, что даже временные показатели централизации симпатической регуляции ИН и АМо наделены «нелинейным» смыслом, демонстрируя природу ригидности ритма сердца на фоне их возрастания. Изображение линейного показателя – длительности кардиоинтерва- лов в виде ритмограммы может быть дополнено огибающей, которая в норме напоминает волну (рис. 1). Чем выше амплитуда волны, тем выше ВСР. Поэтому у плода на фоне удовлетворительного состояния ВСР определяется сложными мультифрактальными взаимодействиями осцилляторов, работающих в нелинейном режиме. Доминирующим можно считать метаболо-гуморальное звено регуляции при наличии выраженной активности центрального симпатического контура, значительно преобладающей над парасимпатической.
Рис. 1. Ритмограмма плода у беременной I группы.
У пациенток II группы показатели ВСР плода также имели определенные особенности (табл. 1). От- мечалось уменьшение TP, снижение мощности VLF диапазона, относительное увеличение мощности в об- ласти LF и незначительная активность HF компонента волновой части спектра. Процесс ЭКГ мониторинга отражен на рисунках 2, 3 и 4. По-видимому, повышенная симпатоадреналовая активность у пациенток с ПЭ легкой степени приводила к вазоспазму, гиповолемии и гиперкинетическому типу гемодинамики матери. Ма- теринские влияния проецировались на изменения гемодинамического режима в маточно-плацентарном и плодово-пуповинном контурах гемодинамики. У плода доминировала центральная симпатическая барореф- лекторная регуляция. Уменьшение SDNN отражало возрастание роли периферических звеньев контроля сердечного ритма и напряженное функционирование гипоталамо-гипофизарно-надпочечниковой оси. Пара- симпатические влияния по данным значений RMSSD и pNN5O не играли значительной роли в регуляции ге- модинамики плода. ИН в этой группе был в пределах 351-550 усл. ед., а АМо – 45,1-55,0 %. Полученные результаты позволяют считать, что наличие повышенной активности стресс-реализующих систем у плодов пациенток II группы были связаны с возрастанием симпато-адреналовых влияний, что угнетало ВСР.
По дан- ным КТГ реактивный НСТ зарегистрирован у 5 (9,3 %) пациенток, гипореактивный – 38 ( 70,4 %), ареакти- вный – 11 случаях (20,3 %). Суммарная оценка БПП составила 6,9±0,8 балла, что можно расценить как суб- компенсированное (умеренное) страдание плода.
В III группе значения показателей ВСР были несколько разнородными, что объяснялось различными адаптационными способностями плодов по отношению к формированию шокогенных реакций у матери. В общем случае возникало дальнейшее по сравнению с показателями I и II группы снижение мощности TP, VLF, относительное увеличение LF-компонента (рис. 5). В отношении уровня HF следует отметить, что ва- гальный тонус возрастал лишь на фоне полной утраты нелинейности в деятельности сердца, то есть появ- ления синусоидального или ригидного ритма. В большинстве наблюдений III группы отмечалось значитель- ное преобладание симпатической регуляции над парасимпатической. При этом наличие тахикардии было проявлением централизации гемодинамики. В случаях появления эпизодов брадикардии (подобия децеле- раций по данным КТГ) выраженного увеличения ВСР не происходило. ИН в этой группе был более 550 усл. ед., а АМо – более 55,1 %. Это дает смелость утверждать, что в патогенезе антенатальных децелераций значительную роль играет доминирование центрального симпатического контура регуляции при наличии формирующегося гипоксического поражения миокарда плода и угнетенного ответа синусового узла. В этой группе формировался дистресс плода, о чем свидетельствовала суммарная оценка БФП – 5,6±1,1 балла.
Таблица 1. Показатели ВСР плодов обследованных беременных
| Показатель, ед. из-мерения | I группа | II группа | III группа |
| SDNN, мс | 46, 2±8,2 | 31,4±6,8* | 12,3±1,7*⁄** |
| RMSSD, мс | 22,4±3,4 | 14,2±2,6* | 8,1±0,8*⁄** |
| pNN5O, % | 8,6±1,0 | 5,6±0,9* | 2,1 ±0,2*⁄** |
| ИН, усл. ед. | 140,6±22,8 | 464,2±52,4* | 1450,2 ± 112,6*⁄ ** |
| АМо, % | 38,2±7,4 | 49,8±6,2* | 62,5±6,6*/** |
| TP, мс² | 2134,8±364,2 | 1048,4±98,4* | 384,8±61,2*⁄** |
| VLF, мс² | 1846,2±282,8 | 670,2±84,6* | 194,2±23,8*⁄** |
| LF, мс² | 192,6±31,1 | 312,2±66,8* | 143,6±25,1*⁄** |
| HF, мс² | 95,2±19,4 | 66,1±14,9* | 48,2±14,1*⁄** |
* – различия статистически значимы по сравнению с контролем (p<0,05);
** – различия статистически значимы по сравнению со II группой (p<0,05).
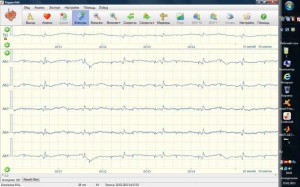
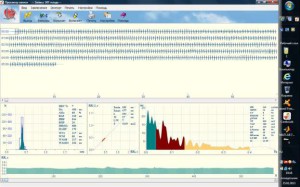
Рис. 2. Запись ЭКГ матери и плода с помощью системы Бэби-Кард.
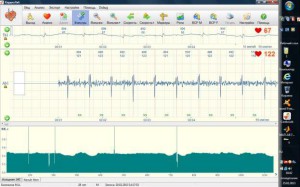
Рис. 3. Общая запись, выделенная ЭКГ плода и ритмограмма плода (длительность RR-интервалов) у пациентки II группы.
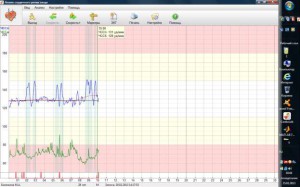
Рис. 4. Конечный результат обработки ЭКГ сигнала – кривая анализа сердечного ритма плода (аналог традиционной КТГ).
Рис. 5. ВСР плода у пациентки III группы.
Возможность оценивать фрактальную структуру сердечного ритма плода по данным антенатальной неинвазивной ЭКГ плода позволяет глубже изучить природу угрожаемых состояний плода. Изучение ВСР по данным ЭКГ плода позволяет объективизировать оценку функционального состояния плода, что проявляет- ся в исключении необходимости учета внутриутробной биофизической активности. Учитывая простоту прак- тического применения метода и совместимость с современными беспроводными средствами коммуникации в будущем возможно широкое внедрение в практику аппаратных комплексов для непрерывного дистанцион- ного мониторинга состояния плода.
Выводы. 1. Антенатальная неинвазивная компьютерная ЭКГ плода позволяет объективизировать мо- ниторинг плода с учетом поправки на «сон».
2. Ухудшение состояния плода у беременных с ПЭ сопровождается уменьшением всех фрактальных составляющих ВСР с относительным преобладанием центрального симпатического контура управления.
3. Появление ригидности ритма и тенденция к брадикардии у плода связаны с центральной симпати- ческой активностью на фоне угнетенного ответа синусового узла.
4. Разработанная методика оценки состояния плода может быть реализована в создании телекомму- никативных систем непрерывного электронного мониторинга.
Литература.
1. Абуладзе Г. В., Папиташвили A. M. Спектральные свойства вариабельности частоты сердечного ритма плода. Норма и клиническое применение // Ультразвуковая и функциональная диагностика. – 2003. –№2. – С.128-137.
2. Лахно И. В. Неинвазивная антенатальная компьютерная электрокардиография плода versus кардиотокография: первый опыт в Украине // Медицина неотложных состояний. – 2012. – № 1 (40). – С. 101-105.
3. Лахно И. В. Новые данные о механизмах симпато-адреналиновых влияний на состояние внутриутробного плода // Здоровье женщины. — 2009. — № 8 (44). — С. 46-48.
4. Лахно И. В. Регуляция гемодинамики плода у беременных с преэклампсией // Проблеми безперер- вної медичної освіти та науки. – 2011. –№ 4. – С. 48-53.
5. Лахно И. В. Синхронизация нейро-гуморальной регуляции матери и плода // Medicus amicus. –2009. – № 4. – С. 24-26.
6. Лахно И. В., Печенин А. В. Неинвазивное выделение электрокардиограммы плода методом анализа независимых компонентов // Медицина сегодня и завтра. – 2002. – № 3. – С. 78-82.
7. Лахно І. В., Шульгін В. І., Грищенко О.В., Печенін О. В., Риженко Ю. В. Технологічні аспекти та власний досвід вивчення варіабельності серцевого ритму плода методом електрокардіографії // Вісник наукових досліджень. – 2005. — № 2 (39). – С. 39-40.
8. Ушакова Г. А., Петрич Л. Н. Нейровегетативная регуляция кардиоритма матери и плода при хрони- ческой плацентарной недостаточности // Мать и дитя в Кузбассе. – 2008. – № 34(3). – С. 21-25.
9. Флейшман А. Н. Медленные колебания гемодинамики. Теория, практическое применение в кли- нической медицине и профилактике. – Новосибирск, 1999. – 224 с.
10. Шульгин В. И., Печенин А. В., Федотенко В. В., Наседкин К. В., Лахно И. В. Использование техники слепого разделения источников для выделения электрокардиограммы плода // Клиническая информатика и телемедицина. – 2004. – № 2. – С.208-212.
11. Amer-Wahlin I., Kallen K., Herbst A. et al. Current status of intrapartum fetal monitoring: cardiotocography versus cardiotocography + ST analysis of the fetal ECG // J. Matern. Fetal Neonatal Med. – 2005. –Vol.18, No 2. – P. 93-100.
12. Comani S., Mantini D., Lagatta A. et al. ST analysis of fetal ECG in premature deliveries during 30th-36th week of pregnancy // Physiol. Meas. – 2004. – Vol. 25, No 5. – P. 1305-1321.
13. Kezi S. V. C., Kanagasabapathy P., Johnson S. Fetal ECG Extraction using Softcomputing Technique // Journal of Applied Sciences. – 2006. – Vol.6, No.2. – Р. 251-256.
14. Kieler H., Cnattingiust S., Haglund B., Palmgren J., Axelsson O. Ultrasound and adverse effects // Ultrasound in Obstetrics and Gynecology. – 2002. – Vol. 20, Issue 1. – Р. 102-103.
15. Pasquini L., Seale A. N., Belmar C. et al. PR interval: a comparison of electrical and mechanical methods in the fetus // Early Hum. Dev. – 2007. – Vol. 83, No 4. – P. 231-237.
16. Pieri J. F., Crowe J. A., Hayes-Gill B. R. et al. Compact long-term recorder for the transabdominal foetal and maternal electrocardiogram // Med Biol Eng Comput. – 2001. –Vol. 39, No1. – P. 118-125.








Комментировать