Термин «хроническое обструктивное заболевание легких»: описание, эволюция. Причины обострений. Тактика лечения и анализ препаратов.
Сидоров Д.Ю., Харьковская медицинская академия последипломного образования 1(1) 2009 / В фокусе внимания
Термин «хроническое обструктивное заболевание легких» (ХОЗЛ) появился около 30 лет назад и был предложен для обозначения медленно прогрессирующей и необратимой обструкции дыхательных путей, в основе которой лежат сужение бронхов за счет воспаления и потери эластического каркаса легких за счет эмфиземы. В большинстве случаев практически невозможно определить конкретный вклад хронического бронхита и эмфиземы у отдельного пациента. ХОЗЛ занимает одно из лидирующих мест среди всех причин смерти в промышленно развитых странах. Смертность от ХОЗЛ растет во всем мире, и ожидается, что к 2020 году она достигнет 6 миллионов человек в год.
Развитие ХОЗЛ связано с нарушением нормальных механизмов защиты легких и репарации, действием поллютантов. Ведущая роль в патогенезе ХОЗЛ принадлежит воспалению, дисбалансу протеаз и антипротеаз и оксидативному стрессу. Морфологические изменения при ХОЗЛ, лежащие в основе функциональных нарушений, затрагивают центральные и периферические дыхательные пути, легочную паренхиму и сосудистую систему. На каждой стадии определяются характерные изменения: катаральное воспаление, гипертрофия и гиперплазия желез подслизистого слоя, гиперсекреция слизи. По мере истощения местных ингибиторов протеаз и под влиянием нейтрофильных протеаз, разрушающих эластическую строму легких, развивается эмфизема, изменяется механика дыхания и формируется экспираторный коллапс, являющийся важнейшей причиной необратимой бронхиальной обструкции. Повреждение слизистой бронхов, развитие бронхоэктазов, воздушных ловушек, нарушение мукоцилиарного и альвеолярного клиренса является непосредственной причиной колонизации нижних дыхательных путей патогенной микрофлорой.
У 70 % больных развивается легочное сердце, возникают множественные спайки в плевральных полостях вплоть до полной облитерации. Буллезные эмфиземы сдавливают окружающие альвеолы, еще более уменьшая емкость легкого и увеличивая угрозу пневмоторакса. В периоды обострения при участии ассоциаций бактериальных возбудителей возникают фиброзногнойные плевриты и абсцессы легких. Причиной смерти при ХОЗЛ являются легочно-сердечная недостаточность, хроническая дыхательная недостаточность, гнойная интоксикация, коллапс легких при пневмотораксах.
Обострение ХОЗЛ — наиболее частая причина обращения пациентов за медицинской помощью [1]. В настоящее время обострение ХОЗЛ определяют как относительно длительное (не менее 24 часов) ухудшение состояния больного, по своей тяжести выходящее за пределы обычной суточной вариабельности симптомов, характеризующееся острым началом и требующее изменения обычной терапии [2]. Тяжесть обострения заболевания может значительно варьировать: от легкой, при которой достаточна терапия в домашних условиях, до тяжелой, жизнеугрожающей дыхательной недостаточности, требующей искусственной вентиляции легких (ИВЛ). В среднем в течение года возникает 1-2 обострения, каждое из которых продолжается приблизительно 12 дней [3]. Общая летальность при обострении ХОЗЛ достигает 5 %.
Обострения являются основной причиной смертности, летальности, госпитализации [2, 4], нарушения качества жизни [5] больных ХОЗЛ. У пациентов с частыми обострениями было отмечено повышение уровня цитокинов, что приводило к усилению активности воспалительного процесса и увеличивало риск развития повторных обострений [6]. Повторные обострения приводят к значительному снижению объема форсированного выдоха за первую секунду (ОФВ1), более длительным и частым госпитализациям, более выраженным и стойким симптомам, более тяжелому течению обострений [7]. Патологический круг замыкается, и последующие обострения связаны с повышением риска смертельного исхода [8]. Летальность при острой дыхательной недостаточности (ОДН) варьирует от 10 до 29 %, а у больных, нуждающихся в искусственной вентиляции легких, — от 32 до 57 %. Смертность после обострения ХОЗЛ с ОДН в течение года достигает 40 % [9]. Снижение частоты обострений и госпитализаций приводит к замедлению прогрессирования заболевания [10-13].
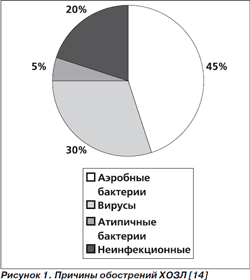
Признаками обострения являются прогрессирование одышки, усиление кашля, увеличение продукции мокроты и изменение ее характера (повышение гной- ности мокроты), а также развитие и усугубление симптомов, отражающих общее самочувствие, снижение толерантности к физической нагрузке. Среди причин обострения ХОЗЛ принято выделять инфекционные и неинфекционные. Примерное их соотношение представлено на рис. 1.
Неинфекционные причины обострения ХОЗЛ: пол- лютанты (диоксид азота, диоксид серы, озон, твердые частицы); лекарственные средства (Р-адреноблокаторы, седативные, снотворные); сердечная недостаточность и нарушения сердечного ритма; пневмоторакс и другие. Иногда причину обострения ХОЗЛ установить не удается.
Инфекции бронхиального дерева традиционно рассматриваются как ведущая причина обострения ХОЗЛ [15]. Бактериальные патогены выявляются у 50-60 % больных. Вирусная этиология может быть причиной до 30 % всех обострений. Однако трудности идентификации вирусов и Chlamydophila pneumoniae чаще всего и вызывают проблемы при установлении причины обострения. Наиболее полезную информацию получают в исследованиях, в которых для забора микробиологического материала используют методику защищенной щеточной биопсии, исключающую контаминацию бронхиального секрета патогенами верхних дыхательных путей.
Подтверждением роли инфекции при обострении ХОЗЛ может быть внутриклеточное выявление Haemophilus influenzae в бронхиальных биоптатах (87 %), тогда как при ремиссии данный микроорганизм обнаруживается внутриклеточно в 33 % случаев, а у здоровых лиц вообще не определяется. В то же время при использовании традиционных микробиологических методов Haemophilus influenzae обнаруживалась в нижних отделах респираторного тракта только у 7 % пациентов с обострением [16]. Частота обнаружения гра- мотрицательных микроорганизмов у больных с ОДН и ИВЛ составила 29 % (Pseudomonas aeruginosa). Четырехкратное увеличение титра антител к Mycoplasma pneumoniae выявлялось в 6-8,7 % случаев. При проведении обычного микробиологического исследования выявленные микроорганизмы одного вида расцениваются как идентичные, хотя микробная популяция при ХОЗЛ является генетически гетерогенной.
При обследовании больных с обострениями ХОЗЛ чаще всего выявляются Haemophilus influenzae, Streptococcus pneumoniae и Moraxella catarrhalis, которые способны вырабатывать субстанции, вызывающие мукоцилиарную дисфункцию, а Haemophilus influenzae оказывает прямое повреждающее действие на эпителий воздухоносных путей [9]. Реже причиной инфекционного процесса могут быть другие пиогенные бактерии: Klebsiella pneumoniae, Staphylococcus aureus, представители семейства Enterobacteriaceae, Pseudomonas aeruginosa, Chlamydophila pneumoniae, Mycoplasma pneumoniae и Legionella spp., а также вирусная инфекция [17].
При обострении ХОЗЛ в мокроте и бронхоальвеолярных смывах обнаруживают палочкоядерные ней- трофилы, доля которых возрастает до 95 %. Просветы бронхов заполняются большим количеством мокроты, содержащей нейтрофилы и некротизированные клетки эпителия. Доля нейтрофилов увеличивается и в толще эпителия, и в собственной пластинке слизистой оболочки. Тяжесть обострения ХОЗЛ значительно варьирует и прямо пропорциональна тяжести течения заболевания [18].
Роль бактерий в прогрессировании ХОЗЛ нашла отражение в гипотезе «порочного круга», согласно которой повреждение дыхательных путей развивается в результате хронической инфекции и колонизации, сопровождающихся постоянной продукцией провоспа- лительных медиаторов (интерлейкин-6 и -8, фактор некроза опухолей а, лейкотриен В4). Продуцируемые бактериями протеазы и активные соединения кислорода вызывают повреждение эпителия, разрушение антител, компонентов Т-рецепторов комплемента, нарушают фагоцитоз и мукоцилиарный клиренс, способствуют притоку нейтрофилов и слизеобразованию, что приводит к снижению бронхиальной проходимости [19].
Согласно гипотезе «подъема-падения» [20], инфекционное обострение ХОЗЛ представляет собой воспалительный процесс дыхательных путей, вызываемый микроорганизмами, концентрация которых превышает определенный количественный порог. При достижении порогового количества микроорганизмов происходит клиническая манифестация обострения. У больных с наличием многих модифицирующих факторов количество бактерий, вызывающих обострение, может быть невелико и не достигать критического порога. Такие обострения с низкой бактериальной нагрузкой протекают как слизистые с низкой вероятностью инфекционной природы. С другой стороны, при отсутствии модифицирующих факторов для появления клинических симптомов обострения требуется значительно большее количество микроорганизмов. При этом проявляется типичная картина бактериальной инфекции. Количественная гипотеза позволяет понять клиническое значение бактериальной инфекции в частоте возникновения и характере обострений, различный ответ на ан- тибиотикотерапию, качество ремиссий и степень риска рецидивов. Более продолжительные ремиссии отмечены у больных, у которых удалось добиться полной эра- дикации этиологически значимого микроорганизма. Согласно гипотезе, при полной эрадикации возбудителя требуется больше времени для достижения пороговой микробной нагрузки и порога клинической манифестации. В случае неполной эрадикации антибиоти- котерапия лишь уменьшает микробную нагрузку ниже порога клинической манифестации, однако ремиссии в этих случаях нестойкие и непродолжительные.
Возможные причины обострений ХОЗЛ:
- инфекции;
- сердечная недостаточность, аритмии;
- тромбоэмболия ветвей легочной артерии, спонтанный пневмоторакс;
- неконтролируемая кислородотерапия;
- лекарственные средства — седативные, диуретики;
- хирургические операции;
- метаболические нарушения;
- аспирация.
При любом обострении развиваются перибронхи- альные рентгенонегативные микропневмонии. Это, в свою очередь, усиливает бронхиальную обструкцию за счет выраженного полнокровия сосудов. Обструкция просвета бронхиол приводит к развитию воздушных ловушек вне зоны эмфиземы. Может также развиваться очаговая или очагово-сливная пневмония, захватывающая значительные объемы легочной ткани, что приводит к усилению дыхательной недостаточности. Пневмония может быть причиной 23-36 % случаев ОДН у больных с обострениями ХОЗЛ [21, 22]. Несмотря на то что ХОЗЛ является наиболее частой фоновой патологией у пациентов с тяжелым течением внебольничных пневмоний [23, 24], данные о микробном спектре возбудителей пневмоний остаются скудными и противоречивыми [25]. У таких больных выше число осложнений, особенно септических, выше летальность [26].
Наиболее универсально обострение ХОЗЛ характеризует определение N. Anthonisen et а1. [27], которое основано на трех кардинальных признаках заболевания: усиление одышки, увеличение объема мокроты и усиление гнойности мокроты. Согласно этому определению, об обострении ХОЗЛ свидетельствует наличие хотя бы одного из перечисленных симптомов. Дополнительными признаками являются: инфекция верхних дыхательных путей на протяжении последних 5 дней, лихорадка без других видимых причин, нарастание числа свистящих хрипов, усиление кашля и повышение частоты дыхательных движений (ЧДД) или частоты сердечных сокращений на 20 %. Наличие комбинации кардинальных признаков позволяет определить и тип течения обострения ХОЗЛ:
- тип I (тяжелое обострение): имеются 3 кардинальных признака;
- тип II (средней тяжести): имеются 2 из 3 кардинальных признаков;
- тип III (легкое обострение): имеется 1 из 3 кардинальных признаков.
Терапия данного состояния остается одной из самых сложных проблем современной медицины, и ее методы несовершенны. Задачами терапии обострения ХОЗЛ являются:
- выяснение и устранение причин обострения;
- снижение нагрузки на аппарат дыхания (повышение проходимости дыхательных путей);
- повышение силы и выносливости дыхательной мускулатуры;
- мобилизация и удаление бронхиального секрета.
В терапии обострений ХОЗЛ в настоящее время используется ряд мероприятий, включающий антибиоти- котерапию, кислородотерапию, бронходилатацию, применение системных и ингаляционных глюкокортикостероидов, респираторную поддержку. Терапия обострений должна осуществляться длительно и не прекращаться после выписки больного из стационара. Это связано с тем, что функция внешнего дыхания восстанавливается очень медленно.
Выбор лечебной тактики основывается на оценке тяжести состояния пациента. Прежде всего, необходимо выявить показания для госпитализации больных [16, 28]:
- значительное усиление интенсивности симптомов;
- обострение у больного с крайне тяжелой стадией ХОЗЛ;
- появление новых симптомов;
- неэффективность амбулаторного лечения;
- тяжелые сопутствующие заболевания;
- возникновение или декомпенсация легочного сердца;
- впервые возникшие аритмии;
- диагностические трудности; пожилой возраст;
- недостаточные ресурсы для терапии в домашних условиях.
Тяжелое обострение и обострение у больных с тяжелыми стадиями ХОЗЛ сопряжено с развитием острой дыхательной недостаточности, что требует экстренной госпитализации в отделение интенсивной терапии. Показаниями для интенсивной терапии являются: тяжелое некупирующееся диспноэ, нарушения сознания, перси- стирующая или прогрессирующая гипоксемия (РаО[1] < 50 мм рт.ст.), и/или нарастающая гиперкапния (РаСО2 > 70 мм рт.ст.), и/или выраженный респираторный ацидоз (pH < 7,3).
Антибиотикотерапию следует расценивать как способ не только купирования текущего обострения, но и профилактики последующих обострений ХОЗЛ.
Необходимо прежде всего определить показания к назначению антибактериального препарата. Появление или усиление гнойности мокроты наряду с увеличением ее количества, а также признаков дыхательной недостаточности свидетельствуют о высокой бактериальной нагрузке, превышающей порог клинической манифестации обострения, и позволяют расценить данную ситуацию как инфекционное обострение ХОЗЛ. Диагностика инфекционного обострения, отвечающая критериям N. Anthonisen et а1., является основанием для назначения антибактериального препарата при I и II типах, с обязательным присутствием гнойной мокроты. У больных с тяжелым обострением ХОЗЛ и острой дыхательной недостаточностью, получавших респираторную поддержку, антибиотикотерапия офлоксацином [29] снижала летальность (4 % против 22 % в группе плацебо) и длительность госпитализации (14,9 против 24,5 суток).
Таким образом, антибактериальная терапия показана больным, у которых обострения ХОЗЛ соответствуют [30, 31]:
- критериям Anthonisen;
- критериям P. Ball: наличие 4 обострений в течение последнего года и/или наличие сопутствующих сердечно-сосудистых заболеваний;
- критериям острой дыхательной недостаточности;
- критериям тяжелой степени бронхиальной обструкции (ОФВ1 < 35 %).
Принципиально важной целью антибиотикотерапии является эрадикация возбудителя. Такой подход отвечает количественной концепции подъема-падения, согласно которой степень эрадикации этиологически значимых микроорганизмов определяет продолжительность ремиссии и сроки наступления последующего рецидива.
Основные антибактериальные препараты, применяемые при обострениях ХОЗЛ [16]:
- р-лактам или р-лактам + ингибитор р-лактамаз;
- макролиды;
- фторхинолоны II генерации и респираторные фторхинолоны;
- цефалоспорины II и III генераций;
- тетрациклины (доксициклин).
Важным шагом в ведении больных ХОЗЛ является выбор оптимального антибактериального препарата. При этом следует ориентироваться на спектр основных возбудителей, тяжесть обострения, вероятность региональной резистентности, безопасность антибактериального препарата, удобство его применения, стоимостные показатели.
Одним из основных критериев выбора первоначального антибактериального препарата является знание спектра основных микроорганизмов в развитии обострений и вероятность этиологической роли того или иного микробного патогена в конкретной клинической ситуации. Антибиотикотерапия обострений ХОЗЛ носит эмпирический характер с учетом ориентировочной этиологической диагностики, основанной на клинической ситуации. При этом не существует ни одного антибиотика, который действовал бы на весь спектр потенциальных возбудителей при обострении ХОЗЛ.
При выборе антибиотика ориентируются на следующие его характеристики:
- высокая активность против большинства наиболее частых и наиболее вероятных микроорганизмов- возбудителей;
- хорошая пенетрация в слизистую бронхов и бронхиальный секрет;
- низкая токсичность, низкая частота развития побочных эффектов;
- простота приема;
- оптимальное соотношение «цена/качество».
Амоксициллин/клавуланат является наиболее подходящим антибактериальным препаратом для лечения обострений ХОЗЛ у большинства пациентов и рекомендован экспертами ВОЗ. Преимущества защищенного амоксициллина заключаются в том, что он эффективен против наиболее частых возбудителей обострений ХОЗЛ: Haemophilus influenzae, Streptococcus pneumoniae, Moraxella catarrhalis, в том числе вырабатывающих р-лактамазы. Амоксициллин/клавуланат является препаратом выбора у больных с I, II или III типами обострения ХОЗЛ и ОФВ1 выше 30 % от должного, у лиц до 65 лет, с частотой обострений до 4 раз в год. Длительность приема этого антибактериального препарата составляет 7-10 дней, по 625 мг каждые 8 часов (или по 875 мг 2 раза в сутки). Недостатком всего класса р-лактамных антибиотиков является субоптимальная легочная фармакокинетика: невысокие концентрации в тканях и жидкостях [32].
У большинства больных эффективны макроли- ды, несмотря на возрастающую резистентность к ним Streptococcus pneumoniae и низкую природную чувствительность Haemophilus influenzae. Данный эффект может быть частично обусловлен противовоспалительной активностью макролидов. Новый макролидный 16-членный антибиотик джозамицин отличается значительно меньшим индуцированием резистентности стрептококков и является препаратом выбора при инфицировании хламидиями, микоплазмой, легионелла- ми. Устойчивость Streptococcus pneumoniae к азитро- мицину и кларитромицину, по данным Российского исследования ПеГАС-1, составила 6 % [33]. По данным другого исследования PROTEKT, устойчивость Haemophilus influenzae к азитромицину и кларитромицину составила 0,2 и 0,5 % соответственно, однако отмечена тенденция к увеличению доли Haemophilus influenzae с промежуточной чувствительностью к кларитромицину [34].
Джозамицин индуцирует значительно меньшую резистентность и проявляет высокую активность в отношении стрептококков. При этом для препарата характерна высокая степень проникновения в ткань легких. В исследовании [35] клиническая эффективность джо- замицина составила 95,2 %, и у 95,2 % пациентов отмечена эрадикация возбудителя. Макролиды показаны к применению в тех же группах больных, что и амоксициллин/клавуланат, и являются препаратами выбора при подозрении на инфицирование Chlamydophila pneumoniae и Mycoplasma pneumoniae. Длительность лечения кларитромицином составляет 10-14 дней, по 500-1000 мг 2 раза в день; азитромицином — 3-5 дней.
Респираторные фторхинолоны (левофлоксацин, моксифлоксацин) высокоэффективны в отношении основных возбудителей при обострениях ХОЗЛ. Длительный период полувыведения и постантибиотиче- ский эффект делает возможным их назначение 1 раз в сутки. Очень важным аспектом терапии является быстрая бактериальная эрадикация и вследствие этого — быстрый клинический эффект [36-38].
Больным с частыми обострениями (не реже 4 раз в год), низким ОФВ1 (< 30 %), неоднократно принимавшим антибиотики в течение года, а также принимающим глюкокортикостероиды, с низким питательным статусом и наличием бронхоэктазов, т.е. когда причиной обострения может быть Pseudomonas aeruginosa [39], рекомендуется парентеральное назначение ципрофлоксацина, цефтриаксона в сочетании с аминогликозидом.
Доксициклин назначается по 100 мг каждые 12 часов в случае невозможности применения амоксицил- лин/клавуланата, макролидов или фторхинолонов.
Длительность антибиотикотерапии у стационарных больных не должна быть менее 7-10 дней.
10-20 % больных не отвечают на антибиотикотера- пию, что требует выявления причин и поиска методов коррекции [20]. Основными причинами могут быть:
- выбор неадекватного антибактериального препарата;
- наличие резистентных штаммов основных возбудителей;
- наличие новых штаммов основных возбудителей;
- наличие более редких возбудителей;
- небактериальная (вирусная) этиология обострения ХОЗЛ;
- высокая частота обострений за предыдущий год;
- некомплайентность больных ХОЗЛ.
Лечение обострений ХОЗЛ предполагает также использование бронходилататоров, восстановление мукоцилиарного клиренса (при обострении ХОЗЛ гиперпродукция мокроты и изменение ее реологических свойств могут быть результатом воздействия этиологического фактора обострения или следствием изменения дыхательного паттерна), респираторную поддержку, применение методов физической терапии (массаж, постуральный дренаж, вибрация грудной клетки, каш- левая техника), дополнительное питание (энтеральное или парентеральное). Кроме основных медикаментозных средств, применяемых для купирования обострений ХОЗЛ, больным данной категории назначаются также дополнительные: для профилактики венозного тромбоэмболизма — низкомолекулярный гепарин или фондапаринукс, для предупреждения стрессовых язв и желудочно-кишечных кровотечений — ингибиторы протонной помпы или Н2-блокаторы.
Прежде чем начать ингаляционную терапию, необходимо выяснить, какое лечение принимает больной и правильно ли он пользуется ингаляторами для базисной терапии.
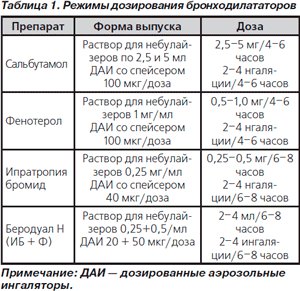
Несмотря на то что ХОЗЛ характеризуется необратимостью бронхиальной обструкции, бронходилатато- ры являются препаратами первой линии в терапии обострения. Даже небольшое повышение проходимости дыхательных путей приводит к уменьшению сопротивления, работы дыхательной мускулатуры, снижению динамической бронхиальной гиперинфляции и улучшению клинического состояния. Некоторые бронходила- таторы обладают положительными внелегочными эффектами. Использование бронходилататоров предполагает увеличение доз и частоты введения. Существующий ряд различных доставочных устройств для ингаляционной терапии позволяет оптимизировать лечение больных путем индивидуального подбора типа ингалятора с учетом возраста пациента, сопутствующей патологии, тяжести состояния [40]. При тяжелых обострениях и у пожилых больных предпочтение должно быть отдано небулайзерной терапии. Режимы дозирования бронходилататоров представлены в табл. 1.
Вопрос о применении теофиллинов короткого действия для купирования обострений ХОЗЛ является предметом дискуссии. Это обусловлено большим потенциалом побочных эффектов. Для уменьшения последних следует строго соблюдать схему дозирования препарата. Во-первых, короткодействующие теофилли- ны (в Украине — эуфиллин) следует применять в случае отсутствия эффекта от ингаляционных бронходилататоров. Во-вторых, препарат должен вводиться только внутривенно капельно. Следует также обеспечить монито- рирование уровня концентрации препарата в плазме. Введение препарата противопоказано больным, получающим пролонгированный теофиллин. Рекомендуется введение эуфиллина в суточной дозе 0,75-1,5 г, при этом доза делится на ударную (240-250 мг) и поддерживающую (0,25—0,9 мкг/час) [41].
Назначение системных глюкокортикостероидов при обострениях ХОЗЛ основано на принципах доказательной медицины. При обострении выявляется увеличение эозинофилов в слизистой бронхов и повышение уровня интерлейкина-6. Воспалительный процесс при обострении, таким образом, может быть подавлен кортикостероидами, в противоположность стабильной фазе заболевания. Терапия системными глюкокортикостероидами должна назначаться всем госпитализированным больным в дозе, эквивалентной 30-40 мг преднизоло- на, на протяжении 10-14 дней.
Кислородотерапия и респираторная поддержка является приоритетным направлением терапии ОДН на фоне ХОЗЛ. Цель кислородотерапии — поддержание РаО2 в пределах 60-65 мм рт.ст. и SaO2 — 90-92 %. У больных ХОЗЛ значительно повышен риск развития кислород-индуцированной гиперкапнии, особенно при выраженной гипоксемии (РаО2 < 49 мм рт.ст.) и респираторном ацидозе (pH < 7,35). Для снижения риска ги- перкапнии Е^М. СатрЬеИ предложил концепцию контролируемой оксигенотерапии, суть которой заключается в строгом количественном учете подаваемого кислорода.
Через 30-60 минут от начала (или изменения режима) кислородотерапии необходимо проведение анализа газов крови и определение рН. Маска Вентури — более предпочтительный способ доставки кислорода, чем носовые канюли, так как позволяет обеспечить более точную дозировку газа. В среднем кислородотерапия с FiO2 (насыщение кислорода во вдыхаемом воздухе) 24 % повышает Ра02 на 10 мм рт.ст. При наличии пневмонии или интерстициального отека легких может потребоваться назначение более высоких фракций О2, что связано с появлением внутрилегочного шунтирования. При развитии кислород-индуцированной гиперкапнии не следует прекращать кислородотерапию, так как снижение парциального давления кислорода будет происходить быстрее, чем СО2. В этом случае следует проводить мероприятия по улучшению бронхиальной проходимости.
В связи с физическими свойствами гелия, плотность которого меньше, чем кислорода и воздуха, дыхание смесью гелия и кислорода (гелиокс) позволяет поддерживать ламинарность потока при значительном повышении его скорости, что позволяет снизить сопротивление потоку в дыхательных путях и риск развития утомления дыхательной мускулатуры. Терапия гелиоксом рассматривается как метод стартовой терапии в наиболее уязвимый период.
Кислородотерапия сопровождается респираторной поддержкой — ИВЛ или неинвазивной вентиляцией легких (НВЛ). Преимуществами НВЛ являются большая комфортность процедуры для больного, чем ИВЛ, возможность незамедлительного прерывания и возобновления процедуры, возможность применения этого метода не только в условиях реанимационного отделения. НВЛ часто сочетают с положительным давлением на выдохе. Преимущество НВЛ на ранних этапах госпитального лечения доказано в многоцентровых рандомизированных исследованиях. Показаниями к проведению НВЛ являются:
- выраженная одышка в покое;
- ЧДД более 25 в минуту, участие в дыхании вспомогательной дыхательной мускулатуры, парадоксальное дыхание;
- РаС02 > 45 мм рт.ст., рН < 7,35, Ра02^Ю2 < 200 мм рт.ст.
Однако имеются состояния, при которых НВЛ противопоказана. К ним относятся: остановка дыхания; нестабильная гемодинамика; невозможность обеспечить защиту дыхательных путей; избыточная бронхиальная секреция; нарушения сознания и неспособность пациента к сотрудничеству с медицинским персоналом; травмы, ожоги, анатомические дефекты, препятствующие наложению маски. В подобных случаях, а также при остановке дыхания, выраженной гипоксии и ацидозе незамедлительно приступают к инвазивной респираторной поддержке (ИВЛ). Основными задачами респираторной поддержки являются: коррекция нарушенного газообмена, разгрузка и восстановление функции дыхательной мускулатуры, возможность купирования причины, вызвавшей ОДН.
Использование традиционного контролируемого режима ИВЛ рекомендовано в течение 24 часов — времени, необходимого для разрешения утомления дыхательных мышц. После этого показан перевод больного на вспомогательные режимы. У больных ХОЗЛ чаще применяют следующие режимы: вспомогательноконтролируемый; поддержка давлением — самостоятельно или в комбинации с синхронизированной перемежающейся принудительной вентиляцией.
Отлучение от ИВЛ — наиболее сложный процесс у больных ХОЗЛ. Тем не менее он должен начинаться как можно раньше. К наиболее эффективным методам относят метод спонтанного дыхания через Т-трубку, вентиляцию в режиме поддержки давлением и НВЛ. Необходим учет следующих факторов: избегать алкалемии; избегать чрезмерной седации больного; необходимо минимизировать работу дыхательного аппарата во время процесса отлучения.
Кроме основных медикаментозных средств, применяемых для купирования обострений ХОЗЛ, больным данной категории назначаются также дополнительные. Для профилактики венозного тромбоэмбо- лизма предпочтительнее использовать низкомолекулярный гепарин. Для предупреждения стрессовых язв и желудочно-кишечных кровотечений — сукральфат или Н2-блокаторы. Используются также методы физической терапии (массаж, постуральный дренаж, вибрация грудной клетки) и дополнительное питание (энтеральное или парентеральное).
Критерии выписки больных из стационара:
- стабильное состояние не менее 12 часов;
- стабильные показатели газового состава крови не менее 12 часов;
- уменьшение потребности в р2-агонистах (не чаще чем каждые 4 часа);
- пациент способен передвигаться по палате, принимать пищу, спать без частых ночных пробуждений от одышки;
- имеются условия для дальнейшего наблюдения и лечения дома, в том числе пациент и члены семьи, осуществляющие уход, обучены приемам амбулаторной терапии.
В дальнейшем больной должен находиться под пристальным вниманием врача, быть осмотрен в течение 4-6 недель, повторно обследован: ОФВ1, сатурация кислорода. Оценивается адаптация к повседневной жизни и потребность в длительной оксигенотерапии. Как правило, если больной получал оксигенотерапию в стационаре, она должна быть продолжена в течение 1-3 месяцев после выписки. В этот период к базисной добавляется физическая терапия.
Таким образом, инфекции бронхиального дерева являются ведущей причиной обострений ХОЗЛ. Назначение антибактериального препарата следует расценивать как способ не только купирования текущего обострения, но и профилактики последующих обострений ХОЗЛ. Цель антибиотикотерапии заключается в эрадикации возбудителя. Эмпирическая антибактериальная терапия, назначаемая при обострениях ХОЗЛ, не является хаотическим подходом и должна быть основана на местных эпидемиологических данных о спектре возбудителей и их чувствительности к антибактериальному препарату. При этом не существует ни одного идеального препарата, который действовал бы на весь спектр потенциальных возбудителей. В настоящее время основное значение для терапии обострений ХОЗЛ имеют антимикробные препараты групп р-лактамов, макроли- дов и фторхинолонов. В большинстве случаев антибактериальные препараты могут быть назначены перорально, кроме тяжелых случаев, требующих интенсивной терапии. Длительность терапии определяется тяжестью состояния пациента и фармакологическими свойствами медикаментов.
Существенную проблему составляют рецидивы обострений ХОЗЛ. Тяжесть заболевания является одной из важных причин рецидива. Связь между выраженностью бронхиальной обструкции и микробной колонизацией многие считают твердо установленной. Основные факторы риска рецидивирования — частые предыдущие обращения к врачу по поводу появления или усиления респираторной симптоматики, наличие сопутствующей кардиальной патологии, частые предшествующие обострения, выраженность исходной одышки, выраженность нарушений функции внешнего дыхания, неконтролируемая оксигенотерапия в домашних условиях. Идентификация факторов риска плохого ответа на ан- тибиотикотерапию позволяет строить программу с использованием современных антибактериальных препаратов и включать факторы риска рецидивов в рекомендации для врачей общей практики по ведению данной категории пациентов.
Профилактика обострений ХОЗЛ есть не что иное, как основная, базисная (или стратегическая) терапия, обязательно включающая вакцинопрофилактику и физическую реабилитацию, основной целью которой является сохранение качества жизни и уменьшение скорости снижения бронхиальной проходимости.







Комментировать