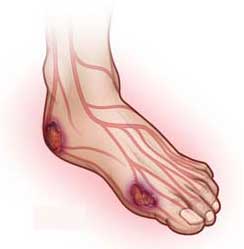
Тема хирургического лечения гнойно-некротических осложнений синдрома диабетической стопы. Результаты проведенных исследований.
Е.В. Ефимов, ГБОУ ВПО «Саратовский государственный медицинский университет»
Проблема лечения больных с критической ишемией нижних конечностей на фоне сахарного диабета является сложной и нерешенной. Несмотря на значительный прогресс в сосудистой хирургии, применение эндоваскулярных и открытых методов реваскуляризации, частота выполняемых ампутаций на уровне голени и бедра не имеет значимой тенденции к снижению. Техника выполнения ампутации как таковая хорошо отработана, вместе с тем частота развития специфических и неспецифических послеоперационных осложнений остается очень высокой [1, 17, 20]. По данным разных исследований, частота послеоперационных осложнений при ампутации бедра выше коленного сустава составляет от 38 до 60%, а летальность, даже в крупных центрах, составляет до 44% [8, 18, 21, 22]. Нередко в послеоперационном периоде возникает нагноение послеоперационной раны культи, необходимость в реампутации. Летальный исход у больных пожилого и старческого возраста, как правило, является результатом сердечно-сосудистых осложнений, сепсиса, пневмонии и печеночно-почечной недостаточности.
Тема хирургического лечения гнойно-некротических осложнений синдрома диабетической стопы является актуальной, в печати имеется большое количество исследований, защищены диссертации, однако до настоящего времени в литературе нет чётко сформулированных показаний к высокой ампутации при диабетической гангрене. Широкий спектр мнений в этом вопросе обусловлен объективными трудностями – затруднениями в определении жизнеспособности тканей, что и является причиной нагноения культи и прогрессирования некроза и последующей реампутации.
Российский консенсус по диагностике и лечению пациентов с критической ишемией рекомендует опираться на показатели чрескожного напряжения кислорода при определении уровня ампутации [8]. Эта позиция близка ряду российских исследователей, таких как В.А. Митиш [19], М.Д. Дибиров [9, 10]. Однако ряд исследований свидетельствует о том, что данный показатель не является абсолютным [11, 12, 16].
Другие исследователи, в том числе Н.Г. Степанов [21], базируясь на своём диссертационном исследовании, утверждает, что выбор уровня ампутации зависит от клинических показателей, таких как кровоточивость мышц, отек и показатели ультразвукового сканирования сосудов.
Не все разделяют данную точку зрения. Ультразвуковое исследование, безусловно, является золотым стандартом обследований данной категории больных.
Однако предоставленная информация отражает характеристики пульсовой волны в магистральных сосудах и не отражает состояние сосудов микроциркуляции.
Более информативные исследования – сцинтиграфия и другие – дороги и не могут использоваться в рутинной работе общехирургических стационаров [23, 28, 32].
Другой проблемой хирургического лечения диабетической гангрены после определения уровня ампутации является выбор способа операции. Дело в том, что выполнение ампутации конечности на уровне бедра весьма травматично. В результате операции образуется большая раневая поверхность, нарушается функция тазобедренного сустава, снижается способность к передвижению пациента. В момент выполнения операции хирург не имеет возможности думать об опороспособности культи для последующего протезирования, так как борьба за каждый сантиметр бедра повышает риск прогрессирования некроза и нагноения раны [8].
Один из наиболее острых дискуссионных вопросов – ведение послеоперационной раны культи бедра после ампутации: открытый способ или ушивание раны.
С одной стороны, как утверждает Pascone M. и соавт. [31], у больных с сосудистой патологией прошивание ткани ведет к ухудшению кровоснабжения и провоцирует образование полостей с экссудатом. Кроме того, мышцы разных групп имеют разную степень кровоснабжения и, по мнению авторов, требуют иссечения, после чего сшить мышцы-антагонисты не представляется возможным. В отечественной практике принято вести ампутационные раны закрытым способом, как рекомендуют А.Д. Гаибов [4], В.А. Митиш [18] и др.
Нельзя не упомянуть и разный взгляд авторов на проведение ампутаций. Так, ряд авторов предпочитают накладывать жгут перед операцией на бедро с целью предупреждения кровопотери, которая, по их мнению, и является одной из основных причин осложнений и летального исхода у больных на фоне анемии и гипопротеинемии [30, 34]. Другие исследователи, в том числе В.А. Митиш [18], категорически не рекомендуют накладывать жгут в связи с тем, что последний приводит к усугублению ишемии из-за разрушения путей коллатерального кровообращения. Данные исследователи рекомендуют в качестве альтернативы жгуту наложение пневматической манжеты.
Самым же спорным и острым вопросом, не решенным до настоящего времени, является проблема выбора между высокой ампутацией и использованием реваскуляризации в одном из возможных методов для сохранения конечности или максимального снижения уровня ампутации. Сторонники выполнения реваскуляризации, пропагандируя лозунг «две ноги не роскошь», утверждают, что современный уровень сосудистой хирургии позволяет даже при гнойно-некротическом процессе на стопе провести успешную реконструкцию кровотока и спустя небольшое время – некрэктомию. В этом лагере различия сводятся к подходу: выполнять некрэктомию первым этапом и затем реваскуляризацию, или сосудистая операция предваряет усечение конечности или некрэктомию. Сроки выполнения реваскуляризации также не определены [3, 5, 6, 13, 15].
Противники данной концепции в защиту своей позиции утверждают, что высокая ампутация после неудачной попытки реваскуляризации сопровождается увеличением риска инфекционных осложнений и намного утяжеляет операционный период. Реконструкция в группе больных СДС не всегда возможна вследствие типичной для этих больных микроангиопатии и отсутствия «путей оттока».
Реконструкция сосудистого русла как правило недолговечна, и в течение первого года у 11–20% больных, по данным А.М. Светухина [20] и других исследований [3, 10, 13, 27], формируется тромбоз сосуда или шунта и вновь стоит вопрос о необходимости ампутации у больного. Ряд авторов говорят, что частота ампутаций после реваскуляризации, проводимых в течение полугода, составляет 50 % [21, 22].
Анализ обращаемости пациентов, проведенный рядом авторов, свидетельствует о позднем обращении пациентов за медицинской помощью, увеличении числа дистальных и мультифокальных форм поражения артериального русла [5–7, 14].
Весьма спорным является и вопрос о качестве жизни больных после ампутации. Ряд авторов утверждают, что после ампутации на уровне коленного сустава протезом пользуются и ходят без труда 69,4 % больных, а после ампутации на уровне бедра – до 31 % больных [1, 3, 9, 31].
Н.Г. Степанов в своем исследовании установил, что из 99 больных, перенёсших ампутацию на бедре, 19 передвигаются на протезе, 31 – на коляске, 15 – на костылях, а 34 неподвижны и прикованы к кровати [21].
Сам процесс протезирования даже при малых ампутациях ограничен соматическим состоянием больных, в большинстве случаев это ограничено нарушениями зрения, перенесёнными инсультами, инфарктами миокарда, трофическими язвами в области культи, атрофией мышц и другими возрастными изменениями.
Нельзя забывать и об экономической целесообразности: при данном подходе стоимость лечения возрастает в несколько раз, но отдалённые результаты остаются неутешительными [30].
Таким образом, при анализе публикаций, посвящённых проблеме хирургического лечения синдрома диабетической стопы за последние 10 лет, можно сделать несколько выводов.
- Значительное количество исследований разработало подходы к лечению гнойно-некротических осложнений СДС с применением разных методов реваскуляризации.
- Вместе с тем ряд вопросов так и не нашли своё отражение в исследованиях, не имеют решения либо дискутабельны.
Так, до конца не решен вопрос о сроках выполнения операции, обоснованности и сроках проведения предоперационной подготовки, критериях выбора уровня операции, способах дренирования послеоперационной раны, целесообразности и длительности проведения антибактериальной терапии. Это требует проведения дальнейших исследований.
Источник: Журнал «Земский врач»
Литература
- Бенсман В.М. Хирургия гнойно-некротических осложнений диабетической стопы: руководство для врачей. – М.: Медпрактика, 2010. – 472 с.
- Брискин Б.С., Дибиров М.Д., Хамитов Ф.Ф. и др. Гнойно-некротические осложнения синдрома диабетической стопы и их отражение в МКБ-10 и стандартах страховой медицины // Хирургия. – 2007. – № 1. – С. 49–54.
- Гавриленко A.B., Скрылев С.И. Отдаленные результаты бедренно-подколенных шунтирований реверсированной веной и по методике in situ // Ангиология и сосудистая хирургия. – 2007. – Т. 13, № 3. – С. 120–124.
- Гаибов А.Д., Калмыков E.JL, Камолов А.Н. Ампутации нижних конечностей при их хронической критической ишемии. Обзор литературы // Кардиология и сердечно-сосудистая хирургия. – 2009. – № 2. – С. 40–46.
- Галстян Г.Р. Роль врача-интерниста в ведении больных с синдромом диабетической стопы // Медицинская кафедра. – 2004. – Т. 1, № 9. – С. 38–47.
- Гурьева И.В. Диабетическая стопа. Возможно ли эффективное предотвращение? // РМЖ. – 2001. – Т. 9, № 24. – С. 1122–1126.
- Дедов И.И., Удовиченко О.В., Галстян Г.Р. Диабетическая стопа. – М.: Практическая медицина, 2005. – 197 с.
- Диагностика и лечение пациентов с критической ишемией нижних конечностей: российские рекомендации. – М., 2007. – 156 с.
- Дибиров М.Д., Дибиров A.A., Гаджимурадов Р.У. и др. Дистальные реконструкции при критической ишемии нижних конечностей у больных старших возрастных групп // Хирургия. – – № 1. – С. 49–52.
- Дибиров М.Д., Брискин Б.С., Хамитов Ф.Ф. и др. Роль реконструктивных сосудистых операций у больных диабетической ангиопатией // Хирургия. – 2009. – № 2. – С. 59–63.
- Зеленов М.А. Ангиографическая семиотика и рентгено-хирургическая коррекция поражений артерий нижних конечностей у больных сахарным диабетом: автореф. дисс. … канд. мед. наук. – М., 2008. – 26 с.
- Зеленов М.А., Ерошкин И.А., Жуков А.О. и др. Баллонная ангиопластика и стентирование артерий нижних конечностей больных сахарным диабетом // Диагностическая и интервенционная радиология. – 2007. – Т. 1, № 4. – С. 71–80.
- Капутин М.Ю. Транслюминальная баллонная ангиопластика в лечении критической ишемии нижних конечностей: автореф. дисс. … д-ра мед. наук. – СПб., 2008. – 35 с.
- Коровин А.Я., Базалов С.Б. Хронологическая изменчивость микрофлоры ран и антибактериальная терапия у больных с гнойно-некротическими поражениями нижних конечностей при сахарном диабете // Инфекции в хирургии. – 2008. – Т. 6, № 4. – С. 47–49.
- Корымасов Е.А., Аюпов A.M., Пушкин С.Ю. и др. Реваскуляризация при синдроме диабетической стопы // Материалы международного симпозиума «Диабетическая стопа: хирургия, терапия, реабилитация». – СПб., 2008. – С. 53.
- Лисин С.В. Комплексное хирургическое лечение IV степени хронической артериальной недостаточности нижних конечностей атеросклеротической этиологии: автореф. дисс. … д-ра мед. наук. – М., 2008. – С. 137.
- Международное соглашение по диабетической стопе / Международная рабочая группа по диабетической стопе. – М.: Берег, 2000. – 96 с.
- Митиш В.А., Покровский A.B. Ампутации конечностей при ишемии // Клиническая ангиология. – М.: Медицина, 2004. – Т. 2. – С. 344–365.
- Митиш В.А., Ерошкин И.А., Галстян Г.Р. и др. Возможности комплексного хирургического лечения гнойно-некротических поражений нейроишемической формы синдрома диабетической стопы // Сахарный диабет. – 2009. – № 1. – С. 8–13.
- Светухин A.M., Земляной А.Б., Колтунов В.А. Отдалённые результаты лечения больных с гнойно-некротическими формами синдрома диабетической стопы //
- Хирургия. – 2008. – № 7. – С. 13–17.
- Степанов Н.Г. Качество жизни и ее продолжительность после ампутации // Ангиология и сосудистая хирургия. – 2004. – Т. 10, № 4. – С. 13–16.
- Bloomgarden Z.T. The diabetic foot // Diabetes Care. – 2008. – Vol. 31, № 2. – P. 372– 376.
- Boulton A.J.M., Cavanagh P.R., Rayman G. The foot in Diabetes. John Wiley and Sons, 2008. – 449 p.
- Canavan R.J., Unvin N.C., Kelly W.F., Connoly V.M. Diabetes and nondiabetes-related lower extremity amputation incidence before and after the introduction of better organized diabetes foot care // Diabetes Care. – 2008. 31, № 3. – P. 459–463.
- Caputo W. J. Surgical Management of the Diabetic Foot // Wounds. – 2008. – Vol. 20, № 3. – P. 74 – 83.
- Chen Hua-Fen, Ching-An Ho, Chung-Yi Li. Age and sex may significantly interact with diabetes on the risks of lower – extremity amputation and peripheral revascularization procedures // Diabetes Care. – 2006. – Vol. 29, № 11. – P. 2409–2414.
- Clayton W., Elasy T.A. A Review of the Pathophysiology, Classification, and Treatment of Foot Ulcers in Diabetic Patients // Clinical Diabetes. – 2009. 27, № 2. – P. 52–58.
- Conrad M.F., Cambria R.P., Stone D.H. et al. Intermediate results of percutaneous endovascular therapy of femoropopliteal occlusive disease: a contemporary series // Vascular Surgery. – 2006. – Vol. 44. – P. 762 – 769.
- Daniels T., Tamir E. Surgical treatment of diabetic foot complications: clinical review // Geriatrics Aging. – 2006. – Vol. 9, № 7. – P. 499–504.
- De Godoy J.M.P., de Godoy M.F., Batigalia F. et al. Lower-extremity amputation: a 6-year follow up in Brazil // Orthopaedic Surgery. – 2005. – Vol. 13, № 2. – P. 164–165.
- Deneuville M., Perrouillet A. Survival and quality of life after arterial revascularization or major amputation for critical leg ischemia in Guadeloupe // Annals of Vascular Surgery. – 2006. – Vol. 20, № 6. – P. 1–8.
- Pascone M., Papa G., Ranieri A. Use of a Novel Hydrosurgery Device in Surgical Debridement of Difficult – to – Heal Wounds // Wounds. – 2008. – Vol. 20, № 5. – P. 139 – 146.
- Zgonis T., Stapleton J.J., Roukis T.S. A stepwise approach to the surgical management of severe diabetic foot infections // Foot and Ankle. – 2008. – Vol. 1, № l. – P. 46–53.
- Zgonis T., Stapleton J.J. Innovative techniques in preventing and salvaging neurovascular pedicle flaps in reconstructive foot and ankle surgery // Foot and Ankle. – 2008. – Vol. 1, № 2. – P. 97–104





Комментировать