Шмак А.И., Слобина Е.Л., Ревтович М.Ю., Котов А.А., Суслов Н.Л., Лобинский А.А., Лашкевич С.В.
РНПЦ онкологии и медицинской радиологии им. Н.Н. Александрова МЗ РБ
Актуальность проблемы разработки новых подходов к лечению рака поджелудочной железы обусловлена, с одной стороны, достаточно высокими показателями заболеваемости и отчетливой тенденцией к ее росту в последние десятилетия как у нас в стране [1], так и за рубежом [18]. С другой стороны, несмотря на разработку и внедрение новых, а также усовершенствование существующих подходов к лечению данной патологии, отдаленные результаты лечения остаются удовлетворительными [22]. Рак поджелудочной железы по-прежнему рассматривают как практически фатальное заболевание [18, 23].
Неудовлетворительные результаты предложенных вариантов лечения связывают со следующими особенностями:
1. Для данной формы рака характерно биологически обусловленное крайне агрессивное течение. Выявляемые «клинически ранние» опухоли являются биологически поздними, сопровождаются большим числом скрытых метастазов. При иммуноцитохимическом исследовании у 33% больных резектабельным раком поджелудочной железы без клинически определяемых метастазов обнаруживаются микрометастазы опухоли по брюшине и у 43%– в костном мозге [20].
2. По данным молекулярного исследования, у подавляющего большинства больных резектабельным раком поджелудочной железы обнаруживается поражение регионарных лимфоузлов (около 90%) [9], более чем у 50% имеется периневральная опухолевая инвазия за пределами железы [5, 44].
3. Описаны факты мультицентрического роста опухоли в поджелудочной железе и способность опухолевых клеток распространяться по панкреатическому протоку с формированием метастатических очагов в других отделах поджелудочной железы. По данным некоторых исследователей, это наблюдается в 30–38% случаев [34, 43].
Таким образом, при кажущейся радикальности любая операция, предпринятая по поводу рака поджелудочной железы, носит характер циторедуктивной, обуславливая паллиативный характер лечения и его неудовлетворительные результаты. Поэтому прогрессирование заболевания после так называемого «радикального» лечения является скорее правилом, нежели исключением. При этом при прогрессировании заболевания в трети случаев развивается изолированный локорегионарный рецидив, в трети случаев– только отдаленные метастазы, в трети их сочетание [4, 23, 43, 44].
В связи с этим оправдана необходимость применения комбинированных и комплексных методов воздействия на опухолевый процесс в поджелудочной железе. Наибольшее распространение в комплексе лечебных мероприятий как дополнение к радикальной операции получила одновременная химиолучевая терапия (ХЛТ) как в неоадъювантном, так и в адъювантном режимах. Остановимся подробнее на каждом из этих вариантов.
Неоадъювантная химиолучевая терапия
В основе неоадъювантного лечения лежит предоперационное применение дистанционной лучевой терапии (ДЛТ) либо самостоятельно, либо одновременно в сочетании с химиотерапией (ХТ). Ожидаемыми эффектами неоадъювантной химиолучевой терапии (НХЛТ) являются:
1. Уменьшение размеров опухоли и, соответственно, увеличение процента резектабельных опухолей.
Кроме того, рестадирование опухоли после окончания ХЛТ позволяет избежать ненужных лапаротомий у пациентов с прогрессированием заболевания несмотря на проводимую ХЛТ. Иными словами, НХЛТ может позволить выявить группу больных, у которой можно рассчитывать на положительный эффект от проводимых лечебных мероприятий, в том числе в случае назначения адъювантной ХЛТ.
2. Снижение имплантационной способности опухолевых клеток, которые выбрасываются в кровоток во время операции, и, таким образом, уменьшение частоты локальных рецидивов [32].
3. Около 25% больных не получают адъювантного лечения после радикального хирургического лечения или получают его не в срок из-за развившихся хирургических осложнений, ослабленного состояния больных и отказа от дальнейшего лечения [11]. В то же время неоадъювантная терапия может быть применена у подавляющего большинства пациентов.
4. Степень постлучевого патоморфоза, как ответа на проведенную терапию (по данным морфологического исследования), позволяет судить об эффективности выбранной схемы лечения и прогнозе заболевания в каждом конкретном случае [32].
Большинство авторов указывают на хорошую переносимость неоадъювантного лечения. Более того, имеются сообщения об уменьшении числа хирургических осложнений (панкреатитов и несостоятельности панкреатикоэнтероанастомоза) после проведения предоперационной лучевой терапии [11, 32,40].
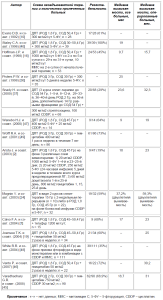
На сегодняшний день в литературе отсутствуют указания на проведение рандомизированных исследований НХЛТ при раке поджелудочной железы. Опубликованные данные нерандомизированных исследований свидетельствуют об увеличении резектабельности процесса до 30% по сравнению с исходным уровнем и увеличении медианы выживаемости до 15–32 мес. (табл.1). Недостатком этих исследований является небольшое количество наблюдений и отсутствие рандомизации.
Таблица 1. Результаты НХЛТ у больных резектабельным раком поджелудочной железы
Впервые об использовании предоперационной одновременной ХЛТ в комплексном лечении рака поджелудочной железы сообщил D.B. Evans и соавт. (1992) [10]. В данном исследовании 28 больным проведена ХЛТ в РОД 1,8 Гр, СОД 50,4 Гр на фоне длительных инфузий 5-ФУ в дозе 300 мг/м2/сут. Через 4–5 нед. после окончания ХЛТ было проведено рестадирование заболевания, у 5 пациентов выявлены отдаленные метастазы. Из оставшихся 23 резекция произведена 17 больным (48%). Авторы сообщили о хорошей переносимости НХЛТ, что послужило основой для выработки стратегии неоадъювантного лечения в дальнейшем. В пилотном исследовании Hoffman и соавт. (1998) [16] пациенты получали длительные инфузии 5-ФУ в дозе 1000 мг/м2/сут и митомицин С в дозе 10 мг/м2/сут, ЛТ в РОД 1,8 Гр, СОД 50,4 Гр. Медиана выживаемости для больных после удаления опухоли составила 45 мес., безрецидивная – 27 мес. На основании данного сообщения, ECOG провела собственное исследование на 53 пациентах [17], при этом результаты оказались несколько хуже: 24 больным выполнено удаление опухоли с медианой выживаемости 15,7 мес. против 9,7 мес. во всей группе.
Несмотря на многообразие предложенных схем неоадъювантной терапии (табл. 1), на сегодняшний день ни одна из них не признана оптимальной для лечения рака поджелудочной железы и, следовательно, не может рассматриваться в качестве стандарта. Тем не менее, как показывает анализ литературы, несколько лучшие результаты были получены при использовании гемцитабина. Включение гемцитабина в схему НХЛТ сопровождалось увеличением медианы выживаемости до 26–34 мес. [11, 29, 42] по сравнению с паклитакселом и 5ФУ, когда этот показатель составлял всего лишь 19 мес. [30, 31]. Это может быть объяснено наличием у гемцитабина радиосенсибилизирующих свойств, повышающих эффективность ХЛТ и позволяющих снизить количество локорегионарных рецидивов, улучшив, таким образом, результаты лечения. Логично было бы ожидать увеличением медианы выживаемости при использовании комбинации гемцитабина с другими химиопрепаратами, тем не менее, сочетание гемцитабина и цисплатина не улучшало отдаленных результатов лечения [45].
Одним из негативных моментов проведения НХЛТ является увеличение продолжительности предоперационного периода, что может отрицательно сказаться на результатах лечения. Сократить длительность предоперационной ХЛТ можно применением режимов гипофракционирования дозы лучевой терапии, чему посвящено несколько исследований. В частности, гипофракционирование дозы одновременно с введением гемцитабина проводилось в исследовании D.B. Evans и соавт. [11] (РОД 3 Гр, СОД 30 Гр, гемцитабин 400 мг/м2), W.Jr. Small и соавт. [36] (РОД 2,4 Гр, СОД 36 Гр, гемцитабин 1000 мг/м2). Получены обнадеживающие результаты: в первом исследовании медиана выживаемости для всей группы составила 22,7 мес. с пятилетней выживаемостью 27%; у больных, перенесших резекцию, – 34 месяца и 36% соответственно, что сопоставимо с данными, приведенными в табл. 1, при классическом фракционировании. В другом исследовании авторы сообщили о 73% однолетней выживаемости в общей группе, после удаления опухоли – 94%. В исследовании T.M. Breslin и соавт. [6] указал на отсутствие различий в переносимости и эффективности при лечении стандартными (1,8 Гр, 28 сеансов) и крупными (3 Гр, 10 сеансов) фракциями ЛТ. Следовательно, увеличение продолжительности предоперационной ХЛТ не оказывает негативного влияния на резектабельность первичной опухоли. В подтверждение этого вывода можно привести результаты исследования G.R. Varadhachary и соавт. [45], который сравнил предоперационную ДЛТ в сочетании с гемцитабином с комбинацией ДЛТ + гемцитабин + цисплатин.
Несмотря на большую продолжительность предоперационного периода в последнем случае, авторы не отметили статистически достоверных различий в частоте резектабельности, которая составила 68% при использовании сочетания гемцитабин + цисплатин и 75% при использовании гемцитабина (р = 0,27).
В противоположность вышеупомянутым положительным отзывам о НХЛТ в литературе имеются сообщения о недостаточной ее эффективности. В частности, P. Vento и соавт. (2007) [46] сообщает об отсутствии статистически значимых различий в медиане выживаемости, которая составила 27 мес. в группе НХЛТ и 20 мес. в группе хирургического контроля. Кроме того, авторы отмечают, что НХЛТ является фактором, предрасполагающим к развитию послеоперационных осложнений, которые составили 45% (в группе хирургического контроля – 32%). Отсутствие статистической разницы может быть объяснено небольшим количеством пациентов в исследовании (общее число наблюдений 30). Тем не менее, несмотря на вывод о неэффективности НХЛТ, продолжительность жизни в основной группе в данном исследовании была выше, чем в контрольной.
Для окончательного вывода об эффективности неоадъювантной терапии необходимы многоцентровые рандомизированные исследования. Учитывая большую медиану выживаемости после НХЛТ по сравнению с адъювантной химиолучевой терапией (АХЛТ), о чем будет сказано ниже, не исключено, что в будущем НХЛТ станет стандартом комбинированного лечения рака поджелудочной железы. В отсутствие таких масштабных исследований роль неоадъювантной терапии в лечении больных раком поджелудочной железы остается недоказанной, несмотря на положительные отзывы использовавших ее онкологов.
Адъювантная химиолучевая терапия
На сегодняшний день опубликовано достаточно большое количество данных как рандомизированных, так и нерандомизированных исследований АХЛТ при раке поджелудочной железы. При этом вопрос о целесообразности включения АХЛТ в комплекс лечения больных раком поджелудочной железы остается открытым.
Первое рандомизированное исследование выполнено в США Группой изучения гастроинтестинального рака GITSG (10) в 1974–1982 гг. [21]. При этом сравнивались 2 группы: ХЛТ – 21 больной и наблюдения – 22 пациента. В первой группе проводился расщепленный курс ЛТ в СОД 40 Гр на фоне 2 курсов болюсного введения 5-ФУ 500 мг/м2/день в течение 3 дней, затем в течение 2 лет (или до прогрессирования заболевания) курсы введения 5-ФУ повторялись каждые 4 недели. Исследование продемонстрировало статистически значимое (р = 0,03) улучшение выживаемости в группе адъювантного лечения: медиана выживаемости составила 20 мес. в сравнении с 11 мес. в группе наблюдения, двухлетняя выживаемость – 42 и 15% соответственно. Необходимо отметить небольшие группы сравнения и несоблюдение дизайна исследования во многих центрах. Несмотря на это, данное исследование послужило основой для выработки стандарта лечения, особенно в США, и эталоном для дальнейших исследований.
Аналогичное исследование (но без длительной монохимиотерапии 5-ФУ) проведено Европейской организацией по исследованию и лечению рака (EORTC 40891) в 1987–1995 гг.: мультицентровое рандомизированное исследование с включение пациентов не только с протоковой аденокарциномой,но и опухолями панкреатодуоденальной зоны [22]. Однако при повторном анализе результатов, проведенном M.C. Garofalo и соавт. (2006) [12] с использованием одностороннего log-rank теста против двустороннего, было отмечено статистически значимое улучшение выживаемости в группе адъювантного лечения больных раком головки поджелудочной железы – двухлетняя выживаемость 37% против 23% в группе наблюдения.
Несмотря на первые положительные отзывы об АХЛТ при раке поджелудочной железы, на сегодняшний день имеются данные об ее недостаточной эффективности. В частности, опубликованный в 2004 г. доклад европейской группы по изучению рака поджелудочной железы ESPAC-1 поставил под сомнение эффективность АХЛТ [26, 27]. Исследование было проведено в 1994–2000 гг. (61 центр в 11 странах) и включало 289 пациентов с протоковой аденокарциномой после R0/R1 резекции, рандомизированных по схеме факториального анализа 2 х 2 (сравнение больных с/без ХЛТ, с ХТ/без ХТ) в 4 группы: 1) ХЛТ – 73 человека; 2) ХТ –75; 3) ХЛТ с последующей ХТ – 72; 4) группа наблюдения – 69 больных. Пациентам первой группы проводилась ХЛТ по схеме GITSG без последующей монохимиотерапии; больным второй группы – болюсное введение 5-фторурацила 425 мг/м2/день с лейковорином 20 мг/м2/день в течение 5 дней подряд, каждые 28 дней, 6 циклов; третьей группы – ХЛТ как в 1-й группе с последующей ХТ как во 2-й группе. При анализе не получено преимущества в выживаемости в группе ХЛТ по сравнению с группой без ХЛТ (медиана выживаемости 15,9 мес. против 17,9 мес., двухлетняя выживаемость 29% против 41%, а пятилетняя – 10% против 20%, (р = 0,05)), а адъювантная ХТ продлила жизнь больным (медиана выживаемости 20,1 мес. против 15,5 мес., двухлетняя выживаемость 40% против 30%, р = 0,009). Более того, авторы констатировали, что успех ХТ в продлении жизни пациентов уменьшается после проведения дополнительной ХЛТ.
Однако достоверность выводов можно поставить под сомнение из-за следующих недостатков исследования:
- отсутствие единого стандарта лучевой терапии в отношении доз и полей облучения;
- отсутствие централизованного контроля за проведением лечения;
- несоблюдение режимов адъювантного лечения во многих центрах;
- около 30% больных не закончили лечение.
В 2006 г. было сообщено о результатах III фазы исследования RTOG 97-04, проведенного в США в 1998–2002 гг. на 538 больных раком поджелудочной железы (локализация в головке – у 381 пациента) [32]. Дизайн исследования: 3-недельная ХТ, затем ХЛТ, затем 3-месячная ХТ. Больные рандомизированы в 2 группы по виду ХТ: одной группе проводились 24-часовые инфузии 5-ФУ 250 мг/м2/ сутки, другой – 30-минутное введение гемцитабина 1000 мг/м2/день. ХЛТ в обеих группах была одинаковой – РОД 1,8 Гр, СОД 50,4 Гр на фоне инфузий 5-ФУ 250 мг/м2/день. При анализе выживаемости больных раком головки поджелудочной железы получено статистически достоверно (р = 0,047) лучшие результаты в группе ХТ с применением гемцитабина (медиана выживаемости 36,9 против 20,6 мес., трехлетняя выживаемость – 32% против 21%).
Однако, несмотря на противоречия в оценке АХЛТ в рандомизированных исследованиях (GITSG, EORTC, ESPAC-1, RTOG 97-04), целый ряд одноцентровых нерандомизированных и ретроспективных исследований продемонстрировали преимущества АХЛТ. Так, в 2008 г. были опубликованы данные АХЛТ при лечении протоковой аденокарциномы в клинике Мейо в 1975–2005 гг. [8]: 274 пациентам проводилась ХЛТ в СОД 50,4 Гр на фоне введения 5-ФУ, из них 28 больным после окончания ХЛТ проведена дополнительная ХТ 5фторурацилом. Результаты исследования свидетельствовали об увеличении выживаемости в группе АХЛТ по сравнению с группой хирургического контроля (180 пациентов) – медиана выживаемости 25,2 мес. против 19,2 мес. в группе сравнения, двухлетняя выживаемость – 50% против 39% (р = 0,01), пятилетняя выживаемость – 28% против 17%. Дополнительное проведение монохимиотерапии 5-ФУ еще более улучшило выживаемость больных (медиана выживаемости 34 мес., двухлетняя выживаемость 61%, а пятилетняя – 34%). При сопоставлении результатов предоперационной ХЛТ с данными клиники Мейо [8] можно сделать вывод, что дополнительная ХТ после завершения курса АХЛТ делает сопоставимой результаты неоадъювантной и адъювантной ХЛТ. В доступной нам литературе мы не нашли данных о сравнительной оценке такого комбинированного подхода, поэтому проведение такого рода исследований представляется нам целесообразным.
В том же 2008 г. были опубликованы результаты проспективного исследования в клинике Johns Hopkins [15], выполненного в период с 1993 по 2005 г. В исследование вошли 616 пациентов, радикально оперированных по поводу протоковой аденокарциномы поджелудочной железы, из них 271 человек получил АХЛТ в РОД 1,8 Гр, СОД 50,4 Гр на фоне монохимиотерапии 5-ФУ. Было отмечено увеличение медианы выживаемости, а также показателей двухи пятилетней выживаемости – 21,2 мес. против 14,4 мес., 43,9% против 31,9% и 20,1% против 15,4% соответственно. Интересно, что включение в комплекс лечебных мероприятий АХЛТ сопровождалось увеличением показателей выживаемости у больных с такими неблагоприятными прогностическими факторами, как наличие опухолевого роста в краях резекции поджелудочной железы (R1), наличие метастазов в лимфоузлах, размер опухоли более 3 см, степень злокачественности опухоли 3 и 4, наличие сопутствующей патологии, сахарного диабета, послеоперационных осложнений. Эти данные согласуются с упомянутыми выше результатами клиники Мейо. Практически аналогичные результаты, демонстрирующие преимущества АХЛТ, сообщили J.E. Lim и соавт. [23] и J.A. Greco и соавт. [13].
Таким образом, проведение АХЛТ после R0/R1 резекций рака головки поджелудочной железы (протоковой аденокарциномы) имело своим результатом статистически достоверное увеличение медианы выживаемости, а также показателей двухи пятилетней выживаемости (в сравнении с пациентами без АХЛТ). Во-вторых, в случае применения АХЛТ продолжительность жизни больных была выше, несмотря на присутствие таких неблагоприятных прогностических факторов, как высокая степень злокачественности опухоли, наличие опухолевого роста в крае отсечения поджелудочной железы, наличие метастазов в региональных лимфоузлах. Принимая во внимание, что вышеперечисленные факторы при протоковой аденокарциноме встречаются достаточно часто и наличие их является скорее правилом, чем исключением, АХЛТ должна быть обязательным компонентом лечебных мероприятий после радикального хирургического лечения рака головки поджелудочной железы.
Заслуживает внимания предложение использования поддерживающей ХТ после завершения курса АХЛТ, поскольку такая модификация схемы лечения имеет своим следствием увеличение общей выживаемости более чем на 9 мес. [8].
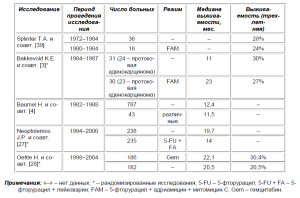
Вполне закономерен вопрос, какой из компонентов комплексного лечения рака поджелудочной железы (ЛТ или ХТ) в большей степени влияет на результаты лечения, и можно ли без ущерба отказаться от какого либо из компонентов. В большинстве схем адъювантного лечения рака поджелудочной железы используется комбинация ЛТ и ХТ. В литературе имеется достаточно небольшое количество исследований по изучению роли ХТ в адъювантном режиме (АХТ) (табл. 2).
Таблица 2. АХТ при раке поджелудочной железы
Splinter et al. [39] в начале 1980-х гг. пролечил 16больных по схеме FAM (5 курсов), группа исторического контроля составила 36 человек. Лечение переносилось плохо, 8 пациентов получили менее 60% от планируемой дозы химиопрепарата (4 человека – менее 20%, 4 – приблизительно 50–60%).
Улучшения выживаемости не произошло, и использованная авторами схема ХТ была признана неудачной ввиду увеличения количества осложнений.
Первое рандомизированное исследование было проведено в Норвегии K.E. Bakkevold и соавт. [3]: 61 больной раком панкреатодуоденальной зоны (из них 47 – раком поджелудочной железы) после радикальной операции рандомизированы в 2 группы – ХТ (30 пациентов) по схеме FAM (500 мг/м2, 40 мг/м2, 6 мг/м2 митомицин С) или наблюдения. Долговременный прогноз был аналогичным представленному в исследовании Splinter и соавт. с практически идентичной выживаемостью: одно-, двух-, трехи пятилетняя выживаемость в основной группе составила 70, 43, 27 и 4% против 45, 32, 30 и 8% в контрольной группе. ПХТ была довольно токсичной, из-за осложнений лечения умер 1 больной, доложено о 4 случаях сепсиса; 16 пациентам потребовалась госпитализация после первого курса ХТ. Оценка эффективности адъювантного лечения изолированно для больных раком поджелудочной железы не проводилось.
H. Baumel и соавт. [4] (Французская ассоциация хирургов) доложил о результатах лечения 787 больных операбельным раком поджелудочной железы за период с 1982 по 1988 г.: 43 человека получили АХТ (единого стандарта лечения не было), 127 после операции проведена ЛТ (или ХЛТ), 527 пациентов составили группу наблюдения. АХТ не улучшила выживаемость больных раком поджелудочной железы (медиана выживаемости составила 11,5 мес. против 12,4 мес. в группе наблюдения). Таким образом, АХТ, увеличивая продолжительность безрецидивного периода в течение 2 лет после радикальной операции, не влияла на отдаленные результаты лечения, что согласуется с данными, полученными K.E. Bakkevold и соавт. [3].
В упомянутом ранее европейском исследовании ESPAC-1 [26, 27] помимо 285 больных, рандомизированных по схеме факториального анализа 2 х 2, включены 256 пациентов, сравниваемых по одному отличительному признаку (фактору). В целом 235 человек получили ХТ в режиме 5-FU + FA, 235 больным ХТ не проводилась, с достоверным улучшением результатов лечения: медиана выживаемости в первой группе составила 19,7 мес. против 14 мес. без ХТ. Переносимость ХТ была значительно лучше, чем в исследовании K.E. Bakkevold и соавт. [3], лишь с 1 смертью от лечения, токсичность 3–4 степени зарегистрирована у 24% больных, что потребовало снижения дозы у 22%. Из 541 пациента, включенного в исследование, у 101 (19%) операция была нерадикальной (R1). Эффективность АХТ в этой группе была меньше (медиана выживаемости 11 мес. против 10,3 мес. без ХТ) в сравнении с R0 группой (медиана выживаемости 20,7 мес. против 15,3 мес. без ХТ) [27]. Таким образом, в данном исследовании была доказана эффективность АХТ после радикальных операций.
Более оптимистичными выглядят результаты исследования CONCO-001 [28], проведенного в Австрии и Германии. Рандомизировано 368 больных после R0/R1 операции по поводу рака поджелудочной железы, 186 из них проводилась АХТ гемцитабином (шесть 4-недельных курсов, 1000 мг/м2/день), 182 пациента без адъювантной терапии составили группу контроля. АХТ переносилась удовлетворительно (3–4 степень токсичности встречалась достаточно редко). В течение периода наблюдения, равного в среднем 53 мес., прогрессирование заболевания имело место у 133 больных (74%) основной группы и 161 пациента (92%) группы хирургического контроля. Медиана безрецидивной выживаемости была выше в основной группе как после R0 (13,1 мес. против 7,3 мес., р < 0,01), так и после R1 резекции (15,8 мес. против 5,5 мес.). Однако различий в основной и контрольной группах соответственно в медиане выживаемости (22,1 мес. против 20,2 мес.), ожидаемой трехлетней (34% против 20,5%) и пятилетней выживаемости (22,5% против 11,5%) отмечено не было.
Таким образом, АХТ у больных раком головки поджелудочной железы увеличивает время до прогрессирования заболевания, не влияя на продолжительность жизни пациентов [3, 4, 28]. Подтверждением этому являются результаты метаанализа 5 контролируемых рандомизированных исследований адъювантного лечения при протоковой аденокарциноме поджелудочной железы, опубликованного в 2005 г. [41]. Было констатировано снижение риска летальности при использовании АХТ на 25% с медианой ожидаемой продолжительности жизни 19 мес. (в отсутствие ХТ – 13,5 мес.). Актуриальные двухи пятилетняя выживаемость составили соответственно при АХТ 38 и 19%, в группе сравнения –28 и 12%. Эти данные свидетельствуют о достаточно высокой эффективности АХТ. В отношении АХЛТ авторы не отметили риска снижения летальности при ее применении, медиана выживаемости составила 15,8 мес. при АХЛТ против 15,2 мес., двухи пятилетняя выживаемость в основной группе и группе сравнения соответственно 30 и 12% против 34 и 17%. Как следует из представленной выше информации, АХЛТ имеет преимущество перед АХТ в плане улучшения отдаленных результатов лечения лишь при нерадикальной операции (R1), то есть при наличии опухолевого роста в крае резекции поджелудочной железы, а также при наличии других неблагоприятных прогностических факторов, как метастазы в регионарных лимфоузлах, высокая степень злокачественности опухоли. Вышеприведенные данные определяют показания для АХТ и АХЛТ, оставляя за АХТ только ситуации когда радикальность выполненной операции не вызывает сомнений.
Итак, в настоящее время необходимость адъювантной терапии резектабельного рака поджелудочной железы не подвергается сомнению, но нет единого мнения в отношении «стандартного» адъювантного лечения. Имеет место географическое различие: в Северной Америке предпочитают ХЛТ, ссылаясь на данные исследований GITSC и RTOG 97-04, в Европе же выбирают АХТ, основываясь на результатах ESPAC-1 и CONCO-001.
Комбинация неоадъювантной и адъювантной ХЛТ
Выбор метода лечения в неоадъювантном или адъювантном режимах до настоящего времени окончательно не определен. Приведенный выше обзор литературы свидетельствует о некоторых преимуществах неоадъювантного лечения в плане увеличения продолжительности жизни пациентов и т. д. Так, Snady и соавт. [37] сообщили о двух исследованиях, в которых доказывали преимущество мультимодальной терапии рака поджелудочной железы. В первом 68 больным раком поджелудочной железы проведено неоадъювантное лечение, включавшее расщепленный курс ЛТ одновременно с ХТ (5-фторурацил + стрептозоцин + цисплатин). После лечения у 22 пациентов достигнуто уменьшение размеров опухоли с переходом из местнораспространенной формы в резектабельную. Медиана выживаемости в группе составила 23,6 мес., у больных после операции – 32 мес. В тот же период другой группе из 91 пациента проведена радикальная операция, 63 из них получили послеоперационную ХТ или ХЛТ. Медиана выживаемости у больных в группе адъювантного лечения составила 16 мес., в группе только хирургического лечения –11 мес. Были сравнены эффективность адъювантной и неоадъювантной терапии в пользу последней. Подобные данные о преимуществе неоадъювантного лечения получены A.R. Sasson et al. в 2003 г. [35]. Сравнивались 2 группы – 61 больной неоадъювантного лечения и 55 – адъювантного. ХЛТ в обеих группах был одинакова – 50,4 Гр на фоне 5-ФУ с митомицином С или гемцитабином. Превосходство в медиане выживаемости неоадъювантной группы составило 23 мес. против 16 мес. адъювантной.
На данном этапе констатировать отсутствие преимуществ у АХЛТ по сравнению с НХЛТ невозможно из-за отсутствия рандомизированных исследований, доказывающих эффективность использования НХЛТ у больных раком поджелудочной железы.
С учетом накопленных данных, должны быть использованы положительные стороны как НХЛТ, так и АХЛТ, воздействие на возможные опухолевые очаги до и после операции в комплексном режиме с использованием цитостатических препаратов с разным механизмом действия. С этой целью в РНПЦ онкологии и медицинской радиологии им. Н.Н. Александрова разработан протокол лечения больных резектабельным раком головки поджелудочной железы, включающий предоперационную и послеоперационную ХЛТ с последующей адъювантной полихимиотерапией. Лечение проводится всем пациентам с морфологически верифицированным диагнозом. Лучевая терапия проводится в условиях трехмерного планирования, используется конформное фотонное излучение в режиме гипофракционирования дозы (РОД 4 Гр, СОД 28 Гр – эквивалент 40 Гр при стандартном фракционировании, 1 сеанс 1 раз в день 5 дней в неделю). Неоадъювантное лучевое лечение проводится на фоне постоянного приема фторафура 1200 мг/м/сут в качестве цитостатика и радиосенсибилизатора. В течение 3 сут после окончания предоперационной ХЛТ выполняется хирургический этап лечения (панкреатодуоденальная резекция), во время которого ложе удаленной опухоли, магистральные сосуды и оставшаяся железа маркируются скрепками. Через 4–6 недель после операции начинается адъювантная лучевая терапия в классическом режиме фракционирования дозы (РОД 2 Гр, СОД 30 Гр) одновременно с непрерывным приемом фторафура 1200 мг/м2/сут и болюсным введением бевацизумаба 5 мг/м2 1 раз в 2 недели. В объем облучения, помимо ложа опухоли и зон регионарного метастазирования, включается оставшаяся поджелудочная железа для воздействия на потенциальные опухолевые очаги в паренхиме железы. После окончания адъювантной лучевой терапии, химиотерапия в прежнем режиме продолжается в срок до 6 месяцев после операции. Первые результаты свидетельствуют о хорошей переносимости предложенной схемы лечения, токсичности 4 степени не было; при наблюдении больных в течение 1 года прогрессирования опухолевого процесса не выявлено.
Представленный обзор свидетельствует о напряженном поиске путей лечения больных раком поджелудочной железы во всем мире. Несмотря на многочисленность исследований, эта проблема далека от решения и требует разработки новых вариантов специального противоопухолевого лечения пациентов с данной патологией. В то же время для выяснения эффективности новых способов лечения необходимо проведение масштабных рандомизированных исследований.
ЛИТЕРАТУРА
1. Залуцкий И.В., Аверкин Ю.И. // Вес. Нац. Акад. навук Беларусi. – 2006. – № 1. – С. 5–11.
2. AristuJ., CañónR., PardoF. // Am. J. Clin. Oncol. –2003. – Vol. 26, N 1. – P. 30–36.
3. Bakkevold K.E., Arnesjo B., Dahl O., Kambestad B. // Eur. J. Cancer. – 1993. – Vol. 5. – P. 698–703.
4. Baumel H., Huguier M., Manderscheid J.C. et al. // Br. J. Surg. – 1994. – Vol. 81. – P. 102–107.
5. Beger H.G., Rau B., Gansauge F. et al. // World J. Surg. – 2003. – Vol. 27. – P. 1075–1084.
6. Breslin T.M., Hess K.R., Harbison D.B. et al. // Ann. Surg. Oncol. – 2001. – Vol. 8. – P. 123–132.
7. Calvo F.A., Matute R., Garcia-Sabrido J.L. et al. //Am. J. Clin. Oncol. – 2004. –Vol. 27. – P. 343–349.
8. Corsini M.M., Miller R.C., Haddock M.G. et al. // J.Clin. Oncol. – 2008. – Vol. 26, N 21. – P. 3478–3480.
9. Demeure M.J., Doffek K.M., Komorowski R.A., Wilson S.D. // Cancer. – 1998. – Vol. 83. – P.1328–1334.
10. Evans B.D., Rich T.A., Byrd D.R. et al. // Arch.Surg. – 1992. – Vol. 127. – P. 1335–1339.
11. Evans D.B., Varadhachary G.R., Crane C.H. et al.// J. Clin. Oncol. – 2008. – Vol. 26, N 21. –P. 3496–3502.
12. Garofalo M.C., Regine W.F., Tan M.T. //Ann.Surg. – 2006. – Vol. 244, N 2. – P. 332–333.
13. Greco J.A., Castaldo E.T., Feurer I.D. et al. // Gastrointestinal Cancers Symposium. – 2007. – Abstract N 109.
14. Hazard L., Tward J.D., Szabo A., Shrieve D.C. // Cancer. – 2007. – Vol. 110, N 10. – P. 2191–2201.
15. Herman J.M., Swartz M.J., Hsu Ch.C. et al. // J.Clin. Oncol. – 2008. – Vol. 26, N 21. – P. 3503–3510.
16. Hoffmann J.P., Weese J.L., Solin L.J. et al. // Am. J. Surg. – 1995. – Vol. 169. – P. 71–77.
17. Hoffmann J.P., Lipsitz S., Pisansky T. et al. // J.Clin. Oncol. – 1998. – Vol. 16. – P. 317–323.
18. Jemal A., Siegel R., Ward E. et al. // CA Cancer J. Clin. – 2006. – Vol. 56. – P. 106–130.
19. Joensuu T.K., Kiviluoto T., Karkkainen P. et al. // Int. J. Radiat. Oncol. Biol. Phys. – 2004. – Vol.60. – P. 444–452.
20. Juhl H., Kalthoff H., Kruger U. et al. // Chirurg. –1994 – Vol. 65. – P. 1111-1115.
21. Kalser M.H., Ellenberg S.S. // Arch. Surg. –1985. – Vol. 120. – P. 899–903.
22. Klinkenbijl J.H., Jeekel J., Sahmoud T. et al. // Ann. Surg. – 1999. – Vol. 230. – P. 776–782.
23. Lim J.E., Chien M.W., Earle C.C. // Ann. Surg. –2003. – Vol. 237. – P. 74–85.
24. Magnin V., Moutardier V., Giovannini M.H. et al. // Int. J. Radiat. Oncol. – 2003. – Vol. 55. – P. 1300–1304.
25. McDade T.P., Hill J.S., Simons J.P. et al. // ASCO Gastrointestinal Cancers Symposium. – 2009. –Abstract N 181.
26. Neoptolemos J.P., Dunn J.A., Stocken D.D. et al.// Lancet. – 2001. – Vol. 358. – P. 1576–1585.
27. Neoptolemos J.P., Stocken D.D., Friess H. et al. // N. Engl. J. Med. – 2004. – Vol. 350. – P. 1200–1210.
28. Oettle H., Post S., Neuhaus P. et al. // JAMA. –2007. – Vol. 297. – P. 267–277.
29. Palmer D.H., Stocken D.D., Hewitt H. et al. // Ann.Surg. Oncol. – 2007. – Vol. 14. – P. 2088–2096.
30. Pisters P.W.T., Abbruzzese J.L., Janjan N.A. et al.// J. Clin. Oncol. – 1998. – Vol. 16. – P. 3843–3850.
31. Pisters P.W.T., Wolff R.A., Janjan N.A. et al. // J.Clin. Oncol. – 2002. – Vol. 20. – P. 2537–2544.
32. Saif MW. // J. Pancreas. – 2006. – Vol. 7, N 4. – P.337–348.
33. Saif M.W. // J. Pancreas. – 2008. – Vol. 9, N 4. –P. 391–397.
34. Sarr M.G., Behrns K.E., van Heerden J.A. // Hepatogastroenterology. – 1993. – Vol. 40, N 5. – P. 418–421.
35. Sasson A.R., Wetherington R.W., Hoffman J.P. et al. // Int. J. Gastrointest. Cancer. – 2003. – Vol. 34, N 2–3. – P. 121–128.
36. Small W.Jr., Berlin J., Freedman G.M. et al. // J.Clin. Oncol. – 2008. – Vol. 26, N 6. – P. 942–947.
37. Snady H., Bruckner H., Cooperman A. et al. // Cancer. – 2000. – Vol. 5. – P. 314–327.
38. Spitz F.R., Abbruzzese J.L., Lee J.E. et al. // J.Clin. Oncol. – 1997. – Vol. 15. – P. 928–937.
39. Splinter T.A., Obertop H., Kok T.C., Jeekel J. // J.Cancer. Res. Clin. Oncol. – 1989. – Vol. 115. – P.200–202.
40. Staley C.A., Lee J.E., Clearly K.R. et al. // Am. J.Surg. – 1996. – Vol. 171. – P. 118–124.
41. Stocken D.D., Buchler M.W., Dervenis C. et al. // Br. J. Cancer. – 2005. – Vol. 92. – P. 1372–1381.
42. Talamonti M.S., Small W.Jr., Mulcahy M.F. et al. //Ann. Surg. – 2006. – Vol. 13. – P. 150–158.
43. van Heerden J.A., ReMine W.H., Weiland L.H. et al. // Amer. J. Surg. – 1981. – Vol. 142, N 3. – P.308–311.
44. van Roest M.H. et al. // Ann. Surg. – 2008. – Vol. 248, N 1. – P. 97–103.
45. Varadhachary G.R., Wolff R.A., Crane C.H. et al. // J. Clin. Oncol. – 2008. – Vol. 26. – P. 3487–3495.
46. Vento P., Mustonen H., Joensuu T. et al. // World.J. Gastroenterol. – 2007. – Vol. 13, N 21. – P.2945–2951.
47. Wanebo H.J., Glicksman A.S., Vezeridis M.P. et al. // Arch. Surg. – 2000. – Vol. 135. – P. 81–87.
48. White R.R., Hurwitz H.I., Morse M.A. et al. // Ann.Surg. Oncol. – 2001. – Vol. 8. – P. 758–765.
49. Wolff R.A., Evans D.B., Gravel D.M. et al. // Clin.Cancer. Res. – 2001. – Vol. 7. – P. 2246–2253.
50. Yeo C., Abrams R., Grochow L. et al. // Ann.Surg. – 1997– Vol. 225. – P. 621–633.
Данная статья взята из журнала «Медицинские новости», № 9, 2010.







Комментировать