Основні причини розвитку шоку у новонароджених. Класифікація шоку. Основні ланки патогенезу шоку. Основні клінічні прояви шоку у новонароджених. Діагностика шоку. Лікування шоку у новонароджених.
Визначення
Визначення шоку як нозологічної форми захворювання запропоновано ще в ХІХ столітті і, незважаючи на велику кількість цих визначень (більше сотні) та значну їх розбіжність, термін „шок” широко використовується в повсякденній практиці, бо він дає можливість правильно орієнтувати лікаря на загрозливу ситуацію, що склалася у хворого і потребує невідкладних профілактичних та лікувальних заходів.
На сучасному етапі шок -це збірне поняття, яке характеризує екстремальний стан організму, що розвинувся в результаті надзвичайної за силою або/чи тривалістю дії патологічного фактору і визначається комплексом патологічних порушень в діяльності усіх фізіологічних систем, порушенням життєво важливих функцій організму, переважно системного кровообігу, мікроциркуляції, метаболізму, ЦНС, дихання, ендокринної системи, гемокоагуляції.
Оскільки сьогодні визначальну роль в патогенезі шоку надається прогресуючій гострій недостатності тканинного кровообігу, то Лебедева Р. Н. визначає шок як специфічний, циркуляторно-метаболічний синдром, при якому порушення мікроциркуляції з наступним пошкодженням метаболізму клітин є провідними ланками в патогенезі, незалежно від причин, що призвели до порушення гомеостазу.
За МКХ – 10 визначають: Р 57.0 -кардіогенний шок, Р 57.1 -гіповолемічний шок, Р 57.8 -інші види шоку (ендотоксичний шок). Р 57.9 -шок не уточнений, А 41.9 -септичний шок, Т 79.4 -травматичний шок
Основні причини розвитку шоку у новонароджених.
1. Гіповолемія:
1.1 Гостре зменшення об’єму циркулюючої крові (ОЦК) внаслідок: відшарування плаценти; трансфузії крові від дитини до матері (підняття дитини вище рівня матки під час кесарського розтину особливо за відсутності переймів до операції тощо); фето-фетальної трансфузії у близнюків; внутрішньочерепної кровотечі; крововиливу у внутрішні органи – розрив печінки, селезінки, магістральних судин тощо; легеневої кровотечі; кровотечі із шлунково-кишкового тракту; кровотечі з катетера, культі пуповини; коагулопатії (геморагічної хвороби новонароджених, синдрому внутрішньосудинного згортання крові), хірургічних операцій.
1.2 Гостре зменшення об’єму рідини в організмі внаслідок: діареї будь-якої етіології; неадекватного діурезу (поліурії); швидкого виходу плазми в позасудинний простір (синдром „капілярного витікання”,СКВ); великих перспіраційних втрат при недостатньому надходженні рідини; втрати плазми (запальні процеси в черевній порожнині), операції на органах грудної і черевної порожнини, гастрошизису.
2. Сепсис.
3, Тяжка асфіксія.
4.Опіки.
5.Біль, травма.
6.Гострі кардіогенно-васкулярні порушення.
Класифікація шоку
В залежності від причини шок у новонароджених визначають як гіповолемічний, септичний (токсикоінфекційний) , асфіктичний, кардіоваскулярний, опіковий, больовий (травматичний).
Таблиця 1.
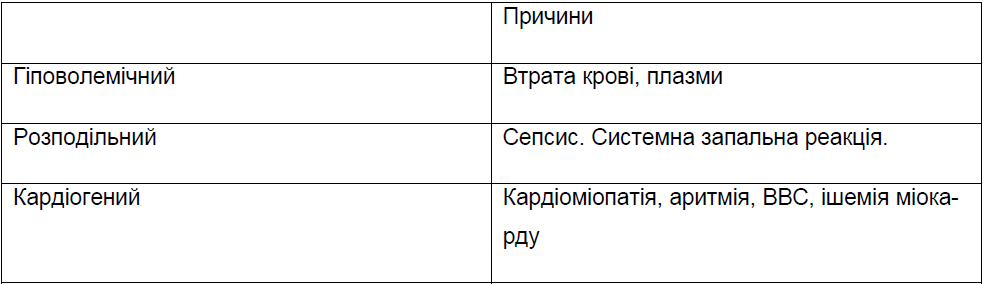
- Кардіогенний шок може розвинутись при порушеннях кровообігу, вадах серця, механічних перешкодах викиду крові і венозного повернення. Причиною кардіогенного шоку може бути персистуюча легенева гіпертензія, затримка закриття артеріальної протоки , дисфункія (ішемічна, гіпоглікемічна, септична, при ацидозі)) міокарду, міокардит, виражені порушення серцевого ритму, вроджена повна блокада серця, механічні перешкоди роботі серця або ж венозному поверненню (напружений пневмоторакс, діафрагмальна грижа, важка інтерстиціальна емфізема, тампонада серця, пневмоперікард, гідроперікард, гостра гіперволемія та інші).
- Гіповолемічний шок зумовлений гострим зменшенням внутрішньо-судинного об’єму крові при втратах крові, плазми, позаклітинної рідини або ж поєднанні цих факторів.
- Розподільний (дистрібутивний) шок розвивається внаслідок патологічного перерозподілу водних просторів в організмі, причиною розвитку якого у новонароджених найчастіше є сепсис, тяжка асфіксія.
В практичній діяльності лікаря окрім гіповолемічного, асфіктичного, септичного, кардіогенного шоку у новонароджених значно рідше але може розвинутись шок при опіках, від болю (політравма тощо).
Основні ланки патогенезу шоку
Анатомо-фізіологічні особливості новонароджених зумовлюють низку відмінностей як в патогенезі шоку так і його клінічних проявах. Це зокрема морфо-функціональна незрілість органів і систем, обмежені енергетичні резерви організму дитини, низькі компенсаторні можливості серцево-судинної, дихальної систем (наявність фетальних комунікацій) та інше. Слід приймати до уваги особливості їх нейровегетативної і гуморальної регуляції вітальних функцій, що зумовлює атиповість клінічних проявів шоку у новонароджених, затрудняючи його діагностику і прогноз.
Загальноприйнято вважати, що шок -це універсальний циркуляторно-метаболічний синдром при патологічних станах будь-якої етіології, коли стресовий фактор перевищує компенсаторні можливості організму, які забезпечують підтримку базального гомеостазу. Шок поняття поліетіологічне але монопатогенетичне. Відмінності спостерігаються лише на початку шоку, коли етіологічні фактори тісно пов’язані з патогенетичними. При прогресуванні синдрому етіопатогенетичні відмінності згладжуються і шок повільно переходить в критичну стадію. Для розвитку шоку характерно формування чисельних „хибних” кіл.
Взаємозв’язок патогенетичних реакцій і клінічної картини шоку розглядаємо дещо спрощено. Пусковим механізмом шокового процесу є кровотеча, гіпоксія, біль, ендо-, екзотоксини бактерій, віруси, серцева, циркуляторна недостатність, які призводять до зменшення серцевого викиду. Зменшення серцевого викиду є пусковим моментом шоку будь-якої етіології. На його зменшення включається механізм активації симпатоадреналової системи, підвищується рівень адреналіна і норадреналіна, що призводить до перерозподілу ОЦК – зменшення кровопостачання шкіри, підшкірної клітковини, нирок, шлунково-кишкового тракту, легенів, частково печінки за умови достатнього постачання життєво важливих органів – мозку, серця, наднирників, гіпофізу. Для цієї стадії шоку характерно нормальне або ж незначне збільшення у новонародженого артеріального тиску, частоти серцевих скорочень, кількості еритроцитів (“відносна поліцитемія”), зменшення або відсутність діурезу. Внаслідок спазму судин ємність судинного русла пристосовується до зменшеного ОЦК. Спазм судин є першою фазою шоку – фазою компенсації. Разом з тим, довготривале “відключення” шкіри, нирок, ШКТ, легень при централізації кровообігу з недостатнім надходженням в їх систему мікроциркуляції крові призводить до глибоких змін в їх капілярах і метартеріолах – розвитку “сладжу” еритроцитів, дисеминованого внутрішньосудинного згортання (ДВЗ), для якого є характерним тромбоцитопенія споживання (коагулопатія споживання), порушення проникливості стінок капілярів, з наступним розвитком глибоких змін в клітинах. Вважається, що ДВЗ є загальнобіологічним, неспецифічним компонентом циркуляторної недостатності будь -якого походження, а тому він відноситься до одних із маркерів розвитку шокової ситуації в організмі.
Таким чином, централізація кровообігу, як компенсаторна реакція на дію шокового фактора, доцільна лише на якомусь відрізку часу, бо згодом розвиваються тяжкі порушення в першу чергу в системі мікроциркуляції виключених органів, котрі при довготривалому існуванні призводять до незворотніх змін. За висновком Лябори Г. (1972) “незрозуміло, чому в еволюції людського організму продовжує існувати відповідна реакція на агресію шляхом вазоконстрікції, якщо остання зразу ж спонукає розвиток стількох неприємностей”.
Внаслідок змін в мікроциркуляції порушується функція клітинних мембран з наступним розвитком електролітного дисбалансу – порушенням обміну натрію, калію, кальцію, магнію, тощо.
Розвиваються глибокі зміни на клітинному рівні (вивільнення нейротрансміттерів, переоксидація ліпідів, білків, зростання кількості вільних радикалів, цитокінів, тощо), які спричиняють розвиток в організмі новонародженого синдрому “цитокінового хаосу”, зриву ауторегуляції, гемокардіодинаміки
Поглиблене вивчення змін в організмі при критичних станах не лише на системному але і органному, клітинному рівнях спонукало до визначення таких понять як „синдром системної запальної відповіді” (ССЗВ), яка є інтегральною частиною розвитку будь-якого критичного стану незалежно від причин його виникнення, з послідуючим розвитком поліорганної недостатності (Сулима Е. Г. 2001; Беляев А. В. 2005). Більш глибокі дослідження критичних станів організму ввели в клінічну практику поняття „синдрому капілярного витікання” (СКВ), який є одним з проявів критичного стану організму за умови реалізації ССЗВ, поліорганної недостатності (ПН). Так А. В. Беляев (2005) вказує, що під час критичного стану на відповідному етапі у хворих розвиваються нові закономірності обміну рідини між судинним простором і інтерстиціальним сектором, які внаслідок ССЗВ, взаємодії активованих лейкоцитів і ендотелія судин супроводжуються підвищеною капілярною проникливістю для білка, порушенням структури інтерстиціального простору і лімфатичного дренажу, що зумовлює стійке накопичення рідини в інтерстиції, призводить до порушення функцій органів і систем. Такий синдром він визначає як „синдром капілярного витікання”.
Виходячи з клінічних критеріїв СКВ визначених для дорослого організму, діагноз СКВ у новонароджених з розподільним (асфіктичним, септичним) шоком ми виставляємо на основі наступних клінічних проявів: нестабільність гемодинаміки на протязі 3-х днів життя за наявності трудно корегованої (рефрактерної) гіпотонії; збільшення маси тіла на >3% за 24 години; поява генералізованих набряків. Найчастіше СКВ розвивається у новонароджених з шоком зумовлених асфіксією, інфекцією (розподільний шок).
За тяжкістю перебігу виділяють наступні стадії шоку:
- Незворотна (критична) стадія шоку.
- Компенсована стадія.
- Некомпенсована стадія.
- Компенсована стадія шоку. Адекватна перфузія мозку, серця, наднирників, гіпофізу підтримується за рахунок підвищення артеріального судинного опору. Мають місце незначні зміни ЧСС, ЧД, АД, температури. Під дією підвищеної секреції ангіотензина і вазопресина нирки починають зберігати воду і натрій, а під дією підвищеного рівня катехоламінів збільшується скоротність міокарду. Для цієї стадії шоку характерно: блідість, зменшення часу наповнення капілярів (синдром „білої плями”), холодні кінцівки, може мати місце невелике підвищення артеріального тиску, частоти серцевих скорочень, кількості еритроцитів (“відносна поліцитемія”), зменшення або відсутність діурезу.
- Некомпенсована стадія шоку. Доставка кисню і метаболічних субстратів в тканини не забезпечує їх потреб і основним джерелом енергії стає анаеробний метаболізм. Це призводить до накопичення в організмі новонародженого молочної кислоти, зростання ацидозу. Ацидоз зменшує чутливість міокарду до дії катехоламінів і порушає його скоротливість. Тканинна гіпоксія і ацидоз змінюють метаболізм в клітинах і призводять до порушення функції практично у всіх органах (поліорганна недостатність), запускаючи багаточисельні «хибні кола», які ще більше поглиблюють катастрофу. Так, при довготривалій гіпоксії розвиваються глибокі зміни на клітинному рівні, порушується функція клітинних мембран, зростає кількість вільних радикалів, цитокінів, нейротрансмітерів та інших продуктів, які, згідно сучасних уявлень, є маркерами формування синдрому ”системної запальної відповіді” (ССЗВ). На сьогодні ССЗВ розглядається як маркер ( а за деякими авторами стадія) шоку. В цей час дезінтегрується робота капілярного ендотеліума, починається витікання плазми з судинного русла, розвивається СКВ , ДВЗ, олігоанурія.
Довготривале порушення в системі мікроциркуляції, коли сформувались ряд взаємозв’язаних „хибних” кіл (ДВЗ, ССЗВ, ПН,СКВ), на відповідному етапі призводить до некорегованого, одночасного відкриття великої кількості прекапілярніх сфінктерів ( синдром „відміни ауторегуляції”, СВА) в першу чергу в органах, які недостатньо забезпечувались кров’ю внаслідок централізації кровотоку. Це призводить до різкого розширення капілярної частини судинного русла, внаслідок чого в ньому може одночасно кумулюватися 30-40% ОЦК (замість фізіологічного 7-12%). В судинному руслі різко зменшується ОЦК в ємкісній (венозній) системі, що спричиняє зменшення венозного повернення крові до серця, а отже і зменшення серцевого викиду, хвилинного об’єму серця, розвитку гіпотонії і недостатнього забезпечення кров’ю всіх, в тому числі і життєво важливих, органів і систем. Швидке, не кореговане зменшення ОЦК до 40-50% може бути однією з основних причин зупинки серця і смерті при шоку.
3. Незворотна стадія шоку. Сьогодні цей стан організму часто визначають як критичний. Для нього характерно наявність в організмі глибоких змін в основних органах і системах (поліорганна недостатність); значні патологічні зміни не лише в судинному руслі, але і в клітинних мембранах, на клітинному рівні, формування каскаду „хибних кіл”, зокрема, ССЗВ, ДВЗ, СКВ, СВА тощо. Часто ця стадія шоку розвивається внаслідок недостатнього або/чи запізнілого проведення лікувальних заходів на попередніх стадіях шоку. Ми в практичній діяльності таку стадію шоку визначаємо не як „незворотну”, а як критичну, що дає надію на збереження життя дитини і доцільність проведення інтенсивних лікувальних закладів.
Основні клінічні прояви шоку у новонароджених
Тахікардія – ЧСС більше 160 ударів за хв., або брадикардія – ЧСС менше 100 ударів за хв..
Гіпотензія – середній артеріальний тиск (САТ) в мм ртутного стовпчика становить менше 45 при масі тіла у дитини більше 2501 г; менше 40 мм рт. ст. у дитини з масою тіла 1500-2500 г; менше 35 мм рт. ст.. у дитини з масою тіла 1001-1500 г; менше 30 мм рт ст. у дитини з масою тіла менше 1000 г.
Зниження периферійної перфузії – блідість при компенсованій стадії шоку, ціаноз – при некомпенсованій. Симптом „білої плями” більше 3 секунд (деякі автори критично оцінюють його діагностичну значимість). Холодні кінцівки, підвищення градієнта між центральною і периферійною температурою.
Зменшення діурезу – у першу добу життя менше 1 млкггодину, в наступні дні – менше 2 млкггодину.
Метаболічні порушення – ацидоз (компенсований, некомпенсований, переважно респіраторнометаболічний), схильність до гіпонатріємії, гіперкаліємії, гіпокальціємії, гіпопротенїмії, гіпоглікемії (але виражене підвищення рівня глюкози при її внутрішньовенному введені).
Зниження рівня насичення крові киснем (SaO2)
При компенсованій стадії шоку – збудження ЦНС, при некомпенсованій стадії – переважно пригнічення ЦНС, можливі судоми.
Ацидоз, гіпоксемія, артеріальна гіпотензія у новонароджених перших днів життя завдяки особливостям їх серцево-легеневої гемодинаміки ускладнюють перебіг шоку персистуючою легеневою гіпертензією.
Таблиця 2.
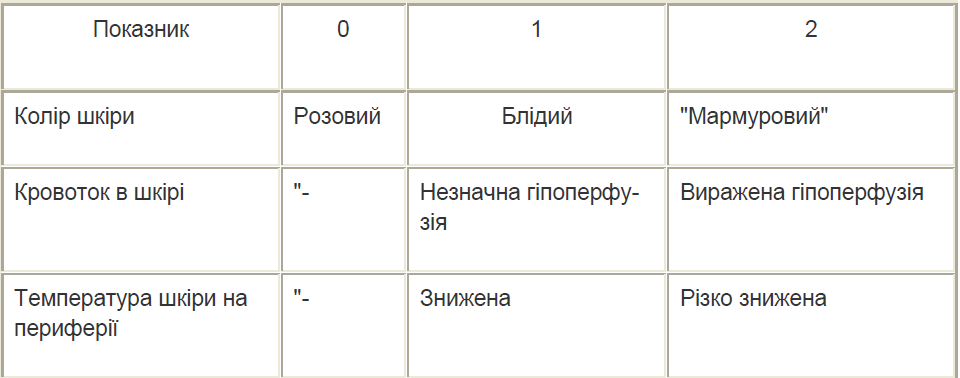
Оцінка 1-3 бала — легка ступінь шоку; 3-7 балів — середня; 7-10 балів – тяжка ступінь.
Діагностика шоку
К л і н і ч н і о з н а к и:
- Контроль температури тіла; характерно зниження шкіряної температури кистей і стоп при нормальній ректальній температурі,
- Кардіореспіраторний моніторинг; ЧСС – тахікардія, в термінальні стадії може бути брадикардія, гіпотензія, ознаки порушення мікроциркуляції (акроціаноз), гіпоперфузія тканин виражена не лише при низькому, але і підвищеному або ж нормальному артеріальному тиску, низький пульсовий тиск, пульс слабкого наповнення.Тахіпное або ж брадіпное.
- Контроль діурезу; зменшення діурезу (<2мл/кг/год і <1 мл/кг/год в перший день життя).
- Вимірювання центрального венозного тиску (ЦВТ) в одній із порожнистих вен. При оцінці ЦВТ слід приймати до уваги, що його величина переважно визначається ОЦК, станом насосної функції серця, судинного опору. У новонароджених величина ЦВТ коливається в межах 4-8 мм рт ст.; збільшення ЦВТ до 8-10 мм рт. ст. частіше обумовлено зменшенням насосної функції серця або ж перегрузкою рідиною (високий ЦВТ є однією з причин появи набряків), зниження ЦВТ (<4мм.рт.ст.) – переважно свідчить про недостатній ОЦК але і високе (нормальне) ЦВТ може бути і при гіповолемії. Слід враховувати відповідь на струйне введення 10 мл/кг 0,9% розчину NaCl (якщо шок зумовлений гіповолемією то буде зменшуватись тахікардія, підвищуватись САТ, ЦВТ, збільшиться темп діурезу).
Л а б о р а т о р н а д і а г н о с т и к а:
- Кислотно-лужний стан (КЛС), гази крові; зазвичай – метаболічний ацидоз, гіпоксемія, зменшення артеріовенозної різниці за О2.
- Гематокрит; зменшений при кровотечі, підвищений при втратах плазми (дозволяє орієнтовано вибрати трансфузійний засіб для інфузійної терапії).
- Клінічний аналіз крові з підрахунком лейкоформули (дозволяє виключити сепсис як причину гіпотензії).
- Визначення в крові вмісту глюкози, натрію , калію, кальцію (дозволяє виключити метаболічні причини гіпотонії).
- Ехокардіографія: за умови порушення скоротності міокарду слід ввести медикаменти, які збільшують серцевий викид.
- ЦВТ: вимірюється за допомогою катетера введеного в порожнисті вени вище купола діафрагми. Корекція низьких цифр ЦВТ (<4 мм рт. ст.) проводиться внутрішньовенним введенням розчинів для поповнення дефіциту ОЦК.
Лікування шоку у новонароджених
- Температура. Дуже важливо підтримувати температуру тіла у новонародженого в межах 36.5 -37.0 С0 при будь-якій стадії шоку. Найкраще, щоб дитина в критичному стані знаходилась в кувезі, менш сприятливим є відкритий пеленальний столик але лише за умови сервоконтролю температури.
- Підтримання адекватного газообміну. У новонароджених з шоком бажано підтримувати SaO2 на рівні 80 -90 %, PaO2 на рівні 80-100 мм рт. ст, а сатурацію змішаної крові (SvO2) — на рівні 70-75%. Перевагу слід надавати штучній вентиляції легень через ендотрахеальну трубку (особливо у новонароджених з розподільним шоком — септичним, асфіктичним) з використанням седативних препаратів, що дозволяє забезпечувати тканини киснем при некомпенсований і критичній стадії шоку. У детей з септичним шоком на работу дихальних м’язів може витрачатись від 15 до 30% поступального кисню, що сприяє збільшенню лактат-ацидозу. Рано розпочата ШВЛ покращує перерозподіл кровотоку в вітальні органи, дозволяє активно регулювати КЛС (зокрема, компенсувати метаболічний ацидоз дихальним алкалозом ).
У новонароджених з шоком важливо контролювати SvO2 змішаної крові, бо на сучасному етапі вважається, що цей показник є індикатором балансу між доставкою кисню в тканини і його споживанням. Відомо, що показники SvO2 залежать від серцевого викиду, споживання кисню, концентрації гемоглобіну і SaO2. Деякі автори вважають, що за наявності стабільної потреби кисню при відсутності гіпоксемії і анемії SvO2 відображає величину серцевого викиду.
- Інфузійна терапія є необхідним компонентом профілактики та лікування шоку у новонароджених. В практичній діяльності при лікуванні некомпенсованого і незворотнього шоку прийнято дотримуватись правила 4-х катетерів: ендотрахеальна трубка в трахеї, катетер в порожнистій вені, катетер в сечовому міхурі і катетер в шлунку. Інфузійна терапія належить до першочергових заходів при загрозі або розвитку шоку у новонародженого, а тому при підозрі на розвиток шоку лікування слід розпочати з забезпечення надійного шляху внутрішньовенного (в/в) введення розчинів, медикаментів, що дозволить активно впливати на ОЦК, адекватне надходження венозної крові до серця, величину серцевого викиду, які є визначальними в прогресуванні шоку і переходу його в критичну стадію. Основним завданням інфузійної терапії є відновлення ОЦК, адекватної тканинної перфузії, нормалізація метаболізму, корекція розладів гемостазу, зниження концентрації медіаторів запальної реакції і токсичних метаболітів тощо. Розпочинати ІТ у доношених дітей доцільно з в/в введення рідини 10 мл/кг за 10 хв. Перевага надається 0,9% розчину натрію хлориду, який вводять під контролем ЧСС, АТ, SaO2. і його введення є орієнтовним тестом для визначення можливої гіпотонії. Якщо ефект від введення фізіологічного розчину відсутній або ж короткочасний, можна повторювати його введення декілька разів на протязі 20 хв до 20-30 мл/кг. Після дослідження за цей час вмісту гемоглобіну в крові, рівня гематокриту, електролітів, КЛС, кількості тромбоцитів, визначається доцільність переливання електролітів, свіжозамороженої плазми, кріопреципітату, еритроцитарної маси тощо. У новонароджених з шоком не рекомендується вводити альбумін, бо він прискорює вихід рідини в позасудинний інтерстиціальний простір і сприяє розвитку генералізованих набряків.
Якщо гіповолемія зберігається, то необхідно додатково вводити рідину до відновлення ОЦК, нормалізацію ЧСС, АТ, ЦВТ, збільшення темпу діурезу. Доза введеної рідини може сягати 100-120 мл/кг/добу. При більших дозах введеної рідини на фоні гіпопротеїнемії, гіпонатріємії розвиваються генералізовані набряки з характерним збільшенням інтерстиціального водного простору (інколи з формуванням патологічних водних просторів — перикардиту, асциту тощо) і зменшеним об’ємом ОЦК. Рекомендується обмежувати об’єм введеної рідини за умови, коли ЦВТ збільшується без відповідного збільшення АТ. Слід враховувати, що у більшості недоношених новонароджених артеріальна гіпотензія, яка розвивається зразу ж після народження, переважно пов’язана з неадекватною периферійною вазоділятацією і/або ж дисфункцією міокарда, а не безпосередньо з гіповолемією. А тому у них агресивне в/в введення рідини небезпечне із-за можливого розвитку ВШК.
- За наявності клініки шоку новонародженим слід обов’язково в/в вводити симпатоміметичні аміни, перевагою яких є швидкий прояв терапевтичного ефекту, короткий період напіввиведення, можливість контролю дози.
У новонароджених для лікування шоку рекомендують вводити допамін, добутамін, норадреналін.
Допамін в низьких дозах (0,5-3 мкг/кг/хв.) діє переважно на периферійні дофінові рецепти; розширює судини нирок, мезентеріальні, коронарні судини і покращує кровопостачання кишечнику, міокарду. Внаслідок специфічної дії на периферійні допамінові рецептори зменшується опір ниркових судин, в них збільшується кровоток , клубочкова фільтрація, а також збільшується виведення іонів натрію та діурез. Слід відмітити, що дією на ниркові і мезентеріальні судини допамін відрізняється від дії інших катехоламінів.
В низьких і середніх дозах (2-10 мкг/кг /хв.) допамін стимулює постсинаптичні β1 – адренорецептори, внаслідок чого реалізується його позитивний інотропний ефект і збільшується хвилинний об’єм крові. Систолічний АТ і пульсовий тиск можуть зростати (хоч діастоличний АТ майже не міняється або ж зростає незначно), системний опір судин не міняється. Коронарний кровоток і споживання міокардом кисню зростають.
В високих дозах (≥10 мкг/кг/хв. ) переважає стимуляція ά1 – адренорецепторів; підвищується системний опір судин, ЧСС, звужуються ниркові судини (а це може зменшувати раніш збільшений кровоток і діурез). Внаслідок підвищення хвилинного об’єму крові і системного судинного опору зростає як систолічний так і діастоличний тиск. При незворотній стадії шоку і рефрактерній гіпотонії доза допаміну може бути збільшена до 20- 30 мкг/кг/хв. Деякі автори вважають, що при зменшені діурезу на фоні високих доз допаміну слід зменшити його дозу. Початок терапевтичного ефекту допаміну – на протязі 5 хв на фоні в/в введення і триває на протязі 10 хв. Препарат розводиться 5% розчином глюкози, 0,9% розчином NaCl, в розчинах натуральних білків.
За відсутності ефекту від введеного допаміну одночасно з ним вводять добутамін в дозі 5-20 мкг/кг/хв.
Введення добутаміну протипоказано при фібріляціїі передсерця, ідіопатичному субаортальному стенозі.
Таблиця 3. Серцево-судинні ефекти препаратів
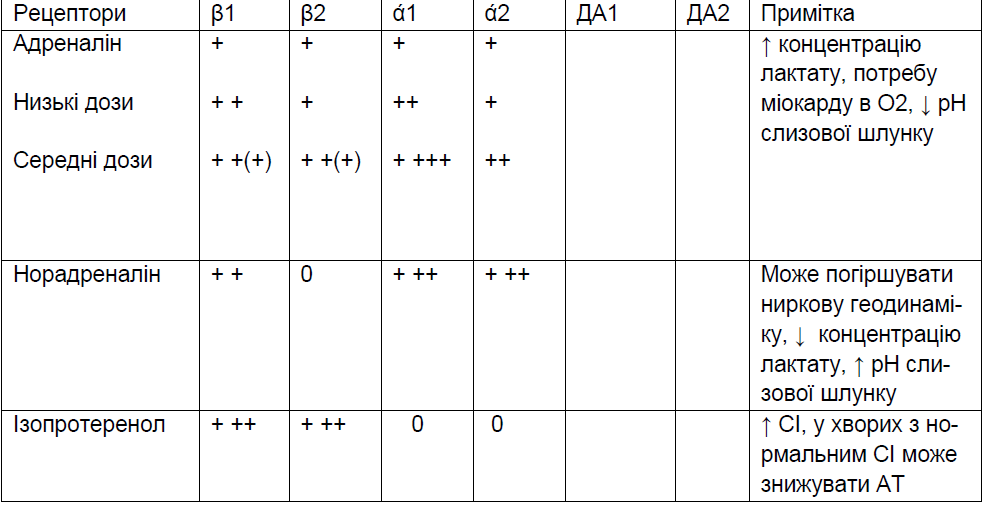
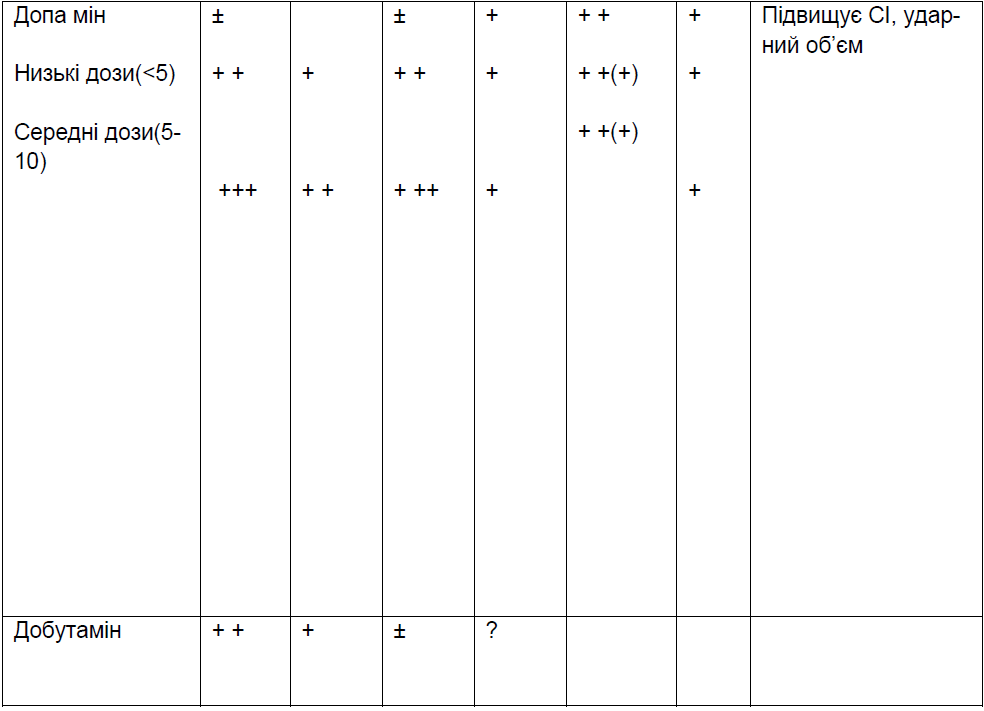
Допускається використання адреналіну або норадреналіну в дозі 0,5-1,0 мкг/кг/хв. в комбінації з допаміном, добутаміном при відсутності ефекту від останніх.
- Корекція електролітів проводиться за загальноприйнятою методикою. Особливо важлива своєчасна
корекція електролітних розладів за умови в/в введення великих об’ємів рідини, бо електроліти в значній мірі визначають осмотичний тиск плазми, величина якого безпосередньо впливає на перерозподіл рідини між водяними просторами, а отже і на формування генералізованих набряків – основних маркерів незворотнього шоку. Високий рівень глюкози в крові краще корегувати крапельним введенням інсуліна ніж зменшенням її концентрації в розчині.
- Корекція анемії. Зменшення в крові еритроцитів зменшує в’язкість крові, збільшує венозне повернення, знижує „постнавантаження”. Але слід пам’ятати, що еритроцити та гемоглобін є основною транспортною системою кисню і при глибокій гемодилюції будуть переважати її негативні ефекти. Рекомендують у новонароджених з шоком підтримувати Нb на рівні 100-120 г/л, а Ht – 25- 30%
- Гормони. У новонароджених з некомпенсованим і незворотнім шоком має місце недостатність наднирників (особливо у недоношених новонароджених, при септичному шоку), а тому при відсутності ефекту від внутрішньовенного введення рідини, вазопресорів та інотропів рекомендується розпочати в/в ведення водного розчину гідрокортизону з розрахунку 2 мг/кг маси тіла, повторюючи введення 1-2 мг/кг маси тіла кожні 6 годин на протязі 3-5 днів.
- Парентеральне харчування доцільно назначати з перших днів розвитку шоку, переважно по системі гіпераліментації. Ентеральне харчування починати з „мінімального трофічного”, розширюючи його об’єм за умови відновлення функції шлунково-кишкового тракту.
- Корекція КЛС (ацидозу, алкалозу) проводиться за загальноприйнятими методиками.
- Корекція гіпокоагуляції. Кровоточивість у новонароджених з шоком переважно зумовлена розвитком ДВЗ, коагулопатіїї споживання, Для її корекції використовують в/в введення діцинону, свіжозамороженої плазми, кріоприципітату.
- Обезболювання, Є важливою складовою ланкою лікування у новонароджених з больовим (травматичним), опіковим шоком. У новонароджених для обезболювання використовують промедол 0,01 мг/кг із діазепамом або седуксеном 0,2 – 0,3 мг/кг в/в повільно.
Опіковий шок у новонароджених
Визначення
Опіковий шок (ОП) – це патологічний процес, що розвивається відразу після отриманих великих і розповсюджених термічних (хімічних) ушкоджень шкіри і глибше розташованих під шкірою тканин. Термічна агресія викликає імунну, нейро-гуморальну реакції і формування ССЗВ у постраждалої дитини. У новонароджених ОШ розвивається при опіках 5-7% поверхні шкіри.
Патогенез ОШ.
Патогенетичні фактори ОШ – сильний біль, розвиток ССЗВ, збільшення проникливості судин і зменшення ОЦК, розвиток синдрому гіпоперфузії органів і тканин.
Відразу ж після травми в розвитку ОШ основну роль відіграє біль; пізніше наростають негативні ефекти гемоконцентрації, які досягають максимуму через 6-8 годин. Сильний біль спричиняє розлад регуляції ЦНС, а втрата плазми, секвестрація клітинних елементів крові в постраждалих тканинах призводять до зменшення ОЦК, згущення крові та розладу її реологічних властивостей. Крім того, в обпечених тканинах утворюється багато біологічно активних речовин. Одночасно з втратою плазми знижується рівень циркулюючих білків крові. Тривалість ОШ залежить від площі та глибини уражень, а також від своєчасності і адекватності лікування. Час тривалості ОШ у дитячому віці становить до 72 годин (Пастернак Г.І. 2008). Опікове ушкодження викликає ССЗВ за загальною моделлю (дивись „Шок у новонароджених”), За своїм генезом ОШ належить до гіповолемічних, але його особливістю є чітка залежність від площі та глибини опіку, відсутність кореляції тяжкості шоку з рівнем артеріального тиску (Цапенко В. І з співавтор., 2008).
Клінічна картина опікового шоку складається із симптоматики шоку та місцевих змін ушкодженої шкіри. На ХХ з’їзді хірургів України виділено 4 стадії опікової хвороби: І стадія – опіковий шок (1-3 дні), ІІ стадія – гостра опікова токсемія (3-7 днів), ІІІ стадія – опікова септикотоксимія (до повного відновлення шкіри), ІV стадія – реконвалесценція.
Опікова токсемія – друга стадія опікової хвороби, яка починає розвиватись уже через декілька годин після опіку. Причиною її розвитку є активація і вихід із клітин кислих протеїназ, активація перекисного окислення ліпідів, білків, Після відновлення мікроциркуляції в судинне русло починають надходити продукти розпаду з обпечених тканин, що призводить до розвитку синдрому ендогенної інтоксикації. Тяжкість опікової токсемії переважно залежить від площі ураження. У новонароджених вона може проявитись уже при пошкодженні 1% шкіри і характеризується в першу чергу порушеннями з боку шлунково-кишкового тракту – поява зригування, патологічного стазу в шлунку, вздуття живота тощо.
Місцеві зміни залежать від глибини опіку, для оцінки якого запропоновано наступну класифікацію: І ступінь – гіперемія шкіри, пошкодження лише епідермісу; ІІ ступінь – загибель епідермісу до сосочкового шару з утворенням опікових міхурів; ІІІ ступінь –пошкодження всіх шарів шкіри до підшкірної жирової клітковини, частковий (ІІІА) або повний (ІІІВ) некроз шкіри; ІV ступінь – обвуглювання, пошкодження всіх шарів шкіри і прилеглих тканин Слід особливо відмітити, що у новонароджених базальна мембрана шкіри розвинута слабо , а тому епідерміс легко відділяється від дерми. Дерма у новонароджених ніжно- волокнистої будови зі слабо вираженим сосочковим шаром. Колагенові волокна мають поперечне направлення, а еластичні майже відсутні, через що відсутні так звані лангеровські лінії (Маргорін Є. М, 1977). Все це зумовлює високу чутливість шкіри новонароджених до термічних пошкоджень. Встановлено, що при контакті зі шкірою новонароджених предметів з температурою більше 39 С○ (навіть при 40-42 С○) уже розвиваються термічні пошкодження. Відповідно до особливостей будови шкіри новонароджених, при міхурах, спричинених термічними опіками, відділяється і гине вся шкіра, а тому у них за наявності термічних міхурів опіки слід оцінювати як ІІІАВ ступеня і лікування проводити сумісно з комбустіологом.
Основні лікувальні заходи при опіках у новонароджених.
- Зупинити дію пошкоджуючого фактору.
- Для профілактики і лікування ОШ провести знеболення шляхом введення ненаркотичних анальгетиків (промедол в дозі 0,01 мг/кг) в поєднанні з бензодіазепінамами (діазепам або седуксен в дозі 0,2 – 0,3 мг/кг в/в).
- Нормалізація функцій життєво важливих органів і систем проводиться за загальноприйнятою методикою. Рівень респіраторної підтримки визначається порушеннями газообміну (дивись розділ „Шок у новонароджених”) та площею опіку. Для ефективного лікування ОШ необхідно якомога швидше розпочати в/в введення розчинів, що дасть можливість відновити ОЦК, стабілізувати гемодинаміку, відновити перфузію тканин, забезпечити їх адекватну оксигенацію. Для проведення інфузійної терапії при поверхні опікової площі більше 1% або наявності супутніх захворювань доцільно катетеризувати одну з центральних вен. Розпочинати інфузійну терапію доцільно з в/в введення 0,9% розчину натрія хлориду. Не рекомендується (Цапенко В. І. з співавтор., 2008) протягом перших 6-8 годин вводити колоїди і лише за умови прогресування шоку на фоні введених кристалоїдів допускається введення колоїдів, які не містять білків (гідроксиетілкрохмалю в дозі 4-8 мл/кг/ годину).
- Захист опікової рани від інфекції – наложити на опікову рану суху асептичну пов’язку (можна з родового пакету).
- При важких опікових ушкодженнях допускається в/в введення глюкокортикоїдів – гідрокортизону 5-10 мг/кг маси тіла або ж преднізолон 2-3 мг/кг маси тіла.
- При важких опіках (>5% поверхні тіла) під час транспортування рекомендується проведення знеболювання, катетеризація магістральних судин, інфузія 0,9% розчину натрію хлориду в дозі 20-30 мкг/годину.
- Госпіталізація в ВІТ або до опікового центру.
Література.
- Беляев А. В. Синдром капиллярной утечки / Беляев А. В. //Мистецтво лікування. – 2005. — №8(024). — С. 92-101.
- Пастернак Г. І. Об’єктивізація шкал тяжкості та алгоритмів інтенсивної терапії у дітей з опіковим шоком (експериментально-клінічне дослідження): Автореф. дис… д-ра мед. наук.: /Пастернак Г. І.- Дніпропетровськ, 2008.- 34 с.
- Сулима Е. Г. Синдром полиорганной недостаточности у новорожденных с асфиксией /Сулима Е.Г //Здоровье женщины. – 2001. — №3(7). – С. 79-83
- Цапенко В. І. Застосування препаратів на основі гідроксиетілкрохмалів при лікуванні хворих з опіковим шоком / Цапенко В. І., Слісаренко С. О., Красюк В. Я., Осауленко П. М. //Україн. хіміотерап. журнал. – 2008. -№1-2 (22). — С. 56-57.
- Шок (термінологія и классификация, шоковая клетка, патофизиология и лечение). /Пер. с румынского Я. Анненкова; Бухарест;Военное издательство. – 1981. – с. 615.
- Landry D. W., Oliver J. A. The pathogenesis of vasodilatory shock// NEJM. – 2001. – V. 345. – P. 588–595.









Комментировать