Методичні рекомендації про пухлиноподібні ураження яєчників. Повний текст.
Установа-розробник: Інститут педіатрії, акушерства та гінекології АМН України
Автори:
доктор мед. наук, проф. Вовк І.Б………………………………………… т. (044) 483-84-23
доктор мед. наук Корнацька А.Г………………………………………… т. (044) 483-38-61
доктор мед. наук, член-кор. АМН України, проф. Чайка В.К… т. (062) 454-49-43
канд. мед. наук Кондратюк В.К………………………………………….. т. (044) 483-38-61
канд. мед. наук Петербурзька В.Ф………………………………………. т. (044) 483-38-61
доктор мед. наук Лук’янова І.С…………………………………………… т. (044) 483-14-46
мол. наук. співробітник Чубей Г.В……………………………………… т. (044) 483-38-61
доктор мед. наук, проф. Задорожна Т.Д………………………………. т. (044) 483-16-12
канд. мед. наук Захаренко Н.Ф……………………………………………. т. (044) 440-03-66
мол. наук. співробітник Сопко Я.О……………………………………… т. (044) 483-14-46
мол. наук. співробітник Ільїна О.І……………………………………….. т. (044) 483-16-12
Академія медичних наук України Міністерство охорони здоров’я України
Український центр наукової медичної інформації та патентно-ліцензійної роботи
Список умовних скорочень:
ЛГ — лютеїнізуючий гормон
ФСГ — фолікулостимулюючий гормон
ШОЕ — швидкість осідання еритроцитів
УЗД — ультразвукове дослідження
КОК — комбіновані оральні контрацептиви
АРUD — дифузна нейроендокринна система
Вступ
За останні роки в усьому світі констатовано зростання частоти пухлиноподібних уражень яєчників, що негативно впливає на стан репродуктивного здоров’я жіночого населення.
Між істинними пухлинами та пухлиноподібними ураженнями існує лише зовнішня подібність, однак їх иа-томорфологічна сутність є глибоко відмінною.
Відсутність специфічної симптоматики, тенденція до росту, можливість малігнізації доброякісних пухлин та пухлиноподібних уражень яєчників диктують необхідність визначення факторів ризику їх виникнення, розробки діагностичного алгоритму, диференційованого підходу до методів лікування.
Методичні рекомендації розроблені для лікарів акушерів-гінекологів, сімейних лікарів і можуть бути використані в навчальних програмах та циклах піс- лядипломної освіти. Методичні рекомендації видаються вперше в Україні.
Класифікація, етіологія та патогенез пухлиноподібних уражень яєчників
Серед доброякісних пухлин виділяється особлива група (класифікація ВООЗ, 1997) — пухлиноподібні ураження яєчників:
- фолікулярні кісти;
- кісти жовтого тіла;
- ейдсгм-етріоїдні кісти;
- прості кісти;
- запальні процеси;
- параоваріальні кісти.
Пухлиноподібні ураження яєчників є досить поширеною патологією у жінок репродуктивного віку. Фолікулярні кісти та кісти жовтого тіла (лютеїнові кісти) складають 25-30% всіх кістозних утворів жіночих гонад. Вони відносяться до функціональних пухлиноподібних уражень. їх найважливішою особливістю, на відміну від інших пухлиноподібних уражень яєчників, є можливий транзиторний характер перебігу.
Пухлиноподібні ураження яєчників — фолікулярні кісти та кісти жовтого тіла являють собою кістозно- проліферативні зміни покривного епітелію, похідні фолікулів і строми яєчника. Вони є наслідком дисбалансу гормональної стимуляції та гормональної активності яєчників.
Серед доброякісних пухлин і пухлиноподібних уражень яєчників фолікулярні кісти складають 22-31%.
Фолікулярна кіста являє собою однокамерну тонкостінну порожнинну структуру. Часто вона є односторонньою, її розміри коливаються від 2 до 7 см в діаметрі.
Інколи фолікулярні кісти є гормонально активними, оскільки містять естрогени, що, в свою чергу, може призводити до гіперплазії ендометрія. Внутрішня поверхня фолікулярних кіст — гладенька, вкрита переважно одним шаром епітеліальних клітин.
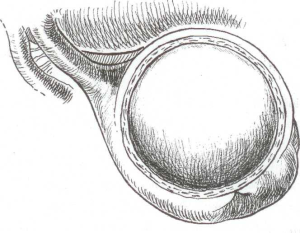
Фолікулярні кісти розвиваються з граафових міхурців за механізмом накопичення рідини в кістозно- атрезуючому фолікулі, як наслідок порушення гіпо- таламо-гіпофізарної регуляції та запального процесу (рис. 1).
Рис. 1. Фолікулярна кіста яєчника
При досягненні кістою досить великих розмірів, при її відносно довготривалій персистенції (2-3 місяці), клітини, котрі вистилають стінку кісти, можуть злущуватись і зазнавати процесу гіалінізації. За рахунок резорбції вмісту, фолікулярна кіста може регресувати протягом 2-4 місяців. Стінки кісти, що спалися, облітеруються з наступним перетворенням у фіброзні (гіалінові) атретичні тіла.
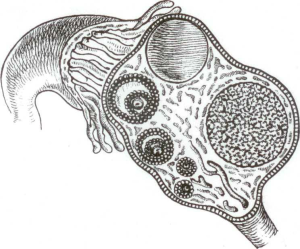
Рис. 2. Етапи формування кісти жовтого тіла
Серед пухлиноподібних утворень частота кіст жовтого тіла коливається від 2 до 15%. Кісти жовтого тіла виникають при двофазному менструальному циклі після овуляції; їх морфологічна будова подібна до фізіологічного жовтого тіла. Патогенетичним моментом у їх виникненні є порушення кровообігу та лімфовідтікання в жовтому тілі, що призводить до накопичення рідини в його просвіті, так званому, ядрі (рис. 2).
Кісти цього типу, як правило, не перевищують 6 см в діаметрі, мають товсті стінки та серозний або серозно-геморагічний вміст. Порожнину кісти вистилають пласти або окремі групи лютеїнових і тека- лютеїнових клітин.
Самостійний регрес кісти жовтого тіла можливий; цей процес продовжується не менше двох місяців, закінчуючись формуванням гіалінового утворення — білого тіла.
Ендометріоїдне ураження яєчників займає перше місце серед усіх нозологічних локалізацій зовнішнього ендометріозу. Ендометріоз яєчників зустрічається в 27-32% випадків під час клінічного та гістологічного досліджень всіх кістозних уражень яєчників.
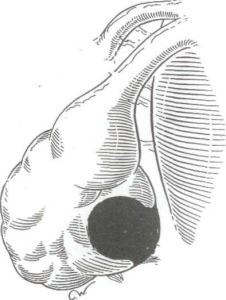
В науковій літературі, поряд з терміном «ендометрі- оїдна кіста яєчника», використовують термін «ендо- метріома». Сучасними авторами ці терміни розцінюють як синоніми, однак термін ендометріома використовується по відношенню до великого за обсягом ендометріоїдного ураження (рис. 3).
Питання генезу зовнішнього ендометріозу до цього часу є предметом дискусій, і особливо це стосується ендометріозу яєчників. Ще в 1957 році Р.Е НидИевЬоп на підставі досліджень серії гістологічних зрізів яєчника показав, що 90% типових ендо- метріом формуються шляхом інвагінації кіркового шару яєчників, являючи собою псевдокісти. Місце ж можливої перфорації кісти являє собою стигму інвагінації, на цьому місці можуть локалізуватись невеликі, але дуже активні, подібні до ендометрія імплантати ендометріозу.
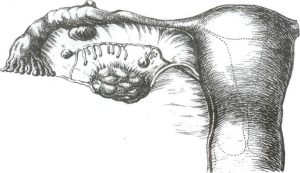
Особливу групу становлять параоваріальні кісти. Частота параоваріальних кіст по відношенню до всіх ретенційних утворів яєчника складає 13-16% (рис. 4).
Рис. 3. Ендометріоїдна кіста яєчника
Рис. 4. Топографія можливого формування параоваріальних кіст яєчника
Параоваріальна кіста являє собою ретенційний утвір, що розміщується між листками широкої зв’язки матки, або ж прикріплений ніжкою до маткової труби. Найчастіше параоваріальні кісти є однобічними, тонкостінними з гладкою поверхнею, прозорими, з вираженими судинами брижейки, рухомими. Зазвичай, на верхньому полюсі параоваріальної кісти розміщена маткова труба, яєчник розміщується біля задньо-нижнього її полюсу. Нерідко парао- варіальна кіста має ніжку, яка складається з маткової труби та власної яєчникової зв’язки.
Пухлиноподібні ураження яєчників зустрічаються практично в будь-якому віці, однак найчастіше в активних для яєчників періодах — періоді статевого дозрівання та репродуктивному.
В періоді статевого дозрівання частота пухлиноподібних уражень яєчників коливається від 9,8 до 14,6%, при цьому фолікулярні кісти становлять до 78,1% від усіх пухлиноподібних утворень яєчників у дівчат 8-16 років.
Відомо, що виникнення всіх форм пухлиноподібних уражень яєчників супроводжується гормональними змінами та порушенням балансу гіпоталамо- гіпофізарної системи. Безумовний інтерес становить вивчення особливостей ендокринної функції яєчників при різних видах пухлиноподібних уражень, зокрема при кістах жовтого тіла яєчника, фолікулярних та ен- дометріоїдних кістах.
При вивченні гормонального статусу хворих з доброякісними пухлинами та пухлиноподібними процесами яєчників виявлено зміни концентрації ФСГ у плазмі крові — від зниженої до такої, що перевищує нормативні показники в декілька разів. При дослідженні ЛГ в більшості хворих відмічається значне пригнічення його циклічної секреції в періовулятор- ному періоді. На фоні порушень секреції гонадотропних гормонів виявлено відхилення у співвідношенні естрадіол/прогестерон у динаміці менструального циклу.
За наявності пухлиноподібних уражень яєчників в крові підвищується концентрація естрогенів, про що може свідчити висока частота поєднання їх з гіпер- пластичними процесами в ендометрії матки, молочних залозах. Згідно з даними літератури, частота поєднання пухлиноподібних процесів яєчників з гіперплазією ендометрія складає від 25 до 80%, з пухлинами молочної залози — 20-50%, з міомою матки- 23-53%.
Розвиток ендометріоїдних кіст яєчника, на думку багатьох авторів, відбувається на фоні двофазного овуляторного циклу при підвищеній базальній секреції ЛГ і ФСГ як в фолікуліновій, так і в лютеїновій фазі менструального циклу з появою додаткових викидів ЛГ і ФСГ, які перевищують за величиною овуляторний пік. Підвищення концентрації ЛГ в фолікуліновій фазі циклу призводить до порушення фолікулогенезу, внаслідок чого не відбувається адекватної секреції стероїдних гормонів в яєчниках. Це, в свою чергу, може створювати несприятливі умови для дозрівання яйцеклітини і, тим самим, стати причиною безплідності.
Існує думка про патогенетичне значення гіперестро- генії у хворих з ендометріоїдними кістами яєчників. При цьому концентрація естрадіолу може перевищувати нормативні показники в кілька разів, поряд з цим спостерігається порушення фізіологічної динаміки концентрації цього гормону.
Відмічається хаотичний характер синтезу естрадіолу в динаміці менструального циклу. Крім того, порушується динаміка секреції прогестерону; характерні двофазні цикли з недостатністю лютеїнової фази.
Таким чином, наукові дослідження свідчать, що у хворих з пухлиноподібними процесами яєчників мають місце порушення взаємозв’язків у системі гіпоталамус-гіпофіз-яєчники, що відбуваються за законом зворотного зв’язку, а це спричиняє подальший розвиток захворювання.
Сучасні погляди на патогенез пухлиноподібних уражень яєчників свідчать про тісний взаємозв’язок між їх виникненням і станом імунної системи організму. Пухлинні процеси розвиваються в організмі на тлі імунодефіциту, сприяючи його поглибленню. З іншого боку, виникнення, прогресування та рециди- вування пухлин і пухлиноподібних уражень яєчників залежить від порушень функціонування імунної системи.
Серед багатьох патогенетичних аспектів виникнення пухлин і пухлиноподібних процесів яєчників одним з найважливіших є взаємодія організму та пухлини. У складному комплексі виникнення захисних реакцій, що забезпечують життєдіяльність організму в цілому, імунній системі належить провідна роль.
Пухлини та пухлиноподібні ураження яєчників є формою патології, яка супроводжується принциповим спотворенням механізмів контролю проліферації та диференціації клітин, мають місце дисфункції клітинної ланки імунної системи, зокрема, серед ряду інших змін, порушення балансу «пропухлинних», «протипухлинних» і «регуляторних» цитокінів: трансформуючих ростових факторів, фактора некрозу пухлини, інтерлейкінів.
За наявності пухлин яєчників у жінок репродуктивного віку має місце значне зниження абсолютної кількості Т-лімфоцитів порівняно зі здоровими, при цьому зменшення числа Т-лімфоцитів і зниження їх функціональної активності залежать від гістотипу пухлини. Вважається, що пригнічення Т-клітинної ланки імунітету може призводити до накопичення пухлинних клітин, перешкоджаючи їх елімінації. Інші дослідники великого значення надають взаємодії різних субпопуляцій Т-лімфоцитів.
Наявність пухлинного процесу в яєчниках супроводжується змінами не тільки клітинного, але й гуморального імунітету. Спостерігається дисглобулінемія, яка виражається збільшенням концентрації ІдМ, деяким підвищенням концентрації ІдА та зменшенням вмісту ІдС порівняно з контролем.
Ряд авторів вказують на роль вірусно-бактеріальної інфекції та запальних захворювань органів малого таза у виникненні пухлиноподібних уражень яєчників. Запальний процес матки та її придатків супроводжується певними змінами яєчникових структур та зниженням активності ферментів стероїдогенезу в кірковій речовині яєчників. При цьому порушується секреція яєчниками стероїдних гормонів, а також біосинтез простагландинів, яким надають провідне значення у виникненні овуляції, що за механізмом зворотного зв’язку призводить до підвищення гіпотала- мо-гіпофізарної активності. Розлади циклічної секреції гонадотропінів запобігають їхньому накопиченню в гіпофізі та ліквідують можливість овуляторного викиду ФСГ та ЛГ, що може призводити до хронічної ановуляції, синтезу якісно змінених естрогенів, гіперплазії тека-клітин та, відповідно, розвитку фолікулярних кіст. Наявність у пацієнток з даною патологією ановуляторної неплідності може розглядатись як підтвердження існування тривалої дисфункції в гіпо- таламо-гіпофізарній системі.
Незважаючи на значні досягнення фундаментальної науки на сучасному етапі етіологія та патогенез пухлиноподібних уражень яєчників є не до кінця вивченими. Правомірний розгляд даного процесу як системного захворювання організму, що виникає на клітинному рівні з втягненням поліморфних ендокринно-обмінних та імунних порушень.
Все це ускладнює діагностику та лікування пухлиноподібних уражень яєчників і в кінцевому підсумку призводить до значного відсотка діагностичних та тактичних помилок у веденні даного контингенту хворих.
З розробкою нових технологій та впровадженням їх в практичну охорону здоров’я набув серйозних змін ряд традиційних уявлень про діагностичні можливості та лікувальні заходи багатьох гінекологічних захворювань, зокрема пухлиноподібних уражень яєчників.
Сучасні принципи діагностики та лікування жінок репродуктивного віку з пухлиноподібними ураженнями яєчників
Складність своєчасної діагностики пухлиноподібних уражень яєчників великою мірою пов’язана з відсутністю у пацієнток з цією патологією виражених симптомів клінічного перебігу.
Враховуючи малоінформативність клінічної симптоматики на початкових стадіях захворювання, обстеження необхідно починати з ретельного збору анамнезу.
При аналізі захворювань інших органів і систем привертає увагу висока частота перенесених дитячих інфекцій (епідемічний паротит, краснуха, кір та ін.). Часті ангіни, хронічний тонзиліт також можна вважати патологічним преморбідним фоном для виникнення пухлиноподібних уражень яєчників.
З особливостей становлення менструального циклу у пацієнток з доброякісними пухлинами яєчників необхідно відмітити пізнє настання менархе, порушення менструальної функції, зниження дітородної функції, високий відсоток неплідності та вкорочення репродуктивного періоду.
Клінічна картина пухлиноподібних уражень яєчників неспецифічна. Тільки пухлиноподібні ураження значних розмірів (більше 8-10 см) можуть викликати явища дискомфорту, тяжкості внизу живота, попереку, порушення менструальної та репродуктивної функцій. Не завжди спостерігається кореляція між розміром вогнища ураження, наявністю та вираженістю больового синдрому. Виникнення та посилення останнього можуть бути викликані подразненням очеревини, що виникло внаслідок впливу вмісту під час перфорації пухлиноподібного утвору, перекрутом його ніжки.
Пухлиноподібні ураження яєчників здебільшого можуть визначатись наявністю супутньої патології міоми матки, ендометріози, запальних захворювань тощо.
Дисонанс у системі гіпоталамус-гіпофіз-яєчники- органи-мішені, який виникає у жінок з пухлиноподібними ураженнями яєчників, несприятливо впливає на функцію інших органів і систем. Можуть спостерігатись: субфебрильна температура, підвищення ШОЕ, лейкоцитоз, порушення функцій шлунково- кишкового тракту, сечовивідної системи.
Найчастіше пухлиноподібні процеси яєчників діагностуються випадково, нерідко після виникнення ускладнень, які вимагають ургентного оперативного втручання, що негативно впливає як на генеративну функцію, так і на якість життя жінки.
Нами розроблено й впроваджено в практику алгоритм обстеження та лікування пацієнток з пухлиноподібними ураженнями яєчників (рис. 5). Гінекологічний огляд повинен включати: огляд зовнішніх статевих органів, визначення характеру волосяного покриву, огляд піхви та шийки в дзеркалах.
Поряд з гінекологічним оглядом проводиться бімануальне обстеження, шляхом якого встановлюються наявність та локалізація патологічного процесу, форма, величина матки та придатків, їх консистенція, рухомість, болючість при пальпації, анатомото- пографічні взаємовідношення органів малого таза.
Серед методів візуалізації перевага віддається ультразвуковому дослідженню. Точність діагностики патології органів малого тазу при Скарги (біль внизу живота, порушення менструального циклу, альгодисменорея, безплідність) Анамнез (менструальна функція, генеративна функція, сексуальна функція, інфекційний індекс, спадковість) Бімануальне гінекологічне обстеження використанні трансаб- домінальної ехографії коливається від 21 до 81%. Збіг результатів ультразвукового дослідження з па- томорфологічним діагнозом складає 72-74%, а за даними деяких дослідників може досягати 97%.
Поряд з трансабдомінальним скануванням органів малого таза за методикою наповненого сечового міхура також слід використовувати й інтравагінальне ультразвукове обстеження, основною перевагою якого є використання акустичних перетворювачів з високою дозволяючою здатністю, та їх безпосередній контакт з об’єктом дослідження. Це дає можливість не тільки констатувати наявність об’ємного утворення яєчника, але й більш детально визначити його структуру. Ультразвукове дослідження дозволяє діагностувати патологічні зміни яєчників у 93,2-96,0% випадків, і, при цьому, точність ультразвукової діагностики в зіставленні з клінікою зростає на 25,0%.
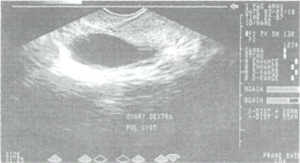
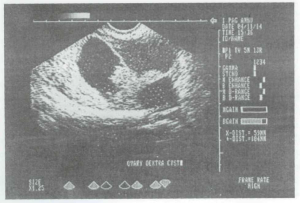
Точність ультразвукової діагностики фолікулярних кіст при первинному ультразвуковому обстеженні складає 96%, кіст жовтого тіла — 94% при динамічному обстеженні. Для ехографічної картини фолікулярних кіст характерною є наявність однокамерного тонкостінного утвору округлої форми розмірами від 30 до 70 мм з високим рівнем ехопровідності, поряд з яким, зазвичай, визначається незмінена тканина яєчника, а позаду кісти візуалізується характерний ефект посилення ультразвуку (рис. 6).
Рис. 6. Фолікулярна кіста яєчника
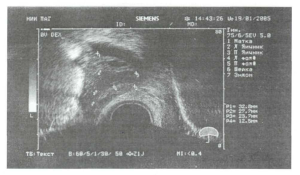
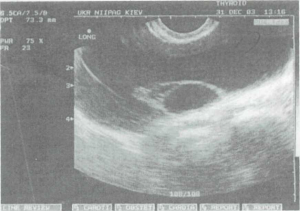
Кісти жовтого тіла, розміри яких коливаються від 3 до 6 см, ехографічно мають більш щільну капсулу та ехопозитивний вміст в порожнині кісти. У деяких випадках в порожнині кіст можуть виявлятись щільні, підвищеної ехогенності згустки крові, як наслідок крововиливу в порожнину кісти (рис. 7).
Рис. 7. Ехограма кісти жовтого тіла з крововиливом
У ряді випадків спостерігається ідентичність ехог- рафічної картини фолікулярної кісти та кісти жовтого тіла (однорідна та анехогенна внутрішня структура). Диференціальною ознакою у цих випадках є товщина стінки пухлиноподібного утвору: якщо у фолікулярних кіст вона тонка (до 1 мм), то у кіст жовтого тіла її товщина може коливатись від 2 до 6 мм.
У деяких випадках виникає необхідність проведення диференціальної діагностики пухлиноподібного ураження яєчника та папілярної цистаденоми (рис.8, 9).
Рис. 8. Ехограма двокамерної фолікулярної кісти Рис. 9. Малігнізована папілярна цистаденома
Допплерографія має вирішальне значення при проведенні диференціальної діагностики між пухлиноподібним ураженням яєчника та папілярною цистаденомою. Візуалізація кровообігу в пристінковому елементі новоутворення свідчить на користь папілярної цистаденоми, а його відсутність — на користь пухлиноподібного ураження яєчника.
Ультразвуковий моніторинг дає змогу виявити ехографічні зміни в динаміці менструального циклу при пухлиноподібному ураженні яєчника, а їх відсутність підтверджує наявність пухлини яєчника.
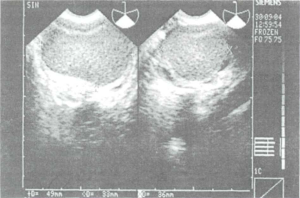
Акустичні ознаки ендометріоїдних кіст мають свої відмінності. їх характерними ехографічними ознаками є: округла форма, дрібнозерниста однорідна структура внутрішнього вмісту на фоні підвищеної звукопровідності, нерівномірно потовщена капсула, локалізація позаду матки. Можливе як однобічне, так і двобічне ураження яєчників ендометріоїдними кістами. Урахування цих особливостей при використанні методики трансвагінального ультразвукового скенуван- ня дає змогу з точністю до 83,3-97,2% правильно встановити діагноз (рис. 10).
Рис. 10. Двобічні ендометріоїдні кісти яєчників
Нові перспективи в діагностиці патології придатків матки відкрили можливість впровадження в практику методики доплерографічного вивчення кровообігу в судинах малого тазу. Особливо це стосується диференціальної діагностики злоякісних та доброякісних уражень яєчників. При виявленні об’ємного утворення яєчників за допомогою ультразвукового дослідження органів малого таза останнє слід доповнювати допплєрографічним обстеженням кровоп- лину в маткових та яєчникових артеріях та кольоровим допплєрівським картуванням.
Головним диференціально-діагностичним критерієм при обстеженні пацієнток з пухлиноподібними ураженнями яєчників, за методикою кольорового до- плерівського картування, є характер кровоплину в яєчниках та їх пухлинних ураженнях. Для неоангіо- генезу злоякісних пухлин характерним є високош- видкісний низькорезистентний тип кровоплину, який оцінюється на підставі значень індексу резистентності та пульсаційного індексу. Саме пограничні значення цих індексів та безпосередньо саме їхнє значення є на сьогодні спірним питанням для багатьох спеціалістів.
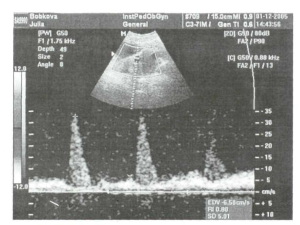
Рівномірне периферичне розміщення судинних елементів при проведенні кольорового доплерівсь- кого картування та середні рівні індексу резистентності в них свідчать про доброякісний характер патологічного процесу (рис. 11).
У патогенезі функціональних порушень центральних і периферичних ланок системи гіпоталамус- гіпофіз-яєчники значна роль відводиться порушенню гормональної функції останніх, що нерідко є наслідком запального процесу. Це підтверджується частим розвитком пухлиноподібних уражень яєчників на фоні високого індексу перенесених інфекційних захворювань бактеріальної та вірусної етіології в пубертаті, запальних захворювань геніталій, ускладнених пологів та абортів.
У всіх пацієнток з пухлиноподібними ураженнями яєчників слід проводити вивчення мікробіоценозу статевих шляхів та діагностику інфекцій, що передаються статевим шляхом, щоб у разі виявлення патогенної мікрофлори або вірусів провести патогенетично обгрунтовану протизапальну терапію.
Рис. 11. Кольорове доплерівське картування та доплерографія яєчникової артерії у пацієнтки з фолікулярною кістою яєчника
Згідно з сучасними уявленнями, питання етіології та патогенезу, а також лікування і профілактики пухлин яєчників і пухлиноподібних процесів розглядаються в тісному та нерозривному зв’язку з порушеннями взаємовідношень в системі гіпоталамус- гіпофіз-яєчники, тому необхідність у визначенні гормонального статусу у даного контингенту хворих й проведенні його динамічного моніторингу не підлягає сумніву. Необхідним є моніторинг гормонального статусу (визначення рівня ЛГ, ФСГ, естрад іолу, прогестерону, тестостерону, пролактину) в динаміці менструального циклу для діагностики можливих їх патологічних відхилень та проведення корекції.
За останнє десятиріччя, завдяки успіхам імунохімії, в повсякденну практику запроваджено методи іму- ноаналізу, які дозволяють визначати специфічні білки, що синтезуються пухлинами різних типів, так звані пухлиноподібні маркери. Необхідним є визначення в крові рівня онкомаркера СА-125, що дасть змогу підтвердити доброякісність пухлинного ураження яєчника.
Моніторинг стану клітинної та гуморальної ланок імунітету, цитокінового статусу, антифосфоліпідних антитіл дозволить визначитись з необхідними заходами щодо корекції виявлених порушень ланок імунної системи.
У жінок з порушеною репродуктивною функцією для визначення стану маткових труб необхідним є проведення метросальпінгографії, результати якої безпосередньо впливають на тактику подальшого ведення пацієнтки.
Якщо за результатами ультразвукового дослідження, даними метросальпінго-графії було виявлено патологію матки, — слід проводити гістероскопію з біопсією ен- дометрія та подальшим патогістологічним дослідженням біоптату.
Раннє та адекватне виявлення етіологічного чинника патологічного процесу, інформативна та достовірна діагностика анатомічного й функціонального стану матки та придатків дає змогу поставити правильний діагноз і, в подальшому, провести патогенетично обгрунтовану корекцію виявлених патологічних зрушень.
Консервативний напрямок ведення пацієнток з пухлиноподібними ураженнями яєчників включає два етапи. Першим є комплекс протизапальної терапії, який повинен призначатися відповідно до виявлених патогенних збудників та їх чутливості до препаратів. Другий етап — проведення корекції гормонального гомеостазу.
При верифікації діагнозу та підтвердженні наявності запального процесу геніталій проводиться комплексна протизапальна терапія (з урахуванням антибіоти- кограми) на фоні імуномодулятора циклоферону, а також антимікотична та десенсибілізуюча терапія. Як відомо, хронічна дисфункція печінки поглиблює порушення клітинно-тканинного гомеостазу, що є проявом дисфункції обмінних процесів у пацієнток з пухлиноподібними ураженнями яєчників. Для запобігання їх виникненню та корекції слід використовувати гепатопротектори.
Після призначення протизапальної терапії та регресу пухлиноподібного ураження яєчників для забезпечення повноцінного функціонування жовтого тіла призначають дідрогестерон (дуфастон) по 10 мг двічі на добу з 16-го по 26-й день менструального циклу протягом 3-6 місяців.
При неефективності першого етапу лікування слід переходити до другого етапу, який проводиться диференційовано із використанням одного з гормональних препаратів (естроген-гестогенних контрацептивів, препаратів прогестогено-вого ряду, агоністів гонадот- ропін-рилізінг-гормонів та антигонадотропінів).
Повідомлення про можливість використання комбінованих оральних контра-цептивів (КОК) з лікувальною метою з’явились протягом останніх 10 років. Механізм лікувальної дії монофазних КОК пов’язують з інгібіцією синтезу гонадо-тропін-рилізінг-гормону, наслідком чого є пригнічення циклічної секреції ФСГ та ЛГ. Для лікування ендометріоїдних та ретенційних пухлиноподібних уражень яєчників використовували сучасний низь- кодозований монофазний препарат Жанін, що містить 30 мкг етинілестрадіолу та 2 мг дієногесту. Препарат призначали як в циклічному, так і в пролонгованому режимі (24+4 — 24 дні прийом, 4 дні перерва; 42+7 — 42 дні прийом, 7 днів перерва; 126+7 — 126 днів прийом, 7 днів перерва).
При значних анатомічних порушеннях органів малого таза (величина кіст > 5 см, виражений злуковий процес та поєднання пухлиноподібних уражень яєчників з лейоміомою або аденоміозом матки) препаратами вибору є агоністи гонадотропін-рилізінг- гормону.
Трипторелін (диферелін) є аналогом природного гонадотропного рилізінг-фактора. Введення препарату після короткотривалої вихідної стимуляції викликає інгібі- цію секреції гонадотропінів з наступним пригніченням секреції статевих гормонів. Механізм дії зумовлений впливом на статеві залози шляхом зниження чутливості периферичних рецепторів до впливу гонадотропін- рилізінг-гормону.
Медикаментозне лікування препаратами агоністами гонадотропін-рилізінг-гормону спрямовано на зменшення симптомів захворювання, розмірів пухлини матки та пухлиноподібного ураження яєчників.
Застосування дифереліну викликає зниження гіперактивності та стійкий стабілізуючий ефект у системі гіпоталамус-гіпофіз-яєчники, розвиток та активний перебіг механізмів імунорегуляції, які спрямовані на активацію ФНП-а, стабілізацію ангіогенезу та урегулювання процесів апоптозу, що сприяє розвитку гіпотрофічних та атрофічних процесів у вогнищах ендометріозу й клінічно проявляється зменшенням розмірів матки, регресом ендометріоїдного пухлиноподібного ураження яєчника, поліпшенням якості життя пацієнток: зниженням вираженості больового синдрому, відновленням фертильності.
У відділенні планування сім’ї Інституту педіатрії, акушерства та гінекології АМНУ застосовували препарат диферелін (трипторелін), який призначали по 3,75 мг один раз в 28 днів протягом 1-3 місяців. При аналізі ефективності лікування на підставі клініко- імунологічних, ендокринологічних та ехографічних досліджень встановлено значний регрес пухлиноподібних уражень яєчників та нормалізація анато- мо-функціонального стану органів малого таза у 80% хворих, серед яких вагітність настала у 45% жінок.
При успішному лікуванні цього контингенту пацієнток в подальшому застосовували довготривалу терапію ізомером природного прогестерону — дідрогестероном (препарат дуфастон) добовою дозою 20-40 мг з 5-го по 25-й день менструального циклу протягом від трьох до шести місяців.
Пацієнтки з кістами жовтого тіла отримували терапію препаратами прогестогенового ряду (норетис- терону ацетат, дідрогестерон) залежно від репродуктивних планів пацієнток.
З цією метою норетистерону ацетат (примолют-нор) призначали по 5 мг двічі на добу з 16-го дня циклу протягом 10 днів. Курс лікування складав 3-6 місяців.
Дідрогестерон (дуфастон) застосовували добовою дозою 20-40 мг з 16-го по 25-й день менструального циклу. Курс лікування — до шести місяців.
Дуфастон є гестагеном вибору завдяки виключно селективній його дії щодо прогестеронових рецепторів, відсутності андрогенного, естрогенного, глю- кокортикоїдного та антигонадотропного ефектів. Важливим є той факт, що дуфастон не пригнічує діяльність гіпоталамо-гіпофізарної системи та не блокує овуляцію, тому є препаратом вибору для лікування жінок з репродуктивними планами на вагітність.
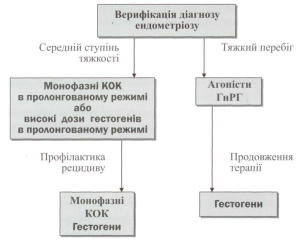
Сучасні погляди на етапність застосування гормональної терапії у лікуванні ендометріозу наведено в алгоритмі (рис. 12).
З метою профілактики рецидивів виникнення ретенційних пухлиноподібних уражень яєчників використовували монофазні низькодозовані комбіновані оральні контрацептиви в циклічному режимі протягом 3-12 місяців. Згідно з сучасними даними ефективність такої терапії значно вища, якщо застосовувати КОК в пролонгованому режимі. Довготривале гормональне лікування поєднували з системною ензимо- та гепатопротекторною терапією.
Рис. 12. Алгоритм застосування гормональної терапії у лікуванні ендометріозу
Дослідження проліферативних процесів та пошук шляхів їх фармакологічної корекції — одна із областей сучасної медицини, що динамічно розвивається та базується на розумінні основ індукції клітинного росту, особливо за умов його пухлинної трансформації, та є невід’ємною частиною правильного підходу до управління та моніторингу проліферативної активності. Альтернативним в цьому аспекті є препарат індинол — фітопрепарат, отриманий з сімейства христоцвітних. Препарат містить високоочищений індол-трикарбінол. Основні фармакологічні властивості індинолу: нормалізує метаболізм жіночого статевого гормону естраді- олу та інгібує синтез 16-а-гідрокси-естрону, який має виражені канцерогенні властивості; інгібує утворення естрогенових рецепторів, зменшуючи їх кількість на тканинах-мішенях; пригнічує ріст естроген-залежних пухлин жіночої репродуктивної сфери; індукує вибірковий апоптоз пухлинних клітин; нейтралізує дію ростових факторів. Рекомендовано: терапевтичний прийом — 300-400 мг (3-4 капсули) на день протягом 3-6 місяців; профілактичний прийом — 300 мг (1 капсула) на день за 20 хвилин до їди протягом 3-6 місяців.
Дотримання зазначених принципів консервативного ведення пацієнток дає можливість уникнути рецидивів захворювання та сприяє відновленню репродуктивної функції пацієнток.
Показаннями до хірургічного втручання слід вважати: неефективність консерва-тивної терапії протягом 3-6 місяців. Наявність параоваріальних кіст, ендометріоїд- них кіст розмірами > 5 см та поєднання пухлиноподібного ураження яєчників з непрохід-ністю маткових труб (у пацієнток з порушеною репродуктивною функцією).
На сучасному етапі використовують лапароскопічні або мікрохірургічні методики: органозберігаючу корекцію виявлених патологічних анатомічних змін як на яєчниках (видалення пухлини яєчника в межах здорової тканини з формуванням останнього), так і на маткових трубах (відновлення їх прохідності) та матці (за показаннями).
Окрім безпосереднього видалення пухлиноподібного утворення яєчника наявність супутньої патології органів малого таза вимагає проведення додаткових хірургічних маніпуляцій: роз’єднання спайок органів малого таза та черевної порожнини, проведення пластики маткових труб (сальпінгостомія, неосальпінгостомія, сальпінго-сальпінгоанастомоз), вилущування пухлино-подібних утворень на другому яєчнику, проведення діатермопунктури яєчників, здійснення консервативної міомектомії.
У пацієнток з виконаною або непорушеною репродуктивною функцією (прохідними матковими трубами) перевагу слід віддавати лапароскопії.
Велике значення для визначення тактики післяопераційного ведення та реабілітації мають результати гістологічного дослідження операційного матеріалу від жінок з пухлиноподібними ураженнями яєчників. Досить часто виявляються зміни запального характеру, а саме у 70,0% — хронічний оофорит з вогнищами склерозу, текоматозу, ангіоматозу, фіброзні тіла, атрезовані кістозно змінені фолікули, поодинокі примордіальні фолікули.
Гістологічно пухлиноподібні ураження яєчників — фолікулярні кісти та кісти жовтого тіла — являють собою кістозно-проліферативні зміни покривного епітелію, похідні фолікулів і строми яєчника.
Макроскопічно фолікулярні кісти — це однокамерні тонкостінні утворення, що містять прозору рідину жовто-лимонного кольору. Оскільки фолікулярні кісти можуть виникати на різних стадіях фолікулогене- зу, то відповідні цьому особливості може мати і їх гістологічна структура. Гістологічно капсули фолікулярних кіст невеликих розмірів (до 5 см), утворені внутрішнім епітеліальним декількашаровим кубічним фолікулярним епітелієм, зовні містять тека- лютеїнові клітини та сполучнотканинний шар. Межі між епітеліоцитами розмиті. Сполучнотканинний шар містить фіброзні та колагенові волокна, поодинокі кровоносні капіляри. Зі збільшенням розміру кісти в фолікулярному епітелії спостерігаються дистрофічні зміни: він витончується та в ряді випадків не диференціюється. В таких випадках роль диференціального маркера такого типу пухлиноподібного ураження яєчника відводиться тека-лютеїновим клітинам.
Гістологічно стінка параоваріальних кіст складається з двох шарів: зовнішнього — сполучнотканинного та внутрішнього — епітеліального. Внутрішній шар оболонки параоваріальної кісти висланий однорядним циліндричним епітелієм, деякі з епітеліоцитів містять апікальні волоски. Серед забарвлених епі- теліо-цитів зустрічаються інтактні до барвників, так звані «світлі» клітини, які відно-сяться до клітин АРUD системи. Характерними їх особливостями є ендокринні та секреторні властивості. Під базальною мембраною епітелію розміщуються колагенові волокна з фібробластами та лімфоцитами, кровоносні капіляри.
Макроскопічно капсули кіст жовтого тіла є більш товстими порівняно з капсулами фолікулярних кіст, внутрішня їх поверхня є складчастою. Вміст являє собою прозору рідину, яка у випадках крововиливу в порожнину кісти може бути геморагічною. Для кіст жовтого тіла на тлі хронічних запальних процесів репродуктивних органів характерною є присутність внутрішньої фіброзної вистилки, за якою локалізуються шари гранульозо-тека-лютеїнових клітин.
В тканинах ендометріоїдних кіст спостерігається наявність строми зі слабко вираженим цитогенним характером та однорядним низьким циліндричним епітелієм ендометріального типу, а також наявність залозистих структур ендометрія (псевдоксантомних клітин). Характерною ознакою яких є нерівномірна інфільтрація стінки кіст лімфоцитами.
Таким чином, пухлиноподібні ураження яєчників є самостійною патологією, яка негативно впливає на процес репродукції та вимагає медикаментозного лікування.
Розвиток пухлиноподібних уражень яєчників відбувається за різними патогенетичними механізмами, але здебільшого вони виникають внаслідок запальних захворювань внутрішніх статевих органів, а також порушення взаємовідношень гіпоталамо- гіпофізарної системи та периферичних органів- мішеней. В зв’язку з цим, підходи до лікування даної патології мають бути диференційованими з урахуванням ураження тієї чи іншої ланки патогенезу.
Висновки
1. Обстеження пацієнток з пухлиноподібними ураженнями яєчників, окрім загальноприйнятих методів, повинно включати допплєрометричний моніторинг та кольорове доплерівське картування, які є маркерами анатомо-функціонального стану органів малого таза, оскільки дозволяють верифікувати виявлений патологічний процес.
2. Діагностика стану гормонального гомеостазу, інфекційний скринінг, визначення стану маткових труб (метросальпінгографія у пацієнток з порушеною репродуктивною функцією) та матки (гістероскопія), імунологічне обстеження дають змогу встановити основну та другорядні причини виникнення патологічного процесу, визначитись в адекватній лікувальній тактиці.
3. Консервативні методи ведення даного контингенту хворих повинні включати:
- динамічний моніторинг;
- протизапальну та гормональну терапію за показаннями;
- неефективність заходів, що проводяться протягом 3-6 місяців, є показанням до хірургічного лікування.
4. Показаннями до хірургічного лікування пухлиноподібних уражень яєчників є:
- рецидиви кіст після консервативного лікування;
- ускладнений перебіг пухлиноподібного утворення (перекрут ніжки кісти, підозра на розрив кісти) в поєднанні з супутньою патологією органів малого таза (спайковим процесом органів малого таза та черевної порожнини ІІІ-ІУ ступеня;
- необхідність проведення пластики маткових труб, консервативної міомектомії
5. Для верифікації діагнозу та з метою бережливої хірургічної корекції виявлених анатомічних змін доцільним є використання лапароскопії, при наявності значних анатомічних порушень органів малого таза показана органозберігаюча їх корекція з застосуванням мікрохірургічної техніки.
6. Проведення лікувальних та реабілітаційних заходів у пацієнток з пухлиноподібними ураженнями яєчників після хірургічного лікування (протизапальна, імуномодулююча, системна ензимотерапія з наступним гормональним лікуванням) сприяє профілактиці рецидивів захворювання та повноцінному відновленню репродуктивної функції даного контингенту хворих.
Перелік рекомендованої літератури:
- Запорожан В.Н., Низова Н.Н., Иркина Т.К. Перспективы внедрения программы «Безопасное материнство в Украине» // Репродуктивное здоровье женщины. — 2002. — № 3. — С. 9-13.
- Кулаков В.И., Гатаулина Р.Г., Сухих Г.Т. Изменения репродуктивной системы и их коррекция у женщин с доброкачественными опухолями и опухолевидными образованиями яичников. — М.: Триада X, 2005. — 254 с.
- Бондаренко Л., Иващенко Э., Свечникова Н. Функциональные кисты. Консервативное лечение // Доктор. — 2004. — № 4. — С. 94-96.
- Запорожан В.М., Венцківський Б.М., Іванюта Л.І., Пирогова B.I., Вовк І.Б. Генітальний ендометріоз у жінок репродуктивного віку (діагностика та лікування). — Метод. рекомендації. — Київ. — 2005. — 34 с.
- Seerly J.P. Endometriosis associated with defective handling of apoptotic cells in the female genital tract is a major cause of autoimmune disease in women // Med Hypotheses. — 2006. — 66 (5). — P. 945-9.
- Dimitriadis E. et all. Interleukin-11, IL-11 receptor alpha and leukemia inhibitory factor are disregulated in endometrium of infertile women with endometriosis during the implantation window // J. Reprod. Immunol. — 2006 Feb. — 69 (1). — P. 53-64.
- Lee K.S. et all. IL-10-dependent down-regulation of MHC class II expression level on monocytes by peritoneal fluid from endometriosis patients // Int. Im- munopharmacol. — 2005 Nov. — 5 (12). — P. 1699-712.
- Nilsson M.B. et all. Interleukin-6, secreted by human ovarian carcinoma cells, is a potent proangiogenic cytokine // Cancer Res. — 2005 Dec 1.-65 (23). -P. 10794-800.
- Liu J. et all. A new format of single chain trispecific antibody with diminished molecular size efficiently induces ovarian tumor cell killing // Biotech- nol. Lett. — 2005 Nov. — 27 (22). — P. 1821-7.
- Haller K. et all. IgG, IgA and IgM antibodies against FSH: serological markers of pathogenic autoimmunity or of normal immunoregulation? // Am. J. Reprod. Immunol. — 2005 Nov. — 54 (5). — P. 262-9.
- Romics L. Jr. et all. Toll-like receptor 2 mediates inflammatory cytokine induction but not sensitization for liver injury by Propioni-bacterium acnes // J. Leukoc. Biol. — 2005 Dec. — 78 (6). — P. 1255-64.
- Daponte A. Novel serum inflammatory markers in patients with adnexal mass who had surgery for ovarian torsion // Fertil Steril. — 2006 May. — 85 (5). -P. 1469-72.
- Hernandez O.T. et all. Endometriosis. Is it a problem of the immunological signs? // Ginecol. Obstet. Mex. — 2005 Sep. — 73 (9). — P. 492-9.
- Szekeres-Bartho J., Kilar E, Falkay G., Csernus V., Torok A., Pasca A.S. Progesterone- threated lymphocytes of healthy pregnant women release a factor inhibiting cytotoxicity and prostaglandin synthesis // Am. J. Reprod. Immunol. Microbiol. — 2001. — 9. — P. 15-19.
- Schweppe K.-W. Current place of progestins in the treatment of endo-metriosis-related complaints // Gynecol. Endocrinol. — 2001. — Vol. 15 (6). -P. 22-28.
- McKenna A., Fabres C, Alam V., Morales V. Clinical management of functional ovarian: a prospective and randomized study // Human Reproduction. — 2000. — Vol. 15 (12). — P. 2567-2569.
- Gambone Josef, Brain S. Mittman, Malcolm G. Munro. Consensus statement for the management of chronic pelvic pain and endometriosis: proceedings of an expert-panel consensus process // Fertil. Steril. — 2000. -Vol. 78 (5). — P. 961-972.












Комментировать