Энисамиум йодид как современный высокоэффективный препарат лечения гриппа. Результаты проведенного исследования энисамиума.
Д. Больц1, С. Пен1, М. Муззио1, П. Даш2, П. Томас2, Р. Мехта1, В. Маргитич3, 1НИИ Иллинойского технологического института, Чикаго, Иллинойс, США !, 2Детский исследовательский госпиталь имени святого Иуды, Мемфис, Теннесси, США, 3ПАО «Фармак», Киев, Украина
Экскурс в проблему
Грипп — это острое респираторное заболевание, вызываемое вирусами гриппа А и В, которые приводят к развитию ежегодных эпидемий с высоким уровнем заболеваемости и смертности, а иногда и пандемий. Хотя вакцины для профилактики гриппа доказали свою эффективность в уменьшении выраженности симптомов заболевания во время эпидемий гриппа, однако в связи с возможным антигенным несоответствием вакцины и относительно продолжительным процессом разработки клинически доступной вакцины против нового штамма вируса создание эффективных противовирусных препаратов для угнетения инфекционного процесса при гриппе является актуальной задачей. На данный момент только один класс противовирусных препаратов (ингибиторы нейраминидазы, такие как осельтамивир и занамивир) рекомендован для использования с целью профилактики и лечения гриппа у взрослых и детей во всем мире.
Сегодня значительные усилия сосредоточены на разработке новых способов лечения и выборе мишеней для действия лекарственных средств, которые дали бы возможность устранить патогенные свойства вируса гриппа. В этом контексте привлекают внимание некоторые препараты, которые на данный момент находятся на рынке стран СНГ и обнаруживают противовирусную активность в отношении вирусов гриппа А и В. Одним из таких препаратов является энисамиум йодид (рис. 1), который зарегистрирован и маркетируется под торговым названием Амизон® в России, Украине, Белоруссии, Казахстане и Узбекистане как противовирусное средство против гриппа.

Клинические исследования, проведенные в России, продемонстрировали высокую эффективность препарата против вирусов гриппа А и В, что позволило говорить о энисамиуме как о перспективном средстве, предназначенном для лечения гриппа. Однако имеющихся экспериментальных данных об эффективности этой производной изоникотиновой кислоты как противовирусного агента, действенного в отношении гриппа, недостаточно. Поэтому целью данного исследования было оценить ожидаемую противовирусную активность энисамиума в отношении вирусов гриппа in vitro. Пилотные исследования на MDCK- и A549-клетках продемонстрировали низкую проницаемость энисамиума — на уровне 0,08 и 0,87% соответственно, а также отсутствие противовирусного эффекта. Поглощение энисамиума дифференцированными нормальными бронхоэпителиальными клетками человека (normal human bronchial epithelial — NHBE) было лучшим в сравнении с клетками A549 и MDCK и варьировало в пределах 1,7-2,1%. Поэтому именно культуры клеток NHBE были избраны для оценки эффективности и наличия противовирусного эффекта энисамиума в отношении вирусов гриппа.
Материалы и методы
Культура клеток: в исследовании были использованы дифференцированные клетки NHBE EpiAirway System компании «MatTek» (Ашланд, Массачусетс, США). Клетки от одного донора были использованы для анализа однородности. Апикальную поверхность клеток подвергали влиянию влажного 95% воздуха / 5% CO2, а также меняли среду и отмывали муцин каждые 24-48 ч.
Исследуемые материалы: исследованный продукт — энисамиум (Амизон®) был предоставлен ПАО «Фармак». Препарат для положительного контроля — осельтамивира карбоксилат, полученный от Toronto Research Chemicals, TRC (Торонто, Канада).
Вирусный агент: в NHBE-клетки были инокулированы вирусы гриппа А через апикальную поверхность. После инкубации в течение 1 ч вирусный инокулят удаляли из клеток, апикальную поверхность клеток промывали натрий-фосфатным буферным раствором (Phosphate Buffered Saline — PBS).
Введение исследуемого материала: для проведения положительного контроля (использование осельтамивира карбоксилата) культура клеток NHBE инкубировалась с базальной стороны с осельтамивиром в течение 60 мин до заражения вирусом. Энисамиум или контроль добавлялся к базальному компартменту культуры клеток до или после инокуляции и инкубировался в течение определенного условиями эксперимента периода.
Результаты
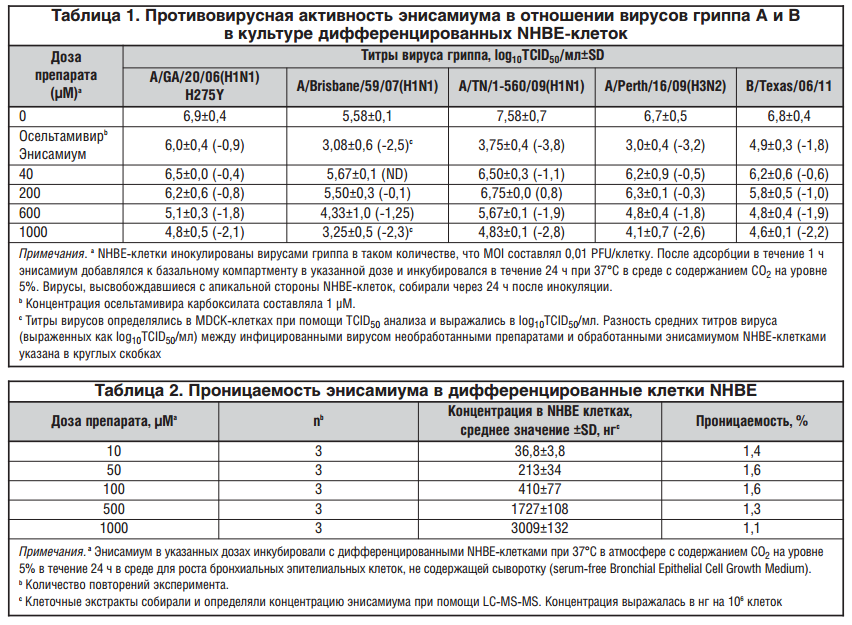
Дифференцированные NHBE-клетки были инфицированы вирусом гриппа A/Brisbane/59/2007 (H1N1) с показателями множественности инфекции (multiplicity of infection MOI), равными 0,01 PFU/клетку (A) (PFU — plaque-forming unit, бляшкообразующая единица — отдельная инфекционная вирусная доля в суспензии вирусов, которую обнаруживают по образованию бляшки), 0,001 PFU/клетку (B) и 0,0001 PFU/клетку (C). Энисамиум (1000; 500; 100; 50 и 10 μM) добавляли к базальному компартменту через 1 ч после инокуляции вируса (табл. 1, 2).
Смывы с апикальной поверхности клеток собирали через 24 ч (черные кружки) и 48 ч (черные квадраты) после заражения и титровали с помощью TCID50-анализа (рис. 2). Межевое значение, которое определяли в ходе анализа, составило 0,75 log10TCID50/мл.

Неинфицированные NHBE-клетки обрабатывали 1000 μM энисамиума, затем клетки отбирали через 0,25; 0,5; 1; 2; 4; 8 и 24 ч после контакта с исследуемым веществом. Представлены концентрации энисамиума в клетках (рис. 3).

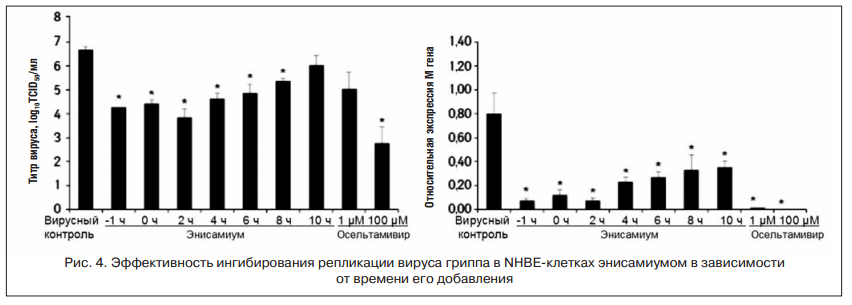
Дифференцированные NHBE-клетки были инфицированы вирусом гриппа A/Brisbane/59/2007 (H1N1) в количестве MOI=1,0 PFU/клетку и экспонировались с энисамиумом 2000 μM. Энисамиум добавляли в базальный компартмент через -1, 0, 2, 4, 6, 8 и 10 ч после инокуляции вируса и оставляли в течение 24 ч. Время инокуляции вируса указывается как 0 ч. Супернатанты собирали через 24 ч после заражения с верхнего отсека и титровали при помощи TCID50-анализа (A). Экспрессия матричного гена (Matrix gene — M gene) связана с контролем уровня вируса, экспрессия гена была нормирована по уровню мРНК β-актина в соответствующем образце (B) (рис. 4).
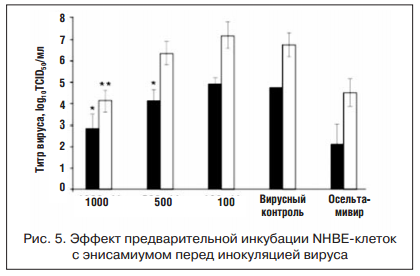
Дифференцированные NHBE-клетки были предварительно обработаны энисамиумом 1000, 500, 100 μM за 24 ч до инокуляции. Через 24 ч к NHBE-клеткам был инокулирован вирус гриппа A/Brisbane/59/2007 (H1N1) в количестве MOI=0,001 PFU/клетку; энисамиум находился в культуральной среде с базальной стороны в течение всего эксперимента. Осельтамивира карбоксилат (1 μM) был добавлен к базальному компартменту за 1 ч до инокуляции вируса, он находился там в течение всего эксперимента. Время инокуляции вируса указывается как 0 ч. Супернатанты собирали через 24 ч (черные столбики) и 48 ч (белые столбики) после инфицирования (рис. 5).
Заключение
- Энисамиум дозозависимо снижает репликацию всех исследуемых вирусов гриппа, в т. ч. сезонного H1N1, который имел мутацию H275Y NA, и таким образом обнаруживает эффективность против осельтамивир-резистентного вируса.
- Противовирусная эффективность энисамиума является дозозависимой, а эффект лучше выражен при более низких инфекционных дозах.
- Максимальная эффективность энисамиума обнаружена при его добавлении в течение 8 ч после заражения.
- Внутриклеточная концентрация энисамиума, достигаемая при его добавлении в количестве 1000 μM во время инфицирования, коррелирует с противовирусной эффективностью энисамиума.
Выявлена противовирусная активность противогриппозного соединения — энисамиума, которая подтверждает данные о его клинической эффективности. Хотя молекулярный механизм действия энисамиума до сих пор до конца не идентифицирован, данные, представленные выше, указывают на то, что препарат влияет на вирусную репликацию вирусов гриппа. В случае, когда энисамиум добавляли перед или вскоре после инфицирования, снижение экспрессии матричного гена и вирусных титров указывает на то, что он ингибирует синтез вирусной РНК. Интересно, что вирусные титры продолжали повышаться в присутствии энисамиума. Поэтому можно сделать вывод, что препарат угнетает репликацию вируса гриппа, но не блокирует ее полностью. Необходимы дальнейшие исследования для обеспечения лучшего понимания механизма действия энисамиума.
Благодарность. Данная работа финансировалась ПАО «Фармак». Мы выражаем глубокую благодарность доктору Дж. Морри (John Morrey), Д. Сми (Donald Smee) и Е. Говорковой (Elena A. Govorkova) за ценные советы и полезные обсуждения в ходе этих исследований.





Комментировать