Гемостаз и его система. Продолжение темы «Патология системы гемостаза».
Продолжение темы «Патология системы гемостаза»
Гемостаз – остановка кровотечения.
Система гемостаза – суперсистема, которая включает:
- плазменные прокоагулянты (система свёртывания)
- клеточные факторы сосудистые факторы
- антикоагулянты (противосвёртывающая система) плазминоген-плазминовую (систему «фибринолиза» калликреин-кининовую систему
- систему комплемента
Система гемостаза – термин, отражающий только одну сторону системы регуляции агрегатного состояния крови (РАСК). Термин «система РАСК» был предложен О.К.Гавриловым. Он точно отражает содержание понятия. Кровь может быть жидкой и свернувшейся – это два агрегатных состояния.
Система РАСК обеспечивает
- свободный кровоток по всем сосудам, включая тончайшие капилляры (т.е. нормальную текучесть крови) – основная первичная задача,
- остановку кровотечения при повреждении целостности сосудов путем образования тромба(в оричная задача)
- с последующей регенерацией тканей и реканализацией тромба.
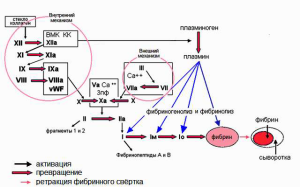
Нормальная текучесть крови (реология) поддерживается равновесием между свёртывающими и противосвёртывающими потенциалами системы. Свёртывание крови происходит в процессе образования тромба только в месте повреждения сосуда, имеющего диаметр более 100 мкм. Обсуждается проблема постоянного внутрисосудистого свёртывания, т.е. образования небольшого количества фибрина, который тут же разрушается плазмином, т.к. активация начала свёртывания и активация плазминогена происходят одновременно (рис.1).
Рис.1. Упрощённая схема свёртывания и фибринолиза.
Активаторами фактора XI и плазминогена может осуществляться ВМК, активным фактором XII и его фрагментами.
ВМК – высокомолекулярный кининоген. КК – элементы калликреин-кининовой системы. 3пф – пластиночный (тромбоцитарный) фактор 3; Iм – мономеры фибрина, Io – олигомеры фибрина. Появление первых молекул тромбина вызывает активацию факторов V, VII, VIII, XIII.
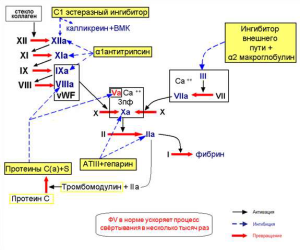
Каждому прокоагулянту противостоит антикоагулянт, что также поддерживают систему РАСК в равновесии, когда свёртывающие и протвосвёртывающие потенциалы равны нулю.
Рис.2. Основные антикоагулянты (выделены жёлтым цветом).
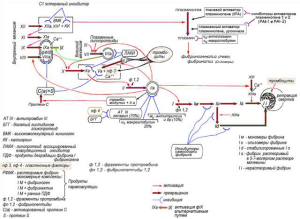
Полная схема системы РАСК представлена на рис.3.
Рис.3. Схем РАСК.
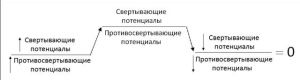
Повышение уровня свёртывающих потенциалов немедленно ведет к усилению противосвёртывающих потенциалов. А снижение одних приводит к снижению других, поэтому интегральный уровень системы всегда равен нулю.
Так же уравновешены агрегационные и антиагрегационные потенциалы тромбоцитов и эндотелия.
Если система РАСК функционирует нормально, то повреждение сосуда диаметром более 100 мкм приводит к образованию тромба. Происходит местное свёртывание крови с образование красного (включает эритроциты) фибринного свёртка (коагуляционный гемостаз). Таким образом выполняется вторая функциональная задача системы РАСК – остановка кровотечения.
Коагуляционный гемостаз осуществляется по внутреннему и внешнему механизмам активации протромбиназы (первая фаза). Оценка этих механизмов проводится разными тестами. Внутренний механизм оценивается в основном по АПТВ, а внешний механизм – по МНО. Также определяется вклад тромбоцитных факторов в активацию протромбиназы по индексу тромбоцитной активности.
В лабораторных тестах используется цитратная плазма, которая получается при взятии крови в пробирку, содержащую 3,8% раствора цитрата натрия в соотношении 9:1, при этом происходит замена натрия на кальций. Декальцинированная кровь не свертывается, и после центрифугирования отделяется плазма. Из факторов свёртывания в свежей цитратной плазме отсутствуют ионизированный кальций и тканевый фактор (ФIII), в то же время имеются все белковые плазменные факторы.
Если в эту плазму добавить кальций (рекальцификация), плазма свернётся. Раньше тест рекальцификации использовался в качестве теста для оценки общей коагуляционной способности крови по внутреннему механизму, как и время свёртывания. Сейчас ни то, ни другое не используется но многие тесты основаны на этом принципе.
При сохранении целостности сосудов и сохранении равновесия между свёртывающим и противосвёртывающими потенциалами кровь свободно течёт по всем кровеносным сосудам. Но существуют ситуации, когда это равновесие между этими потенциалами нарушено, при этом наблюдается геморрагический синдром или развивается склонность к образованию тромбов –тромбофилия. Повышенная кровоточивость (геморрагические синдромы рассмотрены в предыдущих сообщениях.
Тромбофилия
Согласно определению, данному Британским комитетом по гематологическим стандартам в 1990г., тромбофилия – это врождённый или приобретённый дефект гемостаза, приводящий к высокой степени предрасположенности к тромбозам.
Вероятно, термин «гиперкоагуляционный синдром», предложенный в 1997 г. А.И.Воробьёвым (А.И.Воробьев, С. А. Васильев, В. М. Городецкий. Гиперкоагуляционный синдром: патогенез, диагностика, лечение. Тер.архив, 2002, №7, с.73-76), имеет тот же смысл. Выдержки из статьи: «Под гиперкоагуляционным синдромом следует понимать коагулопатию, характеризующуюся определенными клиническими и преимущественно лабораторными признаками повышенного (ускоренного) свертывания крови при отсутствии образования тромбов. При гиперкоагуляционном синдроме не наблюдается образования тромбов ни в артериальной, ни в венозной системе, ни в системе микроциркуляции. Однако при этом регистрируется состояние повышенной готовности циркулирующей крови к свертыванию, но отсутствуют и признаки потребления факторов свертывания». Клинические проявления.
Могут наблюдаться тяжесть в голове, иногда головные боли, признаки эмоциональной и психической заторможенности, быстрая утомляемость и слабость. Один из самых характерных симптомов — при взятии крови из вены она сворачивается в игле, а пунктированные вены быстро выходят из строя — тромбируются и склерозируются.
Лабораторные признаки.
Уменьшение времени свертывания крови, но при этом сгусток рыхлый и нестойкий, уменьшение АПТВ, повышение агрегационных показателей тромбоцитов в ответ на добавление агонистов, постоянное удлинение фибринолиза как свидетельство его истощения. Гиперкоагуляционный синдром может перейти в синдром ДВС или манифестировать появлением тромбоза отдельных вен (нижние конечности, воротная вена и(или) её ветви, синусов мозга и др.) или артерий, часто головного мозга.
Для правильной оценки ситуации, прежде всего, надо вспомнить три ситуации, приводящие к тромбозам, которые описал Р.Вирхов ещё в позапрошлом веке (1884 г.):
- стаз крови в венах нижних конечностей,
- повышенная способность крови к тромбообразованию (тромбофилия) и повреждение стенки сосудов.
Сейчас речь идёт о второй ситуации, о гематогенной тромбофилии, т.е. о повышенной способности крови к тромбообразованию, в том числе независимой от состояния сосудов и наличия застоя крови в венах.
Основные факторы, вызывающие тромбофилию:
– генетические, включая дефицит и(или) аномалии факторов системы РАСК, включая точечные мутации (полиморфизм генов). Тромбоз происходит при наличии других (негенетических) факторов;
– приобретенные (избыток прокоагулянтов при злокачественных опухолях).
Генетические факторы:
1.Обусловленные недостаточностью антикоагулянтов: Дефицит антитромбина III (известно с 1965 г.) Дефицит протеина S (1984 г.)
Дефицит протеина С (1987 г.).
2.Обусловленные полиморфизмом генов, изменяющих качество белков, влияющих на гемостаз и влияющих на многие другие процессы:
- Фактор V Leiden G1691A – отсутствие чувствительности к антикоагулянтному действию комплекса протеинов С(а)+ S (см.рис.)
- PAI-1 (Serpine-1)… -675 4G/5G
- 5,10метилентетрагидрофолат-редуктаза (MTHFR) и другие ферменты, обеспечивающие избыток гомоцистеина
- G20210A (F2 протромбин) FGB: -455 G>A (b-фибриноген)
- Полиморфизм рецептора тромбоцитов ГП IIb/IIIа
Факторы, способствующие клиническому проявлению тромбофилии:
- Иммобилизация
- Травма
- Хирургическое вмешательство
- Ортопедическая хирургия
- Онкология
- Приём оральных контрацептивов
- Гормон-заместительная терапия
- Антифосфолипидный синдром
- Миелопролиферативные заболевания
- Постановка венозного катетера
- Возраст
- Ожирение
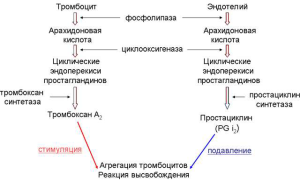
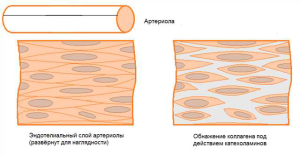
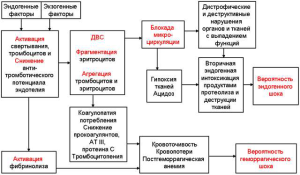
Нельзя исключить и влияние психоэмоциональных факторов. Катехоламины, во время психоэмоционального напряжения, вызывают сокращение клеток эндотелия, что приводит к обнажению коллагена субэндотелия и началу образования тромба по принципу: где тонко, там и рвётся, поэтому после «вызова на ковёр» к начальству вскоре у некоторых людей случается ишемический инсульт (рис.4).
Рис.4. Объяснение в тексте.
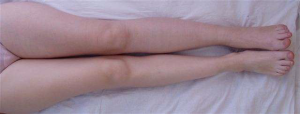
Пример наличия дефицита АТ III, выявленного беременностью. Пациентка 21 года. Ничем не болела. На 9-й неделе первой беременности появились боли в левой паховой области и бедре, отёк бедра быстро распространился на голень и стопу. На 3-й день при УЗДГ диагностирован тромбоз левой общей подвздошной вены с распространением в нижнюю полую вену, тромб флотирующий; начата антикоагулянтная терапия, установлен кава-фильтр, наложен эластичный бинт. Боли постепенно прошли, осталась тяжесть в ноге в вертикальном положении тела, усиливающаяся при ходьбе.
Рис.5. Отёк и цианоз левой ноги. Фото на 5-й день, когда отёк заметно уменьшился.
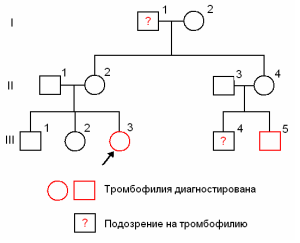
Рис.6. Схема родословной. Дефицит АТ. III3 – наша пациентка. У её двоюродного брата (III5) в возрасте 21 года после травмы также был флеботромбоз и установлен кава-фильтр. Его старший брат 24 лет (III4) после травмы 2-летней давности страдает болями в ногах, но не обследован. Отец матери пробанда (I1) умер после операции (было внутрибрюшинное кровотечение). С помощью ПЦР у пациентки выявлен выраженный дефицит антитромбина III.
Таким образом, генетический дефект проявился во время беременности.
При тромбозах и тромбоэмболиях у молодых пациентов (по крайней мере, до возраста 30 лет) всегда надо проводить дифференциальную диагностику между генетически обусловленной тромбофилией и онкологическими заболеваниями, включая гемобластозы. Тромбогеморрагический синдром и синдром ДВС
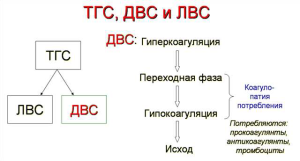
Термин «тромбогеморрагический синдром» (ТГС) был предложен и был описан М.С.Мачабели впервые в 1962 году: «Тромбогеморрагический синдром (ТГС) – это симптомокомплекс, сопровождающий патологию и экстремальные воздействия, обусловленный универсальным и неспецифическим свойством крови, лимфы, тканей, клеточных и межклеточных веществ обратимо и необратимо сгущаться, расслаиваться и растворяться вследствие потери отрицательного заряда». По-видимому, М.С.Мачабели в первые годы своих исследований придавала теории отрицательных зарядов А.Л.Чижевского в отношении ТГС избыточную ценность. Соотношение понятий «тромбогеморрагический синдром» (ТГС), «ДВС-синдром», и «локальное внутрисосудистое свёртыванние» (ЛВС), «коагулопатия потребления» и стадии ДВС представлены на схеме
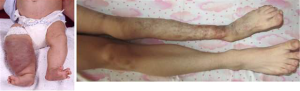
Локальное внутрисосудистое свёртывание наблюдается при синдроме Казабаха-Мерритт – гигантской гемангиоме (рис.7).
Рис.7. Синдром Казабаха-Мерритт, слева – у ребёнка (рисунок из Интернет), справа у молодого человека после многократных операций по поводу рецидивирующих тромбозов вен. Гипофибриногенемия (меньше 2 г/л,, которая имеется у пациента, трудно объяснить коагулопатией потребления, которая в настоящее время отсутствует.
Диагностические тесты про остром ДВС-синдроме:
I-я фаза – комплексная активация системы гемостаза
Клинические проявления отсутствуют
Лабораторные тесты:
тромбоциты, аПТВ, ПТ, ТТ – норма
фрагменты протромбина 1+2, Т-АТ (Т-АТ– комплекс тромбин+антитромбин) АТ чуть мономеры фибрина и РФМК ±
II-я фаза – декомпенсация системы РАСК
Клиниче ски е симпт омы : кровоточивость из раневых поверхностей и мест венепункций на фоне начинающейся полиорганной недостаточности
Лабораторные тесты :
- тромбоциты, фибриноген
- протромбиновое время, активированное парциальное протромбиновое время, тромбиновое время удлинены
- фрагменты протромбина 1+2, Т-АТ, продукты деградации фибрина (ПДФ)
- РФМК и фибринмономеры ++++
- антитромбин III может быть снижен
III-я фаза – развернутая картина ДВС
Клиническая картина – выраженный геморрагический синдром на фоне тяжелой полиорганной недостаточности
Лабораторные тесты:
- тромбоциты <50% исходного уровня
- протромбиновое время, активированное парциальное протромбиновое время, тромбиновое
- время резко удлинены, вплоть до бесконечности
- фибриноген, АТ III <50% исходного уровня
- фрагменты протромбина 1+2, Т-АТ, ПДФ
- мономеры фибрина и растворимые фибрин-мономерные комплексы (РФМК)
Расшифровка сокращений дана на рис.3.
Наличие в плазме повышенного количества РФМК косвенно свидетельствует о присутствии в крови активного тромбина.
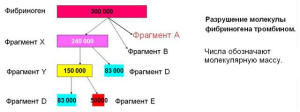
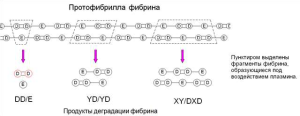
Увеличение D-димеров свидетельствует о наличии продуктов фибринолиза, т.е. о ДВС, т.к. D-димеры плазмином не разрушаются.







Комментировать