Изменения органа зрения при синдроме Марфана. Два основных метода лечения сублюксированного хрусталика. Разработка методов хирургического лечения эктопии хрусталика различной степени у детей с синдромом Марфана на основе усовершенствования способов фиксации и аутопластики капсульного мешка с оценкой их клинической эффективности. Результаты проведенных исследований
Сенченко Н.Я., Иркутский филиал ФГУ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова Росмедтехнологии»
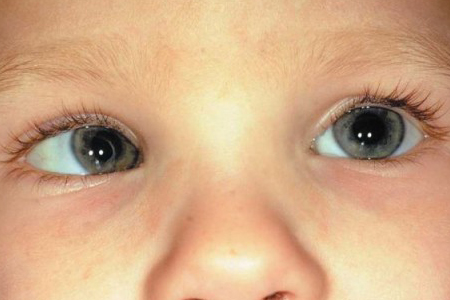
Изменения органа зрения при синдроме Марфана обусловлены наследственными поражениями соединительной ткани и сопровождаются прогрессирующей деструкцией и нарушением целостности волокон цинновой связки [1, 3-5]. Вследствие дисплазии связочного аппарата хрусталик смещается относительно зрительной оси, при этом нередко наблюдаются и другие врожденные аномалии: микросферофакия, колобомы хрусталика и др., что в целом ведет к формированию патологической рефракции глаза и, как правило, к значительному и стойкому снижению зрительных функций [3, 5, 8, 10].
В литературе до сих пор дискутируется вопрос о выборе наиболее эффективных способов хирургической коррекции данного состояния, что свидетельствует об отсутствии единых подходов к лечению этой тяжелой патологии органа зрения.
Существует два основных метода лечения сублюксированного хрусталика [1, 2, 6, 9, 11-13]. Первый способ предполагает удаление хрусталика вместе с капсульным мешком и внекапсульную фиксацию ИОЛ. Во втором случае выполняется факоаспирация с сохранением капсульной сумки, при этом линза имплантируется либо в капсулу хрусталика, либо фиксируется смешанным способом.
Сохранение капсулы в ходе хирургии сублюксированного хрусталика, несомненно, является более физиологичным, поскольку обеспечивает наиболее оптимальные структурные взаимоотношения в переднем сегменте глаза и тем самым создает условия для имплантации и стабильного положения эластичной ИОЛ. Вместе с тем применение традиционной техники, особенно при значительных эктопиях, сопряжено с высоким риском повреждения связочного аппарата хрусталика, потерей стекловидного тела, сложностью фиксации заднекамерной ИОЛ и как следствие — дислокацией линзы, развитием увеита и отслойки сетчатки [1, 7, 10, 14, 15].
Цель
Разработка методов хирургического лечения эктопии хрусталика различной степени у детей с синдромом Марфана на основе усовершенствования способов фиксации и аутопластики капсульного мешка с оценкой их клинической эффективности.
Материал и методы
Обследованы и прооперированы 18 детей (36 глаз) с клинически подтвержденным синдромом Марфана и эктопией хрусталика различной степени. Возраст детей составил от 5 до 14 лет.
Структурные нарушения иридо-витреохрусталикового комплекса оценивались с помощью биомикроскопии в естественных условиях и при медикаментозном мидриазе, ультразвуковой биомикроскопии, а также А- и В-сканирования. Степень эктопии хрусталика определялась в соответствии с классификацией, предложенной О.В. Шиловских [5].
Исследования функционального состояния зрительной системы включали определение остроты зрения вдаль без коррекции и с коррекцией, моно- и бинокулярно; характера зрения с расстояния 0,5, 1, 2, 5 м; глубинного зрения в условиях свободной гаплоскопии и способности к стереовосприятию с использованием тестов Ланга I и II.
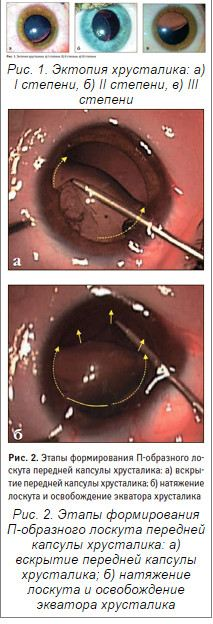
В зависимости от степени морфофункциональных нарушений органа зрения пациенты были разделены на 3 группы. В 1-ю группу вошли 5 детей (10 глаз) с эктопией хрусталика I степени (рис. 1а). У пациентов данной группы экватор хрусталика проецировался в зрачке только в условиях медикаментозного мидриаза (т.е. при его диаметре более 5,0 мм), волокна цинновой связки были растянуты, но сохранены. Исходная острота зрения составила в среднем 0,2±0,01 без коррекции и 0,4±0,02 с миопической коррекцией (5,2±1,6 дптр).
Во 2-ю группу были включены пациенты с эктопией хрусталика II степени (4 пациента, 8 глаз), у которых экватор хрусталика определялся в зрачке обычного диаметра (3,5 мм), зона дисплазии была более обширной, но целостность волокон цинновой связки и передней гиалоидной мембраны стекловидного тела не нарушена (рис. 1б). Острота зрения была равна 0,1±0,01 без коррекции и 0,2±0,02 с миопической коррекцией (11,5±1,8 дптр).
Пациенты 3-й группы (9 детей, 18 глаз) отличались еще более выраженным смещением хрусталика и изменением его связочного аппарата. Эктопия хрусталика III А степени была диагностирована на 12 глазах и III Б степени — на 6 глазах (рис. 1в). У пациентов с эктопией хрусталика III А степени экватор хрусталика располагался вблизи оптической оси, часть волокон цинновой связки разрушена, но передняя гиалоидная мембрана сохранена. У детей с эктопией хрусталика III Б степени, наряду с вышеуказанными изменениями, наблюдались дефекты переднего гиалоида стекловидного тела. Острота зрения была крайне низкой, ее средние величины определялись в пределах 0,05±0,01, коррекция отсутствовала.
У всех детей исследуемых групп были также выявлены нарушения процессов бинокулярного взаимодействия, глубинного и стереоскопического зрения (табл.).
Операции проводились двумя способами, отличающимися техникой вскрытия и фиксации капсульного мешка. У пациентов с эктопией хрусталика I степени передняя капсула вскрывалась методом непрерывного кругового капсулорексиса, при этом края капсулорексиса и зрачка последовательно захватывались ирис-ретракторами и фиксировались в области корнеоцентезов1. Эластичная ИОЛ Acrysof IQ — Acrysof SN60WF (Alcon, США) имплантировалась в капсульный мешок, опорные элементы линзы размещались в положении, перпендикулярном зоне дисплазии.
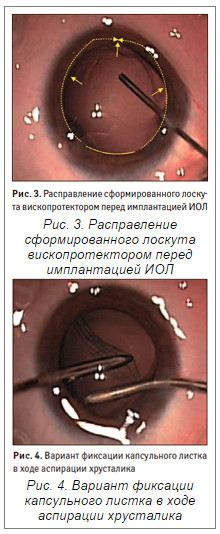
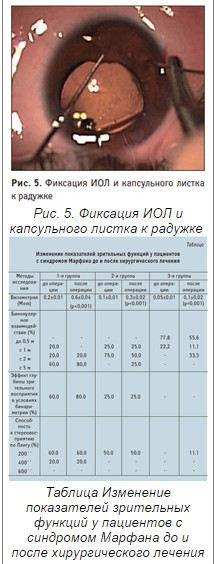
При более выраженной сублюксации хрусталика (II и III степени) выполнялась аутопластика капсульного мешка. В этих случаях в передней капсуле хрусталика формировался П-образный лоскут с дугообразными краями, который постепенно разворачивался в сторону зоны дисплазии волокон цинновой связки (рис. 2а). Путем натяжения капсульного листка экватор хрусталика полностью раскрывался (рис. 2б), лоскут укладывался поверх радужки и фиксировался специальным швом к радужке и роговице. После факоаспирации фиксирующий шов удалялся, лоскут передней капсулы заправлялся за радужку, размещался на измененных волокнах цинновой связки и расправлялся вископротектором Provisc (Alcon, США) 2. (рис. 3). При сохранной передней гиалоидной мембране стекловидного тела лоскут удерживался во время факоаспирации ирригационно-аспирационным наконечником факоэмульсификатора (рис. 4). Факоаспирация проводилась в режиме минимального ирригационного потока с постоянной подачей вископротектора Provisc. При имплантации ИОЛ Acrysof IQ один опорный элемент линзы устанавливался в капсульный свод, а другой — на капсульный листок в зоне дисплазии волокон цинновой связки, равномерно растягивая капсулу хрусталика, и вместе с капсульным листком фиксировался к радужке методом закрытой иридопластики (рис. 5). Таким образом, создавалась капсульная опора, исполняющая роль естественной диафрагмы как в ходе операции, так и в послеоперационном периоде. В целом это способствовало сохранению физиологических взаимоотношений внутриглазных структур и в дальнейшем — стабильному положению эластичной ИОЛ.
Срок наблюдения после операций составил от 1 года до 5 лет.
Результаты
В ходе операций осложнений не отмечено. Во всех случаях в процессе факоаспирации отмечались стабильное положение капсульного мешка и надежное блокирование зоны дисплазии волокон цинновой связки. Ни в одном случае не потребовалось изменения техники и объема вмешательства. В связи с тем, что у детей капсула хрусталика отличается высокой эластичностью, используемые манипуляции с капсульным мешком (фиксация ирис-ретракторами, шовная фиксация к радужке и роговице, натяжение) не вызвали его повреждения. Осложнений при имплантации и фиксации ИОЛ не отмечалось. В одном случае при формировании капсульного листка наблюдались расширение зонулодиализа и пролапс стекловидного тела с угрозой выпадения, однако дополнительное введение вископротектора позволило тампонировать грыжу стекловидного тела и фиксировать капсульный листок к радужке. В отдаленном послеоперационном периоде у 61,1% детей отмечался неравномерный фиброз задней капсулы хрусталика в оптической зоне. Положение интраокулярной линзы даже после лазерной дисцизии задней капсулы оставалось стабильным. Других осложнений, таких как отслойка сетчатки, кистовидный макулярный отек и т.д., не выявлено.
Зрительные функции после операции улучшились у всех пациентов (табл.). У детей 1-й группы острота зрения увеличилась в среднем до 0,6±0,04 (р<0,001), 2-й группы — до 0,3±0,02 (р<0,001). У пациентов 3-й группы функциональные результаты были заметно ниже и составили в среднем 0,1±0,02 (р<0,001). Повышение бинокулярных функций отмечено в 77,8% случаев. Вместе с тем показатели глубины восприятия зрительных образов существенно не изменились, а способность к стереовосприятию определялась только при низких уровнях диспарантности у детей 1-й и 2-й групп.
Выводы
Полученные результаты показывают, что разработанный комплекс методов хирургического лечения эктопии хрусталика разной степени у детей с синдромом Марфана обеспечивает надежную защиту волокон цинновой связки от дополнительного повреждения в ходе операции и тем самым создает условия для имплантации заднекамерной эластичной ИОЛ. Аутопластика капсульного мешка при значительных нарушениях связочного аппарата хрусталика позволяет сформировать новую капсульную опору, что снижает риск потери стекловидного тела и развития других осложнений.
Предложенные методы хирургического лечения создают оптимальные условия для дальнейшей реабилитации детей с тяжелой патологией органа зрения, обусловленной повреждениями его оптического аппарата на фоне системного дисгенеза соединительной ткани.
Литература
1Способ хирургического лечения врожденной эктопии хрусталика I-II степени при синдроме Марфана у детей: Пат. 2352303 Рос. Федерация / Н.Я. Сенченко, С.В. Сташкевич; Заявитель и патентообладатель ФГБУ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; Опубл. 20.04.2009.
2Способ хирургического лечения врожденной эктопии хрусталика II-III степени при синдроме Марфана у детей: Пат. 2353340 Рос. Федерация / Н.Я. Сенченко, С.В. Сташкевич; Заявитель и патентообладатель ФГБУ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» Минздрава России; Опубл. 27.04.2009.
Сенченко Н.Я. Оптимизация методов хирургического лечения эктопии хрусталика различной степени у детей с синдромом Марфана // Офтальмохирургия.– 2014.– No 3.– С.26-30.







Комментировать