Возможности корригирующего влияния системной энзимотерапии на компоненты синдрома инсулинорезистентности. Внедрением новых технологий диагностики и лечения больных с ишемической болезнью сердца, включая инвазивные. Описание. Риски.
В.М. Коваленко, Т.В. Талаева, В.В. Братусь
Национальный научный центр «Институт кардиологии им. акад. Н.Д. Стражеско» АМН Украины, г. Киев
Несмотря на значительные успехи, связанные с разработкой и применением новых фармакологических средств, внедрением новых технологий диагностики и лечения больных с ишемической болезнью сердца (ИБС), включая инвазивные, кардиальная патология остается ведущей причиной смертности среди населения земного шара. Более того, отмечается выраженная тенденция к возрастанию распространенности, повышению тяжести клинического течения и исходов этой патологии, ее развитию в более раннем возрасте.
В значительной мере это связано с тем, что как первичная, так и вторичная профилактика атеросклероза и ИБС имеют запоздалый характер и начинаются на фоне уже развитого процесса, при выраженных его клинических проявлениях. В этих условиях возможности как профилактических, так и терапевтических воздействий ограничены предупреждением развития острых форм течения заболевания, но не прогрессирования основного процесса и, тем более, не приводят к его регрессу. В то же время, ранняя диагностика и проведение специфической терапии на доклиническом этапе развития кардиальной патологии при наличии нарушений, которые имеют в значительной мере обратимый функциональный характер, могут не только предупреждать ее прогрессирование, но и устранять факторы, лежащие в основе патогенеза атеросклероза и ИБС. В оптимальном варианте профилактические и терапевтические воздействия должны начинаться на уровне факторов риска атеросклероза, и потому их определение и определение возможностей целенаправленного воздействия на них является одной из важнейших задач современной кардиологии и фармакологии.
Длительное время патогенетической основой атеросклероза и ИБС считалась гиперхолестеринемия (ГХЕ), и уровень холестерина (ХС) в крови рассматривался как ведущий показатель риска кардиальной патологии и критерий эффективности предупреждения развития и прогрессирования ИБС. Однако последующие исследования показали, что ГХЕ не является обязательным условием для развития атеросклероза и потому не может рассматриваться как его этиологический фактор. В настоящее время установлено уже более 200 факторов риска атеросклероза, и к числу наиболее значимых как по частоте, так и по степени участия в атерогенезе относят нарушения липидного спектра крови, артериальную гипертензию (АГ), системное воспаление, сахарный диабет (СД), курение.
Более того, оказалось, что эти факторы риска в значительном числе случаев возникают не изолированно, а сочетанно, и тогда патогенетическая значимость каждого из них резко возрастает. Эта тенденция особенно отчетливо проявляется на примере АГ. Примерно половина всех лиц с АГ имеют признаки инсулинорезистентности (ИР) [38], а распространенность СД 2-го типа, определенная среди у 12 550 лиц с АГ, была увеличена примерно в 2,5 раза по сравнению с лицами с нормальным артериальным давлением (АД) [16]. Характерной чертой АГ является также эктопическое накопление жировой ткани в висцеральной и эпикардиальной зонах [40].
Кроме того, интегральная значимость риска развития атеросклероза и ИБС при наличии нескольких факторов атерогенеза возрастает в большей степени, чем суммарное значение риска этих факторов. Так, согласно определению Группы по гипертензии (Hypertension Writing Group, HWG), пациенты могут рассматриваться как «гипертензивные» в значительной мере независимо от уровня АД, при случайных или перемежающихся его повышениях, если у них отмечается наличие хотя бы одного из маркеров или факторов риска кардиоваскулярной патологии. К ним относят СД, избыточную массу тела с индексом массы тела, превышающим 24 кг/м2, и окружностью талии более 100 см у мужчин и 90 см у женщин, уровень в крови ХС липопротеинов (ЛП) низкой плотности (ХС ЛПНП) более 3,35 ммоль/л, триглицеридов (ТГ) – 3,9 ммоль/л, глюкозы – 100 мг/дл, ХС ЛП высокой плотности (ХС ЛПВП) – менее 1,30 ммоль/л, возраст более 60 лет, курение, сидячий образ жизни. Несмотря на то, что в настоящее время порогом гипертензии считается АД, превышающее 140/90 мм рт. ст. (130/80 мм рт. ст. у лиц с СД), в ряде исследований показан эффект антигипертензивной терапии, начинающейся при более низком давлении, но при наличии других факторов риска [36, 46]. В то же время, при отсутствии дополнительных факторов риска лечение пациентов с предгипертензивным уровнем давления (между 120/80 и 139/89 мм рт. ст.) не сочеталось с уменьшением частоты летальных исходов на протяжении 12,8 года наблюдения [33]. В проспективном исследовании с участием 49 582 лиц в возрасте 25–74 лет без инсульта и ИБС в исходном состоянии риск развития инсульта в течение 19 лет составил 1,35 для лиц с изолированной умеренной АГ (АД до 150/95 мм рт. ст.), 1,98 – для лиц с АД, превышающим 160/95 мм рт. ст., или получающих антигипертензивную терапию, 2,54 – для лиц с изолированным СД 2-го типа, 3,51 – для лиц с сочетанием СД 2-го типа и умеренной АГ и 4,50 – для лиц с СД 2-го типа и тяжелой гипертензией [21].
Те же соображения применимы к оценке уровня ХС, и риск развития ИБС значительно возрастает уже при низких цифрах ХС у лиц с наличием других кардиальных факторов риска [19, 28]. В исследовании TNT (Treating to New Targets) повышение риска развития основных конечных точек у лиц со стабильной стенокардией отмечено даже при уровне ХС ЛПНП в нижнем квартиле (менее 64 мг/дл, или 1,86 ммоль/л), но при наличии других факторов риска, примерно в той же степени, как и в верхнeм [29]. Установлено, что при всех уровнях ХС ЛПНП риск, связанный с его повышением, значительно ниже у пациентов с отсутствием дополнительных факторов, чем с их наличием.
Отдельные компоненты атерогенеза характеризуются тенденцией не только к сочетанию, но и к взаимопотенцирующему действию. Показано, что при наличии нескольких патогенетических факторов атеросклероза и в результате их сочетанного действия риск развития ИБС может возрастать более чем в 20 раз при том же уровне АД или ХС в крови. Так, в когорте некурящих пациентов среднего возраста без СД с уровнем общего ХС порядка 155 мг/дл (4 ммоль/л), ХС ЛПВП – 1,6 ммоль/л и систолическим АД (САД) 130 мм рт. ст. величина абсолютного риска развития кардиальных явлений на протяжении 5 лет составляет 1 %. Однако риск возрастает в 10 раз, если аналогичные пациенты являются курильщиками с содержанием общего ХС на уровне 7 ммоль/л и ХС ЛПВП – не выше 1 ммоль/л. Если у пациентов отмечается также СД 2-го типа, то 5-летний риск увеличивается в 20 раз при идентичном уровне АД. Поэтому пациенты, которые по стандартному определению относятся к категории лиц с пограничной гипертензией, при наличии СД 2-го типа должны рассматриваться, по определению HWG, как гипертоники и пациенты c высоким кардиальным риском. Это действительно и в случаях, когда у пациентов нет СД 2-го типа, но они являются курильщиками или имеют другие факторы риска [4].
Комплексный характер патогенеза атеросклероза впервые был описан в литературе в 1923 г. на основании частого сочетания АГ, гипергликемии и гиперурикемии [26]. В 1988 г. G. Reaven систематизировал концепцию этой комплексности в понятии «синдрома X» и предположил, что основой сочетанного развития его основных проявлений являются ИР и компенсаторная гиперинсулинемия. В развитие этой концепции другие исследователи предложили более расширенную трактовку природы синдрома с включением в число его компонентов также ожирения, СД 2-го типа, дислипидемии, гипертензии и ряда факторов, вторичных по отношению к ожирению, прежде всего системного воспаления и возрастания коагуляционного потенциала крови [30]. В последнее время для обозначения этого состояния более часто используется термин «метаболический синдром» (МС), при том, что большинство исследователей рассматривают его как синоним термина «синдром ИР».
Исследованию механизмов развития МС, его патогенетической значимости как доклинической стадии ИБС и СД 2-го типа, определению путей профилактики и лечения этого состояния в последние годы уделяется особое внимание. В значительной мере это связано с тем, что наличие МС удваивает риск развития ИБС и в 5 раз повышает риск развития СД 2-го типа. У лиц, умерших на протяжении 10 лет наблюдения от макроваскулярных поражений, отмечены значительно более высокие уровни в крови глюкозы и HbA1c. Возрастание концентрации HbA1c на 1 % сочеталось с увеличением летальности от ИБС или других кардиоваскулярных нарушений на 40 %, а возрастание показателя общей летальности в этих условиях после учета возраста и факторов риска составило 1,46 [23].
Характерным для МС является экспоненциальное возрастание риска по мере увеличения числа компонентов, которое отчетливо проявляется и становится статически достоверным при наличии трех компонентов. Аналогичная зависимость сохраняется, когда явления подразделяются на кардиальные и церебральные [35], и у лиц с наличием всех 5 компонентов МС риск развития инсульта увеличен в 5 раз [10].
Помимо этого, МС характеризуется чрезвычайно высокой распространенностью и высокими темпами ее возрастания. Еще в 1988–1994 гг. распространенность MC в США достигала 25 %, что составило 47 млн человек, а в настоящее время она охватывает более 1/3 взрослого и значительную часть детского населения [12]. По данным последних эпидемиологических исследований, распространенность МС составляет 34–40 % среди мужчин и 35–38 % среди женщин в зависимости от того, какой принцип положен в диагностику синдрома [44], а у пациентов с клиническими проявлениями атеросклероза диагноз МС устанавливается более чем в 45 % случаев [27, 32]. В соответствии с результатами метаанализа 43 крупных исследований, включившего в общей сложности 172 573 лица, риск развития тяжелых клинических проявлений ИБС и летального исхода у лиц с МС составляет 1,78, и наиболее высок он у женщин, достигая 2,63. Риск остается достоверно увеличенным даже после учета традиционных факторов атерогенеза, и это свидетельствует о том, что действие МС не полностью реализуется через их активацию. Помимо этого, наличие МС сочетается также со значительным возрастанием тяжести течения заболевания и снижением эффективности лечения, особенно хирургических и эндоваскулярных вмешательств.
До настоящего времени вопрос о патогенетической основе МС остается дискуссионным, и у клиницистов нет единства в отношении принципа лечения лиц с этой патологией. Ряд исследователей рассматривает МС как искусственное понятие, объединяющее отдельные независимые факторы атерогенеза по принципу случайного совпадения, и на этом основании предложен симптоматический подход к терапии синдрома с коррекцией каждого из его компонентов. Одной из отрицательных сторон этого принципа является то, что воздействие только на один из патогенетических факторов МС без учета влияния на другие может оказывать отрицательный эффект. Так, бета-адреноблокаторы и тиазидные диуретики, являясь высокоэффективными в лечении гипертензии и предупреждении ее тяжелых клинических исходов, вызывают отрицательные метаболические эффекты и снижают чувствительность к инсулину [9].
В то же время, большинство исследователей разделяют точку зрения G. Reaven – основоположника учения о МС – о причинной роли ИР в развитии ведущих его компонентов. Этот патогенетический подход означает, что лечение пациентов с МС должно быть ориентировано не столько на устранение отдельных его компонентов, даже преобладающих в каждом конкретном случае, как на устранение факторов, вызвавших развитие ИР.
В исследованиях последних лет установлено, что ИР имеет многофакторную природу, однако ведущей причиной ее развития является воспаление с накоплением в крови медиаторов воспаления, прежде всего – фактора некроза опухоли-a (ФНО-a) и интерлейкина-6 (ИЛ-6). Это подтверждается наличием в проведенных исследованиях четкой корреляционной зависимости между их концентрацией в крови и признаками синдрома ИР [20]. При этом ФНО-a оказывает прямое угнетающее действие на передачу в клетку инсулинового сигнала, аналогичный эффект оказывает и один из белков острой фазы С-реактивный протеин (СРП) [11,45]. ФНО-a также активирует липогенез с возрастанием внутриклеточного содержания свободных жирных кислот (СЖК) и реализацией их цитотоксического эффекта, прежде всего способности вызывать развитие ИР [42].
Приведенные данные означают, что системное воспаление может лежать в основе снижения чувствительности к инсулину и развития комплекса метаболических нарушений, обозначаемых как «синдром ИР или МС» и являющихся патогенетической основой атеросклероза. Это означает, что угнетение системного воспаления может быть одним из реальных путей предупреждения или устранения всего комплекса факторов синдрома ИР и снижения в результате риска развития ИБС.
В последние годы в клинике заболеваний, сочетающихся с выраженной активацией воспаления, широкое применение находит системная энзимотерапия. Показано, что одним из важнейших компонентов воспаления является активация нейтрофилов с высвобождением нейтральных протеаз (колагеназа, эластаза), которые определяют интенсивность воспалительной реакции и глубину повреждения окружающих тканей. Активность этих протеаз тормозится эндогенными сывороточными ингибиторами a2-макроглобулином, a1-антитрипсином, a1-антихимотрипсином. Однако в динамике хронической воспалительной реакции возникает дефицит ингибиторов в результате их истощения и возрастает повреждающее действие протеаз. Препараты, применяемые для системной энзимотрапии, содержат протеолитические ферменты как животного, так и растительного происхождения, и они восполняют дефицит эндогенных сывороточных ингибиторов протеаз. Основными ингредиентами препаратов, применяемых для системной энзимотерапии, являются бромелаин и папаин. Бромелаин является протеазой, полученной из грейпфрутов; его эффект заключается в предупреждении или устранении отека, содействии расслаблению сосудистых гладкомышечных клеток, угнетении агрегации тромбоцитов, усилении абсорбции антибиотиков. Папаин, получаемый из Carica папайи, эффективен в уменьшении выраженности отека, воспаления; он также способен связывать цитокины, ускорять репаративные процессы. В состав вобензима входят также химотрипсин, трипсин, амилаза, липаза, в состав флогензина – трипсин. Комбинация протеолитических ферментов в препаратах, применяемых для системной энзимотерапии, усиливает их терапевтическую эффективность, так как каждый из ферментов действует на строго определенные пептидные связи в молекулах белков, и потому обладает более узким спектром действия.
Результаты проведенных до настоящего времени экспериментальных и клинических исследований свидетельствуют о высокой эффективности системной энзимотерапии у пациентов с ревматоидным артритом, системной красной волчанкой, другими аутоиммунными заболеваниями. Так, добавление вобензима к стандартной терапии у 78 больных с ревматоидным артритом сопровождалось уменьшением СОЭ, содержания иммуноглобулинов и циркулирующих иммунных комплексов на 42 % на фоне стимуляции клеток, продуцирующих интерферон и возрастание его содержания в крови [1]. Применение вобензима дополнительно к базисной терапии у больных с хроническим течением ИБС проявлялось отчетливой клинической эффективностью у 82 % случаев с уменьшением частоты и тяжести приступов стенокардии, повышением толерантности к физической нагрузке, уменьшением потребности в приеме антиангинальных препаратов. Это сочеталось с уменьшением содержания общего ХС в крови на 25 % в конце 2-недельного курса лечения, уменьшением содержания ХС ЛПНП и ХС ЛПОНП, увеличением содержания ХС ЛПВП на 45 % [2]. У 45 больных с гипертрофической кардиомиопатией применение вобензима на фоне общепринятой терапии сопровождалось нормализацией липидного спектра крови, снижением интенсивности оксидантного стресса, активности ренина и альдостерона, восстановлением нормальных показателей иммунного статуса [3].
Защитное действие вобензима отмечено также при острых воспалительных процессах, и у больных с инфарктом миокарда его применение вдвое уменьшило прирост содержания в крови ФНО-a, концентрацию С3 компонента комплемента. Этот эффект сочетался с нормализацией содержания ХС в крови, выраженной тенденцией к снижению уровня ТГ, повышением уровня антиатерогенных апоА-1-содержащих ЛП и увеличением коэффициента апоА/апоВ. У пациентов после оперативного вмешательства при применении вобензима отмечено интенсивное и достоверное уменьшение содержания в крови СРП.
Наличие у препаратов, применяемых для системной энзимотерапии, выраженного противовоспалительного действия, способности нормализовать липидный спектр крови послужило основанием для проведения нами экспериментального исследования, в котором на модели синдрома ИР исследовалась эффективность вобензима в предупреждении его развития и угнетении ведущих метаболических нарушений и определялись механизмы этого эффекта.
материал и методы
Исследование проведено в хроническом эксперименте на кроликах, находящихся в течение 8 нед на диете, обогащенной липидами. Для этого к стандартной диете добавляли сухие молочные сливки из расчета 0,75 г/кг массы. 30 кроликов составили контрольную группу, 10 получали вобензим из расчета на 1 кг массы с 1-го дня перевода на высокожировую диету, 10 других – с начала 5-й недели. В исходном состоянии, через 2, 4, 6 и 8 нед осуществляли забор крови из краевой вены уха и определяли в ней показатели воспаления (СРП, активность моноцитов (МЦ) по внутриклеточному содержанию малонового диальдегида (МДА)), свободнорадикального окисления липидов (СРО) по содержанию МДА в плазме крови, определяли активность ангиотензинпревращающего фермента (АПФ) как показателя активности ренин-ангиотензиновой системы, осуществляющей в этих условиях сопряжение системного воспаления, оксидантного стресса и нарушений метаболизма. Исследовали спектр ЛП крови, содержание в ней общего ХС и ТГ, СЖК, рассчитывали индекс атерогенности (ИА) по отношению ТГ/ХС ЛПОНП. Для определения чувствительности к инсулину использовали подкожный инсулиновый тест (ПИТ): по изменениям содержания глюкозы в крови через 30 мин после введения инсулина (0,2 МЕ на 1 кг массы) оценивали системную чувствительность к инсулину (СЧИ), содержания ТГ – чувствительность к инсулину гепатоцитов (ГЧИ). Содержание СЖК в крови натощак являлось косвенным критерием чувствительности адипоцитов к инсулину. О нарушениях метаболизма углеводов судили по изменениям содержания в крови глюкозы и гликозилированного гемоглобина (HbA1c). Методом биотестирования с использованием культуры мышиных макрофагов определяли содержание в крови модифицированных ЛПНП (мЛПНП) и ЛПОНП (мЛПОНП). Определяли также концентрацию циркулирующих иммунных комплексов (ЦИК) и содержание в них ХС и ТГ как показателей иммуногенности модифицированных ЛП и включения их в состав ЦИК в качестве антигенов. Методом турбометрии оценивали интенсивность агрегации тромбоцитов, определяли также содержание в крови необратимых тромбоцитарных агрегатов. Весь полученный цифровой материал обработан статистически с использованием пакета анализа программы «Microsoft Exсel». Принцип проведения исследования детально изложен в ранее опубликованной работе [4].
результаты и их обсуждение
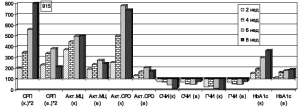
В соответствии с полученными данными, содержание кроликов на диете, обогащенной липидами, сопровождалось развитием комплекса биохимических и функциональных изменений, соответствующих синдрому ИР, и патогенетической основой этих изменений являлось развитие системного воспаления. Содержание в крови СРП – маркера системного воспаления и одного из наиболее важных белков острой фазы – возросло в конце 2-й недели перевода животных на высокожировую диету практически в 4 раза (с (1,75±0,11) до (6,93±0,36) мг/л, Р<0,001). Интенсивность воспаления прогрессивно возрастала в динамике наблюдения, и в конце 8-й недели содержание СРП было увеличено более чем в 18 раз по сравнению с исходным значением (Р<0,001). Значительно возрастала также активность циркулирующих МЦ; ее показатель – внутриклеточное содержание МДА, был увеличен в конце 2-й недели почти в 4 раза (с (0,98±0,06) до (3,63±0,19) мкмоль/мг белка, Р<0,001), прогрессивно возрастал в ходе исследования и в конце 8-й недели превышал исходное значение в 5 раз (Р<0,001). Развитие системного воспаления сочеталось с выраженной активацией СРО, и содержание в плазме крови МДА – его конечного продукта, было увеличено в конце 2-й недели в 2,5 раза (с (0,45±0,03) до (2,83±0,06) ммоль/л, Р<0,001), в конце последнего этапа исследования – в 7,5 раза (Р<0,001). Одним из важнейших факторов, определявших как развитие воспаления, так и возрастание интенсивности CPO, было возрастание активности АПФ. Оно достигало 16 % – в конце 2-й недели, 62; 95 и 250 % – в конце соответственно 4-й, 6-й и 8-й недель. Следствием этого было прогрессирующее снижение активности каталазы – одного из важнейших антиоксидантных ферментов плазмы, соответственно на 20; 34; 48 и 50 %.
Возникновение и прогрессирование воспалительного процесса и оксидантного стресса сопровождалось развитием ИР и характерных для нее метаболических нарушений. Результаты ПИТ свидетельствуют о снижении СЧИ в конце 2-й недели на 26 % (Р<0,05), в конце 6-й– на 54 % (Р<0,01), в конце 8-й недели – на 85 % (Р<0,001). В еще большей степени угнеталась ГЧИ, и ее показатель был уменьшен на этих этапах исследования соответственно на 71 %, 83 % и практически на 100 % (Р<0,001). О развитии ИР адипоцитов можно было косвенно судить по повышению уровня СЖК в крови – более чем в 3 раза (с (0,11±0,01) до (0,37±0,02) ммоль/л, Р<0,001) в конце 2-й недели и в 5 раз – на последнем этапе исследования (Р<0,001). В результате развития ИР происходило закономерное возрастание содержания в плазме HbA1c (на 50 %, с (2,83±0,18) до (4,28±0,22) мкмоль фруктозы/1 г Hb, Р<0,01) в конце 2-й недели, в 3,7 раза (Р<0,001) – в конце 8-й недели, а также глюкозы: на уровне тенденции в конце 2-й недели и на 88 % (с (7,34±0,56) до (13,8±1,1) ммоль/л, р<0,001) – в конце эксперимента.
Эти изменения сочетались с развитием проатерогенной дислипидемии, важнейшим показателем которой было появление и прогрессирование ГТЕ в результате возрастания содержания в крови ЛПОНП. Уровень ТГ в плазме крови повысился на первом этапе исследования практически вдвое (с (0,74±0,05) до (1,45±0,08) ммоль/л, Р<0,001), на последнем – в 3,4 раза (Р<0,001); аналогичным образом увеличилось содержание и ХС ЛПОНП. Это сочеталось с выраженным уменьшением содержания ХС ЛПВП – на 30 % (с (0,49±0,03) до (0,35±0,02) ммоль/л, Р<0,01) в конце 2-й и на 41 % (Р<0,001) – в конце 8-й недели. В результате ИА, который рассчитывался от отношению ТГ/ХС ЛПВП, возрос в конце 2-й недели более чем в 2,5 раза (Р<0,001), в конце 8-й – в 5,7 раза (Р<0,001). Увеличилось также содержание в крови общего ХС – на 70 % (с (0,98±0,06) до (1,68±0,08), Р<0,01) на первом этапе исследования и почти в 2,5 раза (Р<0,001) – на заключительном этапе.
Помимо количественных изменений спектра ЛП крови, отмечены также качественные их нарушения в виде модификации. Это проявлялось прогрессирующим возрастанием содержания в крови проатерогенных мЛПНП – на 120 % (Р<0,001) через 2 нед содержания на липидной диете и более чем на 450 % (Р<0,001) – через 8 нед. Содержание мЛПОНП возросло на этих этапах соответственно в 2 и в 3,7 раза (Р<0,001). Модифицированные ЛП приобретали также антигенные свойства и вызывали развитие иммунной реакции, в результате чего содержание в плазме крови ЦИК возросло в 2,5 раза в конце 2-й недели и более чем в 12 раз в конце исследования. Значительно увеличилось также содержание в ЦИК ХС (в 2,0 и в 4,5 раза, Р<0,001), а также ТГ (в 2,0 и 5,6 раза, Р<0,001) в конце соответственно 2-й и 8-й недели. Эти данные свидетельствовали о включении мЛПНП и мЛПОНП в состав ЦИК в качества аутоантигенов.
Результаты парного корреляционного анализа свидетельствовали о наличии прямой связи между системным воспалением и важнейшими проявлениями синдрома ИР. Так, установлена сильная прямая зависимость между содержанием в плазме крови СРП, количеством мЛПНП и мЛПОНП, содержанием ТГ в ЦИК с коэффициентом корреляции, превышающим 0,9. Прямая сильная корреляционная связь установлена также между уровнем СРП и активностью МЦ (r=0,86), содержанием в крови HbA1c (r=0,73), глюкозы (r=0,6), СЖК (r=0,43), а также ИА (r=0,52).
Таким образом, полученные в контрольной серии исследований данные свидетельствовали о развитии у кроликов, находящихся на высокожировой диете, выраженного системного воспаления и комплекса метаболических изменений, входящих в состав синдрома ИР и обусловливающего его проатерогенное действие. Результаты указывали также на доминирующую роль воспаления в развитии этого синдрома. Эти данные позволили нам рассматривать системную энзимотерапию с применением вобензима как потенциальный путь для коррекции метаболических и функциональных нарушений, которые возникают при воспалении как следствие ИР и являются важнейшими факторами атерогенеза и риска развития ИБС.
Для проверки этого предположения мы воспроизводили синдром ИР на фоне применения вобензима как в режиме профилактики с 1-го дня перевода животных на высокожировую диету, так и в режиме лечения с начала 5-й недели на фоне уже выраженных проявлений синдрома.
Выраженный защитный эффект отмечен при применении вобензима в профилактическом режиме, с первого дня содержания животных на обогащенной липидами диете. В целом, действие вобензима имело кумулятивный характер: начальные его проявления отмечались не ранее чем через 2 нед, и эффект прогрессивно возрастал в динамике исследования. Прирост содержания в крови СРП в конце 4-й нед был незначительно меньше, чем в контроле, в конце 6-й недели он был уменьшен на 32 %, в конце 8-й – более чем в 4 раза. Существенно уменьшался под действием вобензима и прирост активности МЦ: на 48 % – через 4 нед и на 57 % – через 8 нед. Резко ослаблялась активация СРО, и прирост содержания МДА в плазме был уменьшен в 2 раза через 2 нед и на 77 % – через 8 нед. Этому способствовала способность вобензима предупреждать активацию АПФ более чем на 40 % в конце 8-й недели исследования.
Противовоспалительный и антиоксидантный эффекты вобензима сочетались с выраженным защитным действием в отношении развития ИР. Системная чувствительность к инсулину в конце 8-й недели снижалась в 2,5 раза меньше, чем в контроле, чувствительность гепатоцитов сохранялась на уровне 42 % нормальной, тогда как в контроле она полностью отсутствовала. Чувствительность адипоцитов к инсулину была вдвое большей, чем в контроле, о чем свидетельствовал вдвое меньший прирост содержания СЖК в крови. В результате предупреждалось развитие выраженной гипергликемии, и уровень глюкозы в крови был почти на 20 %, уровень HbA1c – на 48 % ниже контрольного.
Применение вобензима в профилактическом режиме оказывало также выраженное защитное метаболическое и антиатерогенное действие. ИА увеличился в конце 4-й и 8-й недели соответственно на 30 и 65 % менее выражено, чем в контроле, свидетельствуя о предупреждении развития дислипидемии, на 30 и 50 % меньше возросло содержание в крови общего ХС, ТГ и ХС ЛПОНП, содержание в крови мЛПНП было меньшим соответственно на 25 и 43 %, мЛПОНП – на 25 и 62 %. На 57 и 73 % меньше возросла концентрация в крови ЦИК, на 36 и 62 % – содержание в них ХС, на 40 и 64 % – ТГ.
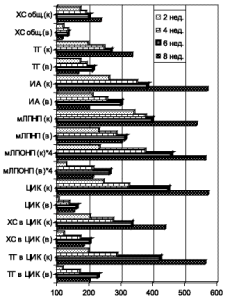
Применение вобензима с начала 5-й недели также не характеризовалось существенным влиянием на показатели метаболизма и факторы атерогенеза в течение первых 2 нед. Однако в конце 8-й недели, то есть через 4 нед применения препарата, отмечен закономерный и выраженный защитный эффект, прежде всего – противовоспалительный. Прирост содержания СРП в плазме был примерно в 3 раза меньшим, чем в контроле, возрастание активности МЦ было меньшим на 40 %. На 30 % меньше возрастала активность АПФ, на 20 % – интенсивность СРО липидов и содержания в крови ее конечного продукта – МДА. В результате предупреждалось развитие ИР, системная чувствительность к инсулину уменьшилась в 6 раз менее выражено, чувствительность гепатоцитов сохранялась на уровне 30 %, тогда как она полностью отсутствовала у животных контрольной группы, возрастание содержания в крови СЖК было меньшим на 40 %, свидетельствуя о пропорционально более выраженной чувствительности адипоцитов к инсулину. В результате на 27 % угнетался прирост содержания в крови глюкозы, на 26 % – HbA1c. Существенно менее выраженными были проявления дислипидемии, на 20 % меньше увеличился ИА, на 40 % меньше возросло содержание в крови ТГ и ЛПОНП, на 28 % – общего ХС. Отмечено также выраженное антиатерогенное действие вобензима, угнетение модификации ЛП, как проатерогенной, так и иммуногенной. Содержание в крови мЛПНП возросло на 43 %, мЛПОНП – на 63 % меньше, чем в контроле, прирост количества ЦИК был меньшим на 16 %, содержания в них ХС меньшим на 36 %, ТГ – на 34 % (рис. 1 и 2).
Рис. 2. Прирост показателей атерогенности и иммуногенности ЛП плазмы (в % к исходному значению), у животных контрольной группы (к) и животных, получавших вобензим с 1-го дня перевода на диету, обогащенную липидами (в).
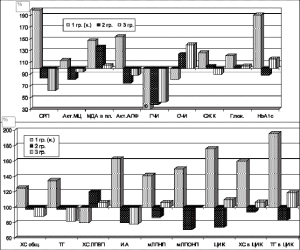
Рис. 3. Сопоставление изменений исследованных показателей между 4-й и 8-й неделями в контроле (1 гр.), при применении вобензима с 4-й недели (2 гр.) и с 1-го дня эксперимента (3 гр.).
Положение о противовоспалительных свойствах вобензима как основе его защитного действия в условиях синдрома ИР было подтверждено результатами парного корреляционного анализа данных, полученных в исходе и в конце 8-й нед во 2-й серии исследования. Отмечена сильная связь между изменениями активности воспаления, проатерогенной и иммуногенной модификации ЛП крови. Коэффициент корреляции между содержанием в крови СРП, мЛПНП, мЛПОНП, содержанием ХС в ЦИК превышал 0,9. Связь между противовоспалительным эффектом вобензима и его способностью ослаблять метаболические проявления ИР подтверждалась высокой степенью корреляционной зависимости между изменениями содержания в крови СРП и HbA1c (r=0,73), глюкозы (r=0,6), ИА (r=0,6), СЖК (r=0,47).
Полученные данные свидетельствовали также об антитромбоцитарном действии вобензима, которая, по-видимому, также определялась его противовоспалительными свойствами. Если при содержании животных на диете, обогащенной липидами, интенсивность агрегации тромбоцитов возросла на 67 и 100 % соответственно в конце 1-й и 2-й недели, то уже через 2 нед применения препарата она возвращалась к исходному значению, а через 4 нед была угнетена втрое. В исходном состоянии в крови отсутствовали необратимые тромбоцитарные агрегаты, однако в конце 2-й недели содержания на диете количество необратимо агрегировавших тромбоцитов достигло 3 %, к концу 4-й недели –22 %. Через 2 нед применения вобензима их количество уменьшилось до 14 %, через 4 нед – до 3 %. При профилактическом режиме применения препарата интенсивность агрегации тромбоцитов в конце 4–8-й недель была уменьшена до 5–6 % при исходном значении 18 % и максимальной интенсивности, отмеченной в контроле в конце 4-й недели, достигавшей 30 %. Количество тромбоцитов в необратимых тромбоцитарных агрегатах в конце 6–8-й недель не превышало 5–6 %.
Таким образом, результаты проведенного исследования свидетельствуют о том, что хроническая липидная нагрузка приводит к развитию системного воспаления и, как следствие, появлению ИР и всего комплекса сопутствующих метаболических нарушений проатерогенной направленности. Развитие подобных изменений при воспалении и, особенно, острой фазе ответа установлено также ранее в ряде как экспериментальных, так и клинических исследований. Показано, что при этом резко активируется липолиз в жировой ткани, возрастает синтез жирных кислот в печени, угнетается окисление жирных кислот. В результате усиливается секреция ЛПОНП, возрастает плазменное содержание липидов. Параллельно усиливается продукция ХС в печени и угнетается клиренс ЛПНП, приводя к развитию ГХЕ. Содержание белков в плазме возрастает в острую фазу примерно на 25 % за счет СРП, сывороточного амилоида А (SAA) и фибриногена, которые являются медиаторами воспаления, тогда как содержание белков, угнетающих изменения острой фазы (альбумина, трансферрина, фетопротеина) уменьшается. Эти изменения определяются цитокинами ФНО-a, интерфероном-g, ИЛ-1 и ИЛ-6, продуцируемыми клетками крови и эндотелиоцитами, и важнейшим свойством этих цитокинов является способность снижать чувствительность клеток к инсулину.
Фибриноген – один из основных белков острой фазы воспаления, определяет развитие при нем гиперкоагуляционного и тромбогенного потенциала, так как влияет на вязкость плазмы, участвует в адгезии клеток крови к сосудистой стенке, обратимой агрегации тромбоцитов и эритроцитов, образуя мостики между ними. Высокий уровень фибриногена в крови отмечается у пациентов с ИР, МС, СД 2-го типа и рассматривается как предиктор развития кардиальных и сосудистых осложнений. Этому способствует также возрастание реактивности тромбоцитов, усиление экспрессии ими гликопротеина GP-1b, увеличение концентрации и активности фактора ван Виллебранда в крови, что является прямым следствием гипергликемии [22].
Предполагают, что нарушения метаболизма в начальной фазе воспаления имеют адаптивный защитный для организма характер. Возрастание содержания ЛП в крови в острую фазу способствует нейтрализации токсического действия бактериальных липополисахаридов (ЛПС) и продуктов активации СРО липидов, а возрастание концентрации в крови субстратов окисления – глюкозы и ТГ – обеспечивает повышенный энергетический запрос организма [6]. Однако в хроническом состоянии эти изменения приобретают патологический характер, способствуя оксидации ЛПНП и ЛПОНП с появлением их модифицированных форм, ЛПВП утрачивают противовоспалительные свойства и приобретают провоспалительные [37]. Эти изменения возрастают в условиях хронической гипергликемии и гиперинсулинемии, оксидантного стресса, определяя развитие СД, ожирения, МС, гипертензии, сердечной и почечной недостаточности [24]. Неоднократно показано, что ключевую роль при острых и хронических воспалительных процессах (травма, сепсис, инфекция, ревматоидный артрит) играет ФНО-a, и возрастание его концентрации сочетается с проатерогенными нарушениями профиля липидов и нарушением толерантности к глюкозе.
Эти положения полностью соответствуют результатам проведенного исследования, которые свидетельствуют о четкой корреляционной зависимости между активностью системного воспаления, выраженностью ИР и сопутствующих ей проатерогенных нарушений метаболизма липидов, ЛП и углеводов.
Помимо этого, в работе показано, что первичные нарушения обмена липидов, вызванные содержанием животных на богатой липидами диете, могут вызывать весь комплекс нарушений, характерных для синдрома ИР. Эти результаты подтверждают данные других исследований о способности гиперлипидемии индуцировать развитие системного воспаления [8]. Неоднократно показано, что гиперлипидемия, возникающая после алиментарной липидной нагрузки, сочетается с возрастанием содержания в крови маркеров воспаления ФНО-a, ИЛ-6, СРП, что предположительно связывают с миграцией моноцитов в висцеральную жировую ткань и их активацией. Показано также, что у лиц с висцеральным ожирением при липидной нагрузке значительно увеличены как выраженность липидемии после приема пищи, так и степень активации системного воспаления. В исследовании, включавшем 38 мужчин с абдоминальным ожирением, установлено, что через 4 ч после липидной нагрузки уровень ИЛ-6 был существенно повышен в тесной корреляции с индексом ИР (НОМА). Помимо этого, выраженность изменений после нагрузки у лиц со сниженной чувствительностью к инсулину была значительно большей с более значительным возрастанием содержания в крови ТГ, глюкозы и инсулина. Эти данные означают, что даже транзиторное возрастание содержания в крови липидов сопровождается развитием провоспалительного состояния, снижением чувствительности к инсулину, развитием гиперинсулинемии [7].
Известно, что как развитие системного воспаления и СРО, так и последующее возникновение ИР связано с активацией ренин-ангиотензиновой системы, способностью ангиотензина II активировать ядерный фактор транскрипции-kB и NADPH-оксидазу эндотелиоцитов и воспалительных клеток крови. Так, зависимость между наличием оксидантного стресса и наличием ИР по индексу НОМА подтверждена в исследовании с участием 2002 лиц без СД, включенных в Framingham Offspring Study. Показано, что распространенность ИР возрастала в каждом тертиле показателя оксидантного стресса, соответственно в 3,2; 3,8 и 4,1 раза. Это позволило рассматривать оксидантный стресс как фактор развития ИР, МС и СД 2-го типа, а его устранение – как один из путей восстановления чувствительности к инсулину [34].
Результаты проведенного исследования и данные парного корреляционного анализа полностью соответствовали этим положениям, что послужило основанием для изучения возможности вобензима – препарата, применяемого в системной энзимотерапии как средства с выраженным противовоспалительным действием – для эффективного вмешательства в течение синдрома ИР. В работе показано, что применение вобензима параллельно с содержанием животных на диете, обогащенной липидами, сопровождалось значительным угнетением воспалительного ответа, снижением интенсивности оксидантного стресса, снижением активности ренин-ангиотензиновой системы, ослаблением иммунной реактивности с резким уменьшением содержания в крови ЦИК. Помимо этого, значительно ослаблялись проявления синдрома ИР, предупреждалось снижение чувствительности к инсулину, нормализовался липидный и липопротеиновый состав крови, ослаблялась проатерогенная и иммуногенная модификация ЛП.
Известно, что основой терапевтического эффекта системной энзимотерапии является протеолитическое действие ферментов, входящих в состав вобензима и флогензима, их способность связывать и инактивировать провоспалительные белковые медиаторы типа цитокинов, способствовать их фагоцитозу в печении и селезенке, клиренсу из крови. Аналогичный механизм элиминации был также показан для иммунных комплексов. Показано также угнетающее действие вобензима на продукцию провоспалительных цитокинов (ФНО-a, ИЛ-1b, ИЛ-6), адгезивных молекул (РЕСАМ, ICAM-1 и др.), образование циркулирующих и связанных с тканями иммунных комплексов [5]. Противовоспалительный эффект энзимотерапии проявляется уменьшением содержания в крови медиаторов воспаления [14, 15] и молекул адгезии [31], уменьшением отека [41]. Помимо этого, полученные нами данные о способности вобензима предупреждать активацию АПФ позволяют рассматривать этот эффект как один из важнейших механизмов его противовоспалительного и антиатерогенного действия.
Противовоспалительное действие и фибриногенолитическая активность вобензима обусловливает также его способность нормализовывать микроциркуляцию и реологические свойства крови [17, 25], ее липопротеиновый спектр, предупреждать модификацию ЛП [18]. Отмечено также улучшение циркуляции крови в результате внутрисосудистого расщепления сгустков крови и тромбоцитарных агрегатов, и эти данные подтверждаются результатами проведенного нами исследования. Сохранение чувствительности к инсулину в результате применения вобензима в условиях системного воспаления также определяется его протеолитической активностью в значительной степени. Показано, что одной из причин развития ИР при системном воспаления является возрастание протеазной активности крови, в частности – возрастание активности матриксной металлопротеиназы-9 (ММР-9) в стенке микрососудов, в тучных клетках и лейкоцитах. В результате разрушаются рецепторы инсулина и уменьшается их плотность на клеточных мембранах. Этот эффект установлен у крыс со спонтанной гипертензией, у которых блокада ММР-9 предупреждала уменьшение экспрессии рецепторов инсулина, нормализовала содержание глюкозы и HbA1c в плазме крови в сочетании с уменьшением АД и снижением активности СРО [13].
Существенное практическое значение имеет установленный нами факт тесной взаимосвязи между активностью воспаления и проявлениями синдрома ИР на высоте воспаления, сохраняющейся и при применении вобензима. Это позволяет оценивать эффект вобензима на весь комплекс компонентов синдрома по изменениям показателей только воспалительного процесса без определения выраженности влияния на отдельные компоненты, что не всегда доступно в клинической практике.
Таким образом, полученные данные свидетельствуют о способности комбинированных препаратов протеолитических ферментов оптимизировать течение воспалительного процесса, иммунных реакций, нормализовать чувствительность к инсулину, устранять метаболические нарушения, связанные с ИР, реологические свойства крови, ее липопротеиновый спектр. Это позволяет рекомендовать применение вобензима для лечения больных с МС, особенно в случаях, когда он сочетается с заболеваниями, сопровождающимися выраженной активацией системного воспаления типа ревматоидного артрита, аутоиммунных процессов.
литература
1. Мазуров В.И., Лила А.М., Стернин Ю.И., Раймуев К.В. Системная энзимотерапия в комплексном лечении ревматических заболеваний // Системная энзимотерапия. Матер. ІІ межд. конференции. – М., 1996. – С. 37-42.
2. Николенко Е.Я., Корж А.И., Лурье С.З. Энзимокоррекция нарушений липидного спектра крови у больных ишемической болезнью сердца/
3. Системная энзимотерапия. Теоретические основы, опыт клинического применения / Под ред. К.Н. Веремеенко, В.Н. Коваленко. – К.: Морион, 2000. – 320 с.
4. Талаева Т.В., Корниенко О.В., Братусь В.В. и др. Атерогенная модификация липопротеинов крови и гиперхолестеринемия как следствие острого воспалительного процесса // Журн. АМН Украины. – 1997. – Т. 3, № 3. – С.463-471.
5. Штаудер Г. Фармакологические эффекты пероральных комплексных энзимных препаратов // Системная энзимотерапия. Матер. ІІ межд. конференции. – М.,1996. – С. 13-24.
6. Berbee J.F., Havekes L.M., Rensen P.C. Apolipoproteins modulate the inflammatory response to lipopolysaccharide// J. Endotoxin Res. – 2005. – Vol. 11. – P. 97-103.
7. Blackburn P., Despres J.-P., Lamarche B. et al. Postprandial variations of plasma inflammatory markers in abdominally obese men // Obesity. – 2006. – Vol. 14. – P.1747-1754.
8. Butler S.O., Btaiche I.F., Alaniz C. Relationship between hyperglycemia and infection in critically ill patients // Pharmaco-therapy. – 2005. – Vol. 25. – P. 963-976.
9. Carter B.L., Einhorn P.T., Brands M. et al. Thiazideinduced dysglycemia // Hypertension. – 2008. – Vol. 52. – P.30-38.
10. Cronin S., Kelly P.J. Stroke and the metabolic syndrome in populations // Stroke. – 2009. – Vol. 40. – P.3-10.
11. D’Alessandris C, Lauro R, Presta I, Sesti G. C-reactive protein induces phosphorylation of insulin receptor substrate-1 on Ser307 and Ser612 in L6 myocytes, thereby impairing the insulin signalling pathway that promotes glucose transport // Diabetologia. – 2007. – Vol. 50. – P. 840-849.
12. DeFerranti S.D., Gauvreau K., Ludwig D.S. et al. Prevalence of the metabolic syndrome in American adolescents: findings from the Third National Health and Nutrition Examination Survey // Circulation. – 2004. – Vol.110. – P. 2494-2497.
13. DeLano F.A., Schmid-Schonbein G.W. Proteinase activity and receptor cleavage. mechanism for insulin resistance in the spontaneously hypertensive rat // Hypertension. – 2008. – Vol. 52. – P. 415-423.
14. Desser L., Rehberger A., Paukovits W. Proteolytic enzymes and amylase induce cytokine production in human peripheral blood mononuclear cells in vitro // Cancer Biother. – 1994. – Vol. 9. – P. 253-63.
15. Emancipator S.N., Chintalacharuvu S.R., Urankar Nagy N. et al. Effects of oral enzymes in collagen II induced arthritis in mice // Int. J. Immunother. – 1997. – Vol. 13. – P.67-74.
16. Gress T.W., Nieto F.J., Shahar E. Hypertension and antihypertensive therapy as risk factors for type 2 diabetes mellitus // New Engl. J. Med. – 2000. – Vol. 342. – P. 905-912.
17. Guggenbichler JP. Einflu? hydrolytischer enzyme auf thrombusbildung und thrombolyse // Med. Welt. –1988. – Vol. 39. – P. 277-280.
18. Hall D.A., Zaiac A.R., Cox R., Spanswick J. The effect of enzyme therapy on plasma lipid levels in the elderly // Atherosclerosis. – 1982. – Vol. 43. – P. 209-215.
19. Heart Protection Study Collaborative Group. MRC/ BHF Heart Protection Study of Cholesterol Lowering with Simvastatin in 20536 High-Risk Individuals: a Randomized Placebo-Controlled Trial // Lancet. – 2002. – Vol. 360. – P. 7-22.
20. Hotamisligil G.S. Inflammation and metabolic disorders // Nature.– 2006.–Vol.444.–P.860-867.
21. Hu G., Sarti C., Jousilahti P. еt al. The impact of history of hypertension and type 2 diabetes at baseline on the incidence of stroke and stroke mortality // Stroke. –2005. – Vol. 36. – P. 2538-2543.
22. Keating F.K., Whitaker D.A., Kabbani S.S. et al. Relation of augmented platelet reactivity to the magnitude of distribution of atherosclerosis // Am. J. Cardiol. – 2004. – Vol. 94. – P. 725-728.
23. Khaw K.T., Wareham N., Luben R. et al. Glycated haemoglobin, diabetes, and mortality in men in Norfolk cohort of European Prospective Investigation of Cancer and Nutrition (EPIC-Norfolk) // Br. Med. J. – 2001. – Vol. 322. – P.15-23.
24. Khovidhunkit W., Kim M.-S., Memon R.A. et al. The pathogenesis of atherosclerosis. Effects of infection and inflammation on lipid and lipoprotein metabolism mechanisms and consequences to the host // J. Lipid Res. –2004. – Vol. 45. – P. 1169-1196.
25. Kleef R., Delohery T.M., Bovbjerg D.H. Selective modulation of cell adhesion molecules on lymphocytes by bromelain protease // Pathobiology. – 1996. – Vol. 64. – P.339-346.
26. Kylin E. Studien hypertoniehyperglykamiehyperurikamie syndrome. Zentralblatt fur innere // Medizin. – 1923. – Vol. 44. – P. 105-127.
27. Lakka H.M., Laaksonen D.E., Lakka T.A. et al. The metabolic syndrome and total and cardiovascular disease mortality in middle-aged men // JAMA. – 2002. – Vol. 288. – P. 2709-2716.
28. LaRosa J.C., Grundy S.M., Kastelein J.J. et al. // Circulation. – 2005. – Vol. 112 (Suppl II). – P. 662-663.
29. LaRosa J.C., Grundy S.M., Waters D.D. et al. Intensive lipid lowering with atorvastatin in patients with stable coronary disease // New Engl. J. Med. – 2005. – Vol. 352. – P.1425-1435.
30. Lawlor D.A., Lean M., Sattar N. ABC of obesity: Obesity and vascular disease // Brit. Med. J. – 2006. – Vol.333. – P. 1060-1063.
31. Lehmann V.P. Immunomodulation by proteolytic enzymes // Nephrol. Dial. Transplant. – 1996. – Vol. 11. – P. 953-955.
32. Lindblad U., Langer R.D., Wingard D.L. et al. Metabolic syndrome and ischemic heart disease in elderly men and women // Amer. J. Epidemiol. – 2001. – Vol. 153. – P. 481-489.
33. Mainous A.G., Everett C.J., Loszka H. et al. Prehypertension and mortality in a nationally representative cohort // Amer. J. Cardiol. – 2004. – Vol. 94. – P. 1496-1500.
34. Meigs J.B., Larson M.G., Fox C.S. et al. Association of oxidative stress, insulin resistance, and diabetes risk phenotypes. The Framingham Offspring Study // Diabetes Care. – 2007. – Vol. 30. – P. 2529-2535.
35. Ninomiya T., Kubo M., Doi Y. et al. Impact of metabolic syndrome on the development of cardiovascular disease in a general Japanese population. The Hisayama Study // Stroke. – 2007. – Vol. 38. – P. 2063-2070.
36. Nissen S.E., Tuzcu E.M., Libby P. et al. Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure: The CAMELOT Study. A randomized controlled trial // JAMA.– 2004. – Vol. 292. – P. 2217-2225.
37. Popa C., Netea M.G., van Riel P.L. et al. Тhe role of TNF-а in chronic inflammatory conditions, intermediary metabolism, and cardiovascular risk // J. Lipid Res. – 2007. – Vol. 48. – Р. 751-762.
38. Rossi R., Turco V., Origliani G., Modena M.G. Type2 diabetes mellitus is a risk factor for the development of hypertension in postmenopausal women // J. Hypertens. –2006. – Vol. 24. – P. 2017-2022.
39. Subba Rao C., Nagy N.U., Emancipator S.N. Phlogenzym® protease therapy ameliorates injury in experimental autoimmune arthritis induced by collagen II. B Lymphocytes and Autoimmunity. International Conference; 1996 May 22; Prague, Czech Republic: The New York Academy of Science.
40. Sironi A.M., Gastaldelli A., Mari A. et al. Visceral fat in hypertension: influence on insulin resistance and betacell function // Hypertension. – 2004. – Vol. 44. – P. 127-133.
41. Steffen C., Menzel J. Grundlagenuntersuchungen zur Enzymtherapie bei Immunkomplexkrankheiten // Wien Klin. Wochenschr. – 1985. – Vol. 97. – P. 376-385.
42. Suganami T., Tanimoto-Koyama K., Nishida J. et al. Role of the toll-like receptor 4/NF-kB pathway in saturated fatty acid-induced inflammatory changes in the interaction between adipocytes and macrophages // Arterioscler. Thromb. Vasc. Biol. – 2007. – Vol. 27. – P. 84-93.
43. Weber M. Should treatment of hypertension be driven by blood pressure or total cardiovascular risk? // Renin-angiotensin system in cardiovascular medicine. –2006. – Vol. 2. – P. 16-19.
44. Wong N.D. The metabolic syndrome and preventive cardiology: working together to reduce cardiometabolic risks // Metabolic Syndrome and Related Disorders. – 2006.– Vol. 4. – P. 233-236.
45. Yuan G., Zhou L,, Tang J. et al. Serum CRP levels are equally elevated in newly diagnosed type 2 diabetes and impaired glucose tolerance and related to adiponectin levels and insulin sensitivity // Diabetes Res. Clin. Pract. –2006. – Vol. 72. – P. 244-250.
46. Yusuf S., Sleight P., Pogue J. et al. Effects of angiotensin-converting-enzyme inhibitor, ramipril, on cardiovascular events in high-risk patients // New Engl. J. Med. – 2000. – Vol. 342. – P. 145-153.












Комментировать