Аллергический ринит и его классификация. Аллергены, вызывающие развитие и обострение аллергического ринита. Биохимические медиаторы, функциональные нарушения и клинические проявления при аллергическом рините. Клиническая картина аллергического ринита и симптоматика. Диагностика и лечение.
Жерносек В.Ф., Белорусская медицинская академия последипломного образования
Аллергический ринит – заболевание, возникающее после контакта с аллергеном и обусловленное IgE-опосредованным воспалением слизистой оболочки носа, с характерными симптомами (ринорея, назальная обструкция, зуд носа, чихание), обратимыми спонтанно или под влиянием лечения [11].
В развитии аллергического ринита имеет значение воздействие внешних и внутрижилищных аллергенов (табл. 1).
Таблица 1 Аллергены, вызывающие развитие и обострение аллергического ринита[3]
Под воздействием аллергенов в слизистой оболочке полости носа формируется хроническое аллергическое воспаление с вовлечением различных типов клеток: эозинофилов, Т-лимфоцитов, тучных и эпителиальных. Степень и продолжительность воспаления зависит от концентрации аллергенов в окружении больного. При постоянном воздействии аллергенов воспаление персистирует круглый год. При сезонном воздействии аллергенов воспаление имеет интермиттирующий характер, оно постепенно угасает при прекращении воздействия причинно-значимого аллергена. Такой характер воспаления имеет место при аллергии к пыльце деревьев и растений, а также при сенсибилизации к микрогрибам, обитающим преимущественно вне жилища. Концентрация спор этих микрогрибов повышается ранней весной и поздней осенью. В процессе аллергического воспаления формируется повышенная неспецифическая реактивность слизистой полости носа. Она представляет собой усиленную реакцию на обычные стимулы в виде чихания, отека и/или секреции слизистой. В качестве неспецифических раздражителей (триггеров) выступают поллютанты жилых помещений, среди которых главным является табачный дым, а также холодный и сырой воздух, резкие запахи (парфюмерия, средства бытовой химии), выхлопные газы автотранспорта и др.
В процессе аллергического воспаления клетки, участвующие в его развитии, выделяют большое количество медиаторов. Наиболее значимы гистамин и лейкотриены. Медиаторы аллергического воспаления вызывают определенные функциональные нарушения и клинические проявления при аллергическом рините (табл. 2).
Таблица 2 Биохимические медиаторы, функциональные нарушения и клинические проявления при аллергическом рините [5]
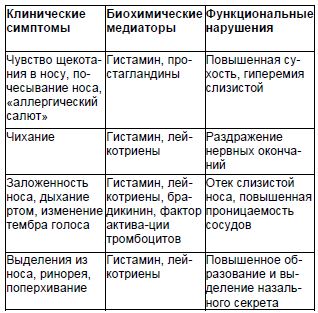
Полость носа, околоносовые пазухи и трахеобронхиальное дерево представляют собой единое целое. Это объясняет частое сосуществование бронхиальной астмы, аллергического ринита и полипозного риносинусита. Возможными причинами сочетания ринита и бронхиальной астмы является сходство строения мерцательного эпителия, участие в патогенезе аллергии и идентичность вызывающих болезнь аллергенов, наследование атопии. Другой возможный нервнорефлекторный механизм развития сочетанной патологии – ринобронхиальная гиперреактивность и ринобронхиальный рефлекс.
Классификация. Согласно последним официальным рекомендациям ВОЗ выделяют две формы аллергического ринита – интермиттирующий и персистирующий, а также две градации тяжести – легкий, умеренный/тяжелый(табл. 3).
Таблица 3. Классификация аллергического ринита [11]
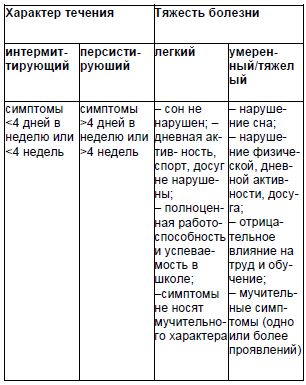
В МКБ-10представлены следующие разновидности ринитов:J 30.1 Аллергический ринит, вызванный пыльцой растений; J 30.2 Другие сезонные аллергические риниты; J 30.3 Другие аллергические риниты; J 30.4 Аллергический ринит неуточненный.Примеры формулировки диагноза: Аллергический ринит, интермиттирующее течение, легкий, период ремиссии, сенсибилизация к пыльце райграса, тимофеевки. Аллергический персистирующий ринит, среднетяжелый, период обострения. Сенсибилизация к Dermatophagoidespteronissinus.
Клиническая картина аллергического ринита складывается из совокупности основных, дополнительных и общих неспецифических симптомов.
Основные клинические симптомы аллергического ринита: 1) ринорея ? водянистые выделения из носа; 2) чихание, нередко приступообразное, чаще в утренние часы, пароксизмы чихания могут возникать спонтанно; 3) зуд, реже чувство жжения в носу, иногда сопровождается зудом неба и глотки, может проявляться характерным симптомом ? «аллергиче-ским салютом» (постоянное почесывание кончика носа с помощью ладони движением снизу вверх), в результате чего у части детей появляется поперечная носовая складка, расчесы, царапины на носу; 4) заложенность носа, характерное дыхание ртом, сопение, храп, изменение голоса; снижение обоняния.
Дополнительные симптомы: 1) раздражение, отечность, гиперемия кожи над верхней губой и крыльев носа; 2) носовые кровотечения вследствие форсированного сморкания и ковыряния в носу; 3) боль в горле, покашливание из-за сопутствующего аллергического фарингита, ларингита; 4) боль и треск в ушах, особенно при глотании, нарушение слуха за счет аллергического туботита; 5) глазные симптомы в результате сопутствующего аллергического конъюнктивита в виде слезотечения, зуда, инъецированности склер и конъюнктивы, фотофобии, темных кругов под глазами, вызванных венозным застоем, причиной которого является отек слизистой оболочки носа и придаточных пазух.
Общие неспецифические симптомы: 1) слабость, недомогание, раздражительность; 2) головная боль, повышенная утомляемость, нарушение концентрации внимания; 3) потеря аппетита, иногда тошнота, чувство дискомфорта в области живота вследствие проглатывания большого количества слизи или при сопутствующих аллергических заболеваниях; 4) нарушение сна, подавленное настроение; 5) повышение температуры (крайне редко) [5, 9].
Диагностика. Диагноз аллергического ринита уточняется в ходе детального обследования пациента.
Основные диагностические исследования и их значение при аллергическом рините [1, 5, 9]:
1. Подтверждение эозинофильного характера воспаления слизистой носа:
-цитограмма мазка слизи из носа (выявление в лейкоцитарной формуле эозинофилов более 10% – вероятный признак аллергического воспаления);
-мазки-отпечатки слизистой оболочки полости носа (эозинофильная инфильтрация слизистой – вероятный признак аллергического воспаления).
2.Оценка активности аллергического воспаления: определение концентрации эозинофильного катионного белка (повышение его уровня – признак активности аллергического процесса).
3.Передняя риноскопия (бледность и отечность слизистой оболочки – характерный признак аллергического воспаления).
4. Функциональные исследования:
-назальная пикфлоуметрия (типично симметричное снижение проходимости носовых ходов);
-активная передняя риноманометрия (типично симметричное повышение сопротивления).
5. Исключение синусита:
-эндоскопия придаточных пазух носа по показаниям;
-рентгенологическое исследование околоносовых пазух, или компьютерная томография, или магнитно-резонансная томография.
6. Мазок из носа на флору и чувствительность к антибиотикам при наличии синусита
7. Диагностика спектра сенсибилизации:
-кожные пробы с аллергенами;
-анализ уровня общего и специфических IgE;
-провокационные тесты с аллергенами по показаниям (осуществляются аллергологом).
Лечение. Лечение аллергического ринита должно быть направлено на достижение и поддержание контроля над симптомами заболевания, профилактику обострений заболевания, улучшение качества жизни больного, лечение сопутствующей патологии, которая усугубляет течение аллергического ринита, а также на предотвращение развития бронхиальной астмы.
Лечение аллергического ринита должно быть комплексным. Основные составляющие программы лечения и реабилитации [2,5]:
1.Устранение причинно-значимого аллергена и создание гипоаллергенного быта.
2.Гипоаллеpгенная диета по показаниям.
3.Симптоматическая терапия.
4.Базисная противовоспалительная терапия.
5.Иммунотерапия причинно-значимым аллергеном.
Организация гипоаллергенного быта.Контроль окружающей среды при аллергическом рините не только уменьшает вероятность обострения заболевания. Создание гипоаллергенного быта предохраняет пациента от расширения спектра сенсибилизации. Поэтому контроль окружающей среды важен не только при рините, обусловленном сенсибилизацией к бытовым, эпидермальным и грибковым аллергенам. Он актуален и должен рекомендоваться пациентам с сезонным аллергическим ринитом, обусловленным пыльцевой сенсибилизацией.
Питание больных.При круглогодичном аллергическом рините, обусловленном бытовой и эпидермальной сенсибилизацией, специальной диеты не требуется. Она назначается только при наличии сопутствующей пищевой аллергией. Определенные ограничения в диете требуются пациентам с аллергией к пыльце растений. Из питания исключаются пищевые продукты, перекрестно реагирующиеили имеющие антигенное родство с пыльцой причинно-значимых растений. Пищевые продукты с антигенным родством или способные вызывать перекрестные аллергические реакции могут поддерживать аллергическое воспаление в полости носа и служить причиной персистенции симптомов в осенне-зимний период года при поллинозах.
Медикаментозная терапия. В настоящее время в лечении аллергического ринита применяются пять групп лекар-ственных препаратов: интраназальные кортикостероиды, антилейкотриеновые препараты, кромоны, Н1-гистаминоблокаторы, деконгестанты, антихолинергики. Влияние различных групп медикаментов на симптомы аллергического ринита представлено в табл. 4.
Таблица 4. Влияние медикаментов на симптомы ринита [12, с дополнениями]
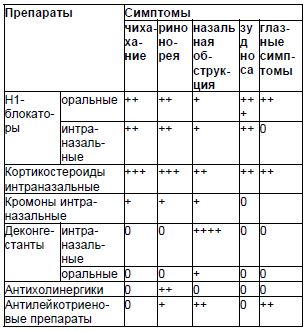
Только интраназальные кортикостероиды способны эффективно купировать все симптомы аллергического ринита [1]. По результатам метаанализа доказано, что интраназальные кортикостероиды более эффективны в лечении аллергического ринита, чем антилейкотриеновые препараты, системные и интраназальные антигистаминные средства [19].
Проблемой больных аллергическим ринитом является наличие сопутствующих глазных симптомов, которые выявляются с частотой до 70% [21]. Интраназальные глюкокортикостероиды также способны купировать глазные симптомы. Механизмы действия интраназальных глюкокортикостероидов, обусловливающие их эффективность в отношении глазных симптомов, в настоящее время хорошо изучены. Ведущий из них – подавление назоокулярного рефлекса, дополнительный – улучшение лакримо-назального оттока.
Широкое применение интраназальных кортикостероидов объясняется не только их высокой эффективностью, но и безопасностью. Безопасность интраназальных кортикостероидов сегодня не вызывает сомнений, хотя системная биодоступность выше у старых препаратов интраназальных кортикостероидов. В рекомендуемых дозах интраназальные кортикостероиды не оказывают отрицательного влияния на состояние гипоталамо-гипофизарной системы [6, 15].
Требования, которые предъявляются к современные инраназальным кортикостероидам, четко сформулированы: высокая аффинность к рецепторам; высокая селективность; высокая тропность к тканям; длительное персистирование в тканях; низкая вероятность развития системных побочных эффектов; минимальная биодоступность; отсутствие активных метаболитов; высокая комплаентность и удобство дозирования [7].
Историческая хроника внедрения в клиническую практику различных интраназальных стероидов следующая: 1973 г. – беклометазона дипропионат, 1981 г. – будесонид, 1990 г. – флутиказона пропионат, 1996 г. – мометазона фуроат, 2007 г.– флутиказона фуроат. Таким образом, если раньше новые интраназальные стероиды вводились в клиническую практику с небольшим интервалом, то самый последний из них поступил на вооружение с самым длительным интервалом – 11 лет.
Флутиказона фуроат (Авамис) – новый синтетический трифторированный глюкокортикостероид с наиболее высокой аффинностью и селективностью к глюкокортикостероидному рецептору среди всех существующих препаратов этой группы. Молекула флутиказона фуроата характеризуется высокой аффинностью, быстрой ассоциацией и медленной диссоциацией по отношению к глюкортикостероидному рецептору. Это приводит к тому, что препарат сохраняется в тканях в значительно большем количестве при изначально одинаковой концентрации по сравнению с другими интраназальными стероидами. Этот феномен позволил уменьшить разовую лечебную дозу препарата. Уменьшение лечебной дозы препарата при сохранении терапевтического потенциала снижает вероятность развития системных нежелательных эффектов [2, 4, 7, 14].
Авамис выпускается в виде назального дозированного спрея по 27,5 мкг флутиказона фуроата в 1 дозе по 120 доз во флаконе. Устройство для доставки препарата является оригинальной инновационной разработкой и имеет ряд преимуществ перед другими средствами доставки лекарственных средств для лечения аллергического ринита. Нажимной клапан находится на боковой поверхности флакона. Боковая кнопка активации требует минимум усилий пациента и обеспечивает снижение вариации дозирования препарата. Отличительной особенностью флакона является наличие индикаторного окна, что позволяет контролировать содержание препарата. Наконечник короткий, что облегчает применение лекарственного средства и обеспечивает однородность его дозирования. К тому же препарат удобно вводить другому пользователю (ребенку). Дозирующее устройство обеспечивает образование мелкодисперсного аэрозоля. Кроме того, одна терапевтическая доза препарата содержится в вдвое меньшем объеме по сравнению с лекарственными формами других инраназальных стероидов, что исключает стекание препарата. Авамис после применения не дает послевкусия. Внешний вид назального спрея мало похож на продукцию медицинского назначения, что не создает для пациента психологического дискомфорта при необходимости применения в присутствии посторонних людей.
Препарат разрешен к применению у детей, начиная с двух лет жизни.
Показания: симтоматическое лечение сезонного и круглогодичного аллергического ринита у взрослых и детей старше двух лет.
Режим дозирования определяется возрастом пациента:
– взрослые и подростки (в возрасте от 12 лет и старше): начальная доза – 2 впрыскивания в каждую ноздрю 1 раз в сутки (общая суточная доза – 110 мкг); при достижении контроля симптомов – 1 впрыскивание в каждую ноздрю 1 раз в сутки (общая суточная доза – 55 мкг);
– дети в возрасте от 2 до 11 лет: начальная доза – 1 впрыскивание в каждую ноздрю 1 раз в сутки (общая суточная доза – 55 мкг); при отсутствии эффекта – до 2 впрыскиваний в каждую ноздрю 1 раз в сутки (общая суточная доза – 110 мкг). При достижении контроля симптомов – 1 впрыскивание в каждую ноздрю 1 раз в сутки (общая суточная доза – 55 мкг).
К настоящему времени хорошо изучены метаболизм и выведение флутиказона фуроата [17]. Системная биодоступность флутиказона фуроата ниже 0,5% [10, 12]. Препарат обладает самой высокой аффинностью к глюкокортикостероидным рецепторам из известных интраназальных стероидов [16]. Для флутиказона фуроата характерна значительно большая селективность в отношении глюкортикостероидных рецепторов по сравнению с другими известными интраназальными глюкортикостероидами [31].
Для флутиказона фуроата по сравнению с другими интраназальными кортикостероидами характерно быстрое начало действия. Доказано, что флутиказона фуроат начинает оказывать положительное влияние на назальные симптомы аллергического ринита через 8 ч от начала лечения [12].
Степень приверженности к лечению при лечении флутиказона фуроатом выше по сравнению с другими интраназальными стероидами [26].
В мультицентровом двойном слепом рандомизированном плацебо-контролируемом исследовании была убедительно доказана эффективность лечения Авамисом аллергического круглогодичного ринита у подростков старше 12 лет и взрослых в режиме приема 1 раз в день в суточной дозе 100 мкг [28]. M. Vasar et al. [34] в рандомизированном двойном слепом плацебоконтролируемом исследовании кроме значительного клинического улучшения у подростков и взрослых с круглогодичным аллергическими ринитом выявили выраженное улучшение функциональных характеристик носового дыхания – повышение показателей назальной пикфлоуметрии.
H.B. Kaizer et al. [18] доказали, что при хорошей переносимости интраназального спрея флутиказона фуроат является эффективным в лечении назальных симптомов сезонного аллергического ринита у пациентов старше 12 лет жизни. К аналогичному выводу пришли украинские исследователи [3].
Для флутиказона фуроата доказано достоверное положительное влияние на степень выраженности глазных симптомов, сопутствующих аллергическому риниту [20]. Так, продемонстрировано, что назальный спрей флутиказон фуроат с успехом подавляет назоокулярный рефлекс [13]. По сравнению с другими интраназальными кортикостероидами у флутиказона фуроата этот эффект при сезонном аллергическом рините был наивысшим [21]. В мультицентровом исследовании в различных географических регионах у взрослых и подростков с сезонным аллергическим ринитом доказано положительное влияние флутиказона фуроата на все назальные и глазные симптомы заболевания [23]. Интересно, что флутиказона фуроат является первым интраназальным глюкортикостероидом, который продемонстрировал одновременную высокую клиническую эффективность во всех исследованиях по отношению к носовым и глазным симптомам при сезонном аллергическом рините [32].
Проведены также многочисленные контролируемые исследования по применению флутиказона фуроата в педиатрической практике. Так, J.F. Maspero et al. [22] убедительно доказали эффективность и безопасность лечения Авамисом круглогодичного аллергического ринита у детей в возрасте от 2 до 11 лет включительно. Также доказана клиническая эффективность лечения сезонного аллергического ринита у детей 6–11 лет жизни [25] при высокой степени его безопасности как при сезонном, так и круглогодичном аллергическом рините у пациентов этой возрастной категории [27]. В систематизированном обзоре P.L. McCormack и L.J. Scott [24] показали не только высокую эффективность Авамиса в лечении аллергического ринита у детей с 2 лет жизни, подростков и взрослых, но также продемонстрировали высокую безопасность лечения флутиказона фуроатом. Частота побочных эффектов при лечении аллергического ринита у детей 2–11 лет жизни, подростков и взрослых не отличалась от плацебо. D.P. Patel et al. [29] показали, что лечение флутиказона фуроатом не вызывает угнетения гипоталамогипофизарной системы как у взрослых, так и подростков старше 12 лет жизни. Лечение флютиказона фуроатом аллергического круглогодичного ринита в течение 12 месяцев не вызывало системных побочных эффектов, свойственных системным глюкокортико-стероидам [31]. В последующем было также доказано, что флутиказона фуроат не оказывает отрицательного влияния на состояние гипоталамо-гипофизарной системы при лечении аллергического ринита у детей 2–11 лет жизни [33].
Лечение флутиказона фуроатом значительно улучшает качество жизни пациентов с аллергическим ринитом [16].
В лечении аллергического ринита используются и медикаменты других групп. Следует отметить, что значительно более слабым противоспалительным эффектом по сравнению с интраназальными глюкокортикостероидами обладают препараты кромоглициловой кислоты и недокромила.
Для лечения аллергического ринита применяются интраназальные и системные антигистаминные препараты второго поколения. В настоящее время для лечения аллергического ринита используются антилейкотриеновые препараты (монтелукаст, зафирлукаст). Для контроля симптомов аллергического ринита также применяются местные деконгестанты коротким, не более 5–7 дней, курсом.
Антихолинергические средства для лечения аллергического ринита в нашей стране не зарегистрированы.
В руководстве ARIA (2008) выделяют три ступени терапии. Первая соответст-вует легкому интермиттирующий риниту, вторая ? умеренному/тяжелому интермиттирующему и легкому персистирующему варианту, третья ? умеренному/тяжелому персистирующему. С учетом нового высокоэффективного интраназального кортикостероида Авамиса, зарегистрованного на нашем фармацевтическом рынке, эту схему можно представить следующим образом (табл. 5).
Таблица 5 Ступенчатая схема терапии аллергического ринита [12, с дополнениями]
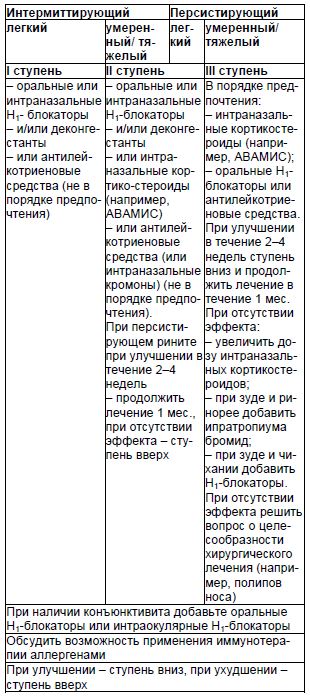
Иммунотерапия у пациентов с аллергическими ринитами причинно-значимыми аллергенами проводится по общепринятым принципам.Измененная иммунологическая реактивность, отек слизистой оболочки носа и околоносовых пазух, снижение местной иммунологической защиты в виде дефицита sIgA у пациентов с аллергическим ринитом приводят к тому, что на аллергическое воспаление часто наслаивается бактериальная инфекция. При появлении гнойного отделяемого из носа, явлений интоксикации больной должен быть осмотрен оториноларингологом для решения вопроса о применении специальных методов лечения. Основной принцип лечения синуситов – создание хороших условий для аэрации пазух и эвакуации секрета через естественные соустья. Несомненно, оптимальным является тот антибиотик, к которому чувствительна выделенная микрофлора. Однако бактериологическое исследование занимает определенный промежуток времени. Поэтому чаще всего используются антибиотики широкого спектра действия. Препаратами выбора могут быть ингибиторзащищенные аминопенициллины. Примером препарата является комбинация амоксициллина и клавулановой кислоты – Аугментин.
Таким образом, в лечении аллергического ринита как у детей, так и у взрослых, страдающих аллергическим ринитом, может быть использован новый интраназальный кортикостероид Авамис. Авамис с учетом высокой эффективности в отношении как носовых, так и глазных симптомов, необходимой низкой лечебной дозы, высокой безопасности может рассматриваться как препарат выбора в лечении аллергического ринита у детей, начиная с двух лет жизни, подростков и взрослых.
Литература
1. Аллергия у детей: от теории – к практике/ под ред. Л.С. Намазовой-Барановой. – М., 2010– 2011. – 668 с.
2.Астафьева Н.Г. // Рос. аллергол. журн. – 2010. – № 3. – С. 74–84.
3.Дитятковска Е.М., Родкiна I.А., Бiлецька С.В., Бендецька Ю.В. // Клiнiчна медицина. – 2010.–№ 1. – С. 1–4.
4. Емельянова А.В. // Рос. аллергол. журн.2010. – № 2. – С. 68–73.
5.Жерносек В.Ф., Дюбкова Т.П. Аллергические заболевания у детей: Рук. для врачей. ? Минск, 2003. ? 335 с.
6.Жерносек В.Ф. // Мед. новости. – 2010. – № 10. – С. 31–35.
7.Курбачева О.М., Павлова К.С. // Рос. аллергол. журн. – 2010. – № 6. – С. 64–68.
8.Международный консенсус в лечении аллергического ринита (Версия Европейской академии аллергологии и клинической иммунологии, 2000 // Рос. ринология. ? 2000. ? № 3. ? С. 5?27.
9. Научно-практическая программа «Аллергический ринит у детей» (Пособие для врачей). ? М., 2002. ? 79 с.
10.Allen A., Down G., Newland A. et al. // Clin. Therapeutics. – 2007. – Vol. 29, N 7. – P. 1415– 1421.
11.Allergic rhinitis and its impact on asthma (ARIA) 2008 Update (in collaboration with World Health Organization, GA2LEN and AllerGen) // Allergy.– 2008 (Suppl. 86). – P. 8–160.
12. Anolik R. // J. Asthma Allergy. – 2010. – N3. – P. 87–99.
13. Baroody F., Shenaq D., DeTineo M. et al. // J. Allergy Clin. Immunol. – 2009. – Vol. 123. – P. 1342–1348.
14. Charpin S. // Prescriber. – 2009. – 5 June.– P. 23–26.
15.Derendorf H., Meltzer E.O. // Allergy. – 2008. – Vol. 63. – P. 1292–1300.
16.Goyal N., Hochhaus G. // Drug Today. – 2008. – Vol. 44, N 4. – P. 251–260.
17.Hughes S.C., Shardlow P.C., Hollis F.J. et al. // Drug Metabolism Disposition. – 2008. – Vol. 36, N 11. – P. 2337–2344.
18.Kaiser H.B., Naclerio R.M., Given J. et al. // J. Allergy Clin. Immunol. – 2007. – Vol. 119. – P. 1430–1437.
19.Kariyawasam H.H., Scadding G.K. // J. Asthma Allergy. – 2010. – N 3. – P. 19–28.
20.Keith P.K., Scadding G.K. // Currents Med. Research Opinion. – 2010. – Vol. 26, N 1. – P.177.
21.Keith P.K., Scadding G.K. // Currents Med. Research Opinion. – 2009. – Vol. 25, N 8. – P 2021–2041.
22.Maspero J.F., Rosenblut A., Finn A. et al. // Otolaryngology – Head and Neck Surgery. – 2008. – Vol. 138. – P. 30–37.
23.Maspero J.F., Walter R.D., Wu W. et al. // Allergy Asthma Proc. – 2010. – Vol. 31. – P. 483–492.
24.McCormack P.L., Scott L.J. // Drugs. – 2007. – Vol. 67, N 13. – P. 1906–1915.
25.Meltzer E.O., Lee J., Tripathy I. et al. // Ped. Allergy Immunol. – 2009. – Vol. 20. – P. 279– 286.
26. Meltzer E.O., Stahman J.E., Leflein J. et al. // Clin. Therapeutics. – Vol. 2008. – Vol. 30, N 2. –P. 271–277.
27. Meltzer E.O., Tripathy I., Maspero J.F. et al. // Clin. Drug Invest. – 2009. – Vol. 29, N 2. – P. 79–86.
28. Nathan R.A., Berger W., Yang W. et al. // Ann. Allergy Asthma Immunol. – 2008. – Vol. 100. –P. 497–505.
29. Patel D., Ratner P., Clements D. et al. // Ann. Allergy Asthma Immunol. – 2008. – Vol. 100. –P. 490–496.
30.Rosenblut A., Bardin P.G., Muller B. et al. // Allergy. – 2007. – Vol. 62. – P. 1071–1077.
31.Salter M., Biggadike K., Matthews J.L. et al. // Am. J. Physiol. Lung Cell Mol. Physiol. – 2007. – Vol. 293. – P. L660–L667.
32.Scadding G., Keith P.K. // Expert. Opin. Pharmacother. – 2008. – Vol. 15, N 9. – P. 2707– 2715.
33.Tripathy I., Levy A., Ratner P. et al. // Ped. Allergy Immunology. – 2009. – Vol. 20. – P. 287–294.
34.Vasar M., Houl P.-A., Douglass A. et al. // Allergy Asthma Proc. – 2008. – Vol. 29. – P. 313–321.











Комментировать