Общие принципы лечения (лекция)
Дубчак А.Е.
ГУ «Институт педиатрии, акушерства и гинекологии АМН Украины», г. Киев
История изучения физиологической и патологической сущности микроэкосистемы влагалища насчитывает не одно тысячелетие. Еще в I в. н. э. основоположник научной медицины Гиппократ и его ближайшие последователи пытались «…взглядом, осязанием, обонянием и вкусом» проникнуть в тайну fluor albus, уже тогда, связав их с воспалительными заболеваниями матки и влагалища. Это же мнение высказывали Ибн Сина в своем «Каноне врачебной науки», а также внучка Владимира Мономаха Зоя в написанном ею труде «Мази». И только спустя столетия, уже после изобретения Левенгуком микроскопа, было установлено, что здоровый человек является хозяином стабильной популяции микроорганизмов.
В половых путях здоровых женщин, начиная с неонатального периода и заканчивая постменопаузой, всегда можно обнаружить небольшое количество жидкого содержимого, которое увлажняет стенки влагалища, канала шейки матки, маточные трубы, делая их поверхность более сочной, гладкой и предотвращая тем самым развитие патологического слипчивого процесса.
Микроэкология влагалища здоровой женщины – многокомпонентная гормонозависимая система, состояние которой в значительной степени определяется иммунологической реактивностью макроорганизма, функциональным состоянием яичников и рН вагинального экссудата.
У здоровых женщин, как правило, отсутствуют видимые и ощущаемые ими выделения из половых путей благодаря равновесию между процессами образования влагалищного содержимого (транссудация, секреция, отторжение клеток эпителия) и всасывания его слизистой оболочкой. Однако под воздействием различных эндо- и экзогенных факторов (табл. 1) физиологический секрет, так же как и физиологический влагалищный транссудат, может стать патологическим, при этом изменяются не только его количественные, но и качественные характеристики. Очевидно, что основными факторами этого превращения являются микроорганизмы, образующие естественную экосистему влагалища, и в меньшей степени те патогенные бактерии, грибы и вирусы, которые проникают извне в половые пути здоровых женщин.
В настоящее время большое значение в развитии воспалительных заболеваний половых органов отводится нормальной микрофлоре влагалища, которая обеспечивает колонизационную резистентность (КР) генитального тракта. КР подразумевает совокупность механизмов, обеспечивающих стабильность количественного и видового состава нормальной микрофлоры, что предотвращает заселение влагалища патогенными микроорганизмами или чрезмерное размножение условнопатогенных микроорганизмов (УПМ), входящих в состав нормального микроценоза, и распространение их за пределы экологической ниши. В разные периоды жизни женщины в зависимости от активности репродуктивной функции микроценоз влагалища имеет определенные особенности, однако в любой период взаимодействие микрофлоры с иммунной системой организма обеспечивает состояние КР.
Вагинальная микроэкосистема состоит из постоянно обитающих (индигенная) и транзиторных (случайная микрофлора) микроорганизмов.
У здоровых женщин детородного возраста общее количество микроорганизмов в вагинальном отделяемом составляет 6–8,5 lg КОЕ/мл (или на 1 г) и состоит из разнообразных видов, число которых может достигать 40 и более. Доминирующим родом влагалищной среды являются Lactobacillus spp. (95–98%) – большая группа бактерий, в основном микроаэрофилов, в сочетании с облигатноанаэробными видами. Несмотря на разнообразие видового состава лактобацилл, выделяемых из влагалища здоровых женщин (более 10 видов), не удается определить ни одного вида, который присутствовал бы у всех женщин.
Среди транзиторных микроорганизмов влагалища чаще других удается выделить коагулазоотрицательные стафилококки, в первую очередь S. epidermidis, Corynebacterium spp., Streptococcus spp., Bacteroides_Prevotella spp., Mycoplasma hominis, которые обычно присутствуют в умеренном количестве (до 4 lg КОЕ/г). Столь же часто, но в меньшем количестве встречаются Micrococcus spp., Propionibacterium spp., Veillonella spp., Eubacterium spp.
Каждый шаг, сделанный различными исследователями в попытке выяснения определенных закономерностей (а они, несомненно, имеются) формирования и сохранения постоянства состава микробной экологии влагалища, впоследствии поможет выработать единую концепцию по данному вопросу, обобщенным ответом на который сегодня являются результаты исследований, проведенных С.Дж.Ф.Пристли и соавторами (1997), изложенные в статье с красноречивым названием «Что такое нормальная влагалищная флора».
Единая точка зрения (с незначительными расхождениями) существует лишь по вопросу о многообразии видового состава нормальной микрофлоры влагалища, представленной в течение жизни в основном строгими и факультативными анаэробными и в меньшей степени – аэробными микроорганизмами.
В состав микрофлоры влагалища могут входить облигатно-анаэробные грамотрицательные (или грамвариабельные) палочковидные бактерии – Gardnerella vaginalis (103 КОЕ/мл) и кокковые грамотрицательные – Neisseria spp. (кроме N. gonorrhoeae).
Представители семейства Mycoplasmataceae- Mycoplasma homnis и Ureaplasma urealyticum могут обнаруживаться у части здоровых женщин с количественным содержанием до 104 КОЕ/мл исследуемого клинического материала.
Знание особенностей вагинальной микрофлоры в различные периоды жизни имеет важное практическое значение для правильной интерпретации субъективных и объективных симптомов заболеваний и проведения дифференциальной диагностики различных клинических ситуаций.
Микроэкология влагалища – сложная экосистема, которая находится в состоянии динамического равновесия. Выраженные гормональнозависимые изменения физиологии на протяжении жизни женщины (менструация, беременность, менопауза) оказывают существенное влияние на количественный состав и качественное содержание вагинальной микрофлоры.
С современных позиций резидентную микрофлору рассматривают как совокупность микробиоценозов, занимающих определенные ниши на коже и слизистых оболочках и обеспечивающих их колонизационную резистентность во взаимодействии с иммунной системой организма хозяина.
При этом достигается идеальное состояние гомеостаза, которое, с одной стороны, позволяет макроорганизму противостоять проникновению в него патогенных (чужеродных) агентов, а с другой – препятствует попаданию сапрофитных бактерий в нетипичную для них среду обитания. Изменение численности того или иного вида микроорганизмов в соответствующем биотипе или появление бактерий, чуждых данным органам и тканям, служит сигналом для обратимых или необратимых изменений в соответствующем звене микроэкологической системы, к которой с полным правом можно отнести альянс резидентных бактерий с клетками эпителия влагалища и канала шейки матки.
Микроэкологические исследования позволяют с новых позиций переосмыслить роль УПМ в патологии, в частности, определить инфекционный, но не воспалительный генез ряда патологических состояний и понять необходимость интегральной оценки состояния микроценоза влагалища как диагностической процедуры, результаты которой следует учитывать при выборе рациональных мер профилактики и/или лечения. Диагностика оппортунистических вагинальных инфекций (вызванных УПМ) принципиально отличается от заболеваний, вызванных абсолютными патогенами (ИППП), тем, что само по себе выделение (индикация) микроорганизмов из патологического материала не является доказательством их этиологической роли, так как те же микроорганизмы колонизируют влагалище в норме. Только количественные микробиологические исследования, определяющие соотношение отдельных видов в микроценозе, могут в относительно полной мере характеризовать состояние микроценоза влагалища и степень его нарушения
Таблица 1
Основные внешние и внутренние факторы, влияющие на микроценоз влагалища
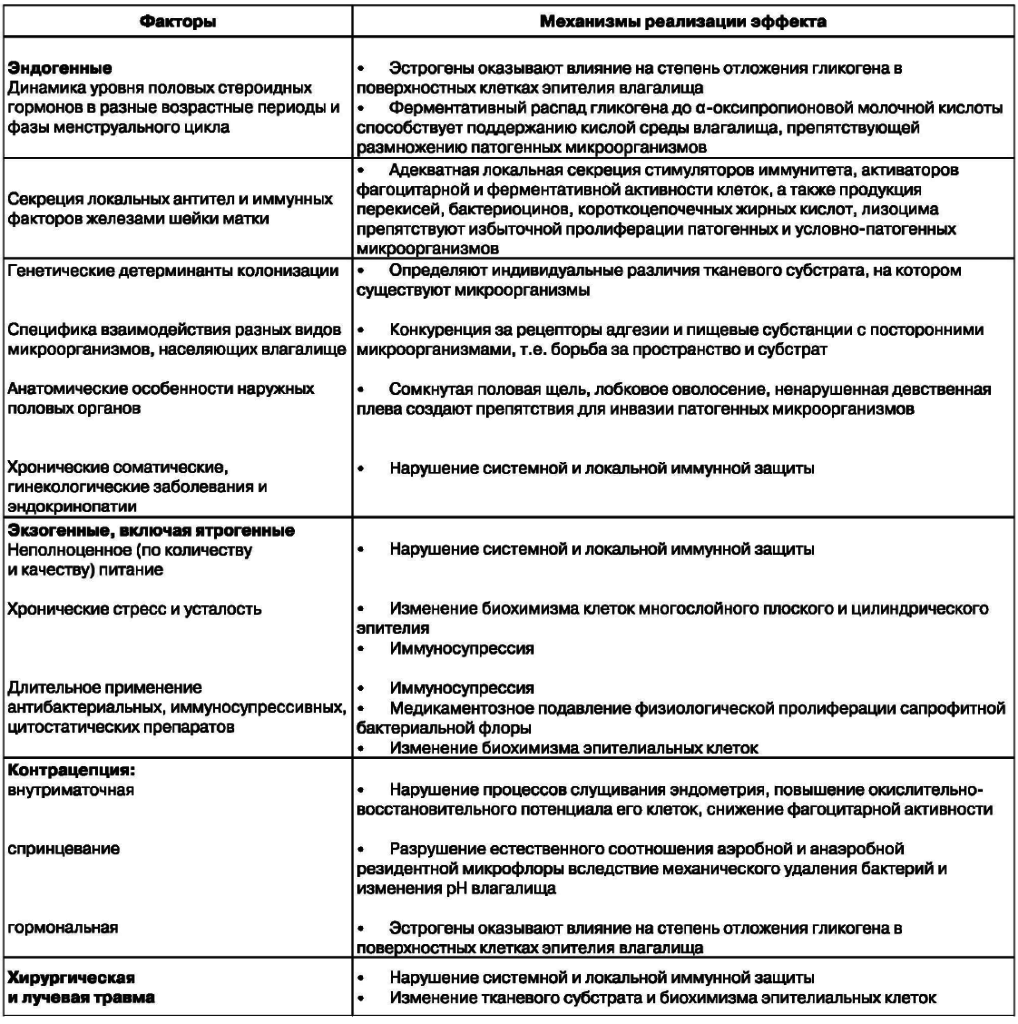
Нарушения состава микрофлоры влагалища у женщин с ИППП (хронические рецидивирующие заболевания урогенитального тракта) характеризуются снижением количества лактобацилл и бифидобактерий. На этом фоне выявляется рост в большом процентном соотношении стафило- и стрептококков – 68% и 79% соответственно. Реже высеваются грибы рода Candida – 46%, Е. coli – 28% и Proteus – 12%.
В микроценозе влагалища здоровых женщин репродуктивного возраста господствующие позиции (95–98%) занимают пероксидпродуцирующие лактобациллы (палочки Додерляйна), которые выполняют защитную функцию, препятствуя избыточной пролиферации более вирулентных микроорганизмов как путем прямой конкуренции с ними за пространство и питательные вещества, так и посредством поддержания неприемлемой для большинства патогенных бактерий кислой реакции содержимого влагалища. Остальная чрезвычайно гетерогенная микрофлора, населяющая половые пути, в настоящее время отнесена к разряду условнопатогенной, т.е она приблизительно с одинаковой степенью вероятности может быть идентифицирована как при отсутствии, так и при наличии воспалительных изменений половых органов. При этом, однако, не столь важен сам факт присутствия аэробной, анаэробной или даже грибковой микрофлоры, сколько количественные показатели уровня колонизации (число бактериальных единиц на 1 мл исследуемого материала), которые наряду с особенностями функционального состояния эпителия влагалища и шейки матки предопределяют принципиальную возможность развития воспалительных заболеваний. Так, клинически выраженная картина вагинального кандидоза наблюдается только при относительно высоком титре грибов рода Candida во влагалищном секрете (>104 КОЕ/мл).
Помимо количественных показателей колонизации влагалища теми или иными микроорганизмами не меньшее значение для поддержания оптимального состояния микроценоза вульвы и влагалища имеет строго определенная пропорция между аэробными и анаэробными бактериями. Известно, что в половых путях здоровых женщин репродуктивного возраста анаэробные бактерии преобладают над аэробами (соотношение ~ 10:1), причем общая численность условно-патогенных микроорганизмов не более 103 – 104 КОЕ/мл.
Микроэкосистема влагалища сугубо индивидуальна и в известной степени генетически детерминирована, она нестабильна даже в течение определенного временного периода, совпадающего с различными фазами менструального цикла. Наименьшее количество условно-патогенных микроорганизмов определяется в содержимом влагалища во время менструации. В первой фазе менструального цикла преобладают аэробные бактерии, a непосредственно перед менструацией значительно (в 100 раз и более) увеличивается количество анаэробов. Однако существует и иная точка зрения, согласно которой численность аэробов на протяжении менструального цикла практически не изменяется, в то время как общее количество анаэробов варьирует в широких пределах. В любом случае эти изменения абсолютно закономерны, поэтому их не следует расценивать как проявление какого-либо патологического процесса.
У здоровых женщин оптимальное соотношение между различными группами сапрофитных бактерий, а следовательно, и идеальное состояние микробиоценоза влагалища регулируются низкой кислотностью его содержимого (pH<4,5), благодаря которой оно обладает бактерицидными свойствами, вследствие чего не только обезвреживает токсины, но и препятствует размножению патогенных микроорганизмов.
В результате апоптоза клеток эпителия влагалища высвобождается гликоген, который с помощью диастатического фермента расщепляется до дисахарида мальтозы, а затем – до глюкозы, которую используют влагалищные бациллы в качестве питательного субстрата.
Единый комплекс химических и биологических защитных факторов, призванный обеспечить сохранность оптимальной микроэкосистемы влагалища, образуют его здоровый эпителий, содержащий достаточное количество гликогена, а также адекватные процессы ферментативного расщепления и брожения, определенный уровень рН, нормальная микрофлора и полноценная функция яичников. Разрушение любого из этих компонентов в отдельности или их совокупности оказывает негативное влияние на хрупкое равновесие внутри данной системы, что влечет за собой адаптивные или дезадаптивные изменения, клиническим отражением которых чаще всего являются патологические выделения из половых путей.
Во всех странах мира именно патологические выделения из влагалища являются основной причиной обращения женщины за советом к акушеругинекологу. Если учесть, что бели нередко являются единственным проявлением существующего заболевания (и не только гинекологического!), становится очевидной необходимость четкого представления об их возможных источниках и причинах возникновения.
Классификация видов и основных причин появления патологических выделений из половых путей
1. Вестибулярные бели
- вульвит бактериальной, вирусной и/или грибковой этиологии;
- бартолинит и абсцесс бартолиновой железы;
- аллергический вульвит;
- пиодермия и/или фурункулез кожи промежности;
- рак вульвы.
2. Влагалищные бели
- вагинит (кольпит) бактериальной, вирусной и/или
- грибковой этиологии;
- гельминтозы (энтеробиоз);
- инородные тела;
- рак влагалища;
- генитальные свищи (травматические, воспалительные,
- онкологические, радиационные);
- аллергический вагинит, в том числе латексный;
- атрофический вульвовагинит.
3. Цервикальные бели
- цервицит и эндоцервицит (острый и хронический)
- бактериальной или вирусной этиологии, включая туберкулезное, сифилитическое поражение шейки матки и пр.;
- рак шейки матки.
4. Маточные (корпоральные) бели
- эндометрит;
- туберкулез половых органов;
- пиометра, в том числе как осложнение рака эндометрия;
- аномалии положения матки (hуреrаnteversio_flexio, пролапсы половых органов).
5. Трубные бели гидро- или пиосальпинкс;
- рак маточной трубы.
Патологические выделения из половых путей по праву относят к разряду наиболее характерных жалоб, предъявляемых, по меньшей мере, 1/2–1/3 гинекологических больных. В большинстве случаев данный симптом рассматривают как тривиальный и не расценивают как возможный сигнал серьезной, иногда смертельной опасности. Именно поэтому ни женщины, ни акушеры-гинекологи не уделяют ему должного внимания, а между тем нельзя забывать, что бели могут быть первым и достаточно долго единственным клиническим проявлением не только относительно безобидных, хотя и очень мучительных для больной, вульвитов и вульвовагинитов, но и крайне тяжелых онкологических, соматических и эндокринных заболеваний.
Только 4 симптома — тазовая боль, диспареуния, зуд и дизурия – с наибольшим постоянством сопутствуют белям, образуя с ними единый комплекс симптомов, часто имеющих общие патогенетические корни, т.е. формируется синдром в истинном понимании этого термина. Однако если зуд, диспареуния и жжение в области вульвы в сочетании с патологическими выделениями из половых путей, как правило, свидетельствуют в пользу локальных воспалительных или, реже, атрофических изменений, то наличие тазовой боли различной интенсивности является основанием заподозрить первичное инфекционное либо опухолевое поражение матки или маточных труб.
Так, внезапное появление необильных зеленоватожелтых или грязно-серых выделений чаще свидетельствует об их инфекционной природе, в то время как эпизодическое истечение серозной жидкости в количестве, превышающем 30 мл, является одним из ранних и весьма характерных симптомов рака маточной трубы.
Зуд, обусловленный выделениями из половых путей, обычно возникает при кандидомикозной инфекции, но может также наблюдаться при атрофическом кольпите, вульвовагините, вызванных действием различных химических веществ, трихомониазе, а также при диабете. Однако усиление зуда во время сна, после водных процедур или полового акта характерно для урогенитального кандидоза, нередко приобретающего рецидивирующее течение у больных, регулярно и достаточно длительно принимающих антибактериальные препараты, и у больных с декомпенсированным сахарным диабетом.
Выраженные диспареуния и чувство жжения в области вульвы в сочетании с серозными выделениями из половых путей и явлениями общей интоксикации характерны для генитального герпеса. В то же время при наличии умеренно выраженной или интенсивной тазовой боли, сопровождающейся, как правило, обильными гнойными белями, изливающимися наружу через различные промежутки времени, в первую очередь необходимо исключить воспалительные заболевания матки и ее придатков, в том числе осложнившиеся образованием генитальных свищей.
У 60–70% женщин детородного возраста причиной белей становятся воспалительные заболевания наружных и внутренних половых органов, вызванные гарднереллами, влагалищными трихомонадами, грибами рода Сапdida, ассоциациями условнопатогенных аэробных и анаэробных бактерий или вирусами простого герпеса и папилломы человека. Удельный вес других патологических процессов, прежде всего злокачественных новообразований влагалища, шейки и тела матки, маточных труб, в этой возрастной группе не столь велик, однако исключение их априори может привести к тяжелым, а иногда – к трагическим последствиям. Вместе с тем к белям, являющимся симптомом указанных гинекологических или одним из проявлений экстрагенитальных заболеваний, не следует причислять физиологическое усиление выделений из половых путей, которое практически всегда наблюдается у женщин репродуктивного возраста в предменструальные дни, при половом возбуждении или во время беременности.
Для правильной интерпретации происхождения патологических выделений из половых путей не менее важными могут оказаться сведения, касающиеся особенностей менструальной и половой функций. Например, при сочетании белей с нарушением менструального цикла (задержка последней менструации, ее атипичное течение) у женщин, живущих половой жизнью, следует предположить наличие беременности, которая нередко служит косвенной причиной появления выделений из половых путей. Однозначно ответить на этот вопрос, т.е. по сути исключить физиологическую причину белей, следует до принятия положительного решения относительно необходимости проведения общего или местного лечения предполагаемого воспалительного процесса (рисунок).
Некоторые закономерности появления белей в различные фазы менструального цикла прослеживаются и при инфекционных заболеваниях половых органов. Так, патологические выделения при трихомонадном кольпите, как правило, возникают впервые или заметно усиливаются во время менструации, реже – сразу после нее; при воспалительных заболеваниях внутренних половых органов появление белей обычно приходится на 6–10-й день менструального цикла.
С клинических позиций не менее ценной может оказаться информация относительно особенностей половой функции женщины. Например, указание на наличие нескольких половых партнеров или частую их смену практически всегда склоняет чашу весов в пользу воспалительного генеза белей, особенно если не исключен риск взаимного инфицирования. Следует отметить, что не только признание, но и категорическое отрицание (часто ложное) случайных или регулярных половых контактов в принципе не исключает возможности сексуально-трансмиссивных заболеваний.
В настоящее время можно считать доказанным тот факт, что при длительном использовании гормональных контрацептивов существенно повышается риск развития вагинального кандидоза, применение внутриматочных противозачаточных средств приводит к увеличению вероятности воспалительных заболеваний матки и ее придатков в 3–9 раз, а широко практикуемые спринцевания не могут не повлиять на частоту развития бактериального вагиноза.
Патологические выделения из влагалища могут быть одним из симптомов основного заболевания, обусловившего нарушение генеративной функции при бесплодии и привычном невынашивании беременности. В таких клинических ситуациях вполне возможны хроническое течение воспалительного процесса и поражение эпителия влагалища, канала шейки матки, матки или маточных труб. Наоборот, указание на наличие в анамнезе тяжелых, длительных, травматичных родов через естественные родовые пути, влагалищной или абдоминальной гистерэктомии в среднем на 2–5% увеличивает вероятность посттравматического генеза белей, а значит, и возможной связи этого симптома с функционирующими кишечно-генитальными или урогенигальными свищами.
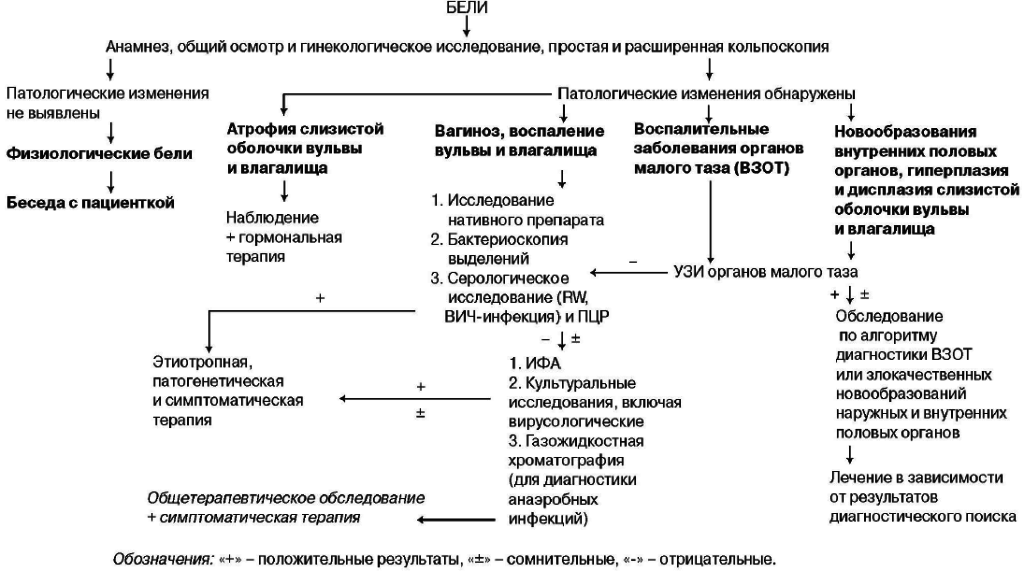
Дифференциальная диагностика при патологических выделениях из влагалища у женщин репродуктивного или перименопаузального возраста (Н.М. Подзолкова, О.Л. Глазкова, 2003).
Физиологический секрет, так же как и физиологический транссудат, может стать патологическим и изменить свой характер не только при заболеваниях половых органов, но и при некоторых соматических, эндокринных, инфекционных заболеваниях, включая болезни крови, гипо- и гипертиреоз, сахарный диабет, гельминтозы и пр. Конечно, бели не являются специфическим симптомом ни одного из них. Однако все эти заболевания, оказывая негатив ное влияние на системные и локальные факторы иммунной защиты и изменяя биохимизм эпителиальных клеток, создают благоприятные условия для появления патологических выделений из половых путей. Игнорирование или недопонимание этого обстоятельства неизбежно отразится на результатах лечения больной и может стать одной из причин постоянного рецидивирования белей. Так, отрицание априори взаимосвязи артрита, конъюнктивита, уретрита (синдром Рейтера) с патологическими выделениями из половых путей затруднит своевременную диагностику генитального хламидиоза. То же относится к сочетанию одностороннего гонита и гноевидных белей – симптомокомплексу, характерному для гонореи. В то же время даже установление не вызывающего сомнения диагноза каких-либо экстрагенитальных заболеваний полностью не исключает наличия иной, нередко более важной причины появления патологических выделений из половых путей. Так, у больной гипотиреозом или анемией вполне может быть обнаружена гонорея или, например, трихомонадный кольпит.
Известно, что хронические, периодически усиливающиеся гомогенные сливкообразные выделения серо-белого цвета, адгезированные на слизистой оболочке влагалища, характерны для бактериального вагиноза, в 20–90% случаев вызываемого гарднереллой. Свойственный этим белям неприятный рыбный запах объясняют распадом аминов, вырабатываемых анаэробными бактериями, активно размножающимися в клетках многослойного плоского эпителия. Сопутствующие выделениям зуд и ощущение жжения в области вульвы отмечает практически каждая вторая больная с бактериальным вагинозом. Однако, как это ни парадоксально, у них крайне редко наблюдаются отек и покраснение наружных половых органов, еще реже – характерные визуальные признаки острого воспаления слизистой оболочки влагалища.
Обильные, густые, творожистые выделения со своебразным кисловатым запахом характерны для генитального кандидоза, основным возбудителем которого (в 90% случаев) является Candida albicans. Выделения плотно прилегают к стенкам влагалища, образуя участки интенсивной гиперемии (огненно-красная кайма) и повышенной кровоточивости слизистой оболочки.
Чрезвычайно обильные, почти профузные водянистые мелкопенистые выделения белого или серозеленого цвета либо с желтоватым оттенком, иногда содержащие прожилки крови, характерны для трихомониаза. Специфический гнилостный запах, свойственный этим выделениям, объясняется особенностями биохимизма трихомонад, в частности образованием в процессе их жизнедеятельности диаминов – путресцина и кадаверина. При трихомонадном кольпите слизистая оболочка обычно резко гиперемирована и отечна. В связи с наличием локальной эритемы и мелких петехиальных кровоизлияний она приобретает своеобразный земляникоподобный вид. Интенсивное истечение едких белей очень часто приводит к мацерации и вторичному инфицированию наружных половых органов и кожи в области промежности.
Наличие вязких, кремообразных зеленоватожелтых выделений, стекающих в виде ленты из наружного зева шейки матки, характерно для гонорейного цервицита. В то же время внезапное излитие наружу большого количества (более 20–30 мл) гнойных белей чаще связано с опорожнением пиометры или пиосальпинкса, значительно реже – с дренированием воспалительных образований придатков матки через сформировавшийся и функционирующий генитальный свищ.
Обильные водянистые, почти прозрачные бели или зловонные выделения цвета мясных помоев практически всегда указывают на злокачественную опухоль влагалища, шейки матки или эндометрия, крайне редко их появление может быть связано с распадом иных патологических тканей – острых кондилом влагалищной стенки, подслизистого миоматозного узла или эндометриального полипа, а также с разложением инородных тел, оставленных во влагалище (презерватив, лекарственные и гигиенические тампоны и др.).
Наконец, постоянное или периодическое подтекание едких светло-желтых выделений, имеющих запах аммиака, патогномонично для пузырновлагалищного и мочеточнико-влагалищного свища, как правило, травматического (после операций на органах малого таза и травматичных родов), несколько реже – воспалительного, онкологического (параметральный вариант рака шейки матки IV стадии) или радиационного генеза.
Микробиологические критерии оценки состояния микроэкологии влагалища
Нормоценоз
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий представлен клетками поверхностных слоев, реже – промежуточных;
- «ключевые» клетки отсутствуют,
- иногда встречаются «ложноключевые» клетки;
- лейкоцитарная реакция отсутствует или слабо выражена — единичные лейкоциты в поле зрения;
- общее количество микроорганизмов «умеренное» или «большое»;
- доминирующий морфотип – лактобациллы.
Другие морфотипы либо отсутствуют, либо количество их исчисляется единицами в поле зрения.
Б. Культуральный метод:
- общая микробная обсемененность — 6–8 lg КОЕ/мл;
- абсолютно преобладают лактобациллы;
- УПМ в низком титре – менее 4 lg КОЕ/мл или отсутствуют.
Промежуточный вариант микроценоза
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий представлен поверхностными клетками, могут встречаться единичные «ключевые» клетки;
- количество лейкоцитов не более 10 в поле зрения;
- общее количество микроорганизмов «умеренное» или «большое»;
- доминируют морфотипы строгих анаэробов и гарднереллы в сочетании со сниженным титром лактоморфотипов.
Б. Культуральный метод:
- общее микробное обсеменение вагинального отделяемого колеблется от 7 до 9 lg КОЕ/мл;
- титр лактобацилл снижен, но может достигатьумеренных величин (5–7 lg КОЕ/мл);
- наличие лактобацилл сочетается с умеренным или высоким титром облигатных анаэробов и гарднерелл (5–7 lg КОЕ/мл).
Примечание: при неиспользовании строго анаэробной техники культивирования будет выявлен рост только лактобацилл.
Бактериальный вагиноз (БВ)
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий представлен клетками поверхностных слоев, редко встречаются промежуточные клетки, присутствуют «ключевые» клетки;
- лейкоцитарная реакция, как правило, отсутствует;
- общее количество микроорганизмов «массивное», реже «большое»;
- преобладают морфотипы строгих анаэробов и гарднереллы, лактоморфотипы отсутствуют или определяются как единичные не во всех полях зрения.
Б. Культуральный метод:
- общая обсемененность превышает 9 lg КОЕ/мл; при использовании только аэробных условий культивирования рост микроорганизмов отсутствует или наблюдается рост сопутствующих УПМ (при сочетанной патологии), чаще в небольшом титре;
- полимикробный характер микрофлоры с абсолютным преобладанием облигатно анаэробных видов и гарднерелл;
- отсутствие роста лактобацилл или их титр резко снижен (менее 4 lg КОЕ/мл).
Вагинальный кандидоз
В зависимости от концентрации грибов в отделяемом влагалища и характера сопутствующей микрофлоры вагинального биотопа мы выделяем 3 формы Candida-инфекции – кандидозный вагинит, сочетание БВ и кандидозного вагинита, а также бессимптомное носительство гриба.
Кандидозный вагинит
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий преимущественно поверхностных слоев, но может быть много промежуточных и даже парабазальных клеток; умеренная (до 10 лейкоцитов в поле зрения) или выраженная (более 10 лейкоцитов в поле зрения) лейкоцитарная реакция;
- общее количество микроорганизмов «умеренное» или «большое»;
- доминирует морфотип лактобацилл, присутствуют дрожжевые клетки, фрагменты псевдомицелия гриба с бластоспорами.
Б. Культуральный метод:
- общее количество микроорганизмов не превышает 8 lg КОЕ/мл;
- дрожжеподобные грибы присутствуют в титре, превышающем 4 lg КОЕ/мл;
- лактобациллы выделяются в большом количестве – 4–6 lg КОЕ/мл.
Сочетание БВ и кандидозного вагинита
А. Микроскопия мазка, окрашенного по Граму:
- влагалищный эпителий преимущественно поверхностный, могут встречаться промежуточные и парабазальные клетки, определяются «ключевые» клетки;
- умеренная (до 10 лейкоцитов в поле зрения) или выраженная (более 10 лейкоцитов в поле зрения) лейкоцитарная реакция;
- общее количество микроорганизмов «массивное», реже «большое»;
- доминируют морфотипы строгих анаэробов и гарднереллы, определяются дрожжевые клетки и/или фрагменты псевдомицелия гриба;
- лактобациллы отсутствуют или выявляются единичные лактоморфотипы в поле зрения.
Б. Культуральный метод:
- массивное микробное обсеменение, превышающее 9 lg КОЕ/мл, но при культивировании в аэробных условиях отмечается рост только дрожжеподобных грибов в высоком титре (4–7 lg КОЕ/мл);
- рост лактобацилл отсутствует или их титр низкий (менее 4 lg КОЕ/мл);
- доминирующая микрофлора — бактероиды, гарднереллы, анаэробные кокки.
Бессимптомное носительство гриба
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий представлен клетками преимущественно поверхностных слоев;
- лейкоцитарная реакция не выражена (единичные лейкоциты в поле зрения);
- общее количество микроорганизмов «умеренное» или «большое»;
- доминируют морфотипы лактобацилл, элементы дрожжеподобного гриба чаще всего не выявляются или обнаруживаются в полях зрения очень редко.
Б. Культуральный метод:
- общее микробное обсеменение не превышает 8 lg КОЕ/мл;
- в вагинальном отделяемом доминируют лактобациллы;
- рост дрожжеподобного гриба в низком титре (менее 4 lg КОЕ/мл).
Неспецифический вагинит
А. Микроскопия мазка, окрашенного по Граму:
- вагинальный эпителий представлен клетками поверхностного и промежуточного слоев, иногда встречаются парабазальные клетки;
- выражена лейкоцитарная реакция (более 10 лейкоцитов в поле зрения);
- общее количество микроорганизмов «умеренное»;
- лактобациллы отсутствуют или их количество резко снижено (до единичных в поле зрения);
- преобладают морфотипы УПМ (колиформные палочки, грамположительные кокки).
Б. Культуральный метод:
- отсутствие роста лактобацилл или их количество минимальное (менее 4 lg КОЕ/мл);
- рост факультативно-анаэробных УПМ, чаще какого-либо одного вида, в высоком титре (5–7 lg КОЕ/мл).
Атрофический кольпит
А. Микроскопия мазка, окрашенного по Граму:
- в зависимости от выраженности атрофии слизистой оболочки вагинальный эпителий представлен промежуточными и парабазальными клетками;
- количество лейкоцитов чаще в пределах 10 в поле зрения;
- микрофлора «скудная», практически отсутствует, могут встречаться единичные лактоморфотипы или морфотипы УПМ в редких полях зрения.
Б. Культуральный метод:
- низкая общая микробная обсемененность вагинального отделяемого (2–4 lg КОЕ/мл);
- низкий титр как лактобацилл, так и УПМ.
Общие принципы и методы лечения белей
В зависимости от того, что известно современной медицине о природе того или иного заболевания, клинически проявляющегося симптомом патологических выделений из половых путей, лечение больных может быть этиотропным, патогенетическим или, реже, только симптоматическим (табл. 2).
Способ введения лекарственных препаратов, их дозировка и длительность лечения зависит не только от клинической формы заболевания, но и от состояния макроорганизма женщины.
Для лечения острого кандидоза (особенно впервые возникшего эпизода), как правило, достаточным является назначение препаратов для местного применения. Эффективность лекарственных средств, содержащих противогрибковые азолы, одинакова (7585%), поэтому выбор препарата осуществляется согласно предпочтению врача или больного. Возможно применение лекарственных средств, оказывающих системное влияние на организм короткими курсами (однократно).
Таблица 2
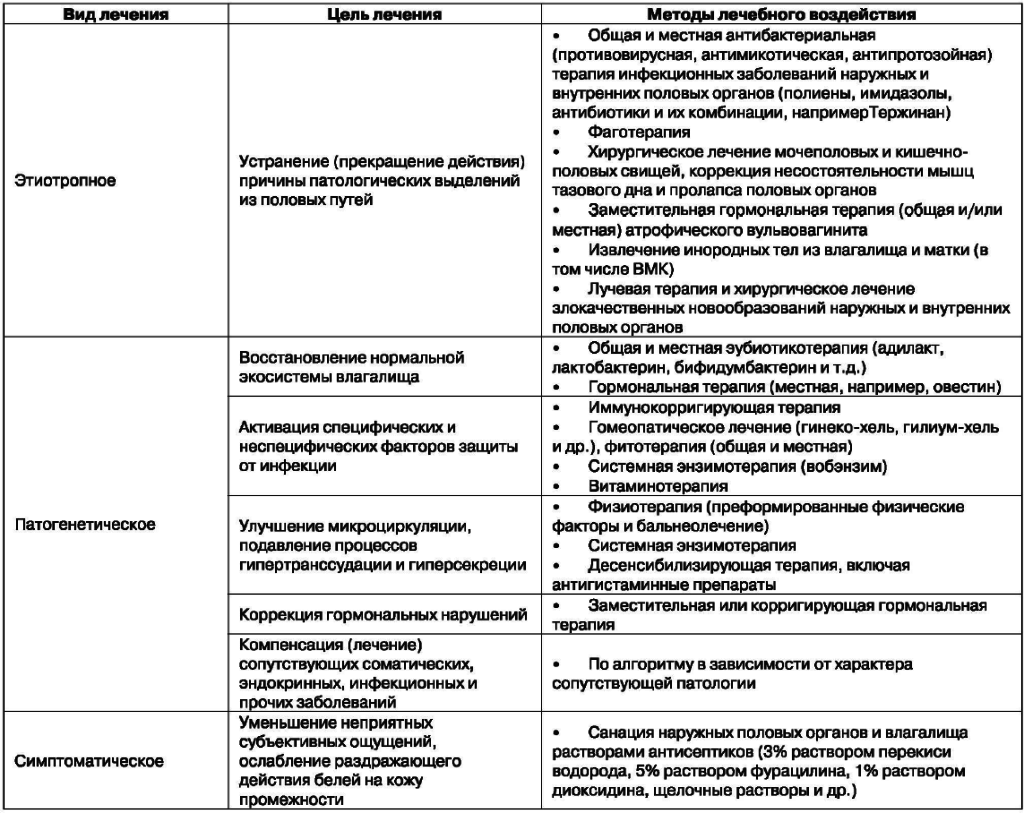
Лечение хронического кандидоза обязательно комбинированное. В первую очередь следует назначать терапию системными препаратами по удлиненной терапевтической схеме в течение 3-7 дней. Для местного лечения целесообразно применять комбинированные препараты или препараты, содержащие имидазол.
В случае, когда имеется место сочетание кандидоза с другими дисбиотическими нарушениями влагалища или, когда нельзя исключить их сочетание, а лечение в силу выраженности клинических симптомов следует начинать, препаратом первого выбора являются вагинальные таблетки Тержинан.
Поскольку при первичном обращении врач, как правило, не знает, какой именно микробный вид инфицировал больную, одновременное назначение веществ с разным спектром активности повышает шансы «попасть» в микроорганизм, следовательно, и эффективность лечения. Согласно современным представлениям, образование устойчивости частично объясняется появлением мутантов и последующей их селекцией при контакте с антимикробным агентом (препаратом). Если таковых несколько, «выживает» только тот мутант, который будет сочетать в себе «факторы устойчивости» ко всем компонентам комбинации, что, разумеется, встречается достаточно редко.
Тержинан используется для лечения БВ, неспецифического, кандидозного, трихомонадного или смешанного вульвовагинита, а также как средство профилактики развития этой патологии.
Этот препарат отличается наиболее полноценным составом, поэтому имеет неоспоримые преимущества по сравнению с другими комбинированными препаратами. Помимо антимикотического действия, Тержинан оказывает влияние на анаэробные микроорганизмы, которые являются наиболее вирулентными, а также на большинство грамположительных и грамотрицательных бактерий. Наличие микродозы преднизолона в составе препарата позволяет быстро купировать острые симптомы воспаления. Препарат назначается по 1 вагинальной таблетке (предварительно смоченной в воде в течение 20-30 с) глубоко в задний свод влагалища. Курс лечения в среднем составляет 6-10 дней, при необходимости может быть увеличен до 20 дней. Препарат хорошо переносится, не имеет побочных эффектов и противопоказаний. Может применяться во время менструации.
Применение других комбинированных средств (КлионД, Микожинакс, Гиналгин) ограничено при беременности и экстрагенитальной патологии, к тому же требует учитывать дозу метронидазола в этих лекарственных средствах в сторону увеличения количества таблеток на прием, необходимость назначения 2 раза в день.
Следует отдельно остановиться на лечении патологических выделений из половых путей у беременных. С целью унификации требований к объему и качеству лечения у беременных ИППП, антибактериальная терапия трихомониаза, вагиноза, кандидоза проводится в соответствии с рекомендациями ВОЗ, Приказа МЗ Украины № 906 «Клінічний протокол з акушерської допомоги. Перинатальні інфекції» .
Нистатин и натамицин – препараты, разрешенные для применения во время беременности и лактации. Оказывают фунгицидный эффект при отсутствии системного действия на организм, клиническая эффективность – 85-95%. Азолы, в том числе кетоконазол, миконазол, противопоказаны при беременности (исключением является иконазол). При местном применении азолы могут вызывать зуд, жжение, гиперемию и отек слизистой оболочки, выделения из влагалища, учащение мочеиспускания. Совместное применение амфотерицина, нистатина, натамицина снижает эффективность азолов.
Во время беременности и лактации (в связи с отсутствием системного влияния на организм) для лечения вагинального кандидоза, в том числе при его сочетании с другими неспецифическими воспалительными процессами во влагалище, высокоэффективен тержинан, который назначается c I триместра беременности – по 1 вагинальной таблетке в задний свод влагалища на ночь в течение 10-20 дней. Применение Тержинана во время беременности позволяет в ряде случаев избежать назначения антибактериальных препаратов, которые могут быть небезопасными для развития и роста плода.
Для этиотропного комплексного лечения трихомониаза используются производные нитроиммидазола, которые входят в международные и отечественные протоколы и рекомендации. Эффективность лекарственные средств этого класса при данной патологии не вызывает сомнений и доказана многими исследованиями. Этого нельзя сказать о других препаратах (хлоргексидин, хлорхинальдол, йод-повидон, нитрофураны, флуконазол, бутоконазол, гамицин, ацетарсол, фуразолидон, мебеданзол, мономицин). Эффективность хлоргексидина, повидон-йода, некоторых азолов, нитрофуранов исследовалась in vitro. Ввиду токсичности и отсутствия данных о безопасности, актуальность использования препаратов других групп ограничена единичными исследованиями.
При выборе лекарственного препарата необходимо учитывать данные Описания активных веществ в соответствии с международными непатентованными наименованиями для фармацевтических субстанций (WHO drug information) относительно способа применения, эффективной дозы, показаний, противопоказаний.
ЛИТЕРАТУРА
- Инфенкции в акушерстве и гинекологии / Под ред. О.В. Макарова, В.А. Алешкина, Т.Н. Савченко. – М.: МЕДпресс_информ, 2007. – 464с.
- Урогенитальные инфекции у женщин: клиника, диагностика, лечение / Под ред. В.И. Кисиной, К.И. Забирова. – М.: ООО «Мед. информ. Агенство», 2005. – 280 с.
- Подзолкова Н.М., Глазкова О.Л. Симптом. Синдром. Диагноз. Дифференциальная диагностика в гинекологии. – М.: ГЭОТАР_МЕД, 2003. – 448 с. 4. Кобозева Н.В., Кузнецова М.Н., Гуркин Ю.А. Гинекология детей и подростков: Руководство для врачей. – Л.: Медицина, 1988. – 295 с.
- Краснопольский В.И., Буянова С.Н. Генитальные свищи. – М.: Медицина, 1994. – 224 с.
- Диагностика, лечение и профилактика заболеваний, передаваемых половым путем: Метод. рекомендации / Под ред. К.К. Борисенко. – М.: Ассоциация САНАМ, 1997. – 72 с.
- Бохман Я.В. Руководство по онкогинекологии. – Л.: Медицина, 1989. – 464 с.
- Ларсен Б. Микрофлора половых путей в норме // Репродуктивное здоровье: Пер с англ.: В 2 т. Т. 1. Общие инфекции / Под ред. Л.Г. Кейта и др. – С. 17–63.
- Муравьева В.В. Микробиологическая диагностика бактериального вагиноза у женщин репродуктивного возраста: Автореф дис. канд. биол. наук. – М., 1997.
- Коршунов В.М., Володин H.H., Макаров О.В. и др. Микроэкология влагалища. Коррекция микрофлоры при вагинальных дисбактериозах. – М.: ВУНМЦ МЗ РФ, 1999. – 80 с.
- Onderdonk A.B., Wissemann K.W. Normal vaginal microflora / In: «Vulvovaginitis». – NY_Basel_Hong Kong, 1993. – P. 285–303.
- Johnson S.R., Petzold C.R., Galask R.P. Qualitatve and quantitative cyanges of the vaginal microbial flora during the menstrual cycle // Am. J. Reprod., Immunol., Microbiol. – 1985. – Vol. 9, № 1. – P. 1–5.
- Воропаева Е.А., Афанасьев С.С, Кудрявцева М.В. и др. Микроэкология и показатели гуморального иммунитета влагалища женщин с неспецифическими воспалительными заболеваниями гениталий // Журн. микробиол. – 2005. – № 3. – С. 65–69.
- Алешкин В.А., Султанова С.В., Афанасьев С.С. и др. Некоторые особенности иммунодиагностики и иммунотерапии торпидных хронических смешанных инфекций гениталий // International J. on Immunorehabilitation. – 2000. – Vol. 2, № 2. – P. 76.
- Gouarin S., Palmer P., Cointe D. et al. Congenital HCM V infection: A collaborative and comparative study of virus detection in amniotic fluid by culture and by PCR // J. Clin. Virol. – 2001. – Vol.– P. 47.
- Guerra B., Lazzarotto T., Quarta S. et al. Prenatal diagnosis of symptomatic congenital cytomegalovirus infection // Am. J. Obstet. Gynecol. – 2000. – Vol. 183, P. 476.
- Povlsen K., Thorsen P., Lind I. Relationship of Ureaplasma urealyticum biovars to the presence or absence of bacterial vaginosis in pregnant women and to the time of delivery // Eur. J. Clin. Infect. Dis. – 2001. – Vol. 20. – P. 65– 67.
- Schrag S.J.. Arnold K.E., Mohle-Boetani J.C. et al. Prenatal screening for infectious diseases and opportunities for prevention // Obstet. Gynecol. – 2003. – Vol. 102. – P. 753.
- Priestley С.J., Jones В.М., Dhar J., Goodwin L. What is Normal Vaginal Flora // Genitourin Med. – 1997. – Vol. 73, № 1. – P. 23–28.
- Кира Е.Ф., Цвелев Ю.В. Терминология и классификация бактериальных инфекционных заболеваний женских половых органов // Вестн. Рос. Ассоц. акуш._гинекол. – 1998. – № 2. – С. 11–18.
- Agnew K.J., Rillier S. L. The Effect of Treatment for Vaginitis and Cerevitis on Vaginal Colonization de Lactobacilli // Sex. Dis. – 1995. – № 22. – P. 269–273.













Комментировать