Миеломная болезнь: этиология, патогенез, клиническая картина, диагностика и лечение. Классификация и симптоматика.
П.Г. Кравчун, д-р мед. наук, профессор, зав. кафедрой госпитальной терапии, клинической иммунологии и аллергологии, А.Н. Шелест, д-р мед. наук, профессор кафедры госпитальной терапии, клинической иммунологии и аллергологии, А.П. Сидоров, канд. мед. наук, доцент кафедры госпитальной терапии, клинической иммунологии и аллергологии, Ю.А. Байбакова, канд. мед. наук, ассистент кафедры госпитальной терапии, клинической иммунологии и аллергологии Харьковского национального медицинского университета, А.Н. Бойко, зав. терапевтическим отделением городской клинической больницы № 27 Харькова
Миеломная болезнь (парапротеинемический гемобластоз) — это разновидность гемобластоза, основной особенностью которого является сохранение способности опухолевых клеток к дифференцировке до стадии иммуноглобулинсекретирующих клеток. Однако в связи с моноклональностью опухолевого роста все иммуноглобулины отличаются однообразием структуры (моноклональный парапротеин — РIg). Известно, что РIg могут соответствовать различным вариантам нормальных иммуноглобулинов (при плазмоклеточных опухолях — IgG, IgА, IgЕ; при лимфоклеточных — IgМ), отличаясь от них строгой однотипностью тяжелых и легких цепей, либо могут представлять структурно аномальные молекулы (субъединицы РIgМ, изолированные фрагменты тяжелых цепей, свободные легкие цепи) [4].
Распространенность миеломной болезни составляет 3 случая на 100 тыс. населения в год; мужчины болеют несколько чаще. Заболевание, как правило, проявляется в пожилом возрасте. Случаи заболевания до 40 лет встречаются крайне редко (менее 3% больных) [12].
Этиология миеломной болезни до конца неизвестна. Однако, по всей видимости, определенную роль может играть ионизирующее излучение. Отмечена более высокая заболеваемость среди японцев, переживших ядерную бомбардировку во время Второй мировой войны, через 20 лет латентного периода. Cуществуют также сведения относительно генетической предрасположенности к этому виду гемобластоза. Прямые доказательства вовлечения онкогенов человека при миеломе отсутствуют. Однако высокая частота хромосомных транслокаций при В-клеточных опухолях и участие РНК типа С при формировании плазмоцитомы мыши дают возможность предполагать роль цитогенетических нарушений в патогенезе болезни [5].
Клиническая картина. Дебют заболевания, как правило, протекает бессимптомно, сопровождаясь только повышением СОЭ. В дальнейшем характерно появление неспецифической симптоматики: снижение работоспособности, уменьшение массы тела, общая слабость, боль в костях. Клинические проявления могут быть следствием поражения костей, нарушения иммунитета, изменений в почках, анемии, повышения вязкости крови.
Боль в костях является наиболее частым признаком миеломы и отмечается почти у 70% больных. Она локализуется в позвоночнике и ребрах, возникает главным образом при движении. При метастазах в костях боль усиливается по ночам [1]. Непрекращающаяся локализованная боль характерна для патологических переломов. Разрушение кости при миеломе обусловлено пролиферацией опухолевого клона и активацией остеокластов под влиянием остеокластактивирующего фактора, выделяемого миеломными клетками. Лизис костей приводит к мобилизации кальция из них и гиперкальциемии, сопровождающейся такими осложнениями, как тошнота, рвота, сонливость, сопорозное состояние, кома. Литические процессы в костях могут быть выражены до такой степени, что опухолевые пролифераты можно пропальпировать, особенно в области черепа, ключиц и грудины. Уменьшение высоты тел позвонков является одним из признаков компрессии спинного мозга. На рентгенограммах выявляют либо очаги деструкции костной ткани, либо общий остеопороз, прежде всего в плоских костях, затем в проксимальных отделах трубчатых костей [10].
Частым клиническим признаком миеломной болезни является подверженность больных бактериальным инфекциям в связи с дисгаммаглобулинемией за счет повышенного количества парапротеинов при снижении продукции нормальных антител.
Патологию почек наблюдают более чем у половины больных. Она связана с фильтрацией в клубочках избыточно продуцируемых легких цепей, которые не могут полностью реабсорбироваться канальцевым эпителием и выделяются с мочой (протеинурия Бенс-Джонса). Большое количество экскретируемых легких цепей повреждает клетки канальцев, приводя к развитию почечной недостаточности. В ее происхождении играет роль и гиперкальциемия. Ранним проявлением канальцевого поражения является синдром Дебре – де Тони – Фанкони у взрослых с нарушением реабсорбции глюкозы, аминокислот и способности почек к ацидификации и концентрированию мочи. Как правило, в моче бывает мало альбуминов, поскольку функция клубочков чаще не нарушена, почти весь белок представлен легкими цепями иммуноглобулинов. При присоединении поражения клубочков возникает неселективная протеинурия, при этом возможно развитие артериальной гипертензии. Следствием гиперкальциемии может быть появление нефрокальцинатов. Кроме того, при миеломной болезни в 15% случаев развивается амилоидоз.
Несмотря на гиперпротеинемию, синдром повышенной вязкости крови не является частым признаком миеломной болезни. Повышенная вязкость, обычно при IgА-парапротеинемии, обусловливает неврологические симптомы: головную боль, повышенную утомляемость, нарушение зрения, ретинопатию. При образовании криоглобулинов отмечают синдром Рейно и нарушение микроциркуляции. Встречающиеся иногда полинейропатия, карпальный туннельный синдром и другие сенсомоторные нарушения могут быть связаны с отложением амилоидных масс вдоль периферических нервов.
У 5–13% больных выявляют спленомегалию и/или гепатомегалию вследствие инфильтрации плазматическими клетками, а также нередко и миелоидной метаплазии [8].
Классификация. Большинство авторов различают следующие варианты парапротеинемических гемобластозов: солитарная плазмоцитома, тлеющая миелома, множественная миелома, плазмобластный лейкоз.
Согласно иммунохимической классификации выделяют 5 основных форм множественной миеломы: G, A, D, E и Бенс-Джонса. К редким относят несекретирующую и М-миелому.
Выделяют клинические стадии множественной миеломы (согласно данным B. Durie, S. Salmon) [13].
Стадия I. Малая опухолевая масса (до 0,6·1012 клеток/м2):
- плазмоциты в костном мозге <30% ядерных клеток;
- уровень кальция в крови <2,75 ммоль/л;
- уровень гемоглобина >100 г/л;
- суточное выделение кальция с мочой
- нет костных изменений или один остеолитический очаг;
- низкий уровень продукции Мпротеина:
- IgG < 50 г/л (5000 мг%),
- IgA < 30 г/л (3000 мг%),
- IgU (легкие цепи в моче, протеинурия Бенс-Джонса)
Стадия II. Средняя опухолевая масса (0,6– 1,2·1012 клеток/м2):
- промежуточные показатели между стадиями I и III.
Стадия III. Большая опухолевая масса (более 1,2·1012 клеток/м2):
- плазмоциты в костном мозге >60% ядерных клеток;
- уровень гемоглобина
- уровень кальция в крови >2,75 ммоль/л;
- суточное выделение кальция с мочой >150 мг/сут (>4 ммоль/сут);
- уровень М-протеина:
- Ig G >70 г/л (7000 мг%),
- IgA >50 г/л (5000 мг%),
- IgU >12 г/сут.
Функция почек:
А — больные, не страдающие почечной недостаточностью (креатинин <176,0 мкмоль/л);
В — больные, страдающие почечной недостаточностью (креатинин >176,0 мкмоль/л).
Ранняя диагностика с использованием рутинных методов достаточно сложна в связи с неспецифичностью проявлений заболевания на начальных стадиях, когда изменения в крови могут отсутствовать, но по мере генерализации процесса у 70% больных развивается прогрессирующая гипохромная анемия, связанная с замещением костного мозга опухолевыми клетками и угнетением гемопоэза опухолевыми факторами. Однако может наблюдаться и мегалобластная анемия, обусловленная дефицитом фолатов и цианокобаламина. Иногда анемия является первым и основным проявлением заболевания.
Классическим симптомом миеломной болезни является резкое и стабильное повышение СОЭ, порой до 80–90 мм/ч. Количество лейкоцитов и лейкоцитарная формула очень варьируют. При развернутой картине заболевания возможна лейкопения (нейтропения), иногда в крови выявляют миеломные клетки, особенно с помощью метода лейкоконцентрации.
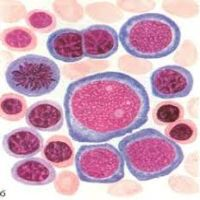
Для цитологической картины костномозгового пунктата характерно наличие более 10% плазматических (миеломных) клеток, отличающихся большим многообразием структурных особенностей; наиболее специфичны для миеломной болезни атипические клетки типа плазмобластов. По характеру пролиферации в костном мозге различают множественные опухолевые, диффузные и диффузно-узловые формы.
Плазмоцитоме характерна гиперпротеинемия с высокой парапротеинемией (РIg 30 г/л), сопровождающейся снижением количества нормоглобулинов, протеинурия Бенс-Джонса (легкие цепи Ig). Для выявления РIg используют метод электрофореза сыворотки и концентрированной мочи в агаровом геле и ацетатцеллюлозе, а также метод радиальной иммунодиффузии в геле с антисыворотками к иммуноглобулинам. Электрофорез дает возможность выявить М-градиент (полосу моноклонового белка в зоне миграции глобулинов и уменьшение фракции вне этой зоны). Исследование сыворотки методом радиальной иммунодиффузии позволяет определить класс РIg, выявить и оценить степень дефицита иммуноглобулинов. Сывороточный М-компонент в 53% случаев относится к IgM-, в 25% — к IgА-, в 1% — к IgGтипу. В 20% случаев М-градиент отсутствует, ав сыворотке крови и моче больных обнаруживают легкие цепи иммуноглобулинов (миелома БенсДжонса, болезнь легких цепей). В 1% случаев в сыворотке крови не обнаруживают ни Мградиента, ни легких цепей иммуноглобулинов (несекретирующая миелома). При несекретирующей миеломе РIg выявляют только внутри опухолевых клеток с помощью иммуноферментного анализа с моноспецифическими антисыворотками против тяжелых цепей.
Обнаружена корреляция между изотипом легких цепей и продолжительностью жизни больных: у пациентов с Х-типом легких цепей более короткая продолжительность жизни, чем у больных с х-типом. Остается неясным, обусловлено ли это генетически детерминированными особенностями клеточной пролиферации или тем, что эти цепи чаще вызывают повреждение почек и образуют амилоид. Несмотря на вовлечение в патологический процесс костей, уровень щелочной фосфатазы обычно не повышен из-за отсутствия остеобластической активности.
Продолжительность жизни больных зависит от стадии, на которой диагностирована опухоль. Причинами смерти могут быть прогрессирование миеломы, почечная недостаточность, сепсис и др.
В настоящее время используют европейские (рекомендации Британского форума по множественной миеломе и Скандинавской исследовательской группы по множественной миеломе, 2005 [7]) критерии диагностики и лечения миеломной болезни [6], адаптированные для Украины [10].
А. Большие:
- наличие плазмоцитов в биоптате тканей;
- плазмоциты в костном мозге >30%;
- уровень М-протеина:
а) IgG >35 г/л (3500 мг%);
б) IgA >20 г/л (2000 мг%); в) IgU >1 г/сут.
Б. Малые:
- плазмоциты в костном мозге 10–30%;
- М-протеин в меньшем количестве, нежели при критериях больших: IgG
- очаги остеолиза в костях;
- IgM < 50 мг%; IgA < 100 мг%; IgG < 600 мг% (резидуальные в норме).
Диагноз считают подтвержденным, если имеется 1 большой критерий плюс 1 малый критерий, или 3 малых критерия, при этом 1-йи 2-й обязательно.
Рентгенологические признаки изменения костей имеют дополнительное значение. Исключение составляет экстрамедуллярная миелома, при которой в процесс часто вовлекается субсерозная лимфоидная ткань носоглотки и параназальных синусов без плазматизации костного мозга [3, 9].
Дифференциальную диагностику проводят с макроглобулинемией Вальденстрема, характеризующейся клональной пролиферацией IgМсекретирующих плазматизированных лимфоцитов. Как и при миеломе, в сыворотке крови обнаруживают М-компонент (более 30 г/л), который представлен в основном IgМ. У 20% пациентов наблюдают экскрецию с мочой легких цепей, в основном М-типа. Избыточная продукция моноклонального IgМ обусловливает синдром повышенной вязкости крови, который значительно более выражен, чем при миеломе. Отмечают также неврологические нарушения, кровоточивость. Преципитация PIgМ на холоде (криоглобулинемия) обусловливает синдром Рейно и периферические сосудистые окклюзии с развитием язвенно-некротических осложнений. Может развиться холодовая гемолитическая агглютининовая анемия. Чаще, чем при миеломе, выявляют спленомегалию и лимфаденопатию, но в отличие от миеломы изменения костей и гиперкальциемия отсутствуют. Поражение почек наблюдается редко. В костном мозге отмечают пролиферацию плазматизированных лимфоидных клеток (более мелкие, чем плазматические, с вакуолизированной базофильной цитоплазмой) [2].
Наибольшие трудности возникают при дифференциальной диагностике миеломной болезни и доброкачественных моноклональных гаммапатий неизвестного генеза (идиопатических). Их выявляют у 1% людей в возрасте старше 50 лет и у 3% — старше 70 лет. В этих случаях концентрация М-компонента ниже 20 г/л, в моче выявляют белок Бенс-Джонса, число плазматических клеток в костном мозге не превышает 5%, анемия отсутствует.
Дифференциальную диагностику необходимо проводить и со вторичными моноклональными гаммапатиями, наблюдаемыми при аутоиммунных заболеваниях, смешанной криоглобулинемии, злокачественных опухолях другого генеза, а также при некоторых вирусных, бактериальных и паразитарных инфекциях.
Миелому Бенс-Джонса, которая может проявляться только протеинурией без повышения СОЭ, часто ошибочно принимают за заболевание почек (нефрит, амилоидоз). При миеломе массивная протеинурия не сопровождается снижением уровня белка в крови, диагноз уточняют по результатам иммуноферментного исследования мочи.
Выбор метода лечения и его объем зависят от возраста, стадии (распространенности) и активности злокачественного процесса. У 10% пациентов с миеломой наблюдают медленное прогрессирование болезни в течение многих лет, редко требующее проведения противоопухолевой терапии. У больных с солитарной костной плазмоцитомой и экстрамедуллярной миеломой эффективна локальная лучевая терапия.
Условно весь период химиотерапии можно разделить на 3 этапа:
- индукция, включающая 3 курса VAD, мобилизацию высокими дозами циклофосфамида и сбор стволовых клеток, курс EDAP;
- консолидация, состоящая из 2 последовательно выполняемых трансплантаций аутологичных стволовых клеток;
- поддерживающая терапия, состоящая из подкожного введения интерферона альфа 3 раза в неделю по 3 млн ЕД в течение длительного периода времени.
- Индукция. Схема VAD:
- винкристин 0,5 мг/сут — дни 1–4-й с постоянной внутривенной инфузией;
- адриамицин 10 мг/м2 в сутки — дни 1–4-й с постоянной внутривенной инфузией;
- дексаметазон 40 мг/сут — дни 1–4-й, 9– 12-й, 17–20-й — прием внутрь.
При удовлетворительной переносимости, отсутствии осложнений и тяжелой миелосупрессии курсы VAD повторяют с интервалом в 7 дней (каждый следующий курс начинают на 28-й день от начала предыдущего).
Всего проводят 3 курса лечения по схеме VAD. В случае развития тяжелых осложнений (инфекционных, печеночной недостаточности, острого гепатита, сепсиса) допускается удлинение интервала между курсами VAD до месяца (следующий курс через 28–30 дней после окончания предыдущего).
В случае недостаточного ответа, при признаках прогрессирования процесса, сохранении симптомов заболевания после двух курсов VAD рекомендовано переходить к следующему этапу химиотерапии (терапии циклофосфамидом в высоких дозах и мобилизации стволовых клеток гранулоцитарным колониестимулирующим фактором (Г-КСФ) — филграстимом в дозе 250 мкг/м2 подкожно, сбор стволовых клеток).
Консолидация. После восстановления кроветворения, купирования осложнений больному выполняют 1-юи 2-ю трансплантацию аутологичных стволовых клеток крови.
Контрольное обследование выполняется после окончания 3 курсов VAD, введения высоких доз циклофосфамида, курса EDAP.
Таким образом, весь период индукции (3 курса VAD, высокие дозы циклофосфамида с последующей мобилизацией и сбором стволовых клеток, курс EDAP) должен занимать 4–5 мес (не более 6 мес) от начала терапии.
Выполнение 1-й трансплантации красного костного мозга (ТСКК) (1-й этап консолидации) начинается через 1,5–2,5 мес после окончания индукции и не позднее 8 мес с момента начала стандартной терапии; 2-ю ауто-ТСКК выполняют не позднее 6 мес с момента выполнения первой.
После выполнения 1-йи 2-й трансплантаций необходимо провести весь комплекс диагностических исследований, включая полимеразную цепную реакцию (ПЦР).
Поддерживающую терапию начинают не позднее 30–45-го дня после 2-й ауто-ТСКК. Обязательным условием для начала поддерживающей терапии является удовлетворительное состояние пациента и восстановление кроветворения: уровень лейкоцитов не менее 2·109/л, тромбоцитов не менее 100·109/л.
Поддерживающая терапия включает подкожное введение интерферона альфа 3 раза в неделю по 3 млн ЕД в течение длительного периода (вплоть до возможного рецидива).
Наблюдение за пациентом осуществляют в течение всего периода проведения поддерживающей терапии с обязательным контрольным обследованием не реже 1 раза в 3 мес (перечень необходимых диагностических процедур аналогичен таковым после курсов химиотерапии в период индукции).
У пациентов с ІА и IIА стадиями рекомендована выжидательная тактика, так как у них возможна медленно развивающаяся форма болезни [9]. При наличии симптомов нарастания опухолевой массы (появлении болевого синдрома, анемии, повышении уровня РIg) необходимо назначить цитостатики. Стандартное лечение состоит в проведении интермиттирующих курсов алкилирующих препаратов — мелфалана (8 мг/м2), циклофосфамида (200 мг/м2 в сутки), хлорамбуцила (8 мг/м2 в сутки).
Не существует единого мнения относительно сроков проведения лечения, но, как правило, его продолжают в течение не менее 1–2 лет при условии эффективности [11].
Кроме цитостатической терапии, проводят лечение, направленное на предупреждение развития осложнений.
1. Для профилактики гиперкальциемии:
- проводят гипергидратацию (не менее 3 л жидкости в сутки). Диурез должен составлять не менее 3–4 л/сут. Каждые 8–12 ч определяют концентрацию электролитов, при необходимости проводят коррекцию уровня калия и магния;
- осуществляют немедленную системную химиотерапию VAD, обязательным компонентом которой должен быть дексаметазон;
- вводят ибандронат натрия, который эффективно уменьшает концентрацию кальция в крови (не используют для длительной терапии). При внутривенной инфузии доза составляет 2–4 мг;
- вводят кальцитонин – пептидный гормон, подавляющий резорбцию костей и усиливающий почечную экскрецию кальция. Кальцитонин вводят каждые 6–12 ч в дозе 4–8 МЕ/кг подкожно или внутримышечно;
- сохраняют активный образ жизни
- проводят пульс-терапию высокими дозами дексаметазона (остается альтернативной программой).
- назначают препараты витамина D и андрогены для уменьшения остеопороза.
- Для предупреждения уратной нефропатии — аллопуринол при достаточной гидратации.
- Плазмаферез может быть средством выбора при синдроме гипервязкости крови и особенно в случае парапротеинемической комы.
- Показания к плазмаферезу: клинические признаки синдрома повышенной вязкости крови (кровоточивость, повышение АД, нарушение зрения, неврологические расстройства) и повышение уровня общего белка сыворотки выше 100 г/л (гиперпротеинемия — уровень IgG или IgA выше 50 г/л). Плазмаферез следует проводить ежедневно до стабилизации контролируемых показателей (общий белок крови, вязкость крови и плазмы). В качестве замещающих растворов используют растворы кристаллоидов, при гипоальбуминемии — растворы альбумина.
- Лучевую терапию назначают при наличии крупных очагов костной деструкции, резко выраженных локальных болях, которые обусловлены переломами и не купируются химиотерапией, корешковом синдроме при компрессии тел позвонков, а также в случае солитарной плазмацитомы. Суммарные дозы на очаг поражения составляют по меньшей мере 45–50 Гр (в зависимости от локализации).
- Для купирования оссалгического синдрома, предупреждения переломов костей в настоящее время используют бисфосфонаты. В случае, если их нет — применяют другие виды лечения: нестероидные противовоспалительные и наркотические препараты, лучевую терапию, ингибиторы остеокластов — кальцитонин. Однако эффективность нестероидных и наркотических препаратов невелика, так как длительного обезболивающего эффекта добиться не удается. Возможность лучевой терапии при множественной миеломе ограничена в связи с наличием большого количества очагов деструкции в костях скелета, мигрирующим характером боли, что требует повторного облучения.
- Препараты и дозы используемых бисфосфонатов аналогичны таковым при гиперкальциемии. Необходимо отметить, что продолжительность терапии клодроновой и памидроновой кислотой (назначают в однократной дозе по 60–90 мг в день каждые 3–4 нед — разводится в 500 мл изотонического раствора хлорида натрия и вводится не менее чем за 2–3 ч) — 6–8–10 мес и более.
- Больным проводят реконструктивные и ортопедические операции в случае тяжелых нарушений функций конечностей с последующей химио-и лучевой терапией. При патологических переломах длинных трубчатых костей необходима хорошая репозиция и фиксация отломков. Если переломы возникли в местах крупных опухолевых узлов с большим диастазом отломков, осуществляют остеосинтез.
Современное лечение продлевает жизнь больных миеломой в среднем до 4 лет вместо 1 года – 2 лет без лечения. Продолжительность жизни во многом зависит от чувствительности к терапии цитостатическими средствами. У больных с первичной резистентностью к лечению средняя выживаемость составляет менее года. При длительном лечении цитостатическими средствами отмечено учащение случаев развития острых лейкозов (до 2–5%).
Критерии ремиссии болезни:
– уменьшение минимум на 50% плазмоцитов в костном мозге;
– уменьшение минимум на 50% уровня Мпротеина; и/или
– уменьшение на 50% моноклонального белка в моче;
– нормализация уровня общего белка крови и белковых фракций крови;
– нормализация СОЭ;
– нормализация показателей общего анализа крови (гемоглобин);
– нормализация уровня кальция в крови.
Данные критерии отвечают частичной ремиссии.
Полная ремиссия — окончательное уменьшение количества парапротеина.
Отрицательные прогностические факторы при множественной миеломе:
– III стадия заболевания по B. Durie, S. Salmon (1975) [13];
– почечная недостаточность;
– тип моноклонального белка;
– наличие белка Бенс-Джонса;
– цитогенетические изменения (в частности, аномалия 13-й хромосомы);
– повышенный уровень р2-микроглобулина (норма 1–2,4 мг/л);
– повышение С-реактивного протеина в сыворотке крови;
– повышенный уровень IL-6 и его растворенного рецептора sIL-6;
– высокий пролиферативный индекс миеломных клеток;
– наличие моноклональных В-лимфоцитов в периферической крови.
Приводим клинические случаи из практики.
В терапевтическое отделение городской клинической больницы (ГКБ) № 27 Харькова поступили двое больных, которым был установлен диагноз «миеломная болезнь». Общим для двух случаев является полиморфность клинических проявлений.
Больной С., 59 лет. Находился в ГКБ № 27 Харькова с 16.01.2007 по 29.01.2007.
Жалобы на кашель со скудной мокротой слизистого характера, сопровождающийся болью в грудной клетке, тошноту, плохой аппетит, сухость во рту, жажду, выраженную слабость.
Анамнез болезни. Считал себя больным с конца декабря 2006 г., когда после переохлаждения стал беспокоить умеренный кашель с отделением небольшого количества мокроты по утрам. После новогодних праздников появились боль в эпигастральной области и диспептические явления, что больной связывал с погрешностями в диете и приемом алкоголя. 15.01.2007 обратился к участковому врачу, который направил его на обследование и лечение в ГКБ № 27.
Из анамнеза жизни известно, что в 1961 г. болел дизентерией, регулярно употреблял алкоголь, курил по полпачки сигарет в день.
Объективно: общее состояние удовлетворительное, сознание ясное, удовлетворительного питания.
Кожа и видимые слизистые оболочки обычной окраски, периферические лимфатические узлы и щитовидная железа не увеличены.
Перкуторно над легкими — легочный звук, аускультативно — на фоне везикулярного дыхания единичные непостоянные сухие хрипы.
Границы относительной сердечной тупости в пределах нормы. Тоны сердца приглушены, сердечная деятельность ритмичная. Частота сердечных сокращений (ЧСС) 96 в 1 мин. Артериальное давление (АД) 135/80 мм рт. ст.
Язык сухой, обложен белым налетом. Живот мягкий, безболезненный. Почки и селезенка без патологии. Симптом Пастернацкого отрицательный с обеих сторон.
Периферические отеки отсутствовали.
Физиологические отправления без особенностей.
В общем анализе крови от 19.01.2007 г.: гемоглобин 81 г/л, эритроциты 3,5·1012/л, цветовой показатель 0,71. Эритроциты частично гипохромные, анизоцитоз, умеренный микроцитоз, пойкилоцитоз. Тромбоциты 188·109/л. Лейкоциты 4,4·109/л (п. 3%, с. 53%, э. 1%, л. 32%, м. 11%). СОЭ 70 мм/ч.
В общем анализе мочи от 17.01.2007: количество 150 мл. Цвет желтый. Реакция слабокислая. Относительная плотность 1010. Прозрачность умеренная. Белок 0,045 г/л. Лейкоциты 8–10 вп/зр. Цилиндры: гиалиновые 1–3, зернистые 1–3 вп/зр. Плоский почечный эпителий 2–3 вп/зр. Слизь — много.
Исследование мочи по Нечипоренко от 18.01.2007: лейкоциты 1250 в 1 мл (N — до 2000), эритроциты 250 в 1 мл (N — до 1000), цилиндры 5 в 1 мл (N — до 20).
При исследовании мочи по Зимницкому от 19.01.2007: гипоизостенурия (колебания относительной плотности 1008–1010).
В биохимическом анализе крови от 19.01.2007: общий белок 85 г/л; альбумины 39,5%; глобулиновые фракции: α1 — 7%, α2 — 7%, β — 9,3%, γ — 37,2%. Кальций плазмы 3,22 ммоль/л. Креатинин 0,27 мкмоль/л. IgG >70 г/л. Мочевина сыворотки 25,4 (N — 2,5–8,3) ммоль/л. Креатинин 0,526 (N — 0,044–0,11) мкмоль/л. Щелочная фосфатаза 109 ЕД/л, аспарагиновая трансаминаза (АсАТ) 12,2 ЕД·ч/л, аланиновая трансаминаза (АлАТ) 15,2 ЕД·ч/л. Общий билирубин 10,5 мкмоль/л (прямой 2,3 мкмоль/л, непрямой 8,2 мкмоль/л). Глюкоза крови 4,6 ммоль/л.
При рентгенографическом исследовании органов грудной клетки (ОГК) от 03.01.2007 г. выявляли усиление легочного рисунка в прикорневых зонах. Корни тяжистые, синусы свободные. Множественные деструктивные изменения костей ребер.
При фиброэзофагогастродуоденоскопии (ФЭГДС) от 17.01.2007 обнаружен дуоденогастральный рефлюкс, признаки очаговой эритематозной гастродуоденопатии. H. рylori не выявлен.
На электрокардиограмме (ЭКГ) от 16.01.2007: синусовая тахикардия.
При ультразвуковом исследовании (УЗИ) органов брюшной полости от 20.01.2007: признаки нефросклероза, саговая инкрустация обеих почек. Очаговый фиброз предстательной железы.
Рентгенография органов пищеварительного тракта (ПТ) от 23.01.2007: признаки гастрита, дуоденогастральный рефлюкс.
Ирригография по Фишеру от 25.01.2007: долихосигма.
При рентгенографическом исследовании черепа (рис. 1) от 25.01.2007 определяли дефекты кости различной величины.
Больной был осмотрен гематологом (29.01.2007), который рекомендовал обследование в условиях гематологического стационара для уточнения диагноза и выработки тактики дальнейшего лечения.
Диагноз больного оставался неясным, однако наличие очаговой деструкции костей черепа и ребер в сочетании с высокой СОЭ (до 70 мм/ч) позволило заподозрить миеломную болезнь с хронической гипохромной железодефицитной анемией средней степени тяжести. Другую причину костной деструкции (например, метастатическое поражение костей) при проведении сонографии органов брюшной полости, рентгеноскопии желудка и ирригоскопии по Фишеру выявить не удалось.
Для верификации диагноза была проведена трепанобиопсия (03.02.2007). В миелограмме выявили 27% плазматических клеток (признак относится к малым критериям этого заболевания, большим критерием является содержание этих клеток более 30%), что в сочетании с увеличением уровня белка до 90 г/л при повышении содержания гамма-глобулинов до 37,2% не исключало наличия миеломной болезни.
Таким образом, диагноз миеломной болезни у больного С. был установлен на основании двух малых критериев этого заболевания и является предположительным, так как считается подтвержденным при наличии 3 малых критериев.
Особенностями данного случая является манифестация миеломной болезни анемией, которую первоначально связывали с наличием патологии пищеварительного тракта, а также невысокая гиперпротеинемия и диспротеинемия при отсутствии высокой протеинурии.
Больному установлен клинический диагноз: множественная миелома, диффузная форма, IIB стадия по B. Durie, S. Salmon, с поражением костей черепа и ребер. Миеломная нефропатия. Хроническая почечная недостаточность II стадии.
Больной З., 65 лет. Находился в ГКБ № 27 с 29.03.2007 по 13.04.2007.
Жалобы на общую слабость, кашель с отделением небольшого количества мокроты по утрам, ноющую боль под обеими лопатками, усиливающуюся при кашле.
Анамнез болезни. Считал себя больным со ІІ декады марта 2007 г., когда появились перечисленные выше жалобы. При рентгенологическом исследовании ОГК 16.03.2007 патологических изменений не выявляли. Амбулаторно проведено лечение по поводу обострения хронического бронхита, в связи с неэффективностью которого 28.03.2007 больной госпитализирован в ГКБ № 27 Харькова.
Из анамнеза жизни известно, что в период с 1958 по 1964 г. неоднократно болел воспалением легких. Находился в исправительно-трудовой колонии. Курил полторы пачки сигарет в день. Алкоголь не употреблял в течение последних 15 лет.
Объективно: общее состояние относительно удовлетворительное, сознание ясное, удовлетворительного питания.
Кожа и видимые слизистые оболочки обычной окраски. Периферические лимфатические узлы и щитовидная железа не пальпируются.
Перкуторно над легкими легочный звук с коробочным оттенком, дыхание с жестким оттенком, выслушивали рассеянные сухие хрипы. Частота дыхательных движений (ЧДД) 18 в 1 мин.
Левая граница относительной сердечной тупости сердца по левой среднеключичной линии. При аускультации сердечная деятельность ритмичная, тоны звучные, определяли незначительный акцент II тона над аортой. АД 170/100 мм рт. ст. ЧСС 84 в 1 мин.
Язык у корня обложен белым налетом. Живот мягкий, умеренно болезненный в эпигастральной области. Печень и селезенка не пальпировались. Симптом Пастернацкого отрицательный с обеих сторон.
Периферические отеки отсутствовали.
Мочеиспускание без особенностей, отмечал склонность к запорам.
В общем анализе крови от 31.03.2007: гемоглобин 108 г/л, эритроциты 4,2·1012/л; ретикулоциты 7%, цветовой показатель 0,77. Лейкоциты 6,2·109/л (п. 2%, с. 46%, э. 3%, л. 39%, м. 10%). СОЭ 70 мм/ч.
В общем анализе мочи от 30.03.2007: количество 50 мл, цвет желтый, реакция слабокислая. Относительная плотность 1020. Прозрачность умеренная. Белок 0,049 г/л. Лейкоциты 8–10, эритроциты неизмененные 10–15 вп/зр. Оксалаты — немного. Слизь — много.
В биохимическом анализе крови от 02.04.2007: общий белок 85 г/л, мочевина 8,0 ммоль/л, креатинин 0,136 мкмоль/л, общий билирубин 9 мкмоль/л (прямой — 1,5 мкмоль/л; непрямой — 7,5 мкмоль/л); АсАТ 0,20 ЕД·ч/л, АлАТ 0,28 ЕД·ч/л. Кальций сыворотки крови 1,39 ммоль/л. Сиаловые кислоты 220 ЕД, серомукоид 170 ЕД, церулоплазмин 0,30 г/л. IgG 65 г/л. Глюкоза крови 3,3 ммоль/л.
При рентгенографическом исследовании ОГК от 30.03.2007 очагово-инфильтративные изменения не выявляли. Корни легких фиброзно уплотнены; легочный рисунок обогащен, деформирован; плевральные наслоения передних синусов с двух сторон. Сердце обычной конфигурации, аорта уплотнена, развернута. Заключение: признаки хронического бронхита.
На ЭКГ от 29.03.2007: ритм синусовый, умеренная гипертрофия миокарда левого желудочка с признаками систолической перегрузки.
При исследовании функции внешнего дыхания от 29.03.2007 выявляли резкое нарушение вентиляционной функции легких по рестриктивному типу; значительное — по обструктивному типу.
Рентгенография органов ПТ от 19.03.2007: признаки умеренного гастродуоденита.
Ирригоскопия по Фишеру от 19.02.2007: долихосигма с нарушением эвакуаторной функции кишечника, косвенные признаки колита.
При УЗИ органов брюшной полости от 03.04.2007 обнаружены гепатомегалия, признаки хронического холецистита, микролиты и фиброзные изменения обеих почек. Гиперплазия предстательной железы.
При рентгенографическом исследовании черепа от 04.04.2007 (рис. 2): очаг деструкции костной ткани 0,3×0,5 см в лобной кости слева. Нельзя исключить миеломную болезнь.
На обзорной рентгенограмме костей таза от 11.04.2007 костнодеструктивные изменения отсутствовали.
Консультация гематолога от 10.04.2007: для исключения заболевания крови проведена стернальная пункция.
В миелограмме: в костномозговом пунктате клеток немного, преимущественно плазмоциты (46%). Мегакариоциты без нарушения отшнуровки тромбоцитов.
Клинический диагноз: множественная миелома, диффузно-очаговая форма, IIA стадия по В. Durie, S. Salmon.
Относительно особенностей данной истории болезни необходимо отметить, что у больного количество плазмоцитов в костном мозге составило 46%, что является большим критерием этого заболевания. Как и в первом случае, уровень общего белка сыворотки крови не превышал 85 г/л, а в моче составил только 0,049 г/л. Однако в указанном случае проводили определение уровня IgG, величина которого более 35 г/л является большим критерием миеломной болезни (у больного З. она составляла 65 г/л). Диагноз был установлен на основании двух больших и одного малого критерия миеломной болезни, что является достаточным для надежного его подтверждения.
Таким образом, при наличии «немотивированной» анемии и высокой СОЭ у лиц пожилого возраста, особенно в сочетании с упорной радикулярной болью, следует помнить о возможности развития миеломной болезни и необходимости проведения диагностических мероприятий, направленных на выявление больших и малых критериев данного заболевания. Ранняя диагностика миеломной болезни с использованием рутинных методов исследования является довольно сложной задачей. Показаниями к углубленному исследованию при подозрении на миеломную болезнь является совокупность симптомов: боль в костях, частые бактериальные инфекции, патология почек, анемия, значительное повышение СОЭ, общая слабость и уменьшение массы тела.
Литература
1. Алиев М.Д., Тепляков В.В., Каллистов В.Е. и др. Современные подходы к хирургическому лечению метастазов злокачественных опухолей в кости//Практ. онкология: Избранные лекции. – СПб, 2004. – С. 738–748.
2. Балашов А.Т., Золотарев А.В. Дифференциальная диагностика поражений позвоночника при миеломной болезни и костных метастазах (по данным рентгеновской компьютерной томографии): Материалы Невского радиологического форума «Наука — клинике». – СПб, 2005. – С. 223.
3. Балашов А.Т. Традиционная рентгенография в диагностике множественной миеломы: Материалы III науч.-практ. конф. с международным участием «Интервенционная радиология». – Петрозаводск, 2006. – С. 56–57.
4. Бессмельцев С.С., Абдулкадыров К.М. Множественная миелома. – СПб: Диалект, 2004. – 442 с.
5. Виниченко Л.Б. Гематологія: навч. посібник//Л.Б. Виниченко, В.Ф. Орловський. – Суми: Вид-во СумДУ, 2006. – С. 111–123.
6. Вотякова Ю.М. Множественная миелома: достижения лекарственного лечения ХХ– ХХI веков//Современная онкология. – 2004. – Т. 6, №1. – С. 1–6.
7. Диагностика и лечение множественной миеломы: Рекомендации Британского форума по множественной миеломе и Скандинавской исследовательской группы по множественной миеломе, 2005. – Режим доступа: www. рractica. ru / SMM / 0206 / 0206 part 3. pdf – 07.11.2008.
8. Егоров И.В. Редкие формы миеломной болезни//Клин. медицина. – 2004. – Т. 82, № 2. – С. 52–55.
9. Золотарев А.В., Солнцева С.В. Рентгеновская компьютерная томография в диагностике поражения позвоночника при миеломной болезни: Материалы III науч.-практ. конф. с международным участием «Болезнь Ходжкина». – Петрозаводск, 2004. – С. 96–97.
10. Матлан В.Л. Миеломная болезнь//Мистецтво лікування. – 2006. – № 1. – С. 10–16.
11.Сидорович Г.И. Результаты стандартной терапии множественной миеломы//Воен.мед. журн. – 2002. – Т. 323, № 2. – С. 58–59.
12.Трапезников Н.Н., Аксель Е.А. Заболеваемость злокачественными новообразованиями и смертность от них населения стран СНГ. – М., 1996. – 302 c.
13. Durie B.G., Salmon S.E. Cellular kinetics staging, and immunoglobulin synthesis in multiple myeloma//Annu Rev.Med. – 1975. – V. 26. – P. 283–288.







Комментировать