Лихорадка и ее патофизология. Лихорадка, гипертермия и повышение температуры тела. История жаропонижающих средств. Лекарственные препараты с жаропонижающим эффектом. Тактика применения жаропонижающих препаратов.
Дворецкий Л.И.
Лихорадка – один из древнейших защитно–приспособительных механизмов организма в ответ на действие патогенных раздражителей, главным образом инфекционных агентов.
Издавна у постели лихорадящего больного перед врачами всех времен возникало две проблемы, требующие по возможности быстрого принятия решения – диагностическая и терапевтическая. Основная проблема, разумеется, заключалась в распознавании причины лихорадки, а следовательно, в выборе адекватного лечения (этиотропная, патогенетическая, симптоматическая терапия). Другая задача касалась воздействия на лихорадку, как на симптом (симптоматическая терапия), влияющий на состояние больного, на различные органы и системы. По мере прогресса медицинской науки обе проблемы и поныне сохраняют актуальность и клиническое значение во врачебной практике.
В данной статье предполагается рассмотреть современное состояние проблемы симптоматического лечения лихорадки с использованием жаропонижающих средств, независимо от ее причины, а также с позиций современного понимания механизмов лихорадочной реакции организма.
Патофизиология лихорадки
Повышение температуры тела является одной из приспособительных реакций живого организма в ответ на воздействие разнообразных патогенных факторов (инфекции, эндотоксины, опухоли, конфликты в иммунной системе, травмы и повреждения, отравления, физические факторы и др.). Показано, что у млекопитающих при повышении температуры тела повышается фагоцитоз, продукция антител, выработка интерферона, стероидных гормонов и альдостерона, что позволяет рассматривать лихорадку, как биологически целесообразную реакцию [1].
Терморегуляция представляет собой процесс, в котором участвует целый континуум нервных структур и соединительных нервных волокон, исходящих из гипоталамуса и лимбической системы и идущих через нижние отделы ствола головного мозга и ретикулярную формацию в спинной мозг и симпатические ганглии. Главную роль в процессе терморегуляции играет участок головного мозга, расположенный в переднем гипоталамусе и в преоптической области, более известный еще со студенческой скамьи, как центр терморегуляции, предназначенный для регулирования температуры тела в норме и патологии [2].
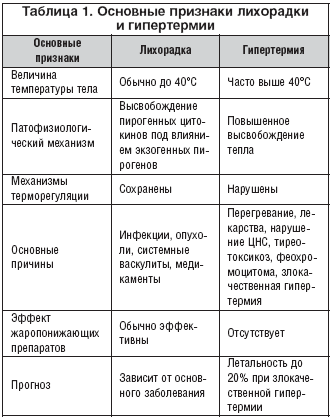
Следует различать понятия «лихорадка» и «гипертермия», которые иногда употребляются как синонимы при обозначении одного и того же состояния. В основе повышения температуры тела при лихорадке и гипертермии лежат разные механизмы. Лихорадка представляет собой сложный патофизиологический ответ организма на различные патогенные воздействия в виде повышения температуры тела, опосредуемого цитокинами, наряду с образованием реактантов острой фазы и активацией многих систем (иммунной, эндокринной и др.). В отличие от лихорадки гипертермия – нерегулируемое повышение температуры тела, в котором пирогенные цитокины непосредственного участия не принимают, а жаропонижающие средства при этом оказываются неэффективными. Иными словами, гипертермия представляет собой сбой терморегуляторного гомеостаза, при котором происходит неконтролируемая выработка тепла, недостаточная теплоотдача или нарушение терморегуляции на уровне гипоталамуса [3]. Теплопродукция может повышаться при тиреотоксикозе и феохромоцитоме. Причиной гипертермий могут быть лекарственные препараты (ингибиторы моноаминоксидазы (МАО), трициклические атидепрессанты, нейролептики, М–холиноблокаторы, антипаркинсонические препараты). Особое место среди гипертермий занимает так называемая злокачественная гипертермия – наследственное заболевание, характеризующееся избыточным накоплением ионов кальция в миоплазме, что вызывает длительную контрактуру мышц. Длительное мышечное сокращение вызывает значительное повышение температуры тела под влиянием анестетиков и мышечных релаксантов (триггерные агенты). Гипертермия развивается обычно во время или после анестезии. В таблице 1 представлены основные признаки лихорадки и гипертермии.
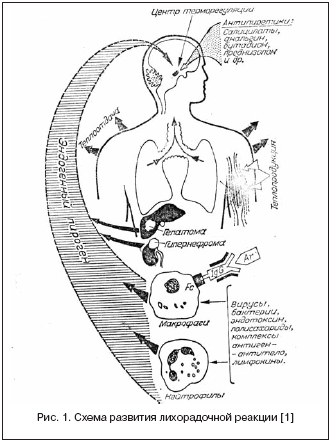
Схема лихорадочной реакции у человека в ответ на воздействие различных патогенных факторов представлена на рисунке 1. Данная схема заимствована из статьи А.И. Воробьева и М.Д. Бриллиант [1], одной из первых посвященных проблеме лихорадок неясного генеза в клинической практике.
Повышение температуры тела происходит при участии экзогенных и эндогенных пирогенов и их взаимодействии друг с другом. Экзогенные пирогены представлены микроорганизмами, токсинами и другими продуктами микробного происхождения (липополисахариды), а также неинфекционными антигенами, иммунными комплексами. Эндогенные пирогены – это клеточные цитокины, являющиеся главным медиатором лихорадки. Под воздействием экзогенных пирогенов происходит стимуляция клеток, главным образом нейтрофилов, моноцитов, макрофагов, вырабатывающих эндогенный пироген (пирогенные цитокины). Способностью к выработке эндогенного пирогена обладают опухолевые клетки (лимфопролиферативные опухоли, рак почки, печени и др.). Этим, по–видимому, и объясняется наличие лихорадки у данной категории пациентов, причем нередко опережающей другие симптомы болезни [4].
В настоящее время известны 11 цитокинов, обладающих пирогенной активностью. К наиболее важным пирогенным цитокинам относятся: интерлейкин–1 (ИЛ–1), интерлейкин–6 (ИЛ–6), фактор некроза опухоли–α (ФНО–α), g–интерферон [5]. Указанные цитокины находятся в тесном взаимодействии друг с другом: некоторые из них в одних условиях усиливают экспрессию других цитокинов или их рецепторов, а в других – снижают ее.
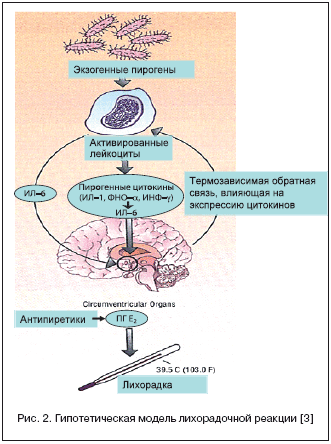
Согласно одной из гипотез предполагается, что при взаимодействии между пирогенными цитокинами и их рецепторами в преоптической области происходит активация фосфолипазы А2, с высвобождением арахидоновой кислоты в качестве субстрата для циклооксигеназного пути. Некоторые цитокины могут вызывать такой эффект посредством прямого увеличения экспрессии циклооксигеназы, в результате чего образуются метаболиты арахидоновой кислоты – простагландина (ПГ) Е2 и ПГF2a [3,6]. Последний легко проникает через гематоэнцефалический барьер и может служить медиатором, активирующим термочувствительные нейроны с последующим повышением температуры тела (рис. 2).
Будучи биологически целесообразной реакцией организма, свидетельствующей о неблагополучии и направленной на борьбу с патогенами, (в частности, инфекцией), лихорадка в то же время может вызывать целый ряд негативных последствий у пациентов всех возрастных групп. Такие ситуации могут возникать у больных при наличии тяжелой сопутствующей патологии и риске ее декомпенсации на фоне лихорадки, а также в случаях индивидуальной плохой переносимости высокой температуры.
Негативные последствия повышения температуры тела до фебрильных цифр сводятся к следующим:
– тахикардия (повышение температуры на 1°С приводит к учащению ЧСС на 10–15 ударов в минуту);
– нарушения ритма (чаще экстрасистолия) вследствие активации симпато–адреналовой системы цитокинами;
– повышение артериального давления (АД) в фазе подъема температуры тела и падение АД вплоть до коллаптоидного состояния при снижении температуры;
– повышенная потеря жидкости (за счет усиленного потоотделения и гипервентиляции). Возможно отделение до 1 литра жидкости за сутки через кожу и легкие, что может способствовать снижению объема циркулирующей крови (ОЦК);
– нарушения двигательной и абсорбционной активности кишечника с соответствующими клиническими проявлениями и последствиями;
– нарушения со стороны ЦНС (общемозговая симптоматика вплоть до развития спутанности сознания), что связывают с высвобождением b–эндорфинов под влиянием ФНО–α и ИЛ–1. Особенно часто нарушения со стороны ЦНС проявляются у детей младшего возраста, пожилых, больных с патологией сердечно–сосудистой системы, а также у лиц, злоупотребляющих алкоголем;
– усиление обменных процессов в клетках (при повышении температуры тела на 0,6°С уровень базального обмена возрастает приблизительно на 10%), ускорение окислительно–восстановительных процессов, увеличение потребления кислорода, повышение катаболизма белка, повышение уровня глюкозы;
– активация латентной герпес–вирусной инфекции. Наиболее часто герпетические высыпания сопровождают заболевания, вызванные бактериальной инфекцией (пневмококки, стрептококки, менингококки), малярию, риккетсиозы.
Вышеуказанные негативные последствия лихорадки могут оказывать особенно неблагоприятное воздействие на больных, страдающих различными сердечно–сосудистыми, неврологическими и другими заболеваниями. С учетом этого лихорадка у данной категории пациентов требует купирования или ослабления ее проявлений, т.е. симптоматического лечения.
Медикаментозные способы купирования лихорадки основаны на знаниях и понимании механизмов повышения температуры тела при различных патологических процессах. Жаропонижающий эффект препаратов осуществляется на уровне центра терморегуляции при их взаимодействии с так называемыми медиаторами повышения температуры – «посредниками» между эндогенным пирогеном (пирогенными цитокинами) и температурными рецепторами преоптической области гипоталамуса. Одним из таких «посредников» является ПГ Е2, производное арахидоновой кислоты. Так, например, салицилаты необратимо связываются с синтетазой простагландина, а глюкокортикоиды подавляют синтез ПГ Е2, ингибируя фосфолипазу А2. Таким образом, мишенью всех антипиретиков является ПГ Е2, а возможно, и другие метаболиты арахидоновой кислоты. Вместе с тем жаропонижающие препараты не оказывают антипиретического действия при повышении температуры, не связанной с пирогенными цитокинами, например, при гипертермиях, обусловленных уменьшением теплоотдачи (атропиновая гипертермия, злокачественная гипертермия, тепловой удар при перегревании и др.).
История жаропонижающих средств
Усилия врачей всех эпох медицины сводились к уменьшению выраженности лихорадки, снижению температуры тела и облегчению состояния больного даже при невозможности воздействовать на основную причину лихорадки. Способы купирования лихорадки были многообразны и диктовались исключительно клиническим опытом медиков, а также самих пациентов и их окружающих. Достаточно указать на воздействие низких температур непосредственно на тело больного (холодные компрессы, обертывания, пузыри со льдом и др.), использование некоторых химических веществ. Иногда эмпирически применяемые у лихорадящих больных «лекарства» оказывались в последующем именно этиотропными препаратами. Об этом свидетельствует опыт использования коры хинного дерева, которая веками применялась индейцами, как жаропонижающее средство. С 1632 г. иезуитский миссионер Бернабе Кобо дал первое описание «иезуитской коры» и привез ее в Европу, где кору стали с успехом применять у лихорадящих больных. Оказалось, что эффект наблюдался только при лихорадках у больных малярией. Это происходило задолго до того, как в 1880 г. французский военный врач Шарль Лаверан предположил, что малярия вызывается простейшими, за что был удостоен впоследствии Нобелевской премии.
В 1763 г. было сделано первое научное сообщение о жаропонижающем действии препарата, полученного из ивовой коры. Позже было установлено, что активным началом этого препарата является салицин, на основе которого в лабораториях немецкой компании Bayer, ранее производившей лишь анилиновые красители и учрежденной в 1863 г. коммерсантом Фридрихом Байером и владельцем небольшой красильни Иоганном Вескоттом, была создана ацетилсалициловая кислота (АСК), появившаяся в немецких аптеках в 1899 г. под торговым названием «аспирин».
Однако задолго до появления на фармацевтическом рынке аспирина компанией Bayer был разработан препарат с жаропонижающими свойствами. Принятый в 1884 г. на службу в компанию 23–летний Карл Дуйсберг, вставший в последующем у руля корпорации, поручил одному из научных сотрудников разработать лекарство на базе паранитрофенола – побочного продукта производства красок, лежавшего на складе мертвым грузом. Так в 1887 г. на свет появился жаропонижающий препарат, для которого Дуйсберг придумал фирменное название – фенацетин. Это лекарство широко использовалось в качестве жаропонижающего и анальгетического средства несколько десятков лет и лишь в 60–70–е гг. ХХ в. из–за негативных побочных эффектов было полностью изъято из употребления.
К тому времени на фармацевтическом рынке появился новый препарат – парацетамол, который позиционировался, как жаропонижающее и болеутоляющее средство, более безопасное по сравнению с АСК для детей и лиц с «язвенным анамнезом» [10]. В 1955 г. начались продажи парацетамола в США («тайленол»), а в 1956 г. – в Великобритании («панадол»). Небезынтересно отметить, что это оказалось вторым рождением парацетамола, который является метаболитом фенацетина и был синтезирован в 1877 г. Однако только в 1887 г. (время внедрения в клиническую практику фенацетина) он был применен у больных Джозефом фон Мерингом. В 1893 г. автор опубликовал результаты клинического применения парацетамола и фенацетина (ацетанилида), утверждая, что в отличие от фенацетина, парацетамол обладает способностью вызывать метгемоглобинемию. Это и открыло дорогу фенацетину, а парацетамол оказался забытым на десятилетия.
В 1949 г. удалось установить, что фенацетин действительно метаболизируется в парацетамол, а метгемоглобинемия возникает у людей в основном под действием другого метаболита – фенилгидроксиламина. Было также высказано предположение, что загрязнение парацетамола 4–аминофенолом (веществом, из которого он был синтезирован фон Мерингом) могло стать причиной ложных выводов [7]. Это и привело к «повторному открытию» парацетамола [6].
Наконец, фенацетин уступил место парацетамолу, который относительно широко стали применять после изъятия из оборота амидопирина и фенацетина. Появилось множество парацетамолсодержащих комбинированных лекарственных форм, в том числе в сочетаниях с ацетилсалициловой кислотой, метамизолом, кодеином, кофеином и другими препаратами.
Лекарственные препараты с жаропонижающим эффектом
Первые попытки воздействовать на лихорадку с помощью лекарственных средств связаны с применением ацетилсалициловой кислоты, уже с момента легализации ее в качестве лекарственного препарата. Однако с учетом ставших впоследствии известными фармакологических свойств АСК жаропонижающий эффект препарата в ряде случаев мог быть обусловлен не только и не столько его антипиретическими свойствами, но и воздействием на механизмы воспаления, одним из проявлений которого оказывалась лихорадка.
АСК до сих пор служит препаратом номер один при лечении многих заболеваний, в том числе используется как жаропонижающее средство. Правда, показания к ее применению при лихорадке в последнее время были серьезно пересмотрены, особенно в педиатрической практике в связи с риском возникновения у детей синдрома Рея.
В настоящее время АСК вытесняют другие жаропонижающие препараты, в первую очередь парацетамол.
Парацетамол ингибирует синтез простагландинов, блокируя обе формы фермента циклооксигеназы (ЦОГ–1 и ЦОГ–2), причем действует преимущественно в ЦНС, воздействуя на центры боли и терморегуляции. Предполагается также, что препарат селективно блокирует ЦОГ–3, которая находится только в ЦНС, не влияя на ЦОГ–1 и ЦОГ–2, расположенные в других тканях. Этим объясняется выраженный анальгетический и жаропонижающий эффекты и низкий противовоспалительный [8]. Отсутствие блокирующего влияния на синтез простагландинов в таких тканях обусловливает отсутствие у него отрицательного влияния на слизистую оболочку желудочно–кишечного тракта (ЖКТ) и водно–солевой обмен (задержка ионов Na+ и воды).
В отличие от АСК и других нестероидных противовоспалительных препаратов (НПВП) парацетамол не вызывает существенных побочных эффектов, прежде всего эрозивно–язвенных процессов в желудке, и поэтому остается предпочтительным для купирования лихорадки. Вместе с тем жаропонижающий эффект парацетамола был менее выраженным по сравнению с НПВП. Однако у АСК есть преимущества перед ним, когда речь идет о лихорадке у пациента с тяжелым поражением печени (в частности, при хроническом алкоголизме) и некоторых других состояниях.
Вслед за АСК и парацетамолом арсенал жаропонижающих средств пополнялся новыми препаратами из группы НПВП, в частности, производными индолуксусной кислоты (индометацин), фенилуксусной кислоты (диклофенак), пропионовой кислоты (ибупрофен, кетопрофен, напроксен), оксикамы (пироксикам, мелоксикам), производные гетероарилуксусной кислоты (кеторолак) и др.
Ибупрофе́н синтезирован и зарегистрирован в 1962 г., а с 1974 г. стал применяться в США в качестве болеутоляющего и жаропонижающего препарата. Самым ярким моментом в истории ибупрофена было получение в 1985 г. Королевской награды в знак признания научно–технических достижений в разработке этого препарата. В 1966 г. арсенал НПВП пополнился диклофенаком, а в дальнейшем были синтезированы пироксикам, напроксен.
Комбинированное использование двух препаратов из группы НПВП обычно не считается рациональным, так как возможны нежелательные реакции со стороны желудочно–кишечного тракта. Вместе с тем, поскольку жаропонижающий эффект парацетамола был менее выраженным по сравнении с НПВП, с клинической точки зрения казалось логичным использовать комбинацию парацетамола с одним из НПВП (ибупрофеном), когда при суммировании обезболивающего эффекта побочные явления не усиливаются.
Таким образом, ибупрофен является НПВП, обладающим противовоспалительным, жаропонижающим и обезболивающим действием, а парацетамол оказывает обезболивающее и жаропонижающее действие. Эффективность комбинации этих препаратов выше, чем отдельных компонентов. Парацетамол и ибупрофен, входящие в состав комбинированного препарата Ибуклин®, полностью отвечают критериям высокой эффективности и безопасности и официально рекомендуются ВОЗ и национальными программами в качестве жаропонижающих средств [WHO, 1993; S. M. Lesko et al., 1997; Практические рекомендации для врачей Российской ассоциации педиатрических центров, 2000]. Ибуклин® имеет существенные преимущества перед монопрепаратами – парацетамолом и ибупрофеном, т.к. в комбинированном препарате сочетается быстрое начало действия и длительный жаропонижающий эффект [13].
Ибуклин® содержит 400 мг ибупрофена и 325 мг парацетамола. Препарат оказывает жаропонижающее, противовоспалительное, аналгезирующее действие, обусловленное неселективным ингибированием ЦОГ–1 и ЦОГ–2 и подавлением синтеза ПГ. Ибуклин® применяется внутрь по 1 таблетке 3 раза/сут. (не более 6 таблеток в сутки). Длительность лечения – не более 3 дней в качестве жаропонижающего средства.
Помимо купирования лихорадочного синдрома, препарат может быть использован в лечении болевого синдрома средней интенсивности. Препарат отпускается по рецепту врача.
Кроме того, зарегистрирована детская форма препарата Ибуклин юниор, содержащая 100 мг ибупрофена и 125 мг парацетамола. Ибуклин юниор отпускается по рецепту врача.
Возможность комбинированного применения ибупрофена и парацетамола в педиатрической практике оценивалась в рандомизированном исследовании у 146 детей в возрасте от 6 мес. до 6 лет [9]. За 24 ч комбинация ибупрофена и парацетамола снизила продолжительность лихорадочного периода на 4,4 ч по сравнению с парацетамолом и на 2,5 ч по сравнению с ибупрофеном. Побочные эффекты при всех вариантах терапии существенно не различались.
Тактика применения жаропонижающих препаратов
При принятии решения о назначении антипиретиков с целью купирования лихорадки врач должен отдавать себе отчет в том, что подобная терапия в данной ситуации носит исключительно симптоматический характер (если назначение НПВП не имеет целью достижение противовоспалительного эффекта, например, при артритах различного происхождения).
При легкой или умеренной лихорадке жаропонижающие препараты назначают только детям с фебрильными припадками, беременным, а также больным с сердечной и дыхательной недостаточностью или сосудистым поражением головного мозга. Необоснованное применение жаропонижающих препаратов не дает возможности проследить за динамикой температуры, а противовоспалительное действие НПВП может маскировать проявления местной инфекции, затрудняя своевременную диагностику, а также способствует ее распространению. Следует помнить о биологической целесообразности лихорадочной реакции, а также о том, что отсутствие повышения температуры при инфекции свидетельствует о вероятности иммунодефицита и является неблагоприятным прогностическим фактором. Поэтому показаниями к назначению жаропонижающих средств являются не столько высокие цифры температуры тела, сколько ее плохая переносимость и риск возможного негативного влияния высокой температуры на различные органы и системы у больных с сопутствующей патологией и факторами риска.
Принятие решения о назначении жаропонижающего средства требует ответа на следующие вопросы:
– выбор препарата,
– путь введения,
– длительность применения.
При выборе препарата среди НПВП следует учитывать не только жаропонижающие свойства, но также и анальгетический эффект, поскольку болевые ощущения (головные боли, миалгии, артралгии и др.) нередко сопутствуют лихорадке. В таблице 2 представлены основные характеристики наиболее часто используемых НПВП, оцениваемые в порядке убывания того или иного свойства.
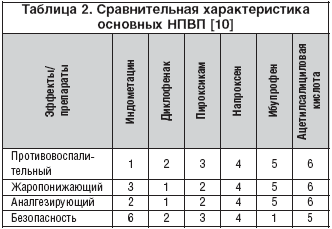
Большой выбор НПВП, обладающих жаропонижающими свойствами, ставит перед врачом проблему выбора препарата не только с точки зрения его антипиретического эффекта, но и минимального побочного действия. При выборе НПВП необходимо учитывать безопасность препарата, в том числе риск ульцерогенного эффекта, гепатотоксичность, цитопеническое действие, нефротоксичность, возможность взаимодействия с другими медикаментами, фармакокинетику препарата (длительность полувыведения, связь с белками, биодоступность и др.). При этом потенциальный риск развития побочных эффектов даже при кратковременном приеме препаратов может превышать их жаропонижающий эффект. Поэтому принятие решения о назначении антипиретиков должно быть взвешенным с учетом конкретной клинической ситуации, знаний особенностей фармакодинамики и фармакокинетики препаратов, имеющихся в распоряжении врача.
Путь введения НПВП должен обеспечивать оптимальную терапевтическую концентрацию препарата в крови, минимизировать риск побочных эффектов со стороны ЖКТ, быть удобным для применения и комфортным для пациента. С целью жаропонижающего эффекта используется прием препаратов внутрь, внутримышечные инъекции, внутривенные вливания и введение ректальных суппозиториев.
Пероральный прием НПВП является наиболее распространенным, но влечет за собой наибольший риск побочных эффектов со стороны ЖКТ (до 15%) [11]. Это зависит от продолжительности печеночной рециркуляции, определяющей длительность контакта со слизистой ЖКТ, что и приводит к гастроэнтерологической токсичности НПВП. С учетом этого при выборе перорального пути назначения НПВП предпочтение следует отдавать препаратам с коротким периодом полувыведения, быстрым всасыванием и быстрой элиминацией (ибупрофен, кетопрофен, диклофенак). Быстрая абсорбция способствует скорому наступлению жаропонижающего эффекта, а короткий период полувыведения снижает риск аккумуляции НПВП.
Внутримышечное (или внутривенное) введение НПВП с целью купирования или ослабления лихорадки широко практикуется врачами из–за более быстрого достижения жаропонижающего эффекта, а также в расчете на меньший риск гастроэнтерологической токсичности. Следует отметить, что различные побочные эффекты НПВП (в том числе и со стороны желудка) обусловлены не местным воздействием препарата, а ингибицией ЦОГ–1 независимо от способов введения их больному. Вместе с тем при внутримышечном введении часто назначаемого диклофенака возможно развитие мышечных некрозов в местах инъекций, а при длительном внутримышечном введении увеличивается риск возникновения инфильтратов и абсцессов мягких тканей. Кроме того, применение инъекционных форм является экономически более затратным.
Лекарственные формы НПВП в виде ректальных суппозиториев, применяемые в качестве жаропонижающих средств, имеют целый ряд преимуществ: в частности, абсорбция лекарственного препарата через кровеносную и лимфатическую систему, отсутствие влияния пищи и других медикаментов на биодоступность НПВП, уменьшение риска побочных эффектов со стороны ЖКТ, особенно при патологии желудка, двенадцатиперстной кишки, высокая биодоступность, сравнимая с таковой при внутримышечном введении.
Не следует назначать АСК детям при вирусных инфекциях из–за опасности развития синдрома Рея (обычно он развивается при гриппе и ветряной оспе, реже – при энтеровирусных инфекциях). Кроме того, АСК обладает антиагрегантным и антифагоцитарным действием, поэтому лучше применять парацетамол. Он почти не угнетает циклооксигеназу в периферических тканях и поэтому не обладает противовоспалительным действием; при окислении парацетамола в ЦНС образуется мощный ингибитор циклооксигеназы, который и отвечает за жаропонижающее действие препарата.
В плане быстроты начала действия и длительности жаропонижающего эффекта комбинация ибупрофена (400 мг) + парацетамола (325 мг) (Ибуклин®) более эффективна в сравнении с монопрепаратами [13].
Продолжительность применения жаропонижающих средств определяется главным образом клинической ситуацией. В большинстве случаев, например, при ОРВИ, инфекциях ЛОР–органов, длительность назначения НПВП для купирования лихорадки не превышает нескольких дней. В то же время у больных с различными бактериальными инфекциями при сохраняющейся лихорадке на фоне неэффективной антибактериальной терапии потребность в назначении НПВП может быть более длительной.
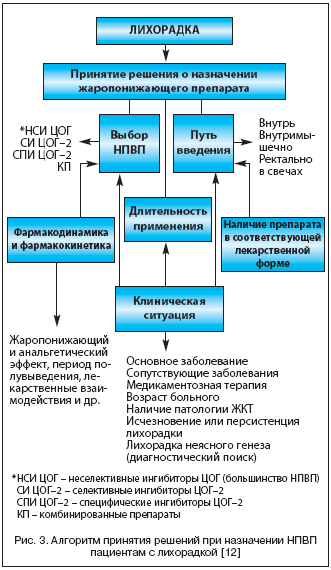
Особое место занимают так называемые лихорадки неясного генеза, причина которых нередко остается нерасшифрованной в течение длительного времени, а сохраняющаяся лихорадка требует более продолжительного использования НПВП. В подобных ситуациях важное значение приобретает эффективность жаропонижающего действия, удобство применения и главное – безопасность используемого препарата. Необходимость более длительного применения должна определяться клинической ситуацией (переносимость препарата, риск развития побочных эффектов, наличие и тяжесть сердечно–сосудистой, психоневрологической патологии и др.). Алгоритм принятия решений при назначении НПВП у больных с лихорадкой представлен на рисунке 3.
Литература
1. Воробьев А.И., Бриллиант М.Д. Гипертермия во внутренней клинике. Тер архив. 1981,10, 4–14
2. Mackowiak PA, Boulant JA. Fever’s glass ceiling. Clin Infect Dis. 1996;22:525–536
3. Mackowiak Ph.A. Соnсерts of fever Arch Intern Med. 1998;158:1870–1881).
4. Дворецкий Л.И., Дидковский Н.А. Лихорадочные маски злокачественных опухолей. Тер архив, 1979,6,82–84
5. Beutler B., Beutler S.M. The Pathogenesis of Fever// CECIL Textbook of Medicine,19 th edition, 1994, p.1568–1571
6. Дидковский Н.А.,Танасова А.Н.. Лихорадка. Русский медицинский журнал, 2003 г. № 4,189
7. Brodie B.B, Axelrod J. The fate of acetophenetidin (phenacetin) in man and methods for the estimation of acetophenitidin and its metabolites in biological material. J Pharmacol Exp Ther 1949,94 (1): 58–67
8. N.V. Hu Dai, K. Lamar Turepu Roos et al. COX–3, a cyclooxygenase–1 variant inhibited by acetaminophen and other analgesic/antipyretic drugs: Cloning, structure, and expression // Proc Natl Acad Sci. 2002, 99,21, 13926—13931.
9. Hay A.D. et al. Paracetamol plus ibuprofen for the treatment of the fever in children (PITCH): ranomised and controlled trial. BMJ, 2008,337, a1302.
10. Перспективы и преимущества суппозиториев с диклофенаком: дикловит. РМЖ, 2002, т.10, №22, с.1006–1008
11. Горячев Д.В. Возможности использования ректальных суппозиториев с НПВП. РМЖ 2003, т.11, №7, 387–389
12. Дворецкий Л.И. Лихорадка: лечить или не лечить? Русский медицинский журнал 2003 г. № 14,820–826.
13. Стремоухов А.А. Отчет о результатах исследования клинической эффективности препарата Ибуклин производства фирмы «Д–р Реддис Лабораторис ЛТД» (Индия) при острых респираторных вирусных инфекциях, проведенного с февраля 2005 г. по апрель 2005г. в поликлинике № 209 ЗАО г. Москвы и на кафедре общей врачебной практики лечебного факультета ММА им. И.М. Сеченова.













Комментировать