Оценка эффективности и безопасности применения препарата Элтацин® у детей с СВД.
М. Панина1, доктор медицинских наук, профессор,Л. Чекулдаева2, С. Обухова2, 1Медицинский университет «Реавиз», Самара, 2Самарская МСЧ №2, Самара
Синдром вегетативной дисфункции (СВД) — это одна из наиболее частых патологий детского возраста (достигает 20% в популяции детского населения). В соответствии с Международной классификацией болезней 10-го пересмотра [3] термины «вегетативно-сосудистая дистония», «нейроциркуляторная дистония», «вегетативный невроз», «вегетативная дизрегуляция», использовавшиеся для обозначения функциональных нарушений вегетативной нервной системы, рекомендуется заменить на «вегетативные дисфункции».
Вегетативная дисфункция — это заболевание организма, характеризующееся симптомокомплексом расстройств психоэмоциональной, сенсомоторной и вегетативной активности, связанное с надсегментарными и сегментарными нарушениями вегетативной регуляции деятельности различных органов и систем. Это состояние характеризуется нарушением вегетативной регуляции работы внутренних органов (сердечно-сосудистой системы, желудочно-кишечного тракта, органов дыхания, желез внутренней секреции и др.). В основе его лежат первичные (наследственно обусловленные) или вторичные (на фоне соматической патологии) отклонения в структурах и функциях центрального и периферического звеньев вегетативной нервной системы [1, 4, 5].
Целью исследования было оценить эффективность и безопасность применения препарата Элтацин® у детей с СВД.
ДИАГНОСТИЧЕСКИЕ КРИТЕРИИ СВД У ДЕТЕЙ.
СВД диагностировали методом исключения, исключив первичную патологию различных органов и систем.
Для оценки стабильных характеристик вегетативных показателей в состоянии покоя использовали диагностические критерии оценки исходного вегетативного тонуса (ИВТ) А.М. Вейна и соавт. [2], модифицированные для детского возраста (табл. 1). Количество приведенных в таблице признаков (45) свидетельствует о ваготонии или симпатикотонии как в определенной системе, так и в организме в целом.
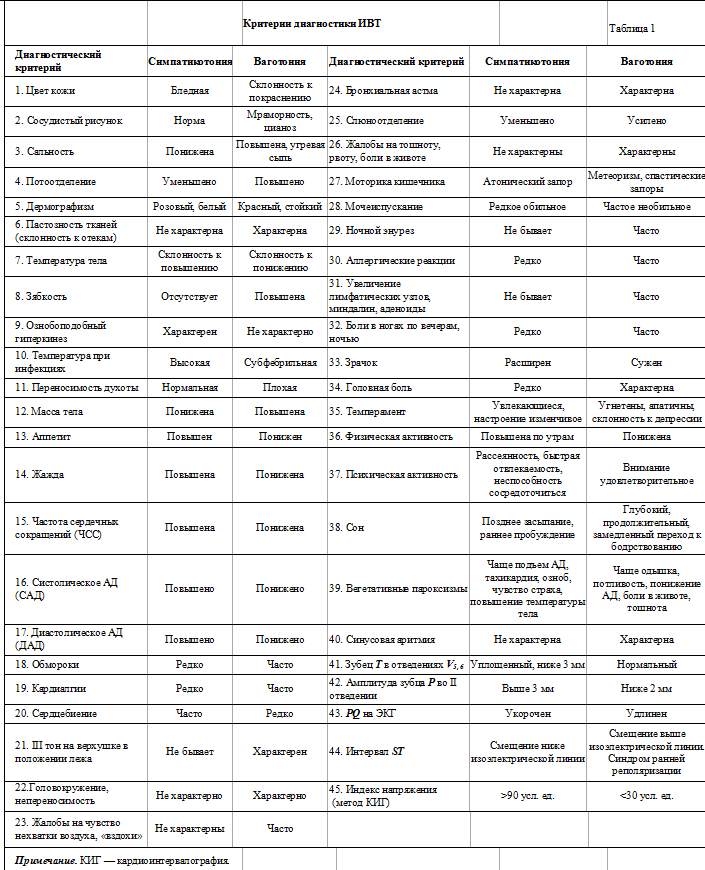
По табл. 1 подсчитывали число ваго- и симпатикотонических признаков. У здоровых детей число ваготонических признаков не превышает 4, симпатикотонических — 2, что соответствует эйтонии. У детей с СВД, у которых отмечается дисбаланс в обоих отделах вегетативной нервной системы, о характере ИВТ судили по преобладанию симпатических или ваготонических признаков по сравнению с их числом у здоровых. ИВТ может быть ваготоническим, симпатикотоническим, дистоническим.
Кроме оценки ИВТ по таблицам, у детей с СВД использовали метод КИГ. В основе этого метода лежит способность синусового узла реагировать на малейшие вегетативные нарушения со стороны сердечно-сосудистой системы.
Методика проведения КИГ.
После 5–10-минутного отдыха ребенка (лежа) записывали 100 кардиоциклов во II стандартном отведении ЭКГ Скорость движения ленты 50 мм/с. Для определения вегетативной реактивности запись КИГ проводили во время выполнения ребенком клиноортостатической пробы (КОП):
после записи КИГ в покое ребенок вставал (ортоклиноположение), и у него сразу же записывали 100 кардиокомплексов ЭКГ.
При анализе КИГ рассчитывали ряд показателей:
- Мо (мода, с) — наиболее часто повторяющийся интервал R–R во всем кардиомассиве;
- ∆Х — вариационный размах (разница между максимальным и минимальным значениями в массиве кардиоциклов);
- АМо — амплитуда моды — частота встречаемости Мо (% в общем кардиомассиве);
- ИН1 — индекс напряжения в покое (усл. ед.) — интегральный показатель, вычисляемый по формуле: ИН=АМо(%)/2Мо*∆Х(с).
Для симпатикотонии в покое характерен ИН1>90 усл. ед., для ваготонии — <30 усл. ед., для эйтонии — от 30 до 90 усл. ед. У некоторых детей с дистонией был нормальный индекс напряжения из-за сочетания ваго- и симпатикотонии. В таких случаях характер СВД определяли по совокупности клинических данных.
По результатам КИГ, кроме оценки ИВТ, определяли и другой важный показатель — вегетативную реактивность, под которой следует понимать изменение вегетативных реакций организма на внешние и внутренние раздражители.
Характер и тип вегетативной реактивности определяли по соотношению ИН2 (индекс напряжения в ортоклиноположении) и ИН1 (в покое). Выделяли 3 варианта вегетативной реактивности: симпатикотонический (нормальная), гиперсимпатикотонический (избыточная), и асимпатикотонический (недостаточная). Данные КИГ, используемые для определения типа вегетативной реактивности в зависимости от показателей ИВТ (ИН1), представлены в табл. 2.
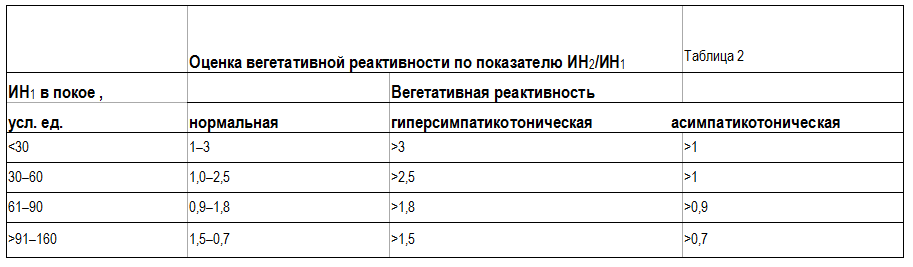
Пациенты методом простой рандомизации были разделены на 2 группы: в основную вошли 55 обследованных с СВД, в контрольную — 30.
При этом в основной группе было 30 пациентов с ваготонией и 25 — с симпатикотоническим типом вегетативных расстройств, в контрольной — соответственно 15 и 15 больных. По степени тяжести с учетом количества клинических признаков ИВТ, характера течения, ведущей органной локализации (функциональная кардиопатия), ИВТ сердечно-сосудистой системы по данным КИГ и вегетативной реактивности группы были сопоставимы.
В основной группе на фоне немедикаментозной терапии пациенты получали Элтацин® (по 1 таблетке 3 раза в день под язык в течение 3 месяцев). Элтацин® — препарат в таблетках для сублингвального применения. Содержит по 70 мг глицина, глютаминовой кислоты и цистина.
Препарат является регулятором обмена веществ: повышает внутриклеточный уровень глутатиона и глутатионзависимых ферментов, нормализует уровень окислительно-восстановительных ферментов, использование кислорода в тканях. Доклинические исследования показали что:
- Элтацин® является индуктором эндогенного глутатиона;
- усиливает образование аденозинтрифосфата, улучшает биоэнергетику клетки (эксперименты проведены на митохондриях);
- снижает уровень окислительного стресса и усиливает антиоксидантную защиту организма;
- положительно влияет на коронарный кровоток.
Пациенты контрольной группы получали только немедикаментозную терапию, которая включала занятия физкультурой, полноценное питание, психотерапию, водные процедуры, физиотерапевтическое лечение, массаж.
Всем больным проводили традиционное обследование (изучали анамнез заболевания, жалобы, данные осмотра и лабораторно-инструментального исследования).
Лабораторные анализы включали общий и биохимический анализы крови. Для измерения АД использовали метод Н.С. Короткова.
Данные электрокардиографии (ЭКГ) позволили определить нарушения сердечного ритма, интервалы P–Q. Кроме того, ЭКГ, эхокардиография (Эхо-КГ), нагрузочные пробы проводили для исключения органической патологии и уточнения характера вегетативных влияний на сердце и сосуды. Рентгенологическое обследование, кроме обзорной рентгенограммы грудной клетки, включало (по показаниям) краниографию, спондилографию.
При первичном осмотре у больных выявлялось много жалоб на изменения со стороны сердечно-сосудистой и нервной системы.
В результате проведенной терапии в обеих группах улучшилось общее самочувствие пациентов, повысилось настроение, уменьшилось количество жалоб. Однако, в группе пациентов, принимавших Эталцин®, количество детей, у которых произошло улучшение в самочувствии составило 87,8%, тогда как во 2-й группе только 34,9% (p<0,05). Дети стали активнее, стали лучше запоминать тексты, переносить транспорт. Улучшалось общее самочувствие, нормализовалось АД, уменьшились экстрасистолия, головные боли, стал нормализовываться сон, проходить страхи, улучшилась память, общая физическая активность. Побочных эффектов за время лечения не отмечалось.
В 1-й группе у детей быстрее наступало улучшение общего самочувствия, возрастала общая активность, повышалось настроение, исчезали гневливость, агрессивность поведения. Дети стали лучше засыпать ночью, исчезли страхи, они стали эмоционально более активными. У них отмечались снижение АД, уменьшение ЧСС. При сравнении 2 групп отмечено, что в группе детей, принимавших Элтацин®, улучшение наступало достоверно раньше, чем в контрольной группе, и показатели также были выше в конце лечения.
По результатам оценки ИВТ, уже через 10–12 дней было выявлено статистически достоверное уменьшение ваготонических и симпатокотонических признаков в группе пациентов, принимавших Элтацин® (в контрольной такие изменения происходили в течение 1,5 месяцев после начала лечения).
Показатели КИГ и вегетативной реактивности по соотношению ИН2/ИН1 продемонстрировали статистически достоверную динамику уже через 10–12 дней терапии Элтацином, при этом в 87,0% случаев отмечен переход пациентов в эйтонию и нормальную вегетативную реактивность, тогда как в контрольной группе соответственно в 35,2% случаев (р<0,05) нормализация показателей происходила к 40–45 дню наблюдения.
Таким образом, проведенное открытое контролируемое, рандомизированное исследование с применением метаболического препарата Элтацин® у детей 11–16 лет с СВД подтвердило целесообразность его назначения на фоне немедикаментозной терапии. Отмечена общая положительная динамика всех показателей в группе пациентов, принимавших Элтацин® на фоне немедикаментозной терапии: дети стали активнее, улучшилось их настроение, быстрее наступала стабилизация общего состояния, нормализовались АД, сердечный ритм, уменьшились головные боли, улучшилось качество жизни в целом. Элтацин® рекомендуется принимать детям с СВД по 1 таблетке 3 раза в день под язык в течение 1–3 месяца (в зависимости от течения заболевания). Препарат Элтацин® полностью безопасен: на протяжении лечения ни у одного больного не отмечалось нежелательных побочных реакций.
Таким образом, проведенное исследование установило, что добавление Элтацина немедикаментозной терапии у пациентов с СВД улучшает их клиническое состояние. Детям с синдромом вегетативной дисфункции показано курсовое лечение метаболическим препаратом Элтацин® в составе комплексной немедикаментозной терапии.
На правах рекламы
Ознакомьтесь с инструкцией
Литература
- Акарачкова Е.М. К вопросу диагностики и лечения психовегетативных расстройств в общесоматической практике // Лечащий врач. – 2010; 10: 60–4.
- Вегетативные расстройства (клиника, диагностика, лечение). Под ред. А.М. Вейна. Клиника, диагностика, лечение / М.: Медицинское информ. агентство, 1998; 752 с.
- Международная классификация болезней (10-й пересмотр). Классификация психических и поведенческих расстройств. Исследовательские диагностические критерии / СПб, 1994; 208 с.
- Robertson D., Haile V., Perry S. et al. Dopamine beta-hydroxylase deficincy: a genetic disordes of cardiovascular regulation // Hypertension. – 1991; 18: 1–8.
- Hyland K., Surtees R, Rodeck P. Aromatic L-amino acid decarboxylase deficiency clinical feathures, diagnosis and treatment of a new inborn error of neurotransmitter amine synthtsis // Neurology. – 1992; 42; 1980–8.













Комментировать