Концепция липидного дистресс-синдрома, сформированная на основе комплексных научных исследований по диагностике и хирургическому лечению нарушений липидного метаболизма при облитерирующем атеросклерозе, проведенных в клинике факультетской хирургии им. С.И. Спасокукоцкого РГМУ. Открытие неизвестных аспектов этиопатогенеза, разработка на их основе новых методик диагностирования и лечения не только атеросклероза артерий нижних конечностей, но многих других заболеваний, обусловленных либо непосредственно связанных с нарушениями липидного метаболизма.
Изучение рисков возникновения сердечных осложнений у пациентов, которым предстоит не связанное с сосудистой хирургией оперативное пособие: основные Рекомендации Американской коллегии кардиологов и Американской ассоциации сердца по стратификации сердечно-сосудистого риска у больных с предстоящим оперативным вмешательством. Оценка риска терапевтом (кардиологом) сердечно-сосудистых осложнений, при выявлении высокого риска – определение возможностей его снижения во время предоперационного обследования пациента.
Верткин А.Л., Тополянский А.В.
Пациент, поступающий в стационар хирургического профиля, обычно осматривается терапевтом уже в приемном отделении; нередко запись хирурга с назначениями «ЭКГ, консультация терапевта» становится трафаретной, а терапевт, в свою очередь, старается «отделаться» от непрофильного больного как можно быстрее. В то же время осмотр терапевтом (а при необходимости – и кардиологом) такого больного – далеко не формальная процедура. По данным, приведенным экспертами Европейского общества кардиологов (ESC, 2009), у пациентов, которым предстоит не связанное с сосудистой хирургией оперативное пособие, риск возникновения сердечных осложнений составляет 2,0–3,5%, риск смерти, связанной с сердечно–сосудистыми проблемами – 0,5–1,5%.
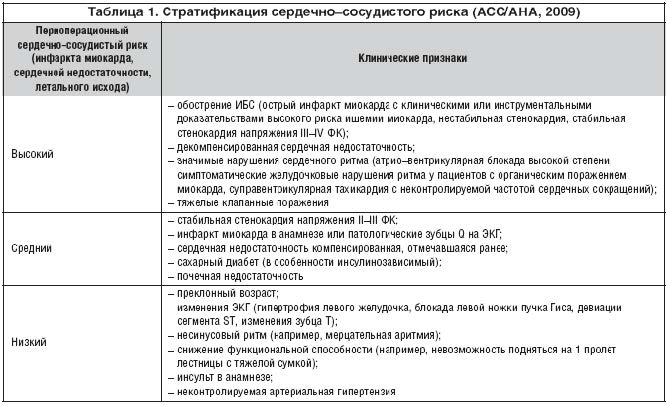
Таким образом, основными задачами терапевта (кардиолога) во время предоперационного обследования пациента должна быть оценка риска сердечно–сосудистых осложнений, а при выявлении высокого риска – определение возможностей его снижения. Рекомендации Американской коллегии кардиологов и Американской ассоциации сердца по стратификации сердечно– сосудистого риска у больных с предстоящим оперативным вмешательством (ACC/AHA, 2009) представлены в таблице 1.
Эксперты Европейского общества кардиологов (ESC, 2009) для оценки связанного с предстоящим оперативным вмешательством сердечно–сосудистого риска предлагают использовать индекс Ли. Этот индекс включает 5 независимых факторов, определяющих вероятность развития серьезных кардиальных осложнений: наличие ИБС, цереброваскулярных заболеваний, сердечной недостаточности, инсулинозависимого сахарного диабета, почечной недостаточности. Шестым фактором считают высокий риск предстоящего оперативного вмешательства. Сердечно– сосудистый риск составляет 0,4% при отсутствии каких–либо других факторов; 0,9% – при наличии только одного фактора; 7% при наличии 2 факторов и 11% при наличии трех и более факторов риска. Каждому из факторов присваивается значение 1 балла, соответственно, индекс Ли рассчитывается, как сумма баллов.
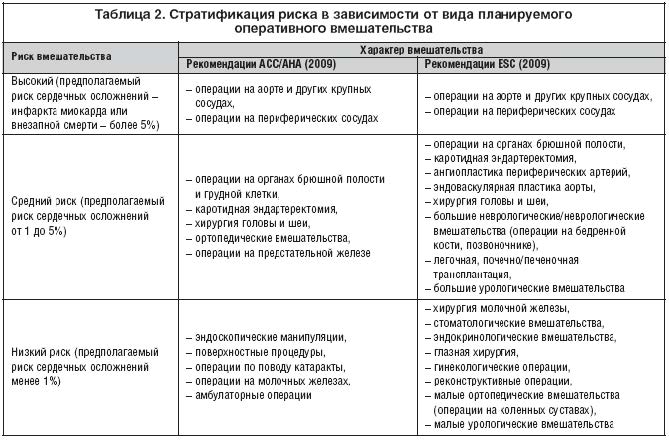
Сердечно–сосудистый риск развития наиболее высок (составляет 5% и более) при операциях на аорте и крупных сосудах (табл. 2). При операциях, сопровождающихся средним риском на вероятность возникновения сердечно– сосудистых осложнений влияют характер и особенности планируемой операции. Риск развития инфаркта миокарда и смерти от сердечных осложнений повышен при экстренных и неотложных вмешательствах. Очевидно, что снизить этот риск в предоперационном периоде невозможно, в таких случаях терапевт (кардиолог) может корректировать терапию в послеоперационном периоде. В некоторых случаях повышенный риск развития сердечных осложнений может повлиять на решение хирурга об объеме предстоящей операции, однако следует учитывать, что, по мнению Европейских экспертов, лапароскопические вмешательства оказывают на сердечно–сосудистую систему такое же влияние, как и открытые операции.
Пациенты с низким сердечно–сосудистым риском могут быть оперированы без задержки; пациентам с повышенным риском перед плановой операцией может потребоваться дополнительное обследование. Определение биомаркеров целесообразно при высоком риске развития сердечных осложнений (уровень NT–proBNP и BNP может служить независимым прогностическим фактором периоперационных и поздних сердечных осложнений у пациентов из группы высокого риска); выполнение эхокардиографии целесообразно, если планируемая операция сопряжена с высоким риском сердечно–сосудистых осложнений; нагрузочные пробы показаны перед операциями, сопряженными с высоким риском сердечных осложнений пациентам с 2–3 клиническими факторами риска, могут быть выполнены перед операциями, сопряженными со средним риском сердечных осложнений.
При выявлении высокого периоперационного риска развития сердечно–сосудистых осложнений задачей терапевта (кардиолога) становится поиск путей его снижения. Известно, что b– адреноблокаторы подавляют интраоперационный выброс катехоламинов, ответственных за нежелательное повышение артериального давления, частоты сердечных сокращений, уровня свободных жирных кислот. В ряде исследований показана способность препаратов этой группы снижать периоперационный риск развития сердечных осложнений. В одной из первых работ такого рода Poldermans и соавт. (1999) показали эффективность применения бисопролола перед плановыми операциями на крупных сосудах у пациентов с факторами риска сердечно–сосудистых осложнений (хроническая сердечная недостаточность, перенесенный инфаркт миокарда, стенокардия, сахарный диабет, возраст старше 70 лет) и индуцируемой добутамином ишемией миокарда. Из 846 пациентов с факторами риска тест с добутамином оказался положительным у 173 больных; из них 61 человек был исключен из исследования в связи с обширными зонами нарушений сократимости. Оставшиеся 112 больных были рандомизированы в группу бисопролола и группу контроля. Лечение начинали, по крайней мере, за 7 дней до операции, дозу препарата титровали до достижения ЧСС 60 в 1 минуту в предоперационном периоде. Терапию бисопрололом продолжали в течение месяца после операции. Применение бисопролола привело к снижению частоты сердечной смерти (3,4% по сравнению с 17% в группе контроля; p=0,02) и нефатального инфаркта миокарда (0% по сравнению с 17% в контрольной группе; p ≤0,001).
В последующем кардиопротективное действие b–адреноблокаторов в периоперационном периоде было подтверждено во многих исследованиях и мета–анализах. Важную роль для выработки оптимальной тактики использования препаратов этой группы сыграли результаты исследования POISE (Perioperative Ischaemic Evaluation). В это масштабное многоцентровое рандомизированное исследование был включен 8351 пациент (4174 составили группу метопролола, 4177 – группу плацебо). Первую дозу метопролола (100 мг) вводили за 2–4 часа до оперативного вмешательства, лечение продолжали в течение месяца после его проведения. Периоперационное применение метопролола приводило к снижению риска инфаркта миокарда, сердечной смерти, остановки сердца на 17%, уменьшало риск нефатального инфаркта миокарда на 30%, но увеличивало риск инсульта на 117% и повышало общую смертность на 33%. Результаты этого исследования послужили основанием для отказа от применения b– адреноблокаторов в высоких дозах без предварительной их титрации.
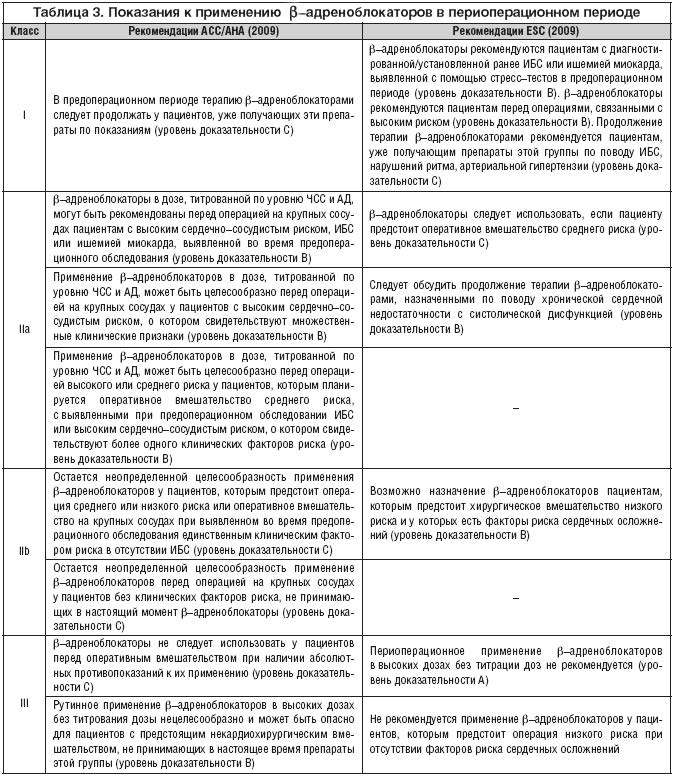
В одно из последних исследований, посвященных этой проблеме, DECREASE–IV, было включено 1066 пациентов с умеренным сердечно– сосудистым риском, которым предстояла сосудистая операция (Dunkelgrun M. И соавт., 2009). Дозу бисопролола в предоперационном периоде постепенно увеличивали, начиная с 2,5 мг в сутки, до достижения ЧСС 50–70 ударов в 1 минуту. Применение бисопролола достоверно снижало частоту периоперативных сердечной смерти и нефатального инфаркта миокарда (2,1% по сравнению с 6,0% в контрольной группе). Результаты всех проведенных исследований позволили экспертам ESC и ACC/AHA сформулировать новые рекомендации относительно применения b– адреноблокаторов в периоперационном периоде (табл. 3).
Таким образом, в соответствии с современными рекомендациями терапию b– адреноблокаторами следует начинать приблизительно за месяц (как минимум, за неделю) до запланированной операции. Дозу препаратов следует постепенно увеличивать (титровать) до достижения ЧСС 60–70 ударов в 1 минуту в покое и систолического АД выше 100 мм рт.ст. Учитывая возможность поздних осложнений, лечение b– адреноблокаторами целесообразно продолжать в течение нескольких месяцев после операции. Противопоказаниями к применению b– адреноблокаторов служат бронхиальная астма, нарушения сердечной проводимости, брадикардия, артериальная гипотензия, декомпенсированная сердечная недостаточность. Целесообразно применять длительно действующие селективные b1–адреноблокаторы без внутренней симпатомиметической активности – бисопролол в начальной дозе 2,5 мг в сутки или метопролола сукцинат в начальной дозе 50 мг в сутки. Очевидно, что можно использовать не только оригинальные препараты, которые изучались в приведенных выше исследованиях, но и сравнимые с ними по эффективности и безопасности генерические, например, появившийся недавно на фармацевтическом рынке Росии Бидоп (Гедеон Рихтер).
Литература
1. 2009 ACCF/AHA focused update on perioperative beta blockade incorporated into the ACC/AHA 2007 guidelines on perioperative cardiovascular evaluation and care for noncardiac surgery. American College of Cardiology Foundation/American Heart Association Task Force on Practice Guidelines; American Society of Echocardiography; American Society of Nuclear Cardiology; Heart Rhythm Society; Society of Cardiovascular Anesthesiologists; Society for Cardiovascular Angiography and Interventions; Society for Vascular Medicine; Society for Vascular Surgery, Fleisher LA, Beckman JA, Brown KA, Cal-kins H, Chaikof EL, Fleischmann KE, Freeman WK, Froehlich JB, Kasper EK, Kersten JR, Riegel B, Robb JF. J Am Coll Cardiol. 2009, 24; 54(22): e13–e118.
2. Guidelines for pre–operative cardiac risk assessment and perioperative cardiac management in non–cardiac surgery: the Task Force for Preoperative Cardiac Risk Assessment and Perioperative Cardiac Management in Non–cardiac Surgery of the European Society of Cardiology (ESC) and endorsed by the European Society of Anaesthesiology (ESA). Poldermans D., Bax J.J., Boersma E. et al.; Task Force for Preoperative Cardiac Risk Assessment and Peri-operative Cardiac Management in Non–cardiac Surgery of European Society of Cardiology (ESC); European Society of Anaesthesiology (ESA). Eur J Anaesthesiol. 2010; 27(2): 92–137.
3. Dunkelgrun M., Boersma E., Schouten O. et al. Bisoprolol and fluvastatin for the reduction of perioperative cardiac mortality and myocardial infarction in intermediate–risk patients undergoing noncardiovascular surgery: a randomized controlled trial (DECREASE–IV). Ann Surg, 2009; 249: 921–926.
4. Lee T.H., Marcantonio E.R., Mangione C.M. et al. Derivation and prospective validation of a simple index for prediction of cardiac risk of major noncardiac surgery Circulation 1999;100: 1043–1049.
5. POISE Study Group. Effects of extended– release metoprolol succinate in patients undergoing non–cardiac surgery (POISE trial): a randomised controlled trial. Lancet (2008) 371: 1839–47.
6. Poldermans D., Boerasma E., Bax J.J., et al. The effect of bisoprolol on perioperative mortality and myocardial infarction in high–risk patients undergoing vascular surgery. N Engl J Med 1999; 341: 1789–94









Комментировать