Когнитивные и некогнитивные психические расстройства (эмоциональные, поведенческие) при синдроме дисциркуляторной энцефалопатии. Сосудистые когнитивные нарушения. Взаимосвязь сосудистых когнитивных и эмоционально-поведенческих нарушений. Ведение пациентов с сосудистыми когнитивными и эмоционально-поведенческими нарушениями.
В.В.Захаров, Н.В.Вахнина Кафедра нервных болезней ГБОУ ВПО Первый МГМУ им. И.М.Сеченова
Минздрава РФ
Когнитивные нарушения, обычно в сочетании с расстройствами в эмоционально-поведенческой сфере, – клиническое ядро синдрома дисциркуляторной энцефалопатии (ДЭ), столь часто встречаемого в практике врача-невролога. Данные неврологические нарушения выявляются уже на начальных стадиях хронической недостаточности мозгового кровообращения, характеризуются определенными узнаваемыми клиническими особенностями и поэтому могут служить основным ориентиром клинической диагностики синдрома ДЭ [1–8]. В то же время так называемые субъективные неврологические симптомы, описываемые на первой стадии ДЭ (головная боль, головокружение, шум и тяжесть в голове и др.), носят неспецифический характер и встречаются не только при этом заболевании, но и при тревожно-депрессивных нарушениях, не связанных с органической патологией головного мозга.
Когнитивные и некогнитивные психические расстройства (эмоциональные, поведенческие) при ДЭ объединены общим патогенезом. Как известно, наиболее характерным морфологическим субстратом ДЭ являются диффузные изменения белого вещества – лейкоареоз. Механизмы формирования лейкоареоза продолжают изучаться. Обсуждается роль хронической ишемии головного мозга, повторные эпизоды транзиторной ишемии без образования кисты («незавершенные» инфаркты), эндотелиальная дисфункция с нарушением гематоэнцефалического барьера. Следствием выраженных изменений белого вещества становится нарушение связи между разными отелами коры головного мозга и подкорковыми структурами («феномен разобщения») [9–11]. В силу функциональных особенностей лобной коры передние отделы головного мозга в наибольшей степени страдают из-за разобщения церебральных структур, поэтому закономерным патофизиологическим событием ДЭ является развитие лобной дисфункции. Многочисленные нейропсихологические исследования свидетельствуют, что именно лобная дисфункция лежит в основе сосудистых когнитивных расстройств и, вероятно, сопровождающих их эмоционально-поведенческих нарушений [1–8]. Сходный патогенез обсуждается и в отношении двигательных нарушений, в первую очередь нарушений постуральной устойчивости, которая развивается при ДЭ. Так, по данным Н.Н.Яхно и соавт., в типичных случаях ДЭ наблюдается параллельное нарастание выраженности когнитивных и двигательных расстройств, что также свидетельствует об общности их патогенетических и патофизиологических механизмов [12].
Сосудистые когнитивные нарушения
Расстройства высших мозговых функций определяются уже на начальных стадиях ДЭ и являются, вероятно, наиболее ранним признаком хронической недостаточности мозгового кровообращения [4,5]. В типичных случаях клинической особенностью сосудистых когнитивных нарушений является относительная сохранность памяти на события жизни. В большей степени страдает быстрота реакции на внешние стимулы, что ведет к снижению темпа когнитивных процессов: больные выглядят несколько замедленными при выполнении интеллектуальных задач. Обычно это сопровождается трудностями концентрации внимания, повышенной утомляемостью при умственной работе, отвлекаемостью. Другим типичным когнитивным симптомом является нарушение интеллектуальной гибкости: пациенты испытывают трудности при необходимости изменить привычную парадигму мышления или деятельности. В обыденной жизни этот феномен проявляется повышенным консерватизмом, неприязнью ко всему новому, значительными затруднениями при приобретении новых навыков (например, при необходимости овладеть новой техникой, такой как мобильный телефон, компьютер и др.).
Когнитивные расстройства при ДЭ не всегда находят адекватное отражение в жалобах пациентов. Поскольку память на события повседневной жизни длительное время остается сохранной, активные жалобы на забывчивость редки. Нередким субъективным эквивалентом когнитивных расстройств являются жалобы на головную боль или неприятные ощущения в голове. При попытке уточнить характер субъективных ощущений пациенты нередко сообщают, что «голова не такая», «чугунная голова», «как будто ударили пыльным мешком» и др. По сути в этих жалобах в несколько завуалированной форме отражается неспособность «головы» быстро реагировать на информацию и решать интеллектуальные задачи. Другой типичной жалобой пациентов, которая также имеет когнитивную природу, является жалоба на повышенную утомляемость при умственной работе. Объективным методом исследования высших психических функций является нейропсихологическое тестирование. Следует, однако, иметь в виду, что на начальных стадиях ДЭ экспресс-методы диагностики деменции, такие как краткая шкала оценки психического статуса, батарея лобных тестов, тест рисования часов, малоинформативны. Для максимально ранней диагностики сосудистых когнитивных нарушений следует использовать стандартные нейропсихологические методики, чувствительные к нарушениям управляющих лобных функций.
По нашему опыту оптимальными являются следующие пробы [13]:
• тест связи цифр и букв (trail making test) – пациента просят как можно быстрее соединить по порядку цифры на тестовом листке (часть А) или соединить по порядку цифры и буквы (часть Б);
• тест «Символы и цифры» (digit symbol) – необходимо как можно быстрее подобрать пары цифр и букв в соответствии с данным образцом;
• тест «вербальные ассоциации» – пациента просят за 1 мин назвать как можно больше слов на букву С, затем как можно больше животных.
В качестве чувствительного диагностического инструмента при когнитивных нарушениях сосудистой природы в последние годы активно позиционируется монреальская когнитивная шкала (мокатест), которая содержит сокращенный вариант теста связи цифр и букв, пробы на конструктивный праксис, запоминание слов, внимание и концентрацию. Исследование по данной методике занимает 10–15 мин времени и высокоинформативно, в том числе при когнитивных нарушениях небольшой выраженности [14].
Важной практической задачей является дифференциальная диагностика когнитивных нарушений сосудистой и нейродегенеративной природы. Следует учитывать высокую распространенность нейродегенеративных заболеваний, в первую очередь болезни Альцгеймера (БА), у пожилых пациентов. БА всегда начинается незаметно и прогрессирует медленно, особенно у лиц пожилого и старческого возраста. При этом заболевании пациенты могут долгое время сохраняют социальнобытовую независимость, продолжают работать, особенно при высоком преморбидном уровне. Широко известны примеры, когда пациенты с начальными стадиями БА продолжали выполнять руководящую, научную и иную работу, требующую высокого интеллектуального напряжения. В повседневной практике до развития выраженной деменции первые симптомы БА нередко принимаются за когнитивные расстройства сосудистой природы, особенно у пациентов с сопутствующими заболеваниями сердечно-сосудистой системы (артериальная гипертензия, атеросклероз и др.). Следует отметить, что наличие указанных заболеваний ассоциировано не только с повышенным риском сосудистых, но и нейродегенеративных когнитивных расстройств, поэтому не может считаться надежным критерием разделения двух указанных распространенных форм когнитивных нарушений. В то же время установление точного нозологического диагноза (ДЭ, БА, другое нейродегенеративное заболевание) имеет большое значение для прогноза и выбора наиболее адекватной тактики ведения больных. Наиболее важные дифференциально-диагностические признаки когнитивных нарушений сосудистой и нейродегенеративной природы указаны в табл. 1 [15, 16].
Однако дифференциальный диагноз весьма затрудняется при коморбидных состояниях, которые наиболее часто встречаются у очень пожилых и старых людей, когда у одного и того же пациента имеются клинические и морфологические признаки как сосудистой, так и нейродегенеративной патологии [16].
Взаимосвязь сосудистых когнитивных и эмоционально-поведенческих нарушений
Как уже говорилось, в основе когнитивной дисфункции при ДЭ лежит в первую очередь разобщение лобной коры с другими церебральными структурами и развитие вторичной дисфункции передних отделов головного мозга. Основная роль префронтальных отделов лобных долей головного мозга состоит в управлении поведением и познавательной деятельностью индивидуума (целеполагание, планирование, контроль, корректировка). Этот процесс во многом осуществляется эмоциональными механизмами (чувство сомнения или, напротив, интуитивная предпочтительность того или иного решения). Поэтому закономерным является то, что при лобной дисфункции сосудистой этиологии одновременно развиваются как когнитивные, так и эмоциональные нарушения. По данным разных авторов, распространенность эмоциональных нарушений на начальных стадиях ДЭ может достигать 80% [3, 4, 6, 8].
Для начальных стадий ДЭ наиболее характерно снижение фона настроения разной степени выраженности: от субдепрессии до большого депрессивного расстройства. Не менее характерны эмоциональная лабильность, часто в сочетании с повышенной раздражительностью, психическая и соматизированная тревога, нарушения сна. Указанные эмоционально-поведенческие расстройства значимо влияют на характер жалоб пациентов. Так называемые субъективные неврологические нарушения (головная боль, несистемное головокружение, нарушение сна), которые предлагались в свое время в качестве индикаторных симптомов для ранних стадий хронической сосудистой мозговой недостаточности, связаны в большинстве случаев с расстройствами тревожно-депрессивного ряда. По мере утяжеления выраженности когнитивных нарушений может несколько изменяться характер эмоционально-поведенческих расстройств: как правило, уменьшается выраженность тревожнодепрессивного аффекта и, напротив, усугубляется снижение активности, мотивации и инициативы [3, 4, 6, 8].
Сосуществование когнитивных и эмоционально-поведенческих расстройств у пациентов с ДЭ делает весьма актуальным вопрос взаимосвязи между ними. Как когнитивные расстройства могут быть следствием депрессии (когнитивный синдром депрессии, псевдодеменция), так и эмоциональные, в первую очередь тревожно-депрессивные расстройства, могут быть реакций личности пациента на формирующуюся когнитивную недостаточность. Позитивные статистические корреляции между выраженностью когнитивных и эмоционально-поведенческих нарушений, отмечаемые рядом исследований, не дают ответа на вопрос о взаимосвязи между ними [6, 8]. С нашей точки зрения, взаимовлияние когнитивных и эмоционально-поведенческих нарушений у пациентов с ДЭ несомненно. Однако ведущим общим механизмом развития как когнитивных, так и других нервно-психических расстройств при хронической недостаточности мозгового кровообращения является органическое поражение головного мозга, что согласуется с представлением о так называемой сосудистой депрессии (табл. 2). По мнению ряда зарубежных авторов, об органическом характере эмоциональных нарушений следует думать при развитии первого эпизода депрессии в пожилом возрасте, преобладании в ее структуре когнитивных и соматических симптомов над эмоциональными, затяжном течении [17,18].
Эмоциональные расстройства существенно влияют на качество жизни как самих пациентов, так и их ближайших родственников. Поэтому у всех пациентов пожилого возраста с сосудистыми факторами риска следует целенаправленно выявлять изменения в эмоциональной сфере. Обоснованные подозрения на наличие расстройств в эмоциональной сфере должны появляться у пациентов с хронической головной болью, хроническим болевым синдромом иной локализации, нарушениями сна, раздражительностью или быстрой сменой настроения, повышенной слезливостью. В качестве формализованного диагностического инструмента для выявления депрессии в пожилом возрасте можно использовать гериатрическую шкалу депрессии (табл. 3) [13].
Согласно общепринятым международным рекомендациям лечение депрессии следует начинать при обоснованных подозрениях на наличие данного вида эмоциональных расстройств, даже при отсутствии полной уверенности в диагнозе (лечение ex juvantibus). При этом следует использовать антидепрессанты без холинолитического эффекта, которые не оказывают отрицательного влияния на когнитивные функции (см. ниже) [19].
Ведение пациентов с сосудистыми когнитивными и эмоционально-поведенческими нарушениями
Важнейшей задачей при ведении пациентов с когнитивными и некогнитивными психическими расстройствами сосудистой природы является достижение адекватного контроля над факторами риска церебральной ишемии: артериальной гипертензией, церебральным атеросклерозом, кардиальной патологией, гиперлипидемией, сахарным диабетом и др. При наличии соответствующих показаний необходимо проведение антигипертензивной, антитромбоцитарной, антикоагулянтной терапии, применение методов сосудистой хирургии. В отсутствие оптимального лечения базисного сосудистого заболевания вероятность прогрессирования когнитивных нарушений и наступления сосудистой деменции весьма велика. В то же время полноценное обследование пациентов и оптимальная терапия выявленных сердечно-сосудистых заболеваний является основой профилактики как сосудистой деменции, так и инсультов, которые часто развиваются у пациентов с ДЭ.
Наряду с медикаментозными методами могут существенно уменьшить риск прогрессирования сосудистых когнитивных расстройств, немедикаментозные методы профилактики. К ним относятся диета, обогащенная натуральными антиоксидантами, модификация образа жизни, тренировка памяти и внимания и рациональные физические упражнения. Так, согласно ряду популяционных исследований приверженность так называемой Средиземноморской диете уменьшает у пожилых лиц риск развития как сосудистой, так и нейродегенеративной деменции [20, 21]. Данный вид диеты предусматривает ежедневное употребление изделий из твердых сортов пшеницы, овощей и фруктов, включение в рацион не реже 1 раза в неделю рыбы или морепродуктов, регулярное употребление цитрусовых и оливкового масла.
Накоплены многочисленные данные о снижении риска возникновения или прогрессирования когнитивных расстройств на фоне умеренных физических нагрузок. Показано, что пешие прогулки или иные виды аэробных упражнений в средние годы жизни в 2 и более раз уменьшают риск развития когнитивных расстройств в пожилом возрасте, даже при наличии генетической предрасположенности к возникновению когнитивных нарушений. Предполагается, профилактический эффект физических упражнений опосредован уменьшением индекса массы тела (известно, что абдоминальное ожирение ассоциировано с увеличенным риском деменции), благоприятным воздействием на сердечно-сосудистую систему и нейрональную пластичность [22–24].
Пациентам с легкими или умеренными сосудистыми когнитивными расстройствами показаны систематические упражнения по тренировке памяти и внимания. Программы когнитивного тренинга включают повышение мотивации пациента к запоминанию и воспроизведению, обучение эффективным стратегиям запоминания, развитие способности длительно поддерживать надлежащий уровень внимания, активное включение эмоциональной поддержки (как известно, эмоционально окрашенная информация запоминается лучше) и воображения [25–27].
Большое значение в ведении пациентов имеют рекомендации по оптимизации образа жизни. Отказ от курения или, по меньшей мере, ограничение курения способствует уменьшению риска повторных острых нарушений мозгового кровообращения и уменьшению риска прогрессирования сосудистых когнитивных нарушений. Аналогичное профилактическое воздействие имеет отказ от злоупотребления алкоголем, другими психоактивными веществами.
Как уже было отмечено, профилактика прогрессирования нервно-психических расстройств представляет собой первоочередную заботу клинициста. Однако не менее важной и трудной задачей лечащего врача является лечение уже имеющихся когнитивных и некогнитивных психических расстройств с целью улучшения качества жизни пациентов и их ближайших родственников, оптимизации взаимодействия с пациентом в процессе лечения основного и сопутствующих заболеваний, осуществлении нейрореабилитации.
При наличии в клинической картине тревожно-депрессивных расстройств, что отмечается у большинства пациентов с начальными стадиями ДЭ, необходимо использование антидепрессантов. По нашему мнению, при выставлении диагноза ДЭ клиницист всегда должен рассматривать вопрос о необходимости и целесообразности назначения антидепрессантов, так как большинство пациентов с этим диагнозом действительно имеют показания к антидепрессивной терапии. На фоне данной терапии, назначенной по корректным показаниям, можно ожидать уменьшения выраженности головной боли и других неприятных ощущений в голове, регресс нарушений сна, иных «субъективных» симптомов начальных стадий ДЭ. Целесообразно использовать препараты без холинолитического эффекта из-за способности холинолитических препаратов ухудшать когнитивные способности (табл. 4). К сожалению, некоторые авторы отмечают относительную фармакорезистентность и тенденцию к затяжному течению сосудистой депрессии [17, 18].
Выбор стратегии лечения сосудистых когнитивных нарушений определяется их тяжестью. При деменции препаратами первого выбора являются ингибиторы ацетилхолинэстеразы (галантамин, ривастигмин, донепизил, ипидакрин) и/или мемантин. На этапе легких и умеренных когнитивных нарушений приоритетны препараты, улучшающие церебральную микроциркуляцию и нейрометаболические процессы.
Вазоактивные препараты (циннаризин, винпоцетин, пентоксифиллин, экстракт гинкго билобы, нимодипин, ницерголин) являются одними из наиболее часто назначаемых препаратов в неврологической практике в целом. Данные препараты способствуют расширению сосудов микроциркуляторного русла, воздействуют на форменные элементы и улучшают реологические свойства крови. Многие сосудистые препараты обладают также дополнительными метаболическими и антиоксидантными свойствами.
Широко применяется при сосудистой мозговой недостаточности нейрометаболическая терапия. Целью данной терапии является стимуляция репаративных процессов головного мозга, связанных с явлением нейрональной пластичности. Благоприятное влияние на нейрометаболические процессы оказывают ГАМКергические препараты (пирацетам, аминофенилмасляная кислота и др.), нейропептиды (церебролизин, актовегин, кортексин), предшественники нейротрансмиттеров (холина альфосцерат, цитиколин).
Патогенетически оправданным и целесообразным является сочетанное проведение вазоактивной и метаболической терапии. В связи с этим в настоящее время выпускаются стандартные препараты, содержащие рациональные комбинации вазоактивного и нейрометаболического препарата. К таким фиксированным рациональным комбинациям относится Омарон® 1 таблетка которого содержит 25 мг циннаризина и 400 мг пирацетама. Циннаризин является блокатором кальциевых каналов, который оказывает почти избирательное воздействие на церебральные артерии. На фоне использования циннаризина уменьшается тонус церебральных артерий микроциркуляторного русла, что способствует восстановлению ауторегуляции мозгового кровообращения. При этом существенного влияния на системную гемодинамику препарат не оказывает [28]. Пирацетам является производным пирролидона, которое было специально синтезировано для воздействия на когнитивные функции. Данный препарат стал родоначальником нового класса лекарственных средств – ноотропных препаратов. В настоящее время известно, что на фоне использования данного препарата отмечается усиление нейронального метаболизма, включая синтез белков и нуклеиновых кислот, что имеет большое значение для репаративных процессов головного мозга после острого повреждения (например, после инсульта или черепно-мозговой травмы). Вторично на фоне пирацетама отмечается увеличение кровенаполнения головного мозга [29–31]. Комбинация пирацетама и циннаризина является рациональной, так как дополняет терапевтические эффекты каждого из препаратов и нивелирует их побочные эффекты. Так, известно, что время достижения максимальной концентрации у циннаризина вдвое меньше, чем у пирацетама. То есть вазоактивный эффект при использовании препарата Омарон® развивается раньше, что способствует лучшей доставляемости пирацетама в пораженные отделы головного мозга. Кроме того, как известно, пирацетам обладает некоторым психоактивирующим эффектом, который не всегда желателен, в то же время циннаризин, напротив, оказывает анксиолитический эффект. Соединение седативного и психоативирующего лекарственного средства в одном препарате позволяет нивелировать возможные побочные эффекты.
Фиксированная комбинация циннаризина и пирацетама имеет богатый опыт применения при хронической цереброваскулярной недостаточности [32–37]. При этом отмечен положительный эффект в отношении как клинических проявлений заболевания, так и показателей церебральной гемодинамики. Большой практический интерес имеет дополнительный противотревожный эффект циннаризина. Как уже неоднократно указывалось, тревожно-депрессивные нарушения типичны для ДЭ и связаны с патогенезом хронического сосудистого поражения головного мозга. По мнению авторов, оценка и при необходимости коррекция эмоционального состояния является обязательной составной частью программы ведения пациентов. Сочетая в себе как сосудистое и метаболическое действие, так и дополнительное противотревожное действие, Омарон® оказывает, соответственно, и патогенетический, и необходимый симптоматический эффект и таким образом позволяет одновременно решить несколько актуальных терапевтических задач.
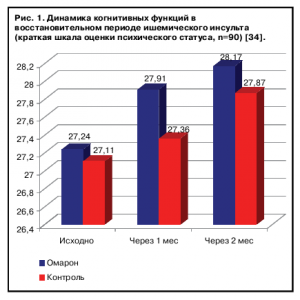
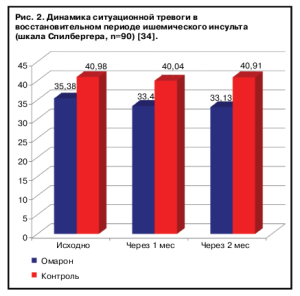
В исследовании В.А.Парфенова и соавт. эффективность препарата Омарон ® исследовалась у пациентов, перенесших ишемический инсульт и имеющих умеренные когнитивные нарушения. По данным литературы, это осложнение развивается не менее чем у 50% больных после инсульта и в подавляющем большинстве случаев связано не только и не столько с самим инсультом, но и с сопутствующим сосудистым или нейродегенеративным поражением головного мозга. 90 пациентов, наблюдавшиеся на базе 4 российских неврологических центров в течение 2 мес, были разделены на две группы: 1-я группа получала Омарон®, а 2-я – только базисную терапию сосудистого заболевания (антигипертензивные препараты, антиагреганты). Было показано, что на фоне применения препарата Омарон® наблюдалось достоверно более значительное улучшение когнитивных функций. Кроме того, в этой же группе отмечен регресс ситуационной тревоги по шкале Спилбергера, в то время как в контрольной группе этот показатель остался неизменным (рис. 1, 2) [34].
Таким образом, лечение пациентов с ДЭ должно быть направлено как на базисное сосудистое заболевание, так и на имеющуюся симптоматику, прежде всего в виде когнитивных и эмоциональноповеденческих нарушений. Наиболее перспективен многомодальный терапевтический подход, включающий как медикаментозные, так и немедикаментозные методы. Целью терапии является уменьшение выраженности имеющейся симптоматики, улучшение качества жизни пациентов, предотвращение или, по меньшей мере, отсрочка наступления сосудистой деменции.
Литература
1. Яхно Н.Н. Когнитивные расстройства в неврологической клинике. Неврол. журн. 2006; 11 (1): 4–12.
2. Яхно Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 2: когнитивные нарушения. Неврол. журн. 2001; 6 (3): 10–9.
3. Яхно Н.Н., Захаров В.В., Локшина А.Б. Синдром умеренных когнитивных нарушений при дисциркуляторной энцефалопатии. Журн. неврол. и психиатр. 2005; 105 (2): 13–7.
4. Локшина А.Б., Захаров В.В. Легкие и умеренные когнитивные расстройства при дисциркуляторной энцефалопатии. Неврол. журн. 2006; 11 (1): 57–63.
5. Преображенская И.С., Яхно Н.Н. Сосудистые когнитивные нарушения: клинические проявления, диагностика, лечение. Неврол. журн. 2007; 12 (5): 45–50.
6. Вознесенская Т.Г. Некогнитивные нервно-психические расстройства при когнитивных нарушениях в пожилом возрасте. Неврол. журн. 2010; 15 (2): 4–18.
7. Старчина Ю.А., Парфенов В.А. Память и другие когнитивные функции у пациентов с артериальной гипертензией. Клинич. геронтология. 2004; 10 (8): 33–9.
8. Парфенов В.А., Рыжак А.А., Старчина Ю.А. Когнитивные и эмоциональные нарушения у больных с артериальной гипертензией. Неврол. журн. 2006; 11 (1): 47–52.
9. Мартынов А.И., Шмырев В.И., Остроумова О.Д. и др. Особенности поражения белого вещества головного мозга у пожилых больных с артериальной гипертензией. Клинич. медицина. 2000; 6: 11–5.
10. Hershey LA, Olszewski WA. Ischemic vascular dementia. In: Handbook of Demented Illnesses. Ed. by J.Morris. New York et al. Marcel Dekker, Inc 1994; p. 335–1.
11. Pantoni L, Garsia J. Pathogenesis of leukoaraiosis. Stroke 1997; 28: 652–9.
12. Яхно Н.Н., Левин О.С., Дамулин И.В. Сопоставление клинических и МРТ-данных при дисциркуляторной энцефалопатии. Сообщение 1: двигательные нарушения. Неврол. журн. 2001; 6 (2): 10–6.
13. Захаров В.В., Вознесенская Т.Г. Нервно-психические нарушения: диагностические тесты. М.: МЕДпресс-информ, 2013. 14. www.mocatest.org 15. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция. Под ред. Н.Н.Яхно. М., 2002; с. 85.
16. Мхитарян Э.А. Преображенская И.С. Болезнь Альцгеймера и цереброваскулярные расстройства. Неврол. журн. (прил.). 2006; 1: 4–12.
17. Krishnan KR. Biological risk factors in late life depression. Biol Psych 2002; 52 (3): 185–92.
18. Alexopoulos GS, Meyers BS, Young RC и др. Vascular depression hypothesis. Arch Ger Psych. 1997;54 (10): 915–22.
19. Lovenstone S, Gauthier S. Management of dementia. London: Martin Dunitz 2001.
20. Scrameas N, Stern Y, Tang MX et al. Mediterranean diet and risk for Alzheimer’s disease. Ann Neurol 2006; 59 (6): 877–9.
21. Solfrizzi V, Colacicco AM, D’Inttrono A et al. Dietary intake of unsaturated fatty acids and agerelated cognitive decline: a 8,5 year follow-up of the Italian Longitudinal Study on Aging. Neuro-biol Aging 2006; 27 (11): 1694–704.
22. Abbott RD, White RD, Ross GW et al. Walking and dementia in physically capable elderly men. JAMA 2004; 292 (12): 1447–53.
23. Laurin D, Verreault R, Linsay J et al. Physical activity and risk of cognitive impairment and dementia in elderly persons. Arch Neurol 2001; 58 (3): 498–504.
24. Rovio S, Kareholt I, Helkala EL et al. Leisure-time physical activity at midlife and the risk of dementia and Alzheimer’s disea-se. Lancet Neurol 2005; 4 (11): 705–11.
25. Olazaran J, Muniz R, Reisberg B et al. Benefit of cognitive-motor intervention in MCI and mild-tomoderate AD. Neurology 2004; 63 (12): 2348–53.
26. Rapp S, Brenes G, Marsh AP. Memory enhancement training for older adults with mild cognitive impairment: a preliminary study. Aging Mental Health 2002; 6 (1): 5–11.
27. Smidt IW, Berg IG, Deelman BG. Memory training for remembering names: initial results in the healthy elderly. Tijdchr Geron-tol Geriatr 1997; 28 (4): 155–62.
28. Попова Н.Ф., Камчатнов П.Р., Рябухина О.В. и др. Результаты применения препарата омарон в комплексном лечении больных рассеянным склерозом. Журн. неврол. и психиатр. 2010; 11: 25–8.
29. Flicker L, Grimley EG. Piracetam for dementia or cognitive impairment. Coch Database Syst Rev 2001;2: CD001011.
30. Winblad B. Piracetam: a review of pharmacological properties and clinical uses. CNS Drug Rev 2005;11: 169–82.
31. Tariska P, Paksy A. Cognitive enhancement effect of piracetam in patients with mild cognitive impairment and dementia. Orv Hetil 2000; 141: 1189–93.
32. Фезам в комплексном лечении нарушений мозгового кровообращения. Журн. неврол. и психиатр. 2008; 108 (2): 24–6.
33. Бойко А.Н., Кабанов А.А., Еськина Т.А. и др. Эффективность фезама у пациентов с хроническими формами нарушения мозгового кровообращения. Журн. неврол. и психиатр. 2005; 1: 36–41.
34. Парфенов В.А., Беланина Г.Р., Вахнина Н.В. и др. Применение омарона у больных с умеренными постинсультными когнитивными нарушениями. Журнал. неврол. и психиатр. им. С.С.Корсакова.2009; 6: 47–51.
35. Стариков П.В., Крылова А.С., Степанова Е.Ю. Эффективность Омарона у пациентов с дисциркуляторной энцефалопатией. РМЖ Неврология, 2011; 9.
36. Строганова И.М., Кипарисов М.А. Омарон в восстановительном лечении больных с хронической цереброваскулярной недостаточностью. Журнал неврологии и психиатрии. 2010; 1.
37. Чуприна С.Е. Применение Омарона при реабилитации перенесших инсульт пациентов на амбулаторном этапе. Журнал неврологии и психиатрии. 2010; 6.







Комментировать