Хроническая железодефицитная анемия: общая характеристика. Принципы лечения. Три группы железосодержащих препаратов
Постникова С.Л., Малышева Н.В., Касатова Т.Б.
Хроническая железодефицитная анемия (ЖДА) – наиболее распространенная форма анемии, относящаяся к группе гипохромных микроцитарных анемий. Дифференциальный диагноз проводится с талассемиями, сидеробластными анемиями, анемиями, обусловленными нарушением синтеза порфиринов и анемиями при хронических заболеваниях.
Известно, что за сутки из пищи организм получает не более 2 мг железа, а суточные физиологические потери железа (независимо от пола) составляют 1 мг. Железо всасывается в тонком кишечнике, преимущественно в двенадцатиперстной и тощей кишках. Этот процесс ускоряется аскорбиновой кислотой, а замедляется – ионами кальция. В случаях недостатка железа в пище (вегетарианское питание), врожденного дефицита железа, повышенного расхода железа (пубертатный период, беременность, лактация, интенсивные физические нагрузки), при нарушенном всасывании железа (резекция тонкого кишечника, энтериты, синдром мальабсорбции) и хронической кровопотере в результате различных заболеваний, развивается ЖДА. Наиболее частой причиной развития ЖДА является хроническая физиологическая потеря железа у женщин, а также потеря крови при различных заболеваниях, преимущественно гинекологических и гастроэнтерологических (хроническая кровопотеря из желудочно– кишечного тракта).
В клинической картине присутствуют как общие признаки анемического синдрома (слабость, повышенная утомляемость, учащенное сердцебиение, одышка при обычных физических нагрузках, головокружения и др.), так и проявления железодефицита в виде извращения вкуса (желание есть мел, глину, зубную пасту, тесто, сырое мясо и т.д.), нарушения восприятия запахов (нравятся запахи бензина, ацетона, красок и др.), повышенной ломкости ногтей, сухости кожи, выпадения волос, значительного снижения умственной и физической работоспособности. Также отмечается патология желудочно–кишечного тракта (субатрофический и атрофический гастрит, колит, отсутствие аппетита, вздутие кишечника, понос, запоры), гепатобилиарной системы (формирование жирового гепатоза, дискинезии желчевыводящих путей), сердечно–сосудистой системы (анемическая миокардиодистрофия, проявляющаяся кардиалгией, нарушениями ритма и др., нейроциркуляторная дистония), центральной нервной системы (снижение памяти, способности концентрировать внимание).
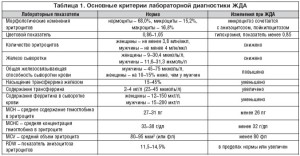
Диагноз подтверждается лабораторными результатами, свидетельствующими о низкой концентрации сывороточного железа, ферритина, повышении общей железосвязывающей способности сыворотки крови, снижении коэффициента насыщения трансферрина, увеличении содержания трансферрина в крови (табл. 1). Все исследования проводятся до назначения лечения, в частности – препаратов железа.
Сразу после верификации диагноза ЖДА необходимо установить причину развития дефицита железа и начинать терапию препаратами железа. Следует помнить, что дефицит железа в организме может быть вызван сочетанием нескольких факторов, особенно у людей пожилого и старческого возраста. Анемия может быть единственным проявлением рака желудка или кишечника.
Принципы лечения ЖДА:
- необходимая терапия основного и возможных сопутствующих заболеваний, приведших к развитию ЖДА;
- длительное назначение препаратов железа до стойкой нормализации показателей красной крови и восполнения тканевого дефицита железа (нормализация уровня ферритина);
- не прибегать к гемотрансфузиям без жизненных показаний (ими являются анемическая прекома и кома);
- парентеральная ферротерапия допустима только в случаях анэнтерального состояния и заболеваний желудочно–кишечного тракта с нарушением всасывания;
- при сохраняющихся потерях крови (мено– и метроррагии) следует проводить противорецидивное лечение препаратами железа в период менструации [1–3].
Cредством выбора для коррекции дефицита железа у больных ЖДА являются лекарственные препараты железа. В настоящее время в продаже имеется большой арсенал медикаментозных средств в различных лекарственных формах, которые различаются по содержанию в них железа, наличию дополнительных компонентов, влияющих на биодоступность железа, а также по своей стоимости.
В зависимости от активного действующего вещества выделяют 3 группы железосодержащих препаратов:
- препараты солей железа (ПСЖ);
- препараты железосодержащих комплексов (ПЖК), например, гидроксид железа в виде полимальтозного комплекса;
- комбинированные средства, содержащие комплексы, в состав которых входит железо или соли железа в сочетании с различными витаминами, аскорбиновой или фолиевой кислотой.
Из препаратов солей железа последнее всасывается в двухвалентной форме, в последующем превращается в трехвалентное, которое связывается с трансферрином и используется для построения молекулы гемоглобина. В препаратах железосодержащих комплексов железо находится в трехвалентной форме и всасывается как бы в готовом виде. В частности, в гидрооксиполимальтозном комплексе оно содержится как в физиологическом состоянии в молекуле ферритина. Существуют различия в механизмах всасывания железа из ПСЖ и ПЖК. Всасывание железа из ПСЖ происходит главным образом в виде пассивной диффузии согласно градиенту концентрации и в меньшей степени активно, в то время как абсорбция железа из ПЖК является активным процессом в виде конкурентного обмена. Это ведет к различному уровню железа в сыворотке, объему распределения, константам элиминации после абсорбции. Всасывание железа из ПЖК и нарастание его концентрации в сыворотке происходит медленно, но оно быстро поступает в запасы.
При применении ПСЖ могут возникать нарушения окислительных процессов (оксидативные повреждения) вследствие превращения ионов двухвалентного железа в трехвалентное, которое соединяется с трансферрином и включается в молекулу гемоглобина. При окислении образуются свободные радикалы, которые вызывают клеточные повреждения, такие как перекисное окисление липидов, нарушение структуры мембранных и клеточных белков, повреждение клеточной ДНК и РНК. ПЖК в отличие от ПСЖ не вызывают «оксидативного стресса», поскольку ионы железа не меняют свою валентность в процессе всасывания. Для лучшей абсорбции ПСЖ рекомендуется принимать за 1 ч до еды, т.е. натощак, что может вызывать нежелательные явления со стороны желудочно–кишечного тракта. Современные технологии производства препаратов железа позволяют производить ПСЖ с замедленным высвобождением железа в тонком кишечнике, что уменьшает токсическое воздействие ионов железа на слизистую желудка. Для лучшей переносимости ПСЖ следует принимать во время еды, хотя следует иметь в виду, что всасывание железа лучше при приеме лекарственных препаратов перед едой.
Всасывание железа может уменьшаться под влиянием содержащихся в некоторых пищевых продуктах веществ – фитинов (рис, соя), фосфатов (рыба, морепродукты), танина (чай, кофе). Многие больные склонны запивать лекарства чаем, что в случаях приема препаратов железа в виде солей недопустимо, поскольку образуются плохо растворимые комплексы с низкой их абсорбцией в кишечнике. Кроме того, всасывание железа из препаратов железа в виде солей ухудшается при одновременном приеме ряда медикаментов (тетрациклины, антациды, соли магния). С учетом этого следует рекомендовать прием препаратов солей железа в различное время с другими вышеуказанными медикаментами.
В то же время пища и медикаменты не оказывают влияния на всасывание железа из ПЖК. Однако темпы прироста показателей гемоглобина при использовании ПСЖ и ПЖК примерно одинаковые.
В большинстве случаев для коррекции дефицита железа при отсутствии специальных показаний препараты железа следует назначать внутрь. Путь их введения у больных ЖДА определяется конкретной клинической ситуацией, в частности, состоянием кишечного всасывания.
Основными показаниями для парентерального введения препаратов железа являются:
- патология кишечника с нарушением всасывания (различные энтериты, синдром недостаточности всасывания);
- резекция тонкой кишки;
- резекция желудка по Бильрот II с формированием «слепой петли».
Многие врачи обосновывают назначение препаратов железа парентерально выраженностью анемического синдрома в расчете на якобы больший и быстрый их эффект, что не обосновано и не подтверждается клинической практикой. Темпы прироста уровня гемоглобина при назначении препаратов железа внутрь и парентерально оказались приблизительно одинаковыми, в связи с чем предпочтение препаратов железа в инъекционных формах при необходимости более быстрой нормализации содержания гемоглобина (например, при подготовке к оперативному вмешательству) следует считать неоправданным. Плохая переносимость пероральных препаратов железа также не является основанием для их назначения в парентеральном виде. В этих ситуациях требуется уменьшить дозу препарата железа и/или сменить его.
Выбор препарата железа и оптимального режима его дозирования должен определяться количеством и биодоступностью содержащегося в нем железа, переносимостью, стоимостью. При этом необходимо иметь в виду, что адекватный прирост показателей гемоглобина у больных ЖДА может быть обеспечен поступлением в организм от 30 до 100 мг элементарного железа. Учитывая, что при развитии ЖДА всасывание железа увеличивается по сравнению с нормой и составляет 25– 30% (при нормальных запасах железа – всего 3– 7%), необходимо назначать от 100 до 300 мг элементарного железа в сутки. Применение более высоких доз не имеет смысла, поскольку всасывание железа при этом не увеличивается и остатки его выводятся через кишечник. Поэтому при выборе препарата железа следует ориентироваться не на содержание в нем общего количества соединения железа, а на количество элементарного железа. Например, при назначении препаратов сульфата железа с низким содержанием элементарного железа (менее 100 мг) количество принимаемых таблеток должно быть от 3 и выше (в зависимости от содержания железа в каждой таблетке), в то время как препараты сульфата, фумарата или гидроксиполимальтозного комплекса железа с содержанием 100 мг элементарного железа можно принимать в количестве 1–2 таблеток в сутки. Основные ПСЖ представлены сульфатом железа, глюконатом, хлоридом, фумаратом, глицин сульфатом.
Наибольшей степенью абсорбции обладают препараты сульфата железа, а наименьшей – глицин сульфата. Среди ПЖК на отечественном рынке имеются гидроксиполимальтозный комплекс, железо–сорбитоловый комплекс, протеин сукцинилат железа, железо–сахарозный комплекс.
При адекватной терапии на 7–10–й день от начала лечения наблюдается повышение количества ретикулоцитов. Достоверное повышение уровня гемоглобина отмечается через 3–4 нед. от начала лечения. Нормализация показателей гемоглобина обычно происходит в сроки 4–9 нед. Иногда наблюдается резкое скачкообразное повышение гемоглобина. Эти индивидуальные колебания могут быть обусловлены, с одной стороны, выраженностью ЖДА, степенью истощения запасов железа, а с другой – эффективностью назначенного лечения (количество содержащегося железа, биодоступность и др.). Имеет также значение некомплаентность больных (нерегулярность приема препаратов железа, побочные эффекты).
Оптимальная тактика ведения больных ЖДА предполагает насыщающую и поддерживающую терапию препаратами железа. Длительность насыщающей терапии зависит от темпов прироста и сроков нормализации показателей гемоглобина, составляя в среднем 4–6 недель. Поддерживающая терапия показана в тех ситуациях, когда причина дефицита железа сохраняется (меноррагии, беременность) или в силу различных ситуаций является трудноустранимой (патология кишечника, носовые и другие кровотечения при геморрагических диатезах). Женщинам, страдающим ЖДА на фоне меноррагий, после нормализации показателей гемоглобина рекомендуется поддерживающая терапия препаратами железа в течение 5–7 дней после очередной менструации. Больным надо разъяснять необходимость поддерживающего лечения в связи с продолжающимися избыточными потерями железа. Беременные с ЖДА должны получать препараты железа до конца беременности в целях обеспечения адекватной потребности плода в железе.
Среди побочных эффектов на фоне применения препаратов железа внутрь наиболее часто возникают тошнота, анорексия, металлический вкус во рту, запоры, поносы. В большинстве случаев современная ферротерапия вызывает незначительные побочные явления, не требующие отмены препарата и перехода на парентеральный путь введения. Диспептические расстройства могут уменьшаться при приеме препаратов после еды или снижении суточной дозы препарата [2–4].
К новым высокоэффективным и безопасным препаратам железа относятся комбинированные средства, содержащие в состав которых входит железо комплексы, или соли железа в сочетании с различными веществами, например, аскорбиновой кислотой, усиливающие всасывание железа и улучшающие биодоступность препарата, а также витамины (фолиевая кислота, цианокобаламин). Фолиевая кислота является кофактором витамина В12. Она участвует, как и витамин В12, в синтезе пуриновых и пиримидиновых оснований, т.е. в синтезе ДНК. Она значительно увеличивается при беременности, у детей и подростков, при гемолизе, миелопролиферативных заболеваниях, а также при приеме некоторых лекарственных препаратов (барбитураты, дифенин, триамтерен, метотрексат) и этанола. Дефицит фолиевой кислоты у беременных может привести к дефектам развития нервной системы плода. Неадекватное поступление фолиевой кислоты с пищей наблюдается у лиц пожилого и старческого возраста, но особенно характерно для больных хроническим алкоголизмом. Нарушение всасывания фолатов в кишечнике наблюдается при глютеновой болезни, анэнтеральных состояниях, а также при приеме противосудорожных препаратов (фенобарбитал, дифенин, мизодин). Все лекарственные препараты, нарушающие синтез ДНК, также могут привести к дефициту фолиевой кислоты. К ним относятся ингибиторы синтеза ДНК прямого действия (азатиоприн, 6–меркаптопурин, 5–фторурацил, цитозинарабинозид, гидроксимочевина) и антагонисты фолиевой кислоты (метотрексат).
Из препаратов двухвалентного железа высокой эффективностью обладает Ферро– Фольгамма® (фармацевтическая компания «Вёрваг Фарма», Германия). В 1 капсуле содержится сульфат железа 112,6 мг (эквивалентно 37 мг иона железа), цианокобаламин 0,010 мг, фолиевая кислота 5 мг, аскорбиновая кислота 100 мг. Учитывая вышеописанное, показаниями к приему данного препарата являются: лечение и профилактика ЖДА у беременных, при хроническом алкоголизме, при приеме противосудорожных средств, цитостатиков. Рекомендованная дозировка составляет не менее 3 капсул в сутки. В отечественной литературе существует много доказательств успешной терапии ЖДА Ферро–Фольгаммой® у беременных [5,6], в том числе и при сравнении Ферро–Фольгаммы® по 2 капсулы в сутки (100 мг элементарного железа в сутки) с препаратом полимальтозного комплекса гидроксида трехвалентного железа по 2 таблетки в сутки (200 мг элементарного железа в сутки). Под наблюдением были 35 беременных с анемией легкой степени тяжести. Срок начала лечения – от 20 до 34 недель беременности. Продолжительность приема препарата составляла в среднем 59±13 дней. Уровни гематологических показателей до и после лечения у беременных обеих групп достоверно не различались. Не было отмечено побочных эффектов в обеих группах. Таким образом, доказана сравнительная эффективность и безопасность применения Ферро–Фольгаммы® у беременных [6].
Таким образом, ЖДА характеризуются неспецифическими клиническими проявлениями и лабораторными признаками. Тактика лечения ЖДА предусматривает выбор пути введения препаратов с учетом клинической ситуации, с достаточным содержанием в них железа и дополнительных веществ, оценку их эффективности и переносимости, длительность насыщающей и обоснованность поддерживающей терапии. В настоящее время существует большой выбор разнообразных эффективных и безопасных препаратов для коррекции железодефицита. Препарат Ферро–Фольгамма® позволяет эффективно корригировать анемический синдром и, таким образом, обеспечивать оптимальную терапию и уровень жизни данной категории пациентов.
Литература
- Демидова А.В. Анемии. М.: МЕД–пресс информ, 2006, 63с.
- Дворецкий Л.И. Железодефицитные анемии. М., 1998, 37с.
- A.F. Goddard, MW James, A s Mclntyre and BB Scott on behalf of the British Society of Gastroenterology. Guidelines for the management of iron deficiency anaemia. 2005–2010.
- S. Killip, J M Bennett, M D Chambers. Iron deficiency anemia. Am Fam Physician 2007 Mar 1; 75(5): 671–678.
- Касабулатов Н.М. Железодефицитная анемия беременных. РМЖ. 2003,
- Коноводова Е.Н., Бурлев В.А. Сравнительная эффективность лечения манифестного дефицита железа у беременных различными препаратами железа. РМЖ. 2003, № 16, 899–901.












Комментировать