Изучение фенотипических форм хронической обструктивной болезни легких, критерии ранней диагностики, профилактики и лечения. Факторы риска. Изучение вопроса. Рентгенологические и функциональные фенотипы хронической обструктивной болезни легких. Патогистологические фенотипы хронической обструктивной болезни легких.
М. А. Карнаушкина, А. Г. Малявин, Московский государственный медико-стоматологический университет им. А. И. Евдокимова, Д. Ю. Овсянников, Российский университет дружбы народов, г. Москва, Е. В. Бойцова, Санкт-Петербургский государственный медицинский университет им. академика И. П. Павлова
Начиная с 2010 г. одним из ведущих направлений в развитии пульмонологии стали изучение фенотипических форм хронической обструктивной болезни легких (ХОБЛ), выработка критериев ее ранней диагностики, профилактики и лечения [6, 20].
Хорошо известно, что ХОБЛ имеет множество факторов риска и большое разнообразие клинических форм, которые позволяют с высокой вероятностью выделять различные ее фенотипы. В федеральной программе «Хронические обструктивные болезни легких. 1998 год», подготовленной по инициативе Всероссийского научного общества пульмонологов (Айсанов З. Р., Кокосов А. Н., Овчаренко С. И., Хмелькова Н. Г., Цой А. Н., Чучалин А. Г., Шмелев Е. И.), указывается, что, возможно, ХОБЛ — собирательное понятие, которое объединяет группу хронических болезней дыхательной системы: хронический обструктивный бронхит, эмфизему легких, бронхиальную астму тяжелого течения. В США и Великобритании в понятие ХОБЛ включают также муковисцидоз, облитерирующий бронхиолит (ОБ) и бронхоэктатическую болезнь. Признак, по которому формируется группа ХОБЛ, — медленно прогрессирующая необратимая бронхиальная обструкция с нарастающими явлениями хронической дыхательной недостаточности [30].
Наиболее изученным фактором риска развития ХОБЛ является курение табака. Однако проведенными эпидемиологическими исследованиями установлено, что от 20% до 30% больных ХОБЛ никогда не курили и не испытывали воздействия вредных производственных факторов [6, 20]. Более того, это были лица молодого и среднего возраста. Следовательно, помимо курения существуют другие факторы риска развития ХОБЛ. Знание этих факторов имеет важное значение для проведения лечения и разработки мер профилактики ХОБЛ у данной категории пациентов. В «Глобальной инициативе по хронической обструктивной болезни легких» (Global Initiative for Chronic Obstructive Lung Disease, GOLD) пересмотра 2011 г. к факторам риска отнесены: генетические факторы, вдыхание вредоносных частиц (табачный дым, производственная и домашняя пыль), загрязнение окружающей среды, особенности роста и развития легких, оксидативный стресс, пол, возраст, респираторные инфекции, питание, коморбидные состояния [3, 20].
В своем обзоре нам хотелось бы привлечь внимание к факторам риска развития ХОБЛ, которые встречаются преимущественно в детском возрасте и, возможно, приводят к развитию ХОБЛ у молодых взрослых [4–6, 20].
В первую очередь, это особенности роста и развития легких. Данный процесс зависит от многих факторов, воздействующих во время беременности, родов и в первые годы жизни ребенка. По данным последних исследований, дети с бронхолегочной дисплазией (БЛД) и ОБ с большой вероятностью могут пополнить группу больных ХОБЛ во взрослом возрасте. Немаловажную роль в развитии ХОБЛ у детей играют и тяжелые респираторные инфекции, среди которых на первом месте стоят корь, коклюш, риносинцитиальный вирус [2–5]. Большое значение уделяется также воздействию оксидативного стресса на детскую бронхолегочную систему. Агрессивные экологические факторы, вызывающие оксидативный стресс, могут привести к снижению ОФВ1. Кроме экологических факторов, такие последствия у детей может иметь длительное проведение кислородотерапии, неинвазивной вентиляции легких [2–4, 12, 15].
Таким образом, если предположение о существовании разных фенотипов ХОБЛ верно, то подходы к их профилактике и лечению также должны различаться.
История вопроса
Различия в клинической, а также в патоморфологической картине ХОБЛ были замечены еще 40–50 лет назад. В 1966 г. больные ХОБЛ в соответствии с клинической картиной были разделены Burrows и соавт. на два типа: тип А («розовые пыхтельщики») и тип В («синие отечники») [35]. Это было сделано для того, чтобы различать пациентов с преобладанием в клинике эмфиземы или хронического бронхита.
Практическим врачам хорошо известно, что пациенты типа А и типа В имеют различную клиническую картину заболевания и им должны назначаться разные схемы лечения [35]. Затем с целью оптимизации методов лечения и профилактики заболевания была введена классификация ХОБЛ по степени тяжести, определявшейся степенью ограничения скорости воздушного потока [1, 6]. Однако эта классификация не учитывала текущую выраженность симптомов, меру ухудшения спирометрических показателей, риск обострений, наличие сопутствующих заболеваний и, следовательно, не позволяла управлять терапией и разработать оптимальные схемы профилактики ХОБЛ [1, 6].
В GOLD (2011) большое внимание было уделено вопросу новой классификации по интегральной оценке течения ХОБЛ у конкретного пациента [6]. Данная классификация позволяет учитывать риск и частоту развития обострений, тяжесть прогрессирования ХОБЛ, влияние сопутствующих заболеваний на ее течение, раннее назначение профилактических мероприятий и адекватного лечения.
Как мы видим, ХОБЛ является гетерогенным заболеванием с различными фенотипами. Эти фенотипы, безусловно, зависят от генетической предрасположенности человека, однако на их формирование могут оказывать влияние и другие факторы, такие как формирование легочных структур, перенесенные бронхолегочные заболевания в детском возрасте. Сохраняется неопределенность в отношении возможности и необходимости проведения лечебных и профилактических мероприятий у детей, имеющих в анамнезе БЛД или ОБ. Этот вопрос требует дальнейшего изучения. Появление последней классификации говорит о том, что в настоящее время ХОБЛ не рассматривается как однородное заболевание, ученые ищут индивидуальные подходы к ее лечению и профилактике.
Рентгенологические и функциональные фенотипы хронической обструктивной болезни легких
Разработаны клинические, функциональные и рентгенологические методы, которые демонстрируют результаты, достоверно коррелирующие с данными патоморфологических исследований, и позволяют поставить диагноз той или иной клинической формы ХОБЛ. Так, степень паренхиматозной деструкции, выявляемой при патоморфологических исследованиях, коррелирует с рентгенологической картиной эмфиземы, изменениями, обнаруживаемыми при проведении бодиплетизмографии и при определении диффузионной способности легких. Однако не отмечено корреляции между степенью паренхиматозной деструкции и признаками легочного воспаления, что говорит о неоднородности форм ХОБЛ с патоморфологической точки зрения [38].
- J. Kim, Saetta и соавт. показали, что несмотря на то, что у пациентов с ХОБЛ выявляются два вида эмфиземы легких (панлобулярная и центрилобулярная), первый вид эмфиземы преобладает у больных типа А, второй — типа В. Это коррелирует с изменениями, выявляемыми при проведении бодиплетизмографии и исследовании диффузионной способности легких [35], что подтверждено в ходе современных исследований при выполнении компьютерной томографии в режиме высокого разрешения (КТВР) с проведением функциональных проб [26, 31].
В этих исследованиях установлено, что у пациентов, страдающих ХОБЛ, степень выраженности признаков эмфиземы (увеличение объема легких, разрушение легочной паренхимы и наличие «воздушных ловушек») коррелирует с повышением остаточного объема легких (ООЛ) и снижением диффузионной способности легких.
КТВР позволила оценить также выраженность воспалительных изменений в бронхах. Показателем воспалительного процесса является утолщение стенок бронхов — «перибронхиальные муфты». В группе пациентов с наличием перибронхиальных изменений значимо чаще отмечалось снижение ОФВ1 и выявлялись признаки воспалительных изменений в бронхах (кашель, выделение мокроты). С этим согласуются данные исследований O`Donnell и соавт., показавших, что количество нейтрофилов в индуцированной мокроте достоверно коррелирует со степенью обструкции дыхательных путей. Однако выраженность воспалительных изменений в бронхах не коррелирует со степенью тяжести эмфиземы [6, 26]. Исследования показали, что у больных ХОБЛ с преобладающей эмфиземой нарушение легочной вентиляции связано с деструкцией легочной ткани. Тогда как у больных ХОБЛ с преобладающей хронической обструкцией дыхательных путей нарушение легочной вентиляции связано с воспалительными изменениями в бронхах и бронхиолах и их склерозированием [21, 27].
Все вышеприведенные исследования свидетельствуют о разнородности форм ХОБЛ.
Патогистологические фенотипы хронической обструктивной болезни легких
Данные последних патогистологических исследований [18] также подтверждают гипотезу о неоднородности ХОБЛ. Они показывают, что ХОБЛ — это более чем сочетание обструкции вследствие хронического воспаления в бронхах и бронхиолах и центрилобулярной эмфиземы легких [18].
При патогистологических исследованиях выявлены три варианта ХОБЛ [18].
- Бронхоинтерстициальный вариант чаще всего встречается у пациентов, которые имели частые обострения в течение года с наличием большого количества гнойной мокроты. Патогистологические изменения в респираторной ткани можно трактовать как диффузное паренхиматозное заболевание.
- Эмфизематозный вариант характеризуется наличием картины эмфиземы легких без явлений бронхиолита.Обострения редки, в клинической картине преобладает прогрессирующая одышка с развитием легочного сердца.
- Истинно обструктивный вариант отличается поражением как крупных бронхов, так и бронхиол с развитием констриктивного или облитерирующего бронхиолита и центрилобулярной эмфиземы. Клинически проявляется выраженным обструктивным синдромом и прогрессирующей дыхательной недостаточностью. Таким образом, данные патогистологических исследований у пациентов с ХОБЛ позволяют предположить различия в этиологии и патогенезе вариантов данного заболевания. Исходя из этого, можно говорить о наличии различных его фенотипов.
Фенотипы хронической обструктивной болезни легких. Три или больше?
В настоящий момент нет четких критериев для выделения отдельных фенотипов ХОБЛ. Так, M. H. Cho и соавт. (2010) разделили пациентов, страдающих ХОБЛ, на четыре группы: 1 — с преобладанием эмфиземы, 2 — быстро реагирующие на пробу с бронходилататором и с высоким ОФВ1, 3 — дискордантные с низким ОФВ1, несмотря на слабо выраженную эмфизему и незначительное утолщение бронхиальной стенки, и 4 — с преимущественным поражением бронхов [36].
В некоторых национальных рекомендациях по ХОБЛ предлагается выделять три основных клинических фенотипа ХОБЛ: «в сочетании с бронхиальной астмой», «с частыми обострениями» и «эмфизема — гиперинфляция», — а хронический бронхит рассматривать как модифицирующий фактор этих фенотипов [1].
Возможно, именно воздействие различных этиологических факторов приводит к развитию разных форм ХОБЛ. По данным многочисленных эпидемиологических исследований [6, 11, 20, 34, 35], ХОБЛ возможна как у курящих, так и у некурящих людей. В GOLD (2011) отмечено, что любой фактор, оказывающий неблагоприятное влияние на рост легких во время внутриутробного развития и в детском возрасте, может увеличить индивидуальный риск формирования ХОБЛ [5, 6, 20]. К заболеваниям бронхолегочной системы, которые встречаются преимущественно в детском возрасте и могут привести к развитию ХОБЛ у молодых взрослых, относятся в первую очередь ОБ и БЛД [5].
Возможная роль облитерирующего бронхиолита и бронхолегочной дисплазии в патогенезе хронической обструктивной болезни легких у молодых взрослых
ОБ — это хроническое воспалительное заболевание мелких бронхов и бронхиол, которое характеризуется полной или частичной окклюзией дистальных дыхательных путей фиброзной тканью и клинически проявляется необратимой обструкцией (Е. В. Бойцова) [2–5, 9].
Сравним данное определение с определением ХОБЛ, данным в GOLD (2011): «ХОБЛ — заболевание, характеризующееся персистирующим ограничением скорости воздушного потока, которое быстро прогрессирует и связано с повышенным хроническим воспалительным ответом легких на действие патогенных частиц или газов.
Хроническое ограничение скорости воздушного потока вызывается как поражением мелких бронхов (обструктивный бронхиолит), так и деструкцией паренхимы (эмфизема)» [2, 19]. Данные определения очень сходны: в них подчеркивается, что оба заболевания проявляются хроническими обструктивными и рестриктивными нарушениями, вызванными повреждением мелких дыхательных путей и деструкцией легочной ткани.
Как и при ХОБЛ, в патоморфологических исследованиях при бронхиолитах выявляют ремоделирование легочной ткани и явления бронхиальной обструкции. Эти изменения обнаруживают преимущественно в терминальных и респираторных бронхиолах. Молекулярные нарушения при поражении малых дыхательных путей при бронхиолитах в целом повторяют реакции, наблюдаемые при ХОБЛ. Большинство авторов считают, что бронхиолит является неспецифической универсальной воспалительной реакцией с формированием фиброза на уровне бронхиол, развивающейся в ответ на различные стимулы. Данными стимулами могут являться курение, вирусные инфекции, аспирации и/или ингаляции различных веществ (аспирация мекония, желудочного содержимого, термические или химические ожоги дыхательных путей), системные заболевания соединительной ткани, иммунная реакция после трансплантации органов [2, 3, 11, 12, 21, 29].
По данным одного из крупных исследований, проведенного G. B. Fischer и соавт., установлено, что респираторные инфекции в раннем детском возрасте предрасполагают к развитию ХОБЛ. Выявлено, что факторы, приводящие к повреждению бронхолегочной системы у детей, оказывают такое же влияние на функцию легких, как и курение во взрослом возрасте [20, 22, 30, 37]. В исследованиях, выполненных в СПбГМУ им. акад. И. П. Павлова, и в ряде зарубежных исследований выявлена роль вирусно-бактериальных патогенов, прежде всего адено- и респираторных синцитиальных вирусов,Streptococcus pneumoniae и Haemophilus influenzae, в формировании и поддержании хронического воспалительного процесса при ОБ у подростков и молодых взрослых [2, 3, 10, 13, 14, 24, 25]. Следовательно, профилактика развития ХОБЛ у данной категории пациентов — это основа совершенствования методов профилактики и лечения ХОБЛ у молодых взрослых.
Опубликованные в нашей стране [2, 3] результаты длительного (до 19 лет) наблюдения детей с ОБ свидетельствуют, что с возрастом происходит урежение обострений, выраженность физикальных изменений в легких уменьшается, в то же время рентгенологические и функциональные изменения остаются стабильными.
Прогноз болезни у взрослых не известен. По мнению многих исследователей, ОБ прогрессирует, постепенно трансформируясь в ХОБЛ у взрослых [1, 22, 37]. Однако этот вопрос требует дальнейшего изучения. Другим заболеванием, при наличии которого в анамнезе молодые люди могут пополнить ряды пациентов с ХОБЛ, является БЛД (как старая, так и новая форма) [4, 5, 13, 16]. БЛД — это полиэтиологическое хроническое заболевание морфологически незрелых легких, развивающееся у новорожденных, главным образом глубоко недоношенных детей, в результате интенсивной терапии респираторного дистресс-синдрома и/или пневмонии.
БЛД протекает преимущественно с поражением бронхиол и паренхимы легких, развитием эмфиземы, фиброза и/или нарушением репликации альвеол, проявляется кислородозависимостью в течение первых 28 дней жизни, бронхообструктивным синдромом и синдромом дыхательной недостаточности и характеризуется специфическими рентгенологическими изменениями в первые месяцы жизни и регрессом клинических проявлений по мере роста ребенка [4, 5, 19]. Согласно данным научно-практической программы «Бронхолегочная дисплазия у детей», БЛД является наиболее распространенным хроническим заболеванием у детей грудного и раннего возраста. По мере улучшения выхаживания глубоко недоношенных детей она встречается все чаще [5].
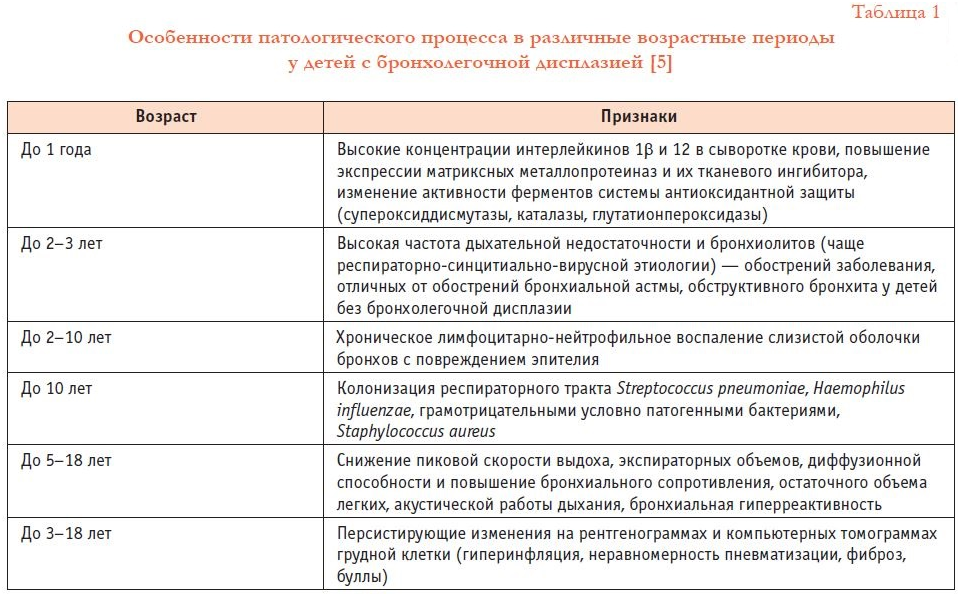
По результатам последних исследований, проведенных у детей, подростков и молодых взрослых, имеющих в анамнезе БЛД, выявлены длительно сохраняющееся нарушение функции внешнего дыхания и структурные изменения в легочной ткани [5, 11, 12, 17]. Данные этих исследований приведены в таблице 1 [5].
По данным многочисленных исследований, в раннем периоде развития БЛД выявляется выраженное нарушение вентиляционной способности легких. Однако в дальнейшем может происходить «перерастание» болезни. Последствия БЛД для респираторной системы взрослых недостаточно изучены. Можно предположить, что лежащий в основе заболевания обструктивный синдром обусловлен стойкими морфологическими изменениями в стенке дыхательных путей, нарушением архитектоники легочной ткани и функциональными нарушениями, связанными с гиперреактивностью дыхательных путей. Это придает БЛД большое сходство с ХОБЛ [5, 7, 19]. В последнее время были предприняты попытки оценить последствия БЛД у подростков и молодых взрослых [3, 7, 8, 10, 23, 32, 39].
- M. Wrong и соавт. наблюдали группу взрослых с БЛД в анамнезе, из которых у 10% имелись респираторные проблемы [39]. В наблюдениях Howling и соавт. у троих из пятерых взрослых с БЛД в анамнезе также имелись респираторные проблемы. Исследования, проведенные Northway, подтверждают эти данные: из 26 пациентов с БЛД в анамнезе 23% имели проблемы с легкими. В ходе этих и других исследований нарушения ОФВ1 были выявлены приблизительно у 67–80% пациентов. В 24% случаев обструкция была необратимой. Обнаруживались также снижение объемной скорости выдоха у 25–75%, у 28% выявлялось повышение ООЛ; причем эти показатели не имели тенденции к нормализации с возрастом. Авторами была высказана мысль, что, наоборот, с достижением зрелого возраста у таких пациентов могут развиваться быстро прогрессирующие респираторные заболевания [3, 7, 10, 39].
Изучение влияния состояния недоношенности без признаков БЛД на изменения показателей функции внешнего дыхания у пациентов разного возраста привело к противоречивым результатам. Но по данным большинства исследований, значения ОФВ1 у подростков и молодых взрослых, родившихся недоношенными, находятся на нижней границе нормы. При проведении бодиплетизмографии не выявляется достоверного увеличения остаточной емкости легких [17, 33, 39], в некоторых исследованиях отмечено незначительное повышение ООЛ [28, 40]. Исследование диффузионной способности легких проведено лишь в небольшом числе случаев.
В работах Howling, Vrijlant и соавт. снижение этого показателя не выявлено ни у пациентов с БЛД в анамнезе, ни у недоношенных. В исследованиях P. M. Wong и соавт. получены другие результаты: так, у 84% молодых взрослых с БЛД в анамнезе отмечено снижение диффузионной способности легких [39]. КТВР органов грудной клетки, являющаяся одним из стандартов диагностики ХОБЛ и эмфиземы, проводилась у пациентов с БЛД в анамнезе в ограниченном количестве случаев. В отечественных исследованиях были выявлены повышение воздушности легочной ткани, «воздушные ловушки» (83%), буллы (54%), линейные участки фибро- за и перибронхиальные изменения (63%) у пациентов от 5 до 9 лет [26, 31]. По данным Havling, Aquino, P. M. Wrong и соавт., при проведении КТВР у пациентов 20–26 лет с БДЛ в анамнезе обнаруживаются мозаичность легочного рисунка, «воздушные ловушки», буллы, утолщение стенок бронхов, уменьшение отношения диаметров мелких бронхов и сосудов, линейный фиброз. В частоте встречаемости тех или иных структурных изменений отмечены значительные колебания [3, 11, 27, 31].
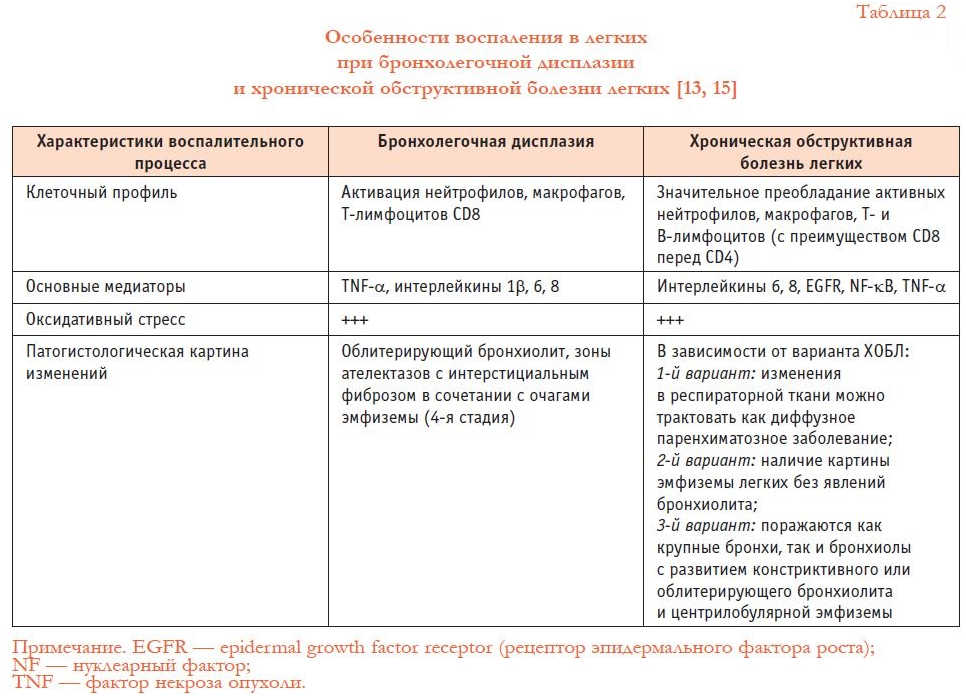
По результатам патогистологических исследований, БЛД является хроническим воспалительным процессом в легких [3, 4, 9, 11, 12, 20]. Это подтверждается наличием в бронхоальвеолярном лаваже у детей с БЛД повышенного содержания нейтрофилов, активированных макрофагов; повышенной активностью эластазы и таких медиаторов воспаления, как лейкотриены, фактор активации тромбоцитов; повышением содержания цитокинов. Морфологической основой БЛД является развитие интерстициального фиброза на фоне незрелых анатомических структур легких. Сравнение особенностей воспаления в легких при БЛД и ХОБЛ приведено в таблице 2 (в таблице использованы данные из работ Д. Ю. Овсянникова) [1, 8, 13, 15, 23, 25, 32, 38]. Из представленного материала видно выраженное сходство воспалительного процесса в легких при этих заболеваниях.
Основываясь на результатах приведенных выше исследований, некоторые авторы высказывают мнение, что БЛД — вариант ХОБЛ [5, 19]. В научно-практической программе 2012 года «Бронхолегочная дисплазия у детей» отмечено, что cведений о частоте различных исходов БЛД, сформированных на ее фоне рецидивирующих и хронических заболеваний легких в настоящее время недостаточно. «Безусловно, дети с бронхолегочной дисплазией в анамнезе, став взрослыми, могут стать группой с потенциальным риском развития хронической обструктивной болезни легких, однако необходимы масштабные исследования для подтверждения такой возможности» [5].
Заключение
Таким образом, многочисленные исследования последних лет доказывают, что хроническая обструктивная болезнь легких (ХОБЛ) является гетерогенным заболеванием, имеющим три фенотипа или более.
Возможно, стойкие нарушения бронхолегочной системы, выявленные в проведенных исследованиях у пациентов с бронхолегочной дисплазией или облитерирующим бронхиолитом в анамнезе, являются маркерами высокого риска развития ХОБЛ и/или могут рассматриваться как отдельный фенотип ХОБЛ (при сохранении воспалительного процесса в бронхолегочной системе и прогрессировании деструкции паренхимы легких). Данная гипотеза требует проведения дальнейших масштабных исследований.
Литература
- Авдеев С. Н. Фенотипирование пациентов с ХОБЛ: ключ к успешной терапии // Эффективная фармакотерапия. 2013. № 10. URL: http://medi.ru/doc/a799712.htm (дата обращения — 01.03.2014).
- Бойцова Е. В. Облитерирующий бронхиолит у детей // Дет. медицина Северо-Запада. 2011. Т. 2. № 1. С. 21–25.
- Бойцова Е. В., Богданова А. В., Овсянников Д. Ю. Последствия бронхолегочной дисплазии для респираторного здоровья детей, подростков и молодых взрослых / Вопр. диагностики впедиатрии. 2013. Т. 5. № 1. С. 5–11.
- Бронхолегочная дисплазия у детей: Научно-практическая программа // Российское респираторное общество, Российская ассоциация специалистов перинатальной медицины, Федерация педиатров стран СНГ, Педиатрическое респираторное общество. М., 2012. С. 72–74.
- Бронхолегочная дисплазия у детей: Научно-практическая программа // Педиатрия им. Г. Н. Сперанского. 2013. Т. 92. № 4. Прил. 1. С. S1–15.
- Глобальная стратегия диагностики, лечения и профилактики хронической обструктивной болезни легких (пересмотр 2011 г.) / Пер. с англ. Под ред. А. С. Белевского. М.: Российскоереспираторное общество, 2012. 78 с.
- Давыдова И. В. Формирование, течение и исходы бронхолегочной дисплазии у детей: Автореф. дис. … докт. мед. наук. М., 2010. 47 с.
- Давыдова И. В., Яцык Г. В., Бершова Т. В., Басаргина М. А. и др. Матриксные металлопротеиназы как биомаркеры формирования бронхолегочной дисплазии у детей // Пульмонология. 2009. № 4. С. 80–84.
- Классификация клинических форм бронхолегочных заболеваний у детей. М.: Российское респираторное общество, 2009. 18 с.
- Ковалева Л., Гембицкая Т., Суркова Е. Облитерирующий бронхиолит в подростковом и молодом возрасте: некоторые аспекты инфекционного воспаления // Врач. 2012. № 1. С. 7–10.
- Козарезов С. Н. Клинико-патогенетические аспекты бронхолегочной дисплазии в стадии хронической болезни: Автореф.дис. … канд. мед. наук. Минск, 2010. 20 с.
- Козарезов С. Н., Войтович Т. Н. Бронхолегочная дисплазия в стадии хронической болезни: Учеб.-метод. пособие. Минск: изд-во БГМУ, 2009. 32 с.
- Овсянников Д. Ю. Бронхолегочная дисплазия у детей первых трех лет жизни: Автореф. дис. … докт. мед. наук. М., 2010. 52 с.
- Овсянников Д. Ю. Система оказания медицинской помощи детям, страдающим бронхолегочной дисплазией: Руководство для практикующих врачей / Под ред. Л. Г. Кузьменко. М.: изд-во МДВ, 2010. С. 14–27.
- Овсянников Д. Ю., Гитинов Ш. А., Пушко Л. В., Горбунов А. В. и др. Посткоревой облитерирующий бронхиолит у ребенка 1 года 1 месяца // Трудный пациент. 2013. № 2–3. С. 14–16.
- Самсонова М. И., Чойдонова О. Г., Николаева Л. Е. Результаты бактериологических исследований при хронических неспецифических заболеваниях легких у детей в РС // Сб. трудов XIX национального конгресса по болезням органов дыхания / Под ред. А. Г. Чучалина. М.: ДизайнПресс, 2009. С. 105.
- Старостина Л. С. Функция внешнего дыхания у детей раннего возраста с различными заболеваниями бронхолегочной системы: Автореф. дис. … канд. мед. наук. М., 2009. 21 с.
- Черняев А. Л., Самсонова М. В. Патологическая анатомия хронической обструктивной болезни легких // В кн.: Хроническая обструктивная болезнь легких (серия монографий Российскогореспираторного общества) / Под ред. А Г. Чучалина. М.: Атмосфера, 2008. С. 182–198.
- Шабалов Н. П. Неонатология: Учеб. пособие. В 2 тт. Т. 1. М.: МЕДпресс-информ, 2009. С. 669–684.
- Шмелев Е. В. Факторы риска хронической обструктивной болезни легких // В кн.: Хроническая обструктивная болезнь легких (серия монографий Российского респираторного общества) / Под ред. А. Г. Чучалина. М.: Атмосфера, 2008. С. 41–48.
- Baraldi E., Filippone M. Chronic lung disease after premature birth // N. Engl. J. Med. 2007. 357. N 19. P. 1946–1955.
- Fischer G. B., Sarria E. E., Mattiello R., Mocelin H. T. et al. Post infectious bronchiolitis obliterans in children // Paediatr. Rev. 2010. Vol. 11. N 4. P. 233–239.
- Głowacka E., Lis G. Bronchopulmonary dysplasia — early and long-term pulmonary sequelae // Pneumonol. Pol. 2008. Vol. 76. N 6. P. 437–445.
- Hayes D. Jr., Meadows J. T. Jr.
- , Murphy B. S., Feola D. J. et al. Pulmonary function outcomes in bronchopulmonary dysplasia through childhood and into adulthood: implications for primary care // Prim. Care Respir. J. 2011. Vol. 20. N 2. P. 128–133. 25. Hurst J. R. Bronchial and systemic inflammation in chronic obstructive pulmonary disease // Hot topics in respiratory medicine COPD: a complex disease. 2012. Vol. 5. N 15. P. 17–21.
- Kim W. J., Oh Y. M., Sung J., Lee Y. K. et al. CT scanning-based phenotypes vary with ADRB2 polymorphisms in chronic obstructive pulmonary disease // Respir. 2009. Vol. 103. N 1. P. 98–103.
- Lee Y. K., Oh Y. M., Lee J. H., Kim E. K. et al.; KOLD Study Group. Quantitative assessment of emphysema, air trapping, and airway thickening on computed tomography // Lung. 2008. 186. N 3. P. 157–165.
- Liu J. L., Chen Z. M. Neutrophil activation and protease imbalance in respiratory tract of infants with respiratory syncytial virus bronchiolitis // Zhonghua Yi Xue Za Zhi. 2009. 89. N 6. P. 397–399.
- Mallol J., Aguirre V., Espinosa V. Increased oxidative stress in children with post infectious bronchiolitis obliterans // Allergol. (Madr.). 2011. Vol. 39. N 5. P. 253–258.
- Montes de Oca M. Impact of chronic bronchitis on chronic obstructive pulmonary disease // Hot topics in respiratory medicine COPD: a complex disease. Vol. 5. N 15. P. 12–16.
- Ogawa E., Nakano Y., Ohara T., Muro S. et al. Body mass index in male patients with COPD: correlation with low attenuation areas on CT // Thorax. Vol. 64. N 1. P. 20–25.
- Paoletti M., Camiciottoli G., Meoni E., Bigazzi F. et al. Explorative data analysis techniques and unsupervised clustering methods to support clinical assessment of Chronic Obstructive Pulmonary Disease (COPD) phenotypes // J. Biomed. 2009. Vol. 42. N 6. P. 1013–1021.
- Patel B. D., Coxson H. O., Pillai S. G., Agustí A. G. et al.; International COPD Genetics Network. Airway wall thickening and emphysema show independent familial aggregation in chronic obstructive pulmonary disease // Am. J. Respir. Care Med. 2008. Vol. 178. N 5. P. 500–505.
- Pistolesi M., Camiciottoli G., Paoletti M., Marmai C. et al. Identification of a predominant COPD phenotype in clinical practice // Respir. 2008. Vol. 102. N 3. P. 367–376.
- Pistolesi М., Bigazzi F., Cestelli L., Paoletti М. et al. Phenotypes of chronic obstructive pulmonary disease // Hot topics in respiratory medicine COPD: a complex disease. 2012. Vol. 5. N 15. P. 7–11.
- Roy K., Smith J., Kolsum U., Borrill Z. et al. COPD phenotype description using principal components analysis // Respir. 2009. 10: 41. DOI: 10.1186/1465-9921-10-41.
- Soulsby N., Greville H., Coulthard K., Doecke C. Renal dysfunction in cystic fibrosis: is there cause for concern? // Pediatr. 2009. Vol. 44. N 10. P. 947–953.
- Weatherall M., Travers J., Shirtcliffe P. M., Marsh S. E. et al. Distinct clinical phenotypes of airways disease defined by cluster analysis // Eur. J. 2009. Vol. 34. N 4. P. 812–818.
- Wong P. M., Lees A. N., Louw J., Lee F. Y. et al. Emphysema in young adult survivors of moderate-to-severe bronchopulmonary dysplasia // Eur. J. 2008. Vol. 32. N 2. P. 321–328.
- Yüksel H., Yilmaz O., Urk V., Yüksel D. et al. Clinical significance of lung perfusion defects in children with post-infectious bronchiolitis obliterans // Tuberk. 2009. Vol. 57. N 4. P. 376–382.







Комментировать