Результаты обследования 141 ребенка с сахарным диабетом (СД) І типа.
Е.А. Толстикова, Е.В. Прохоров, В.Л. Шевелева
Донецкий национальный медицинский университет им. М. Горького
Резюме. В работе представлены результаты обследования 141 ребенка с сахарным диабетом (СД) І типа, у 89 (63,1%) из них диагностирована диабетическая гастропатия, преимущественно в виде хронического гастрита с повышенной секреторной функцией. Показано, что течение диабетической гастропатии зависит от длительности диабета и характеризуется маломанифестными проявлениями. В 50,6% случаев диабетическая гастропатия обусловлена хеликобактерной инфекцией. Своевременная диагностика и адекватная терапия диабетической гастропатии позволяют улучшить состояние метаболического контроля у детей с СД І типа.
Вступление
Поражение пищеварительной системы у детей при сахарном диабете (СД) І типа является относительно малоизученным аспектом диабетологии. Между тем, патология желудка и двенадцатиперстной кишки у детей, страдающих диабетом, встречается чаще, чем диагностируется.
При длительности течения СД І типа свыше пяти лет частота поражений верхних отделов пищеварительной системы, по данным ряда исследователей, составляет от 60,0% до 80,0%[1,2]. В формировании данной патологии наряду с нарушением метаболизма важную роль играют вегетативные нарушения, явления микроангиопатии и т.д.
Также течению СД сопутствует депрессия показателей, характеризующих иммунологическую резистентность организма ребенка, что создает условия для активации разнообразной бактериальной флоры, в том числе и хеликобактерной, этиологическая роль которой в развитии воспалительных процессов слизистой оболочки желудка общеизвестна. Согласно современным представлениям, морфологическим субстратом поражения желудка при СД І типа является лимфоцитарная инфильтрация, которая, по мнению специалистов, подтверждает иммунную природу развития гастропатии при данном заболевании[2,4]. Не исключена также роль генетической предрасположенности рассматриваемых изменений верхнего отдела желудочно-кишечного тракта, связанных с особенностями главной системы гистосовместимости [1,3].
Целью настоящего исследования явилось изучение частоты и характера морфофункциональных нарушений верхних отделов желудочно-кишечного тракта у детей с СД І типа и их коррекция.
Материал и методы исследований
Частота и характер морфофункциональных нарушений верхних отделов ЖКТ изучены у 141 ребенка в возрасте 8–16 лет с СД І типа, которые находились в эндокринологическом отделении ОДКЛ г. Донецка. В 89 случаях (63,1%) зарегистрированы признаки поражения ЖКТ. При этом дети с СД, состоявшие на учете по поводу гастроэнтерологической патологии до дебюта СД, в разработку не включались. Диагностика гастропатий осуществлялась на основании клиникоанамнестических и лабораторноинструментальных данных, в том числе эндоскопии желудка и двенадцатиперстной кишки, определения H.Pyloriинфицирования и Рh-метрии.
Результаты исследований и их обсуждение
Результаты проведенных исследований позволили онстатировать, что диабетическая гастропатия отмечалась у детей с длительностью течения заболевания 5,7±1,02 лет. При этом нами установлено, что имеется ряд особенностей гастропатии в зависимости от возраста пациентов и длительности заболевания. Так, у 55 (61,8%) детей 11–16 лет боли локализовались не только в эпигастральной области, но и в других отделах живота, иррадиировали в область спины и позвоночника. У 14 (15,7%) подростков наблюдались ощущения онемения и жжения в области нижней части живота. Примечательно, что интенсивность боли варьировала от минимально выраженной (дети с длительностью СД более 5 лет) до умеренной (у пациентов младшего возраста). У трети обследованных (31 больной, 34,8%) отсутствовали жалобы на боли в животе, однако периодически возникали симптомы диспепсии. В частности, у 15 (16,8%) больных наблюдалась отрыжка съеденной пищей или воздухом, у 9 (10,1%) пациентов — быстрая насыщаемость, у 10 (11,2%) — чувство тяжести в правом подреберье после приема пищи. В 12,3% случаев отмечалось снижение аппетита, чувство переполнения в верхней части живота во время или вскоре после еды, потеря массы тела.
У 19 (21,3%) пациентов симптомы диабетической гастропатии были нерезко выраженными и непостоянными, в то же время у большинства детей они оказывали существенное негативное влияние на самочувствие и качество жизни.
Вышеупомянутые симптомы диспепсии отмечались у детей, страдающих СД менее 5 лет, в то время как у пациентов с боль шей длительностью заболевания регистрировалась более скудная клиническая симптоматика, о бусловленная, вероятно, развитием автономной и гастроинтестинальной нейропатии, что затрудняет диагностику у подростков и ведет к усугублению состояния в виде нарастания астеновегетативного синдрома.
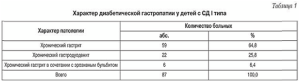
Выполненная у 87 больных фиброгастродуоденоскопия позволила констатировать у 59 (67,8%) из них признаки хронического гастрита, у 22 (25,8%) — хронического гастродуоденита, у 6 (6,4%) — хронического гастрита с явлениями эрозивного бульбита (табл. 1).
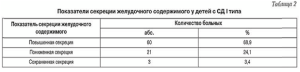
Повышенная секреция желудочного сока имела место у 51 ребенка (62,1 %), пониженная — у 25 детей (30,6 %), сохраненная секреция — у 6 (7,3 %) (табл. 2). Только в трех случаях (3,4 %) каких-либо изменений слизистой желудка и двенадцатиперстной кишки не отмечалось, в связи с чем наличие у обследованных болевого и диспепсического синдромов расценено как проявление функционального нарушения пищевой системы. У 2 детей (2,3 %) фиброгастродуоденоскопия не была выполнена ввиду отказа родителей от исследования. В 55,4 % случаев уреазный тест оказался положительным.
Всем детям наряду с лечением основного заболевания проводилась терапия гастропатии с учетом характера выявленной секреции. Пациенты с H.Pylori-инфекцией получали курсы эрадикационной терапии в соответствии с протоколами Маастрихтского соглашения, включающими кларитромицин, амоксициллин, блокатор протонной помпы и одно из пробиотических средств. Последующая коррекция выявленных нарушений позволила не только купировать гастроэнтерологическую симптоматику, но и достичь благоприятного характера течения основного заболевания и улучшения гликемического контроля.
Выводы
1. Поражение верхних отделов желудочно-кишечного тракта у детей с СД 1-го типа регистрируется в 62,6 % случаев, преимущественно в виде хронического гастрита с повышенной секреторной функцией.
2. Формирование и характер течения диабетической гастропатии во многом зависят от длительности заболевания и чаще характеризуются маломанифестными проявлениями.
3. Более чем в половине случаев (55,4 %) в генезе диабетической гастропатии существенную роль играет H.Pylori-инфекция.
4. Своевременная диагностика и адекватная терапия диабетической гастропатии позволяют не только устранить ее проявления, но и улучшить состояние метаболического контроля у пациентов.
Список литературы / References
1. Кривоносова Е.М. Диабетические гастропатии: клиника, диагностика, лечение // Врачебная практика. — 2002. — № 1. — C. 28-32.
2. Arstan D., Kendirci M., Kurtoglu S., Kula M. Helikobacter pylori infection in children with insulin dependent diabetes mellitus // J. Pediatr. Endocrinol Metab. — 2000. — Vol. 13 (50). — P. 553-556.
3. Salardi S., Cacciari E., Menegatti M., et al. Helicobacter pylori and type 1 diabetes mellitus in children // J. Pediatr. Gastroenterol. Nutr. — 1999. — Vol. 28 (3). — P. 307-309.
4. Dore M.P, Bilotta M., Malaty H.M. et al. Diabetes mellitus and Helicobacter pylori infection // Nutrition. — 2000. — Vol. 16 (6). — P. 407-410.













Комментировать