Гистиоцитоз из клеток Лангерганса: что это такое? Группы. Морфология. Описание клинического случая.
Гистиоцитоз из клеток Лангерганса (ГКЛ; гистиоцитоз Х) – это группа редких заболеваний, характеризующаяся клональной пролиферацией и аккумуляцией клеток системы фагоцитирующих мононуклеаров (к которым относятся все клетки моноцитарного ряда, начиная с монобластов и заканчивая гистиоцитами и макрофагами разных субпопуляций) в пораженных органах и тканях, а также разнообразными клиническими проявлениями. Этиология и патогенез остаются малоизученными. Известно, что в патогенезе ГКЛ задействованы механизмы, характерные как для опухолевых, так и для реактивных процессов [1]. Заболевание может встречаться в разных возрастных группах, но чаще всего диагностируется в детском возрасте. Частота встречаемости у детей в возрасте от 0 до 15 лет составляет 3–5 случаев на 1 млн, у новорожденных – 1 случай на 1 млн [1–6], пик заболеваемости приходится на первые 4 года жизни. Мальчики болеют в 2 раза чаще девочек.
Согласно современной классификации гистиоцитозов, принятой в 1997 г. Международным обществом по изучению гистиоцитарных болезней, гистиоцитозы делят на 3 большие группы:
- Гистиоцитозы из дендрических клеток.
II. Гистиоцитозы из макрофагальных клеток.
III. Злокачественные гистиоцитозы [1, 11].
ГКЛ относится к I группе. Выделяют следующие основные клинические варианты ГКЛ [3, 9, 10]:
– моносистемный вариант (включающий моно- или полифокальное поражение костной системы, изолированные поражения: костной системы, кожи, одной или более групп лимфатических узлов);
– полисистемный вариант (поражение 2-х или более органов и систем с дисфункцией жизненно важных органов; поражение 2-х или более органов и систем без дисфункции жизненно важных органов).
Кожа вовлекается в патологический процесс в 30–50% случаев, иногда кожные проявления становятся основным клиническим симптомом заболевания. Для ГКЛ характерен полиморфизм кожных высыпаний. Чаще поражение кожи носит симметричный, распространенный характер. Элементы экзантемы располагаются на коже туловища, верхних и нижних конечностей, включая ладони и подошвы, волосистой части головы, лица, в области крупных кожных складок, промежности. Представлены у детей раннего возраста поражениями, напоминающими атопический, себорейный дерматиты, в виде эритемы, на фоне которой отмечаются множественные папулы розового цвета, иногда с геморрагическим компонентом, покрытые желтыми чешуйчатыми корочками с участками мокнутия и поверхностных эрозий, с последующим образованием плотных геморрагических корочек, а также папуло-везикулами [1, 2, 4, 5].
У новорожденных детей при ГКЛ преобладают везикулезно-буллезные высыпания, которые могут быть расценены как герпетическая инфекция или врожденная ветряная оспа [1, 2]. Реже высыпания представлены узловатыми, гранулематозными и язвенными образованиями с характерной локализацией в области промежности. При диссеминированной форме ГКЛ в патологический процесс могут вовлекаться слизистые оболочки, на деснах возникают эритема, геморрагии, эрозии. Иногда у детей ГКЛ манифестирует с эрозивного процесса на деснах. В результате может развиться тяжелый гингивит с последующей деструкцией костей альвеолярных отростков и челюстей и выпадением зубов. Возможно поражение кожи наружного слухового прохода, приводящее к развитию хронического наружного отита [2, 4–8].
Морфология. Патологические клетки Лангерганса, являющиеся основным морфологическим субстратом, фенотипически отличаются от нормальных клеток Лангерганса. При проведении электронной микроскопии определяются зазубренный контур цитоплазмы с псевдоподиями, обилие органелл, наличие гранул Бирбека.
Диагностика. В биоптатах кожи, полученных из очагов поражения, обнаруживают инфильтрацию тканей патологическими клетками Лангерганса, гигантскими многоядерными клетками. При иммуногистохимическом исследовании выявляются положительная реакция на антиген CD1а, экспрессия S-100 белка. Диагноз ГКЛ ставится на основании клинических данных, гистологического исследования, при котором выявляются атипичные клетки Лангерганса, которые имеют положительные маркеры S-100 и СD1а. При электронной микроскопии выявляются гранулы Бирбека в цитоплазме клеток.
Клинический случай
Ребенок С., девочка, дата рождения: 12.05.2011 г., находилась в отделении новорожденных и недоношенных детей «Мать и дитя» ГБУЗ НО ОДКБ (г. Нижний Новгород) с 27.05 по 20.06.2011 г. с диагнозом: изолированный лангергансоклеточный в�ожденный гистиоцитоз кожи; перинатальное поражение ЦНС гипоксического генеза, синдром вегето-висцеральных нарушений средней степени тяжести; малая аномалия развития сердца: открытое овальное окно с гемодинамически незначимым шунтированием.
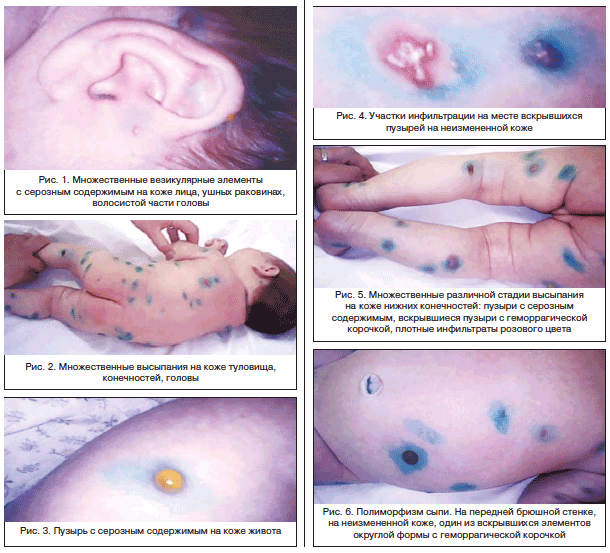
Из анамнеза: ребенок от 2-й беременности, протекавшей на фоне многоводия, обострения генитальной герпетической инфекции, 2-х срочных родов. Масса тела при рождении – 3700 г. Состояние в роддоме расценено как средней степени тяжести. С рождения у ребенка на коже волосистой части головы, верхних и нижних конечностей, груди, живота отмечались полиморфные высыпания в виде пузырей диаметром от 0,5 до 1,0 см с желтым прозрачным содержимым, на неизмененной коже элементы розовой папулезной сыпи диаметром до 0,5 см, плотной консистенции, возвышающиеся над поверхностью кожи. Гипертермии не отмечалось. Самочувствие ребенка нарушено не было. На 6-е сут жизни ребенок выписан домой. Дома было отмечено появление новых элементов. Ребенок был проконсультирован врачом-дерматологом, выставлен диагноз: герпетиформный дерматит Дюринга. На 15-е сут жизни поступил в отделение патологии новорожденных и недоношенных детей для обследования и лечения. Состояние на момент поступления в отделение средней степени тяжести. Самочувствие ребенка удовлетворительное. Вес при поступлении – 4070 г. При первичном осмотре: телосложение правильное, тургор тканей удовлетворительный, реакция на осмотр адекватная, крик громкий, границы сердца – в пределах возрастной нормы, тоны ритмичные, чистые, частота сердечных сокращений (ЧСС) – 134/мин. Дыхание проводится по всем легочным полям, пуэрильное, дополнительных дыхательных шумов нет, частота дыхания – 38/мин, перкуторно: ясный легочный звук. Живот мягкий, доступен пальпации, печень +1,5 см из-под края реберной дуги, селезенка не увеличена. На коже лица, волосистой части головы (рис. 1), верхних и нижних конечностей, туловища отмечено большое количество полиморфной сыпи – пузыри с тонкой крышкой на неизмененной поверхности кожи (рис. 2, 3) диаметром до 0,8 см, участки округлой и неправильной формы диаметром до 0,5–1,0 см плотной инфильтрации, цианотичного цвета (рис. 4), возникающие на месте «старых» пузырей (рис. 1–6), слизистые чистые.
На фоне удовлетворительного самочувствия отмечались в динамике почти ежедневное появление новых кожных элементов и трансформация ранее возникших.
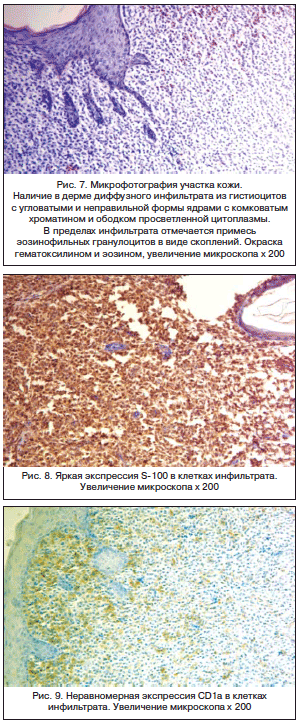
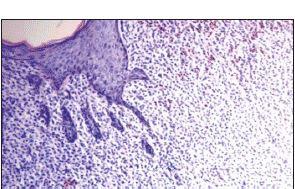
При обследовании в клиническом анализе крови: Hb – 133 г/л, Er – 4,17х1012/л, Tr – 422,8х10/л, Le – 7,5х10/л, п – 2%, с – 23%, Эоз – 7%, Li – 61%, Mn – 7%, CОЭ – 1 мм/ч. Белки острой фазы воспаления: С-реактивный белок – отрицательный, гаптоглобин – 9,0 ммоль/л, биохимические показатели – в пределах возрастной нормы. Концентрация нейрон-специфической енолазы в сыворотке крови – 5 мкг/л, концентрация α-фетопротеина – 562 МЕ/мл. Ребенок в паре с матерью обследован на внутриутробные инфекции (ВУИ) методом иммуноферментного анализа и амплификации ДНК – полимеразной цепной реакции (включая герпес-группу с учетом материнского анамнеза) – данных за течение ВУИ нет. Проведено цитологическое исследование содержимого пузыря: на фоне эритроцитов видны лейкоциты от 1 до 10 в поле зрения, по составу: нейтрофилы – 71%, эозинофилы – 14%, моноциты – 2%, лимфоциты – 13%. По данным рентгенографии грудной клетки отмечено усиление легочного рисунка в нижнемедиальном поле справа. Срединная тень сердца расширена в верхней и средней трети за счет вилочковой железы, удлинена дуга левого желудочка. Рентгенография черепа не выявила костно-деструктивных изменений в своде черепа. На рентгенограмме костей таза – костно-деструктивных изменений не обнаружено, головки бедренных костей отсутствуют, суставные щели симметричные. По данным ЭХО-КГ признаки диагональной трабекулы полости левого желудочка, открытое овальное окно с гемодинамически незначимым шунтированием. ЭКГ: ритм синусовый, ЧСС – 136–147/мин, правограмма. УЗИ органов брюшной полости: деформация желчного пузыря, эхографических признаков структурных изменений других органов брюшной полости, почек, надпочечников не выявлено. Нейросонография: признаки гипоксического поражения головного мозга. Ребенок консультирован онкологами – даны рекомендации проведения биопсии патологически измененных участков кожи. 7.06.2011 г. проведена открытая биопсия кожи спины под наркозом с дальнейшими гистологическим и иммуногистохимическим исследованиями. Гистологическое исследование кожи: наличие в дерме диффузного инфильтрата из гистиоцитов с угловатыми и неправильной формы ядрами с комковатым хроматином и ободком просветленной цитоплазмы. В пределах инфильтрата отмечается примесь эозинофильных гранулоцитов в виде скоплений (рис. 7). Иммуногистохимическое исследование выявило, что клетки инфильтрата позитивны к S-100 (рис. 8) и CD1а (рис. 9). Таким образом, был выставлен диагноз: изолированный врожденный лангергансоклеточный гистиоцитоз кожи.
Костномозговые пунктаты из 2-х задних подвздошных гребней от 17.06.2011 г. – без патологии.
Для определения тактики дальнейшего ведения ребенок был проконсультирован в НИИ ДОГ, г. Москва. Морфологические препараты пересмотрены, диагноз подтвержден, рекомендована химиотерапия (ХТ) по протоколу LCH III: винбластин, преднизолон. После уточнения диагноза ребенок был переведен в отделение онкологии. Лечение согласно протоколу (индуктивный курс и поддерживающая ХТ) проведено полностью и закончено в 2012 г. В процессе терапии элементы на коже постепенно регрессировали. В настоящее время ребенок находится на диспансерном наблюдении. Признаков рецидива опухоли нет. Следует отметить, что ребенок относится к группе часто болеющих детей, что, вероятно, обусловлено вторичным иммунодефицитом на фоне основного заболевания и перенесенной ХТ.
Выводы. ГКЛ относится к группе очень редких заболеваний периода новорожденности, кожные проявления при изолированной форме схожи с нозологическими формами другой этиологии (атопический дерматит, герпес-инфекция, мастоцитоз и др.) и являются единственным симптомом данного заболевания, в связи с чем необходима настороженность неонатологов и педиатров в отношении данной патологии. Своевременная диагностика позволит начать продуктивное лечение, что в значительной степени оптимизирует прогноз. Современный опыт показывает, что ГКЛ с изолированным поражением кожи у новорожденных при своевременно начатом лечении имеет благоприятное течение.
Литература
- Румянцев А.Г., Самочатова Е.В. Гематология и онкология детского возраста. М.: Медпрактика-М, 2004. С. 577–590.
2. Горланов И.А., Заславский Д.В., Минеева О.К. с соавт. Гистиоцитоз из клеток Лангерганса (гистиоцитоз Х): клиническое наблюдение // Вестник дерматологии и венерологии. 2013. № 1. С. 51–55.
3. Короткий Н.Г., Лебедева О.Е., Шемшук М.И., Тихомиров А.А. // Клиническая дерматология и венерология. 2012. № 2. С. 37–42.
4. Weston W.L., Lane A.T., Morelli J.G. Color Textbook of Pediatric Dermatolog. Third edition. Mosby, 2002.
5. Hurwitz L. Clinical pediatric dermatology. Fours edition. Elsevier saunders, 2011.
6. Nezelof C., Basset F., Rousseau M.F. Histiocytosis X histogenetic arguments for a Langerhans cell orgin // Biomedicine. 1973 Sep. Vol.18 (5). Р. 365—371.
7. Zhu Li, Yanqiu Li, Xiaoying Qu et al. Two case report studies of Langerhans cell histiocytosis with an analysis of 918 patients of Langerhans cell histyocytosis in literatures published in China // Int J Dermatol. 2010. Vol. 49. Р. 1169—1174.
8. Minkov M. Multisystem Langerhans Cell Histiocytosis in Children // Paediat Drugs. 2011. Vol. 13 (2). Р. 75—86.
9. Lichtenstein L., Histiocytosis X. Integration of Eosinophilic Granuloma of Bone, «Letterer-Siwe Disease» and «Schueller-Christian Disease» as Related Manifestations of a Single Nosologic Entity // Arch Pathol. 1953. Vol. 56. Р. 84—102.
10. Nezelof C., Basset F., Rousseau M.F. Histiocytosis X. Histogenetic Arguments for a Langerhans Cell Origin. Biomedicine, 1973.
11. Гистиоцитозы детского возраста / под ред. Х. Гаднера, А.Г. Румянцева. М. — Вена: Макс-Пресс, 2005.
Источник: Журнал РМЖ Мать и дитя. Акушерство. Гинекология. Педиатрия. 29 июля 2015 г, № 14








Комментировать