Патологии шейки матки. Патології шийки матки. Результати дослідження.
О.О. Хаустова, д. мед. н. Український науково-дослідний інститут соціальної і судової психіатрії та наркології МОЗ України, Київ
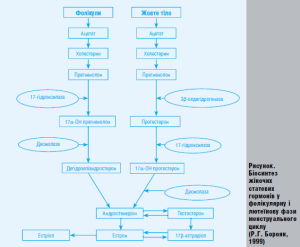
Протягом життя жінки існують специфічні періоди, під час яких вона має підвищений ризик розвитку психічних захворювань. Під час цих критичних періодів обізнаний клініцист, збираючи анамнез і обстежуючи ментальний статус пацієнтки, має ставити спеціальні запитання для виявлення психічних розладів. Адже щоразу, коли в організмі жінки відбуваються зміни гормонального балансу (рисунок), спостерігаються також певні зміни в її фізичному та психічному стані.
У дитинстві частота психічних захворювань у дівчаток менша або така сама, як у хлопчиків їхнього віку. Частота випадків депресії у хлопців і дівчат однакова до початку пубертатного періоду, а гормональні зміни можуть стати тригерним механізмом для депресивного епізоду в особи жіночої статі. У дівчат також підвищений ризик шкільних фобій, тривожних розладів, синдрому гіперактивності з дефіцитом уваги і розладів навчання. У підлітковому віці – підвищений ризик порушень харчової поведінки [4, 7].
Під час менархе у 2% дівчат розвивається передменструальна дисфорія. Це порушення настрою характеризується симптомами великої депресії, зокрема тривожністю і лабільністю настрою, що настають в останній тиждень менструального циклу і припиняються в перші дні фолікулінової фази. Передменструальна емоційна лабільність зустрічається у 20–30% жінок, її тяжкі форми трапляються значно рідше – у 3–5% жіночої популяції.
Після пубертату різко зростає ризик розвитку депресії; у жінок цей показник удвічі, а за деякими даними – утричі вищий, ніж у чоловіків того самого віку. У жінок з великою депресією, як і з маніакально-депресивним психозом, психічні порушення загострюються в передменструальний період.
Жінки більшою мірою піддаються психічним розладам під час вагітності і після неї. Жінки з психічними розладами в анамнезі часто при плануванні вагітності відмовляються від медикаментозної підтримки, що підвищує ризик рецидиву. Після пологів у більшості жінок відмічено зміни настрою: спостерігається короткий період депресії «baby blues», що не потребує лікування. У деяких жінок у післяпологовий період розвиваються тяжкі симптоми депресії, що порушують працездатність, у невеликої кількості – розвиваються психотичні розлади.
У більшості жінок ці зміни настрою відбуваються в перші шість місяців після пологів, наприкінці цього терміну всі ознаки дисфорії минають самостійно. Вже доведено, що більшість випадків післяпологової депресії виникають у жінок, які преморбідно схильні до депресивних розладів, мали ларвовані або масковані депресії. Тому у деяких жінок депресивні симптоми зберігаються протягом багатьох місяців після пологів. Відносний ризик прийому препаратів під час вагітності і годування груддю утруднює вибір лікування, у кожному випадку питання співвідношення користь/ризик терапії залежить від питомої ваги симптоматики. Раннє визначення симптомів і адекватне лікування необхідні як для матері, так і для дитини, оскільки депресія може впливати на здатність матері адекватно доглядати за дитиною.
Період середнього віку також характеризується високим ризиком тривожних розладів і порушень настрою, а також інших психічних розладів, таких як шизофренія. У жінок може порушитися сексуальна функція, якщо ж вони приймають антидепресанти з приводу афективних або тривожних розладів – у них підвищується ризик розвитку побічних ефектів, зокрема зниження сексуальної функції.
Хоча немає чітких доказів того, що менопауза асоційована з підвищеним ризиком депресії, у більшості жінок у цей період відбуваються серйозні зміни в житті, особливо в родині [1, 24]. Активна роль стосовно дітей змінюється на
роль доглядальниць при старих батьках, адже догляд за літніми батьками майже завжди здійснюють жінки. Ми вважаємо за необхідне моніторинг ментального статусу цієї групи жінок для виявлення можливих порушень якості життя.
По мірі старіння у жінок збільшується ризик розвитку деменції та психіатричнихускладнень соматичних хвороб. Оскільки тривалість життя у жінок більше, ніж у чоловіків, а ризик розвитку деменції зростає з віком, у більшості жінок розвивається деменція. У жінок похилого віку з множинними соматичними захворюваннями і великою кількістю медикаментів, що вони їх приймають, високим є ризик розвитку деліріозних станів. У жінок також підвищений ризик розвитку парафренії – психотичного розладу, що може з’явитися після 60 років. Внаслідок більшої тривалості життя і значного ступеня залучення в міжособистісні відносини жінки частіше і сильніше переживають втрати близьких людей, що також підвищує ризик розвитку психічних захворювань.
Дуже важливим є те, що багато в чому особливості психічного стану жінки дійсно зумовлені індивідуальним балансом оваріальних стероїдів. У гіпоталамічній ділянці зосереджені центральні стероїдчутливі системи (рецептори), що беруть участь у механізмі зворотного зв’язку. Саме нормальне функціонування гіпоталамічної ділянки та інших відділів головного мозку характеризується певним співвідношенням дофаміну, серотоніну й ацетилхоліну. Настрій, сексуальна поведінка, особливості харчування, болісні відчуття і нейроендокринна регуляція системи гіпоталамус–гіпофіз–яєчники забезпечується ендорфінами, що секретуються в гіпоталамусі.
Ще у 20-х роках ХХ століття американські вчені Е. Allen та Е. Doisy (1923) заклали підвалини сучасних уявлень про оваріальні стероїди. Вони з’ясували, що яєчник виробляє дві різні речовини: одна відповідальна за ріст і функціонування статевих органів (естрогени), друга – за секреторні зміни в ендометрії та збереження вагітності (гестагени) [6].
У головному мозку естрогени діють і як трофічний фактор, і як нейротрансмітер. Щільність
розташування їх рецепторів найбільша в преоптичній зоні гіпоталамуса, проте певна кількість міститься також у мигдалеподібному ядрі, СА1 і СА3 ділянках гіпокампа, поясній звивині, синій плямі, ядрах шва і центральній сірій речовині. У багатьох ділянках мозку кількість естрогенових рецепторів змінюється протягом менструального циклу, у деяких ділянках (зокрема в лімбічній системі) їх рівень залежить від сироваткового рівня естрогенів.
Естрогени – як ендогенні, так і в складі комбінованих пероральних контрацептивів (КПК), – впливають на активність моноамінооксидази (МАО), що бере участь в окислюванні біогенних амінів: норепінефрину, епінефрину, серотоніну і дофаміну. Епінефрин викликає нудоту, підвищений рівень серотоніну – нервове напруження, безсоння, серцебиття, порушення уваги. Дофамін порушує баланс цих трьох амінів, зумовлюючи розлади психіки.
Естрогени блокують активність МАО типу А (що дезактивує всі 4 аміни) і підвищують активність МАО типу В (що дезактивує лише допамін). При естрогенній стимуляції утворюється багато серотоніну, норепінефрину і епінефрину при
відносному дефіциті дофаміну, що сприяє появі дратівливості, нервового напруження, плаксивості.
Крім того, існує оптимальний рівень серотоніну, тому коливання його рівня у бік підвищення або зниження призводять до агресії або депресії. При вираженій депресії спостерігається зниження метаболізму серотоніну. Зі зміною рівня серотоніну в спинномозковій рідині пов’язують прояви суїцидальних спроб і агресії у жінок у передменструальний період.
Впливаючи на рівні нейротрансмітерів на холінергічну систему, естрогени також активують ацетилхолінестеразу (АХЕ). У дослідженнях на людях і тваринах підвищення рівня естрогенів поліпшує дрібну моторику, проте знижує здатність просторової орієнтації. При базально зниженому рівні естрогенів у жінок його підвищення поліпшує словесну короткочасну пам’ять.
У свою чергу, прогестагени, у тому числі й ті, що входять до складу гормональних контра цептивів, мають здатність видозмінювати нейрогормони і нейропептиди мозку шляхом зв’язування з рецепторами до прогестерону в центральній нервовій системі (ЦНС).
Прогестерон і його метаболіти здатні зв’язуватися з рецепторами гамма-аміномасляної кислоти (ГАМК) – природним медіатором мозкової тканини – і чинити психотропну дію на організм жінки, що знайшло своє місце в лікуванні деяких форм депресії, мігрені тощо [4].
Прогестерон також має гіпнотичний ефект, який використовується для лікування передменструального синдрому і психологічного стресу; зокрема, їх особливо доцільно призначати жінкам-жертвам зґвалтування, зважаючи на той факт, що гестагени викликають незначне пригнічення ЦНС [1–4, 23].
Взагалі, ГАМК відіграє важливу роль в активності дофамінергічних систем, психотропні ефекти яких описано вище. ГАМК – природний медіатор мозкової тканини. Зниження рівня ГАМК у мозковій тканині тварин призводить до появи судом. Збільшення його супроводжується атаксією, зниженням рухової активності, підвищенням судомного порога. При значному збільшенні концентрації прогестерону, за рахунок того, що його метаболіти зв’язуються з рецепторами ГАМК, може спостерігатися сонливість [4, 6, 21] Підсумовуючи роль індивідуального балансу оваріальних стероїдів жінки у нейротрансмісії та розвитку депресивних розладів, варто зауважити, що прогестерон та різні його синтетичні версії працюють на зниження рівня ендогенного серотоніну, тим самим провокуючи клінічні депресивні розлади у жінок, які мали депресію або схильність до неї в анамнезі.
У свою чергу, естрогенна стимуляція підвищує рівень нейромедіатора серотоніну, що сприяє покращенню настрою та сну, а також є значущим фактором для редукції депресії. Особи з клінічною депресією мають низький рівень ендогенного серотоніну, тому селективні інгібітори зворотного захоплення серотоніну (СІЗЗС), блокуючи його зворотне захоплення, лікують депресивні розлади.
Дослідження останніх років підтверджують та поглиблюють ці дані. Виявилося, що високий рівень естрогенів поглиблює реакцію на стрес, збільшує стресогенний когнітивний дефіцит. Важливо, що поза умовами стресу рівень естрогену не впливає на когнітивні функції. Підтвердженням є гендерна динаміка стресорних розладів із відповідним зростанням у жінок у пубертатний період, максимальним рівнем у репродуктивний період та зниженням після менопаузи до рівня таких розладів у популяції чоловіків [4, 15].
Учені лише починають вивчати взаємовплив естрогенів, серотоніну та настрою з метою подальшої терапії депресивних розладів. Поширеність депресії та тривоги серед хлопців і дівчат до пубертатного періоду є однаковою. З появою менструальної функції збільшується кількість афективних розладів. Узагалі, жінки незалежно від вживання КПК, утричі частіше хворіють на депресивні розлади, вдвічі – на тривожні розлади та посттравматичні стресові розлади (ПТСР) порівняно з чоловіками [16].
Незважаючи на те, що коливання гормонального фону впливають на настрій та самопочуття жінок, депресивні прояви корелюють лише з віком менопаузи (тільки серед жінок із низьким рівнем освіти), фрустрацією, психічною та фізичною інвалідністю, прийомом антидепресантів або депресією в анамнезі. Більше того, тривалий прийом КПК може запобігати проявам депресії [4, 20].
Відповідно до результатів 30річного дослідження у жінок репродуктивного віку раптова відміна, коливання рівня та перманентний дефіцит естрогенів корелюють зі значними афективними розладами. Клінічне видужання від післяпологової, перименопаузальної та постменопаузальної депресій має враховувати стабільний (оптимальний) рівень естрогенів [12].
Отже, якщо під час великих гормональних змін у житті жінки змінюється і психічний стан, штучне маніпулювання гормонами за допомогою КПК має внести зміни в емоційний стан жінки.
Пероральні контрацептиви (ПК) складають групу найбільш досліджених i широко використовуваних рецептурних засобів [2, 5, 15]. ПК вперше з’явилися у 1960-х роках, а вже на сьогодні їх щодня використовують понад 63 млн жінок в усьому світі, з них 46 млн – у країнах, що розвиваються [21]. Відповідно до підрахунків у 1989 р. обсяг всесвітнього ринку ПК дорівнював 1,8 млрд доларів США [6]. У Великій Британії в 1987 р. приблизно 45% жінок у віці 20–29 років використовували ПК. Якщо серед жінок, що народилися в 1930-х роках, ПК використовували лише близько 40%, то серед народжених у 1950-х роках ними користувалися вже 80% [22].
У США в 1991 р. 28% жінок у віці від 15 до 44 років користувалися ПК – це найвищий показник з 1975 р. А от у Мексиці, де в 1970-ті роки ПК були найбільш поширеними контрацептивними засобами, на сьогодні за популярністю вони поступаються ін’єкційним контрацептивам, внутрішньоматковим засобам і стерилізації. Причина: мексиканки вважають, що ймовірність шкідливих побічних ефектів у ПК більша, ніж у інших контрацептивних засобів [9].
За даними статистичного опитування нині понад 60–70% жінок дітородного віку в США і країнах Європи віддають перевагу комплексним гормональним контрацептивам з метою запобігання вагітності. Крім цього, препарати даної групи використовують в терапії різних захворювань у гінекологічній ендокринології. Ці засоби мають масу побічних ефектів, тож постає питання безпечності їх застосування [2–4, 6, 21, 22].
Сучасні КПК характеризуються зниженим вмістом естрогенів і прогестагенів, завдяки чому істотно знизилася частота виникнення побічних явищ. Ефект стандартних доз гормонів, які містяться у КПК, залежить від індивідуальної чутливості кожної конкретної жінки, тому він може виявитися надмірним або недостатнім. На практиці це означає, що той самий препарат у різних жінок може викликати симптоми як надлишку, так і нестачі естрогену або прогестагену
[2, 4, 20]. У жінок із підвищеною гормональною чутливістю КПК можуть спровокувати посилення фізичних та емоційних симптомів передменструального синдрому (ПМС), особливо в перші 2–3 місяці.
На жаль, при використанні КПК дійсно можливе виникнення деяких побічних ефектів, кількість їх у перші місяці прийому сягає 10–40%, потім знижується до 5–10%.За даними літератури та за інструкціями до застосування КПК мають низку побічних дій, що, в свою чергу, поділяються на загальні та специфічні.
До загальних побічних ефектів належать:
• головний біль;
• дискомфорт у травному каналі;
• нудота, блювання;
• дискінезія жовчних протоків, загострення жовчнокам’яної хвороби;
• напруженість у молочних залозах (мастодинія);
• нервозність, роздратованість;
• зміни лібідо;
• депресія;
• запаморочення;
• надмірна маса тіла.
Специфічними побічними діями КПК є порушення менструального циклу:
• міжменструальні мажучі кров’янисті виділення;
• проривні кровотечі;
• аменорея під час або після прийому КПК [11].
Отже, за офіційно визнаними джерелами всього налічується 13 побічних ефектів, що можуть проявитися у жінки при застосуванні КПК.
Варто зауважити, що можливі неприємні відчуття у жінок, які приймають КПК, пов’язані з метаболічною дією (естрогенабо гестагензалежною) статевих стероїдів. До естрогензалежних ефектів належать: нудота, блювання, набряки, запаморочення, рясні менструальноподібні кровотечі; до гестагензалежних – дратівливість, депресія, підвищена втомлюваність, зниження лібідо. Головний біль, мігрень, нагрубання молочних залоз, кров’яні виділення можуть бути зумовлені дією обох компонентів КПК. Нині ці ознаки розглядають як симптоми адаптації до КПК, зазвичай вони не вимагають додаткового призначення коригуючих засобів і самостійно минають до кінця 3-го місяця регулярного прийому.
За даними «жіночих» сайтів в інтернеті кількість небажаних явищ, пов’язаних із прийомом КПК, значно більша. До побічної дії КПК деякі жінки можуть відносити такі прояви: занепокоєння, постійне нервове напруження; дратівливість, уразливість, конфліктність і раптові вибухи гніву; плаксивість; депресію, тугу; швидкі зміни настрою; слабкість, підвищену втомлюваність; нерішучість; відчуття, що все валиться з рук, підвищену схильність до побутових травм (опіки, порізи і т.д.); неуважність і погану реакцію (наприклад, за кермом); плутанину у думках і безпам’ятність; загальмованість, утруднену мову; різкий спад або сплеск сексуальних бажань; безсоння або сонливість; головний біль; запаморочення і непритомність; нудоту і блювання; загострене сприйняття шуму; хворобливі відчуття у грудях і нагрубання молочних залоз; біль унизу живота й у попереку; підвищену температуру тіла; підвищену схильність до інфекцій, ослаблення імунітету; прискорене серцебиття; хворобливість суглобів, біль у м’язах; алергічні реакції; носові кровотечі; дизурію; загострення геморою; погану переносимість алкоголю; задишку; набряки; метеоризм; напади булімії або підвищений апетит; зміну смакових відчуттів (потяг до гостренького, солоного тощо); нестримний потяг до солодкого і борошняного; нове сприйняття запахів (раптом хочеться понюхати бензин, гуталін або лак); погіршення стану шкіри і волосся; поколювання, відчуття оніміння або «мурашок» у руках.
Аналізуючи зміст «жіночих» сайтів в інтернеті, K. BurnettWatson ще у 2005 р. виявила, що накопичення великої кількості негативних відгуків щодо побічної дії КПК зумовлено тим, що інтернетпошуком інформації щодо КПК займалися переважно жінки, які відчули на собі якусь побічну дію і не мали достатньої інформації від лікаря. Більше того, жінки наполягали на тому, що деякі лікарі ігнорували повідомлення про симптоми депресії та інші побічні дії.
Існує низка інших досліджень, які пов’язують депресію з прийомом КПК, проте наполягають на необхідності більшої інформованості лікарів і жінок з метою запобігання її гіпердіагностики [20]. Цікаво, що жінки, які брали участь в освітній КПК-програмі, менше скаржилися та краще справлялися з побічними діями препаратів [26].
Насправді ж, частота випадків депресії у жінок, які приймають КПК, не вища, ніж у тих, хто їх не приймає. Причому, після відміни КПК кількість жінок з проявами депресії тимчасово дещо збільшується. Жінки, що приймали КПК з метою контрацепції, на 1/3 рідше сповіщали про відчуття депресії порівняно з особами, які приймали КПК за іншим призначенням [13].
Інтенсивність депресії більше залежить від віку, особистості та зайнятості (по роботі), ніж від прийому КПК. Частота депресії у жінок збільшується з віком, а також переважає у домогосподарок порівняно з особами, що працюють повний робочий день [14].
Мета-аналіз показав: дані 12 клінічних досліджень свідчили про наявність симптомів депресії у 16–56 % жінок, що приймали КПК. Дані трьох досліджень заперечували наявність цього зв’язку. Проте в усіх цих дослідженнях не проводилася оцінка афективного статусу до вживання КПК. Відомо, що КПК індукують триптофан оксигеназу, а це у деяких жінок може спричинити дефіцит піридоксину. Отже, останній може бути корисним для попередження та терапії депресії у жінок, що приймають КПК [19,25]. КПК також сприяють редукції проявів атипової депресії як застережного симптому мігрені [18].
Більше того, здорові жінки без афективних або тривожних розладів в анамнезі при прийомі КПК не скаржилися на побічні психологічні симптоми всупереч значній редукції нейроактивних стероїдів [23]. Субклінічні коливання настрою (поєднання тривоги, депресії та знервованості) були визначені в період 21–7 дня КПК циклу, з підвищенням безпосередньо перед 7-денним «hormone-free» інтервалом та піком протягом цього інтервалу [11]. Дослідники наголошують на тимостабілізуючому ефекті похідних прогестерону, що є його позитивною психотропною дією [17].
Отже, питання діагностики та лікування жіночої депресії виходить за межі проблеми прийому КПК. Термін «депресія» як
психіатричний діагноз, як психопатологічний феномен і як побутове вираження має різний зміст. Психіатричний діагноз має відповідати на чотири запитання щодо наявності/відсутності: критеріїв психічного захворювання за МКХ-10; розладу особистості; розладів поведінки; розладів соціально-психологічної адаптації.
Такі жорсткі критерії пояснюються тим, що при діагностиці досить складно розрізнити короткочасні періоди смутного настрою, пов’язаного з життєвими обставинами, і депресію як психічний розлад. Ключем до диференціального діагнозу є розпізнавання типових симптомів і моніторинг їх динаміки. У людини без психічних відхилень зазвичай немає порушень самооцінки, суїцидальних думок, почуття безнадійності, нейровегетативних симптомів, таких як порушення сну, апетиту, відсутність життєвої енергії протягом тижнів і місяців.
Діагноз великої депресії ґрунтується на зборі анамнезу й обстеженні ментального статусу. Основними симптомами є знижений настрій і ангедонія – втрата бажання і здатності отримувати задоволення від звичайних життєвих проявів. Крім депресії й ангедонії, що тривають протягом мінімум двох тижнів, епізоди великої депресії характеризуються наявністю як мінімум чотирьох з таких нейровегетативних симптомів: значна втрата або збільшення маси тіла, безсоння або підвищена сонливість, психомоторна загальмованість або пожвавлення, втома і втрата сил, знижена здатність
до концентрації уваги і прийняття рішень. Крім того, багато людей страждають на підвищену самокритику з відчуттямбезнадійності, надлишкової провини, суїцидальними думками, відчуттям себе як тягаря для своїх близьких і друзів.
Велика депресія, якщо її адекватно не лікувати, може погіршувати прогноз соматичних захворювань і збільшувати загальний обсяг необхідної медичної допомоги. Депресія може підсилювати і збільшувати кількість соматичних скарг, знижувати поріг болю, підвищувати функціональну недієздатність. Так, дослідження пацієнтів, що часто користуються медичною допомогою, виявило депресію у понад 50% із них. Більше того, лише у тих, у кого протягом року спостереження зменшилася вираженість симптомів депресії, спостерігалося поліпшення функціональної активності. Симптоми депресії (знижений настрій, безнадійність, відсутність задоволення від життя, втома, порушення концентрації уваги і пам’яті) порушують мотивацію звернення за медичною допомогою. Своєчасна діагностика і лікування депресії допомагають поліпшити прогноз і підвищити ефективність терапії.
Таким чином, перед призначенням адекватної терапії депресії як психіатричного випадку лікар повинен мати відповіді на такі чотири запитання: етіологія захворювання, час його початку, особливості попередньої відповіді на фармакотерапію; особливості соціальної взаємодії пацієнтки відповідно до рис її особистості; цілеспрямова-
ні розлади поведінки; адаптивність існуючої життєвої стратегії (які події в житті жінки сприяли формуванню її особистості, які висновки вона з них зробила).
Оптимальна тактика психофармакотерапії, враховуючи переважне приєднання феномена тривоги до депресивних проявів у жінок, передбачає призначення антидепресантів, що впливають на обидва психопатологічні феномена. Найоптимальніша тактика вибору антидепресанта спирається на такі фактори:
• мішень терапії: симптом, синдром, синдромокомплекс (вибір препарату з однієї з груп антидепресантів за хімічною структурою: ТЦА – ІМАО – СІЗЗС – ІЗЗН – ІЗЗСН – МСЗ);
• побічна дію препарату;
• індивідуальність ефекту;
• можливість продовжити підтримуючу терапію препаратом першої допомоги;
• ефект ресоціалізації;
• комплайєнс-ефект;
• вартість лікування. Очевидно, що для успішного
лікування необхідні нові антидепресанти з більш високою ефективністю і/або поліпшеною переносимістю.
Найбільш уживаною нині є група СІЗЗС, її представники – есциталопрам, циталопрам, флувоксамін, флуоксетин, сертралін та пароксетин. Причому саме ці антидепресанти найчастіше призначають як препарати першої лінії. Відповідно до принципів доказової медицини СІЗЗС розглядають як стандарт при терапії усіх тривожно-фобічних розладів.
Більша ефективність СІЗЗС у жінок зумовлена впливом естрогену на серотонінову систему. Так, відповідно до результатів STAR*D (Sequenced Treatment Alternatives to Relieve Depression), опублікованих
у Journal of Psychiatric Research, жінки з рекурентним депресивним розладом частіше досягають ремісії на СІЗЗС, ніж чоловіки [10, 12].
Серед антидепресантів усіх груп (не лише СІЗЗС) пароксетин є найбільш сильним інгібітором транспортера серотоніну. В на номолярних концентраціях він також взаємодіє з транспортером норадреналіну, що розширює його лікувальний вплив і поєднує його з групою ІЗЗСН.
Аналізуючи особливості скарг на «депресію», дослідники зауважили, що частина жінок сприймає зниження лібідо або відчуття втоми як прояви депресії. Також було з’ясовано, що ймовірність появи сексуальної дисфункції у жінок, що одночасно приймають СІЗЗС та КПК, залежить від особливостей їхнього генотипу [10].
Отже, для лікування депресивних та тривожно-депресивних розладів у жінок доцільно використовувати антидепресанти класу СІЗЗС, а серед них віддавати перевагу пароксетину, який має найбільшу протитривожну дію та незначний спектр побічних дій.
Жінки, що приймають антидепресанти, можуть почуватися нещасними навіть після клінічного одужання від депресії. Протягом 1–3 місяців адекватного лікування відновлюються позитивні емоції, виробниче та соціальне функціонування, проте зберігається відчуття безнадії, яке є небезпечним як фактор суїцидального ризику, що знаходить своє відображення у скаргах пацієнток. Допоміжними в таких випадках є когнітивно-біхевіоральні стратегії психотерапії [8].
Тож зв’язок між прийомом КПК і депресією може мати лише опосередкований характер через особливості індивідуальної чутливості жінки до компонентів КПК та її сімейного й особистого анамнезу відносно депресивних розладів. Поява ознак клінічноїдепресії є підставою для призначення адекватної антидепресивної терапії, де препарати першої лінії – СІЗЗС, зокрема пароксетин. Невелика частота та вираженість побічної дії препаратів істотно не впливає на якість життя жінки. Впровадження до програм медичного менеджменту жінки технологій когнітивнобіхевіоральної психотерапії та психокорекції сприяє формуванню у неї адаптивних копінг-стратегій без фіксації на дискомфортних відчуттях і негативних подіях життя.
Література
1. Бенюк В.О., Усевич І.А. Практичні аспекти гормональної контрацепції// Мед. аспекты здоровья женщины. – 2006. – № 2 (2).– http://woman. healthua.com/article/19.html.
2. Звычайный М.А., Воронцова А.В., Коновалов В.И. и др. Безопасность и приемлемость микрои низкодозированных комбинированных оральных контрацептивов// Пробл. репродукции. – 2001. –№ 3.– http://www. rusmedserv.com/
problreprod/2001/3/article_253.html.
3. Никитин С.В. К вопросу о современных прогестагенах и комбинированных оральных контрацептивах// Гинекология. – 2003. – № 5 (5).
4. Половые гормоны и аффективные расстройства у женщин// Бюлл. по депрессиям WPA. – 2002. – http://maulder/narod/ru/depression/gormones/htm.
5. Прилепская В.Н. Новые технологии в контрацепции: гормональные рилизинг-системы// Гинекология. – 2005. – № 7 (1). – С. 41–44.
6. Современные аспекты контрацепции/ Под ред. Я.М. Сенчука, Б.М. Венцковского. – К.: ТМК, 2001.
7. Тихомиров А.Л. Оральные контрацептивы в сохранении и восстановлении репродуктивного здоровья// Гинекология. – 2004. – № 6 (5). – С. 249–251.
8. Aikens J.E. Antidepressants less than effective for feelingsof hopelessness// Gen. Hosp. Psychiatry. –
2009. – Feb 14. – PMID: 24582315.
9. Anon. Decline of oral contraceptive use in Mexico// Scrip. – 1992. – № 1684. – Р. 20.
10. Bishop J.R., Ellingrod V.L., Akroush M., Moline J. The association of serotonin transporter genotypes and selective serotonin reuptake inhibitor (SSRI)associated sexual side effects: possible relationship to oral contraceptives/ Hum. Psychopharmacol. –
2009. – Feb 9. – PMID: 19204908.
11. Coffee A.L., Kuehl T.J., Sulak P.J. Comparison of scales for evaluating premenstrual symptoms in women using oral contraceptives// Pharmacother. –2008. – Vol. 28, № 5. – Р. 576–583.
12. Douma S.L., Husband C., O’Donnell M.E. Estrogenrelated mood disorders: reproductive life cycle factors// Adv. Nurs. Sci. – 2005. – Vol. 28, № 4. –Р. 364–375.
13. Duke J.M., Sibbritt D.W., Young A.F. Is there an association between the use of oral contraception and depressive symptoms in young Australian women? // Contraception. – 2007. – Vol. 75, № 1. – Р. 27–31.
14. Fleming O., Seager C.P. Incidence of depressive symptoms in users of the oral contraceptive// Br. J. Psychiatry. – 1978. – Vol. 132. – Р. 431–440.
15. Gilman A.G., Rail T.W., Nies A.S., Taylor P., eds. Goodman and Gilman’s The Pharmacological Basis of Therapeutics. – New York: Pergamon Press, 1990. –1402 р.
16. Hegadoren K., Lasiuk G. Hormone-depression link merits urgent research// Biol. Res. Nurs. – 2009. – Feb 5. – PMID: 14502308.
17. Huber J.C., Heskamp M.L., Schramm G.A. Effect of an oral contraceptive with chlormadinone acetate on depressive mood: analysis of data from four observational studies// Clin. Drug Invest. – 2008. – Vol. 28, № 12. – Р. 783–791.
18. Kawamura S., Sakai A., Endo T., Maruta M. Atypical depression as a premonitory symptom of migraine managed by an oral contraceptive// Psychiatry Clin. Neurosci. – 2008. – Vol. 62, № 3. – Р. 365.
19. Kulkarni J. Depression as a side effect of the contraceptive pill// Expert Opin. Drug Saf. – 2007. – Vol. 6, № 4. – Р. 371–374.
20. Kulkarni J., Liew J., Garland K.A. Depression associated with combined oral contraceptives – a pilot study// Aust. Fam. Physician. – 2005. – Vol. 34,
№ 11. – Р. 990.
21. Medical Eligibility Criteria for Contraceptive Use. 3rd edition// WHO, 2004.
22. Milne R., Vessey M. The pill and mortality – an overview// J. Public Health Med. – 1992. – Vol. 14,
№ 1. – Р. 9–16.
23. Rapkin A.J., Morgan M., Sogliano C. et al. Decreased neuroactive steroids induced by combined oral contraceptive pills are not associated with mood changes// Fertil. Steril. – 2006. – Vol. 85, № 5. –
Р. 1371–1378.
24. Ryan J., Carriere I., Scali J. et al. Lifetime hormonal
factors may predict late-life depression in women// Int. Psychogeriatr. – 2008. – Vol. 20, № 6. – Р. 1203–
1218.
25. Slap G.B. Oral contraceptives and depression: impact, prevalence and cause// J. Adolesc. Health Care. – 1981. – Vol. 2, № 1. – Р. 53–64.
26. Thamkhantho M., Jivasak-Apimas S., Chiravacharadej G. et al. Preliminary report on characteristics of women participating in the meeting of the Oral Contraceptive Pill Members Club at Siriraj Hospital// J. Med. Assoc. Thai. – 2008. – Vol. 91,№ 6. – Р. 781–786.










Комментировать