Мета лікування серцевої недостатності
Мета діагностики та лікування серцевої недостат-ності (СН) не відрізняється від такої для будь-якого ін-шого клінічного стану, тобто полягає у зниженні смерт-ності, профілактиці можливих ускладнень та поліпшен-ні якості життя хворих. Зважаючи на надміру високий рі-вень щорічної смертності внаслідок СН, особливу увагу в клінічних дослідженнях було приділено саме цій кін-цевій точці. Однак для багатьох людей, особливо літньо-го віку, досягнення такої мети, як можливість провадити самостійне життя, усунення вкрай неприємних симпто-мів, а також уникнення госпіталізації, може прирівнюва-тися до подовження тривалості життя.
На рисунку представлено алгоритм лікування пацієн-тівізсимптомамиСНісистолічноїдисфункції.Важливимє такожвизначеннятактикилікуванняпоширенихсерцево-судиннихінекардіологічнихсупутніхзахворювань.
Інгібітори ангіотензинперетворювального фер-менту
За винятком випадків протипоказання чи неперено-симості, інгібітори ангіотензинперетворювального фер-менту (ІАПФ) слід використовувати в усіх пацієнтів із симптомами СН і фракцією викиду (ФВ) лівого шлуноч-ка (ФВЛШ) ≤ 40%. Лікування за допомогою ІАПФ покра-щує шлуночкову функцію і самопочуття пацієнта, зни-жує частоту госпіталізації з приводу прогресування СН та підвищує виживаність. У госпіталізованих хворих те-рапію ІАПФ необхідно розпочинати ще до виписування зі стаціонару.
Клас рекомендацій І, рівень доказовості А
Ключові докази
• У двох ключових рандомізованих контрольованих дослідженнях (РКД) (CONSENSUS і SOLVD-Treatment) приблизно 2800 пацієнтам із СН різної тяжкості було при-значено плацебо чи еналаприл. Більшість із них також отримували діуретик або дигоксин. Менш ніж 10% паці-єнтів у кожному дослідженні ліковано із застосуванням β-адреноблокатора (БАБ). У дослідженні CONSENSUS 53% пацієнтів із тяжкою СН призначали спіронолактон.
• У кожному зі згаданих РКД лікування ІАПФ знижу-вало смертність (зниження відносного ризику [ЗВР] на 27% у CONSENSUS і на 16% – у SOLVD-Treatment). У дослі-дженні SOLVD-Treatment також установлено ЗВР госпіта-лізації з приводу прогресуючої СН на 26%. Указана ко-ристь від застосування ІАПФ була додатковою до корис-ті від стандартної терапії.
• Зниження абсолютного ризику (ЗАР) смертності у пацієнтів з легкою або помірною СН (SOLVD-Treatment) становило 4,5%. При цьому показник кількості хворих, яких необхідно пролікувати (ХНП) для відстрочення од-ного випадку смерті (в середньому більш ніж на 41 міс), дорівнював 22. При тяжкій СН
(CONSENSUS) ЗАР сягало 14,6%, ХНП – 7 (при відстро-ченні смерті в середньому через 6 міс).
• Наведені результати підтверджено метааналізом даних досліджень із невеликою кількістю включених пацієнтів і недовготривалих плацебо-контрольованих РКД, який показав чітке зниження смертності протягом тільки 3 міс терапії. У цих РКД також продемонстрова-но, що ІАПФ зменшують вираженість симптомів захво-рювання, підвищують толерантність до фізичних наван-тажень, покращують якість життя і якість виконання фі-зичних вправ.
• У дослідженні ATLAS 3164 пацієнтів із переважно помірною і тяжкою СН було рандомізовано на прийом лізиноприлу в низькій або високій дозі. При цьому спо-стерігалося ЗВР смерті чи госпіталізації з приводу СН на 15% у групі високих доз лізиноприлу порівняно з гру-пою низьких доз.
• Додаткові підтвердження стосовно доцільності ви-користання ІАПФ одержано в РКД, що включали паці-єнтів із низькою ФВЛШ, але без симптомів СН (так зва-ною асимптомною лівошлуночковою систолічною дис-функцією); а також у трьох великих (5966 пацієнтів) РКД за участю пацієнтів із СН або лівошлуночковою систо-лічною дисфункцією (чи з обома цими станами) після ін-фаркту міокарда (ІМ). У дослідженні SOLVD-Prevention (4228 пацієнтів з асимптомною лівошлуночковою сис-толічною дисфункцією) ЗВР смерті чи необхідності госпі-талізації з приводу СН становило 20%. У дослідженнях з вивчення ІМ, у яких використовували каптоприл (SAVE), раміприл (AIRE) і трандолаприл (TRACE), спостерігалося ЗВР смерті на 26% та ЗВР смерті або необхідності госпі-талізації з приводу СН на 27%. Також було показано, що ІАПФ знижують ризик ІМ у пацієнтів із СН чи без неї без-відносно до ФВЛШ.
• ІАПФ іноді спричиняють погіршення функції нирок, гіперкаліємію, симптоматичну гіпотензію, кашель, зрід-ка – ангіоневротичні набряки. Тому ці лікарські засоби (ЛЗ) слід застосовувати лише у пацієнтів з адекватною функцією нирок та концентрацією калію в крові у межах норми.
Групи пацієнтів, яким необхідно призначати ІАПФ Показання за результатами РКД:
• ФВЛШ ≤ 40% незалежно від наявності симптомів.
Протипоказання
• Ангіоневротичні набряки в анамнезі. • Двобічний стеноз ниркових артерій.
• Концентрація калію в крові > 5,0 ммоль/л.
• Рівень креатиніну в крові > 220 мкмоль/л (~ 2,5 мг/ дл).
• Виражений аортальний стеноз.
Принципи використання ІАПФ при СН
Початок терапії
• Перевірити функцію нирок і концентрацію електро-літів у крові.
• Провести повторне обстеження протягом 1-2 тиж після початку лікування.
Титрування дози
• Розглянути доцільність титрування дози після 2-4 тиж лікування. Не підвищувати дозу за суттєвого погір-шення ниркової функції чи при гіперкаліємії. Повторно перевірити функцію нирок і рівень електролітів у крові через 1 і 4 тиж після підвищення дози. Більш швидке ти-трування може проводитися за умови гарної переноси-мостітаможливостіздійсненняретельногомоніторингу. • За відсутності протипоказань слід намагатися до-сягти цільової (за даними доказової медицини) чи мак-
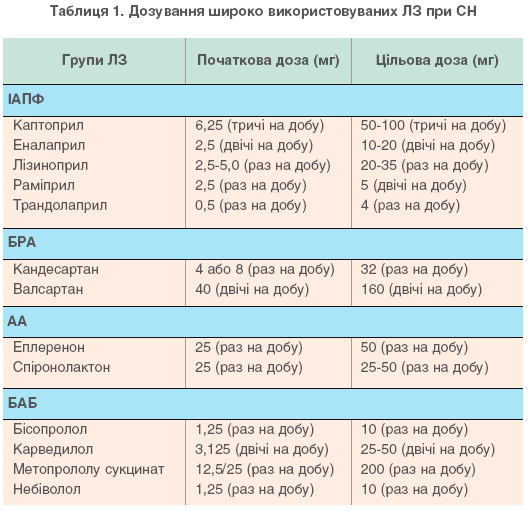
симально переносимої дози (табл.1).
• Повторно перевіряти функцію нирок і рівень елек-тролітів у крові через 1, 3 і 6 міс після досягнення підтри-мувальної дози та кожні 6 міс надалі.
Потенційні побічні реакції
• Погіршення ниркової функції. Деяке підвищення рівня сечовини (азоту сечовини в крові) та креатиніну є очікуваним після початку терапії ІАПФ і не вважається клінічно значущим, якщо відбувається повільно й на не-значнувеличину.Слідперевірити,чиприймаєпацієнтЛЗ із можливою нефротоксичною дією (наприклад, несте-роїдні протизапальні засоби). За необхідності потрібно знизити дозу ІАПФ або припинити його вживання. Зрос-таннярівнякреатинінудо50%відвихідногоабодоабсо-лютної концентрації 265 мкмоль/л (~ 3 мг/дл) є прийнят-ним.Якщорівенькреатинінуперевищує265мкмоль/л(~ 3,0мг/дл),аленижче310мкмоль/л(~3,5мг/дл),слідзни-зити дозу ІАПФ удвічі і в подальшому здійснювати моні-торинг біохімічних показників крові. Якщо рівень креа-тиніну зростає до 310 мкмоль/л (~ 3,5 мг/дл) або вище, необхіднонегайноприпинитивживанняІАПФірозпоча-тиретельниймоніторингбіохімічнихпоказниківкрові.
• Гіперкаліємія. Слід з’ясувати, чи приймає пацієнт інші ЛЗ, що можуть спричинити гіперкаліємію (напри-клад, калійвмісні добавки чи калійзберігаючі діурети-ки, такі як амілорид), та припинити їх вживання. Якщо концентрація калію зростає понад 5,5 ммоль/л, потріб-но знизити дозу ІАПФ удвічі і в подальшому здійснювати моніторинг біохімічних показників крові. Якщо рівень калію перевищує 6,0 ммоль/л, необхідно негайно при-пинити вживання ІАПФ та розпочати ретельний моніто-ринг біохімічних показників крові.
• Симптоми гіпотензії (наприклад, запаморочення) є поширеними побічними реакціями і зникають з часом, про що слід запевнити пацієнтів. Необхідно розгляну-ти доцільність зниження дози діуретиків або інших гі-потензивних ЛЗ (за винятком блокаторів рецепторів ан-гіотензину [БРА], БАБ, антагоністів альдостерону [АА]). Асимптомна гіпотензія не потребує втручань.
• Кашель. Якщо ІАПФ спричиняють кашель, який не-покоїть пацієнтів, потрібно перейти на вживання БРА.
β-Адреноблокатори
Окрім випадків протипоказань або непереносимос-ті, БАБ потрібно використовувати в усіх пацієнтів із симп-томами СН та ФВЛШ ≤ 40%. Блокада β-адренорецепторів покращує функцію шлуночків серця і самопочуття паці-єнтів, знижує частоту госпіталізації з приводу прогресу-вання СН, а також підвищує виживаність. Якщо це мож-ливо, у госпіталізованих хворих лікування БАБ слід по-чинати під пильним наглядом ще перед виписуванням зі стаціонару.
Клас рекомендацій І, рівень доказовості А
Ключові докази
- Більшість РКД, що включали пацієнтів із СН, стосу-валися вивчення ефективності БАБ, а не ІАПФ.
- У трьох ключових дослідженнях (CIBIS II, COPERNICUS і MERIT-HF) близько 9000 пацієнтів з СН різної тяжкості рандомізували на прийом плацебо чи БАБ (бісопроло-лу, карведилолу або метопрололу сукцинату CR). Понад 90% пацієнтів уживали ІАПФ або БРА. Переважна біль-шість хворих також отримували діуретики, частина – ди-гоксин.
- У всіх трьох згаданих дослідженнях показано, що лі-кування БАБ знижувало смертність (ЗВР приблизно на 34% у кожному дослідженні) та частоту госпіталізації з приводу прогресування СН (ЗВР на 28-36%) протягом близько 1 року після початку терапії. Також спостеріга-лося підвищення оцінки пацієнтами якості їхнього жит-тя у дослідженнях COPERNICUS і MERIT-HF. Вказана ко-ристь від застосування БАБ була додатковою до користі від стандартного лікування, з ІАПФ включно.
- ЗАР смертності (після 1 року лікування) у пацієнтів зі ступенем тяжкості СН від легкого до тяжкого (комбіно-вані дані досліджень CIBIS II і MERIT-HF) становило 4,3% при ХНП 23 (для 1 відстроченого випадку смерті через 1 рік). Аналогічні показники для тяжкої СН (COPERNICUS) становили відповідно 7,1% для ЗАР і 14% для ХНП.
- Ці результати підтверджуються даними іншо-го плацебо-контрольованого РКД (SENIORS) за участю 2128 літніх (≥ 70 років) пацієнтів, 36% з яких мали ФВЛШ > 35%. Терапія небівололом сприяла ЗВР первинної ком-бінованої кінцевої точки (смерті або госпіталізації з при-воду серцево-судинних причин) на 14%.
- Вищезазначеніданібулотакожпідтвердженорезуль-татами програми з вивчення карведилолу (US carvedilol studies), метааналізу інших невеликих досліджень БАБ, а такожплацебо-контрольованогоРКДна1959пацієнтахіз ФВЛШ≤0,40післягострогоІМ,уякомуЗВРсмертностіна тлі прийому карведилолу становило 23% протягом пері-одуспостереженнявсередньому1,3року.
- В одному великому РКД (BEST) з вивчення буциндо-лолу (БАБ із властивостями часткового агоніста) не ви-явлено суттєвого зниження смертності, хоча його ре-зультати загалом узгоджувалися з даними вищезгада-них досліджень.
- Результати РКД COMЕТ засвідчили, що карведилол підвищував виживаність порівняно з метопрололу тар-тратом короткої дії (який відрізняється від лікарських форм тривалої дії на основі сукцинату, що використову-валися у MERIT-HF).
- Терапію БАБ здебільшого призначають пацієнтам, які знаходяться у стабільному стані. Особам із деком-пенсацією СН, що розвинулася недавно, БАБ потрібно призначати з обережністю, в умовах стаціонару. У до-слідженні COPERNICUS було продемонстровано безпеч-ність призначення БАБ таким хворим.
- У пацієнтів, госпіталізованих з приводу прогресу-вання СН, може знадобитися зниження дози БАБ. У тяж-ких випадках можна тимчасово припинити використан-ня БАБ. Терапію БАБ у низьких дозах та титрування дози слід розпочинати відразу ж після нормалізації клінічно-го стану пацієнта, краще перед виписуванням зі стаціо-нару.
- Групи пацієнтів, яким необхідно призначати БАБ
Показання за результатами РКД:
- ФВЛШ ≤ 40%.
- Ступінь тяжкості симптомів від легкого до тяжкого (функціональний клас [ФК] за критеріями Нью-Йоркської асоціації серця [NYHA] II-IV); пацієнтам з асимптомною лівошлуночковою систолічною дисфункцією після ІМ та-кож показано БАБ.
- Досягнення оптимальної дози ІАПФ та/або БРА (а також АА, якщо їх було призначено).
- Стан хворих має бути клінічно стабільним (напри-клад, упродовж останнього часу не було змін у дозуван-ні діуретика).
- Обережний початок терапії БАБ можливий у пацієнтів, у яких нещодавно розвинулася декомпенса-ція СН, перед виписуванням зі стаціонару за умови, що їхній стан покращено за допомогою інших препаратів, вони не залежать від лікування внутрішньовенним іно-тропним ЛЗ і за ними буде встановлено нагляд протягом принаймні 24 год після початку терапії БАБ.
Протипоказання
• Бронхіальна астма (хронічне обструктивне захво-рювання легень не є протипоказанням).
• Серцева блокада II чи III ступеня, синдром слабкості синусового вузла (за відсутності постійного водія ритму серця), синусова брадикардія (< 50 уд/хв).
Принципи використання БАБ при СН
Початок терапії
• Початкова доза: бісопрололу 1,25 мг раз на добу, карведилолу 3,125-6,25 мг двічі на добу, метопрололу CR/XL 12,5-25 мг раз на добу чи небівололу 1,25 мг раз на добу (під амбулаторним наглядом).
• З обережністю можна починати терапію БАБ у паці-єнтів, у яких нещодавно розвинулася декомпенсація СН, перед виписуванням їх зі стаціонару.
Титрування дози
• Кожні 2-4 тиж необхідно проводити титрування дози БАБ (у деяких пацієнтів слід застосовувати повіль-ніше титрування). Не потрібно підвищувати дозу БАБ, якщо під час кожної наступної консультації спостеріга-ються ознаки прогресування СН, симптоми гіпотензії
(наприклад, запаморочення) або виражена брадикардія (< 50 уд/хв).
• За відсутності протипоказань слід підвищувати дозу БАБ удвічі під час кожної наступної консультації до досягнення цільової дози з доведеною ефективніс-тю (бісопрололу 10 мг раз на добу, карведилолу 25-50 мг двічі на добу, метопрололу CR/XL 200 мг раз на добу або небівололу 10 мг раз на добу) чи максимально перено-симої (див. табл.1).
Потенційні побічні реакції
• Симптоми гіпотензії, як правило, з часом зникають. Доцільно розглянути необхідність зниження дози інших гіпотензивних ЛЗ (окрім ІАПФ/БРА), наприклад діурети-ків, нітратів. Асимптомна гіпотензія не потребує втру-чань.
• Прогресування СН. За можливості потрібно підви-щити дозу діуретика (часто це лише тимчасова необхід-ність) і продовжити терапію БАБ (можливо, у більш низь-ких дозах).
• Виражена брадикардія. Слід провести електрокар-діографію (або амбулаторний моніторинг за необхіднос-ті), аби виключити серцеву блокаду. Необхідно припи-нити вживання глікозидів дигіталісу, якщо їх було рані-ше призначено. Може знадобитися зниження дози або припинення прийому БАБ.
Антагоністи альдостерону
Окрім випадків протипоказань або непереносимос-ті, АА у низьких дозах додатково призначають усіх паці-єнтам із ФВЛШ ≤ 35% і тяжкою СН (тобто при ФК III або IV за NYHA) за відсутності гіперкаліємії та суттєвої нирко-вої дисфункції. АА знижують частоту госпіталізації з при-воду прогресування СН та підвищують виживаність при додаванні до поточної терапії, з ІАПФ включно. У госпі-талізованих пацієнтів, які відповідають вищезгаданим критеріям, лікування АА необхідно розпочинати перед виписуванням зі стаціонару.
Клас рекомендацій І, рівень доказовості В
Ключові докази
• З метою дослідження ефективності АА спіроно-лактону було проведено одне велике РКД (RALES), яке включало пацієнтів із тяжкою СН.
• У дослідженні RALES 1663 пацієнтів із ФВЛШ = 35% і ФК ІІІ за NYHA (які мали ФК IV протягом останніх 6 міс) було рандомізовано на прийом плацебо чи спіронолак-тону 25-50 мг 1 раз на добу додатково до стандартного лікування, що включало діуретик, ІАПФ (95%) і дигоксин (74%). У час, коли проводилося це дослідження, БАБ ши-роко не використовувалися для терапії СН, тому тільки 11% пацієнтів було призначено лікування цими препа-ратами.
• Застосування спіронолактону приводило до ЗВР смерті на 30% та госпіталізації з приводу прогресування СН на 35% у середньому протягом 2 років після початку терапії. Спіронолактон також покращував ФК за NYHA. Указана користь була додатковою до користі від стан-дартного лікування, з ІАПФ включно.
• ЗАР смертності (у середньому після 2 років лікуван-ня) у пацієнтів із тяжкою СН становило 11,4% при ХНП 9 (для відстрочення 1 випадку смерті через 2 роки).
• Вищенаведені результати підтверджуються даними іншого РКД (EPHESUS), до якого було залучено 6632 па-цієнтів із ФВЛШ ≤ 40% та СН або цукровим діабетом че-рез 3-14 днів після гострого ІМ. Пацієнтів було рандомі-зовано на прийом плацебо чи еплеренону 25-50 мг що-денно додатково до стандартного лікування, що вклю-чало ІАПФ/БРА (87%) і БАБ (75%). Терапія еплереноном приводила до ЗВР смерті на 15%.
• Спіронолактон і еплеренон можуть спричиняти гі-перкаліємію й погіршення ниркової функції. Такі побічні реакції не часто спостерігалися під час проведення РКД, однак є непоодинокими у звичайній клінічній практи-ці, особливо в людей літнього віку. Обидва ЛЗ слід вико-ристовувати лише у пацієнтів із належною функцією ни-рок і нормальною концентрацією калію в сироватці кро-ві. При використанні цих ЛЗ обов’язковим є моніторинг концентрації електролітів у крові та ниркової функції.
• У чоловіків спіронолактон також може викликати неприємні відчуття у грудних залозах та їхнє збільшення (за даними RALES – у 10% порівняно з плацебо). Ця по-бічна реакція спостерігається нечасто при використанні еплеренону. Тому, крім призначення у постінфарктний період, основним показанням для використання епле-ренону в чоловіків є дискомфорт у грудних залозах та їхнє збільшення, спричинені спіронолактоном.
Групи пацієнтів, яким слід призначати АА
Показання за результатами РКД:
• ФВЛШ ≤ 35%.
• Помірні або тяжкі симптоми (ФК III-IV за NYHA).
• Оптимальна доза БАБ та ІАПФ або БРА (але не одно-часно ІАПФ + БРА).
Протипоказання
• Концентрація калію в крові > 5,0 ммоль/л.
• Рівень креатиніну в крові > 220 мкмоль/л (~ 2,5 мг/ дл).
• Супутній прийом калійзберігаючих діуретиків або калійвмісних добавок.
• Комбінація ІАПФ і БРА.
Принципи використання спіронолактону (або еплеренону) при СН
Початок терапії
• Перевірити функцію нирок і рівень електролітів у крові.
• Початкова доза спіронолактону (або еплеренону) – 25 мг/добу.
• Повторно перевірити функцію нирок і рівень елек-тролітів у крові через 1 і 4 тиж після початку лікування.
Титрування дози
• Розглянути доцільність титрування дози після 4-8 тиж лікування. Не підвищувати дозу в разі погіршення
ниркової функції чи при гіперкаліємії. Повторно переві-рити функцію нирок і рівень електролітів у крові через 1 і 4 тиж після підвищення дози.
• За відсутності протипоказань намагатися досягну-ти цільової дози з доведеною ефективністю (спіроно-лактону 50 мг/добу чи еплеренону 50 мг/добу) або мак-симально переносимої (див. табл.1).
• Повторно перевіряти функцію нирок і концентра-цію електролітів у крові через 1, 2, 3 і 6 міс після досяг-нення підтримувальної дози, а також кожні 6 міс надалі.
Потенційні побічні реакції
• Гіперкаліємія. Якщо рівень калію перевищує 5,5 ммоль/л, слід знизити дозу спіронолактону (чи еплере-нону) вдвічі, наприклад до 25 мг через день, і ретельно моніторувати біохімічні показники крові. Якщо рівень калію сягає 6,0 ммоль/л, необхідно негайно припини-ти прийом спіронолактону (чи еплеренону) та проводи-ти ретельний моніторинг біохімічних показників крові; може знадобитися специфічне лікування гіперкаліємії.
• Погіршення ниркової функції. Якщо рівень креа-тиніну перевищує 220 мкмоль/л (~ 2,5 мг/дл), потрібно знизити дозу спіронолактону (чи еплеренону) вдвічі, на-приклад до 25 мг через день, і ретельно моніторувати бі-охімічні показники крові. Якщо рівень креатиніну сягає > 310 мкмоль/л (~ 3,5 мг/дл), необхідно негайно припи-нити прийом спіронолактону (чи еплеренону) і ретель-но моніторувати біохімічні показники крові; може зна-добитися специфічне лікування ниркової дисфункції.
• Болючість та/або збільшення грудних залоз. Слід перейти зі спіронолактону на еплеренон.
Блокатори рецепторів ангіотензину
За винятком випадків протипоказань і непереноси-мості, БРА рекомендовано пацієнтам із СН та ФВЛШ ≤ 40%, у яких симптоми зберігаються незважаючи на за-стосування ІАПФ і БАБ, окрім випадків супутнього при-йому АА. Лікування БРА покращує шлуночкову функцію і самопочуття пацієнтів, а також знижує частоту госпіталі-зації з приводу прогресування СН.
Клас рекомендацій І, рівень доказовості A
Лікування знижує ризик смерті внаслідок серцево-судинної патології.
Клас рекомендацій IIa, рівень доказовості B
БРА можуть використовуватися як альтернатива у хворих із непереносимістю ІАПФ. У таких пацієнтів БРА знижують ризик смерті внаслідок серцево-судинних за-хворювань і частоту госпіталізації з приводу прогресу-вання СН. У госпіталізованих пацієнтів лікування БРА слід починати ще перед виписуванням зі стаціонару.
Клас рекомендацій I, рівень доказовості B
Kлючові докази
• У двох ключових плацебо-контрольованих РКД (Val-HеFT і CHARM-Added) близько 7600 пацієнтів з СН різної тяжкості рандомізували на прийом плацебо чи БРА (валсартану і кандесартану). Крім того, ІАПФ прийма-ли 93% пацієнтів у Val-HeFT та всі хворі у CHARM-Added. БАБ було призначено 35% пацієнтів у Val-HeFT і 55% – у CHARM-Added. Спіронолактон використовували 5% па-цієнтів у Val-HeFT і 17% – у CHARM-Added.
• В обох згаданих дослідженнях лікування БРА знижу-вало частоту госпіталізації з приводу прогресування СН (ЗВР на 24% у Val-HeFT і на 17% у CHARM-Added), але не загальну частоту госпіталізації. При лікуванні кандесар-таном у CHARM-Added спостерігалося ЗВР смерті вна-слідок серцево-судинної патології на 16%. Указана ко-ристь від застосування БРА була додатковою до корис-ті від стандартного лікування, що включало, зокрема, ді-уретик, дигоксин, ІАПФ і БАБ.
• У дослідженні CHARM-Added показано ЗАР первин-ної комбінованої кінцевої точки «смертність–захворю-ваність» на 4,4% у пацієнтів з СН різної тяжкості; показ-ник ХНП становив відповідно 23 (для відстрочення 1 ви-падку в середньому через 41 міс). У Val-HeFT ЗАР стано-вило 3,3% при ХНП 30 (для відстрочення 1 випадку в се-редньому більш ніж через 23 міс).
• У дослідженнях CHARM і Val-HeFT також показано, що БРА зменшували вираженість симптомів і покращу-вали якість життя. В інших дослідженнях продемонстро-вано, що ці ЛЗ підвищували фізичну активність пацієнтів. • CHARM-Alternative – плацебо-контрольоване РКД
з вивчення кандесартану на 2028 пацієнтах із ФВЛШ ≤40%, у яких спостерігалася непереносимість ІАПФ. Лі-кування кандесартаном приводило до ЗВР щодо смерт-ності внаслідок серцево-судинної патології на 23% або частоти госпіталізації з приводу прогресування СН на 7%, при цьому показник ХНП становив 14 (після 34 міс спостереження).
• Додаткові докази щодо застосування БРА одержа-но у VALIANT – РКД, у якому 14 703 пацієнти з СН, ліво-шлуночковою систолічною дисфункцією або з обидвома цими станами після гострого ІМ приймали каптоприл, валсартан або їхню комбінацію. Ще одне подібне дослі-дження – OPTIMAAL не виявило переваг лозартану над каптоприлом.
Групи пацієнтів, яким слід призначати БРА
Показання за результатами РКД:
• ФВЛШ ≤ 40%.
• Як альтернатива у пацієнтів із СН різної тяжкості (ФК II-IV за NYHA), у яких спостерігається непереноси-мість ІАПФ.
• У пацієнтів із симптомами, що зберігаються (ФК II-IV за NYHA) незважаючи на лікування ІАПФ і БАБ.
• БРА можуть спричиняти погіршення ниркової функ-ції, гіперкаліємію і симптоми гіпотензії подібно до ІАПФ, однак вони не викликають кашлю.
Протипоказання
• Такі само, як і для ІАПФ, окрім ангіоневротичного набряку.
• Прийом ІАПФ і АА.
• БРА слід застосовувати тільки у пацієнтів з адек-ватною нирковою функцією і нормальною концентра-
цією калію в крові. Обов’язковим є моніторування рів-ня електролітів у крові та функції нирок, особливо якщо БРА певний час приймалися разом з ІАПФ.
Принципи використання БРА при СН
Початок терапії
• Перевірити функцію нирок і рівень електролітів у крові.
• Початкова доза: кандесартану 4-8 мг/добу чи вал-сартану 40 мг двічі на добу.
• Повторно перевірити функцію нирок і рівень елек-тролітів у крові протягом 1 тиж після початку лікування.
Титрування дози
• Розглянути доцільність титрування дози після 2-4 тиж лікування. Не підвищувати дозу в разі погіршення ниркової функції або при гіперкаліємії. Повторно пере-вірити функцію нирок і рівень електролітів у крові через 1 і 4 тиж після підвищення дози.
• За відсутності протипоказань намагатися досягти цільової дози з доведеною ефективністю (кандесартану 32 мг/добу чи валсартану 160 мг двічі на добу) або мак-симально переносимої (див. табл.1).
• Повторно перевіряти функцію нирок і рівень елек-тролітів у крові через 1, 3 і 6 міс після досягнення підтри-мувальної дози та кожні 6 міс надалі.
Потенційні побічні реакції
Такі само, як і для ІАПФ, за винятком кашлю.
Гідралазин та ізосорбіду динітрат
У пацієнтів із симптомами СН при ФВЛШ ≤ 40% ком-бінація гідралазину та ізосорбіду динітрату (Г+ІД) може використовуватися як альтернатива при непереноси-мості ІАПФ і БРА. Призначення Г+ІД може бути доціль-ним у пацієнтів із симптомами, що зберігаються незва-жаючи на лікування ІАПФ, БАБ і БРА (чи АА). Лікування Г+ІД у таких пацієнтів може знизити ризик смерті.
Клас рекомендацій IIa, рівень доказовості B
ЛЗ знижують частоту госпіталізації з приводу прогресування СН.
Клас рекомендацій IIa, рівень доказовості B
ЛЗ покращують функції шлуночків серця та під-вищують фізичну активність.
Клас рекомендацій IIa, рівень доказовості A
Kлючові докази
• У двох плацебо-контрольованих (V-HeFT-I і A-HeFT) та одному активно контрольованому (V-HeFT-II) РКД ви-вчали ефективність комбінації Г+ІД.
•УV-HeFTI642чоловіківбулорандомізованонапри-йом плацебо, празозину або Г+ІД на додаток до призначення діуретика чи дигоксину. Жоден із учасників дослі-дженнянелікувавсяБАБчиІАПФ.Показникисмертності невідрізнялисяугрупіплацебоіпразозину.Призастосу-ванні Г+ІД спостерігалася тенденція до зниження смерт-ності від усіх причин протягом усього періоду спостере-ження (у середньому 2,3 року): ЗВР становило 22%, ЗАР – 5,3%, ХНП – 19. Комбінація Г+ІД підвищувала здатність дофізичноїактивностійФВЛШпорівнянозплацебо.
• В A-HeFT 1050 афроамериканських чоловіків і жінок із ФК III і IV за NYHA було рандомізовано на прийом пла-цебо чи Г+ІД. Крім того, хворі приймали діуретик (90%), дигоксин (60%), ІАПФ (70%), БРА (17%), БАБ (74%) чи спі-ронолактон (39%). Дослідження було завершено перед-часно, після періоду спостереження тривалістю 10 міс, оскільки отримані результати показали суттєве знижен-ня смертності (ЗВР становило 43%, ЗАР – 4,0%, ХНП – 25). Комбінація Г+ІД також знижувала частоту госпіталізації з приводу СН (ЗВР на 33%) і покращувала якість життя пацієнтів.
• У V-HeFT-II 804 чоловіків, в основному з ФК II і III за NYHA, було рандомізовано на прийом еналаприлу або Г+ІД. Окрім того, пацієнти отримували діуретик чи ди-гоксин. Жоден із учасників дослідження не вживав БАБ. Спостерігалася тенденція до підвищення смертності від усіх причин протягом усього періоду спостереження (у середньому 2,5 рокy): відносне зростання ризику стано-вило 28%.
• Найпоширенішими побічними реакціями на Г+ІД у згаданихдослідженняхбулиголовнийбіль,запаморочен-ня/гіпотензіяінудота.УV-HeFTIіIIартралгія,щовимагала відміниЛЗабозниженнядози,виникалау5-10%пацієнтів, астійкезростаннятитруантинуклеарнихантитіл–у2-3% (протевовчаковийсиндромспостерігавсярідко).
Групи пацієнтів, яким слід призначати Г+ІД
Показання за результатами РКД:
• Як альтернатива до ІАПФ/БРА, коли пацієнти не пе-реносять обидві ці групи ЛЗ.
• Як додаткова терапія при застосуванні ІАПФ, якщо пацієнти не переносять БРА чи АА.
• Найбільшу ефективність показано у пацієнтів афро-американського походження.
Протипоказання
• Симптоми гіпотензії.
• Вовчаковий синдром.
• Тяжка ниркова недостатність (може виникнути по-треба у зниженні дози).
Принципи використання Г+ІД при СН
Початок терапії
Початкова доза: гідралазину 37,5 мг та ізосорбіду ди-нітрату 20 мг тричі на добу.
Титрування дози
• Розглянутидоцільністьтитруваннядозипісля2-4тиж лікування.Непідвищуватидозуприсимптомахгіпотензії.
• При переносимості ЛЗ намагатися досягти цільо-вої дози з доведеною ефективністю (гідралазину 75 мг та ізосорбіду динітрату 40 мг тричі на добу) або макси-мально переносимої.
Потенційні побічні реакції
• Симптоми гіпотензії (наприклад, запаморочення), як правило, з часом минають. Слід оцінити доцільність зниження дози інших гіпотензивних ЛЗ (за винятком ІАПФ, БРА, БАБ, АА). Асимптомна гіпотензія не потребує втручань.
• При виникненні артралгії/болю в м’язах, набряків, перикардиту/плевриту, висипу чи лихоманки необхідно провести діагностику з метою виявлення медикамен-тозного вовчакового синдрому; перевірити наявність антинуклеарних антитіл і припинити застосування Г+ІД.
Дигоксин
У пацієнтів із симптомами СН і миготливою аритмі-єю (МА) дигоксин може використовуватися для сповіль-нення прискореного серцевого ритму. У хворих із МА і ФВЛШ ≤ 40% цей ЛЗ слід застосовувати для контролю серцевого ритму додатково до БАБ або навіть перед призначенням останніх.
Клас рекомендацій I, рівень доказовості C
У пацієнтів із синусовим ритмом, симптомами СН і ФВЛШ ≤ 40% лікування дигоксином (додатково до ІАПФ) покращує шлуночкову функцію і самопочуття, знижує частоту госпіталізації з приводу прогресування СН, але не впливає на виживаність.
Клас рекомендацій IIa, рівень доказовості B
Ключові докази
Дигоксин у пацієнтів із СН і МА
• Дигоксин є корисним для початкового контролю шлуночкового ритму у пацієнтів з пароксизмами МА, а також може призначатися при декомпенсованій СН пе-ред застосуванням БАБ.
• У довготривалій перспективі БАБ – самостійно чи в комбінації з дигоксином – є терапією вибору для контр-олю серцевого ритму (та отримання інших позитивних результатів) у пацієнтів із ФВЛШ ≤ 40%.
• Хоча монотерапія дигоксином дозволяє контролю-вати ритм скорочення шлуночків у спокої (цільовий рі-вень – 80 уд/хв), зазвичай вона не забезпечує достатньо-го контролю серцевого ритму під час фізичних наванта-жень (цільовий рівень – ≤ 110-120 уд/хв).
• У пацієнтів із ФВЛШ > 40% верапаміл або дилтіазем можутьвикористовуватисяокремочивкомбінаціїздигок-синомдляконтролюритмускороченняшлуночківсерця.
Дигоксин у пацієнтів із СН, ФВЛШ ≤ 40% і синусовим ритмом
• Було проведено одне велике проспективне РКД із вивчення дигоксину у хворих із СН і низькою ФВЛШ.
• У дослідженні DIG 6800 пацієнтів із ФВЛШ ≤ 45% і ФК II-IV за NYHA, які отримували терапію діуретиком чи ІАПФ, було рандомізовано на прийом плацебо або ди-гоксину (0,25 мг/добу). На час проведення цього дослі-дження БАБ для лікування СН широко не застосовува-лися.
• Лікування дигоксином не впливало на смертність від усіх причин, але приводило до ЗВР госпіталізації з приводу прогресування СН на 28% протягом у серед-ньому 3 років після початку терапії. При цьому ЗАР ста-новило 7,9% відповідно до ХНП 13 (для відстрочення 1 випадку госпіталізації через 3 роки).
• Вищенаведені дані узгоджуються з результатами метааналізу, але абсолютно не підтверджуються дослі-дженням DIG, у якому якість життя не покращувалася й не було відмічено користі від лікування у пацієнтів з СН зі збереженою ФВ.
• Дигоксин може спричиняти передсердні та шлу-ночкові аритмії, особливо за наявності гіпокаліємії, тому в таких пацієнтів необхідно моніторувати концентрацію електролітів у крові та ниркову функцію.
Групи пацієнтів із СН, яким слід призначати дигоксин
Показання за результатами РКД:
1. МА:
• Частота скорочень шлуночків у спокої > 80, а при фізичному навантаженні > 110-120 уд/хв.
2. Синусовий ритм:
• Лівошлуночкова систолічна дисфункція (ФВЛШ ≤ 40%).
• Ступінь вираженості симптомів від легкого до тяж-кого (ФК II-IV за NYHA).
• Досягнуто оптимальної дози ІАПФ та/або БРА, БАБ і АА (якщо вони призначалися).
Протипоказання
• Атріовентрикулярна блокада ІІ чи ІІІ ступеня (за від-сутності постійного водія ритму). Необхідно бути обе-режними при підозрі на синдром слабкості синусового вузла.
• Синдроми передчасного збудження.
• Випадки непереносимості дигоксину в анамнезі.
Принципи використання дигоксину при СН
Початок терапії
• Початкова доза: навантажувальні дози зазвичай не потрібні у пацієнтів із синусовим ритмом, що перебува-ють у стабільному стані. Добова однократна доза 0,25 мг широко використовується в дорослих з нормальною функцією нирок. У людей літнього віку та осіб із нир-ковою недостатністю дозу слід знижувати до 0,125 чи 0,0625 мг/добу.
• Концентрацію дигоксину в крові треба моніторува-ти від самого початку тривалої терапії, навіть у пацієнтів із нормальною нирковою функцією. За наявності ознак ураженння нирок досягнення стабільного стану може потребувати довшого часу.
• Не існує доказів того, що регулярне вимірювання концентрації дигоксину дозволяє досягти кращих ре-зультатів лікування. Терапевтична концентрація дигок-сину в сироватці крові повинна становити 0,6-1,2 нг/мл, тобто нижче, ніж рекомендувалося раніше.
• Деякі ЛЗ можуть підвищувати концентрацію дигок-сину в плазмі крові (аміодарон, дилтіазем, верапаміл, окремі антибіотики, хінідин).
Потенційні побічні реакції
• Синоатріальна й атріовентрикулярна блокади.
• Передсердні та шлуночкові аритмії, особливо за на-явності гіпокаліємії (при шлуночкових аритміях, спричи-нених токсичністю високих доз дигоксину, слід призна-чати дигоксинспецифічні антитіла).
• Симптоми отруєння дигоксином включають: по-тьмарення свідомості, нудоту, анорексію і розлади ко-льорового зору.
Діуретики
Діуретики рекомендовано пацієнтам із СН, що су-проводжується симптомами затримки рідини.
Клас рекомендацій I, рівень доказовості B
Kлючові положення
• Діуретики усувають симптоми легеневого й систем-ного венозного застою у пацієнтів із СН.
• Діуретики спричинюють активацію ренін-ангіотензин-альдостеронової системи у пацієнтів зі сла-бо вираженими симптомами СН, а тому їх слід признача-ти в комбінації з ІАПФ/БРА.
• Дозу ЛЗ визначають відповідно до індивідуальних потреб пацієнта, також слід проводити постійний лікар-ський моніторинг.
• Петльові діуретики здебільшого потрібні при по-мірно вираженій або тяжкій СН.
• Тіазиди можна застосовувати в комбінації з петльо-вими діуретиками для лікування стійких набряків, але з обережністю, уникаючи зневоднення, гіповолемії, гіпо-натріємії та гіпокаліємії.
• Протягом терапії діуретиками важливо моніторува-ти концентрацію калію, натрію і креатиніну.
Діуретики та ІАПФ/БРА/АА
• При терапії ІАПФ/БРА зменшення об’єму циркулю-ючої крові та гіпонатріємія внаслідок надмірного діуре-зу можуть підвищувати ризик виникнення гіпотензії та ниркової дисфункції.
• Якщо разом із діуретиком застосовується ІАПФ/ БРА/АА, замісна терапія препаратами калію не потрібна. • При застосуванні калійзберігаючих діуретиків, зо-крема АА, разом із ІАПФ/БРА може виникати тяжка гі-перкаліємія. Тому слід уникати призначення неальдос-теронових калійзберігаючих діуретиків. Комбінація АА й ІАПФ/БРА повинна використовуватися тільки під пиль-
ним наглядом лікаря.
Принципи використання діуретиків при СН
Початок терапії
• Перевірити функцію нирок і концентрацію електро-літів у крові.
• Більшості пацієнтів призначають петльові діурети-ки, а не тіазидні, через вищу ефективність перших щодо стимулювання діурезу і натрійурезу.
Дозування діуретиків
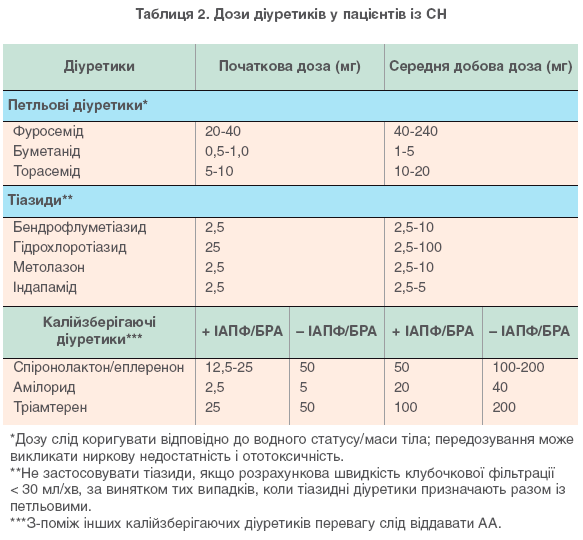
• Починати з низької дози та підвищувати її до до-сягнення зменшення вираженості симптомів застою (табл.2).
• Дозу слід коригувати, зокрема після встановлення «сухої» маси тіла пацієнта, задля уникнення ризику нир-кової дисфункції та зневоднення. Намагатися підтриму-вати сталу «суху» масу за допомогою якомога нижчої дози діуретика.
• При амбулаторному лікуванні СН пацієнт може са-мостійно коригувати дозу діуретика на основі резуль-татів щоденного вимірювання маси тіла та вираженості симптомів затримки рідини. Для цього пацієнтові необ-хідно надавати відповідну інформацію.
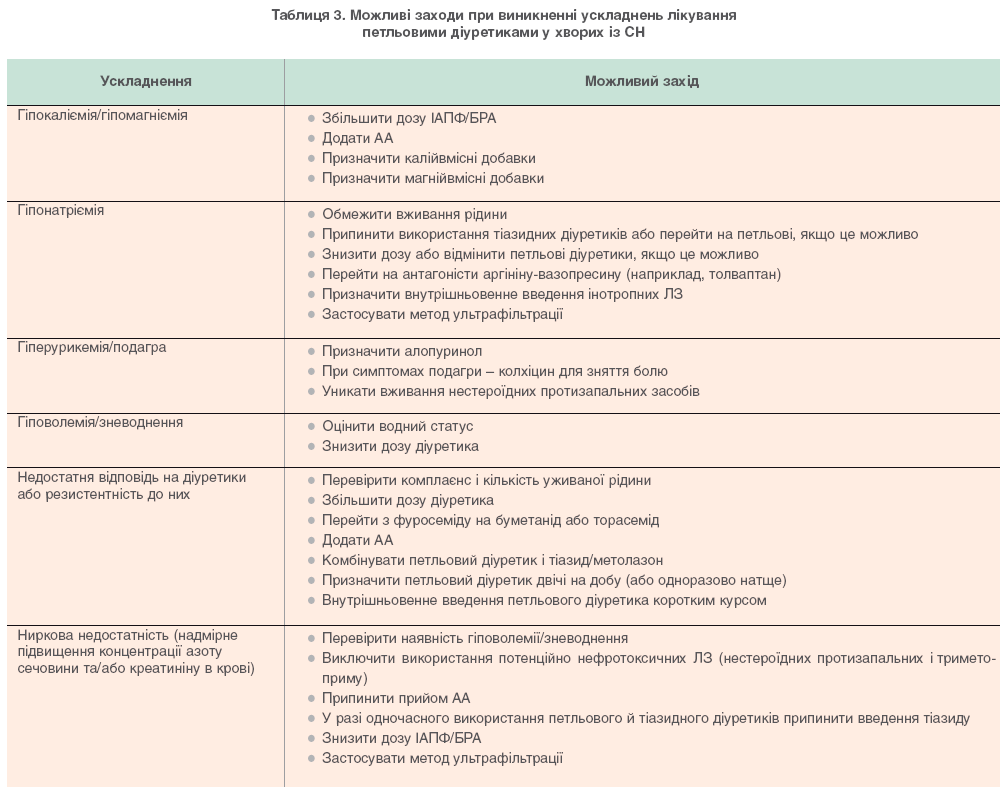
• Можливі заходи щодо усунення ускладнень при лі-куванні діуретиками наведено в табл.3
Антикоагулянти (антагоністи вітаміну К)
Варфарин (або інший альтернативний пероральний антикоагулянт) рекомендовано пацієнтам із СН і постій-ною, персистуючою чи пароксизмальною МА за відсут-ності протипоказань до призначення антикоагулянтів. Застосування антикоагулянтів в адекватній дозі знижує ризик тромбоемболічних ускладнень, у т.ч. інсульту.
Клас рекомендацій I, рівень доказовості A
Антикоагулянтну терапію також рекомендовано па-цієнтам із внутрішньосерцевим тромбом, наявність яко-го підтверджено методом візуалізації, чи з ознаками сис-темної емболії.
Клас рекомендацій І, рівень доказовості C
Ключові докази
• Докази ефективності антикоагулянтів щодо зни-ження ризику тромбоемболій у пацієнтів з МА зібрано у зведених рекомендаціях Американської колегії карді-ологів, Американської асоціації серця та Європейського товариства кардіологів.
• У серії РКД із залученням пацієнтів з МА і, зокрема, СН варфарин знижував ризик інсульту на 60-70%.
• Варфарин був ефективнішим за антитромбоцитар-ну терапію щодо зниження ризику інсульту, а також при застосуванні у пацієнтів з високим ризиком інсульту (зо-крема, в осіб із СН).
• Не існує доказів ефективності антикоагулянтної те-рапії в усіх інших пацієнтів із СН, за винятком хворих зі штучним клапаном серця.
Антитромбоцитарні ЛЗ
Ключові докази
• Антитромбоцитарні ЛЗ не є такими само ефектив-ними, як варфарин, щодо зниження ризику тромбоем-болій у пацієнтів з МА.
• В об’єднаному аналізі даних двох невеликих дослі-джень, у яких порівнювали варфарин і аспірин в осіб із СН, ризик госпіталізації з приводу СН був суттєво вищим у пацієнтів, лікованих аспірином.
• Не існує доказів того, що антитромбоцитарні ЛЗ знижують ризик атеросклерозу в пацієнтів із СН.
Інгібітори гідроксиметилглутарил-коензим-А-редук-тази (статини) У літніх пацієнтів, які страждають на СН із систолічною дисфункцією внаслідок ішемічної хворо-би серця, лікування статинами може знижувати частоту госпіталізації з приводу серцево-судинної патології.
Клас рекомендацій IIb, рівень доказовості B
Ключові докази
• У більшості проведених досліджень із використан-ням статинів не брали участі пацієнти з СН. Тільки в од-ному дослідженні – CORONA спеціально вивчали дію статинів на пацієнтах із СН ішемічного походження і зни-женою ФВ. При цьому розувастатин не знижував ризик первинної кінцевої точки (смерть унаслідок серцево-судинної патології, інсульт, ІМ) чи смертність від усіх при-чин. Частота госпіталізацій з приводу серцево-судинної патології знизилася суттєво.
• Користь статинів у пацієнтів із СН неішемічного по-ходження невідома.
Лікування хворих на СН зі збереженою ФВЛШ
• Наразі не розроблено жодної ефективної схеми лі-кування СН зі збереженою ФВЛШ, яка би забезпечувала значне покращання стану та зниження смертності. Діу-ретики використовують для контролю затримки натрію і води, а також для усунення задишки та набряків. Важ-ливим є також адекватне лікування гіпертензії та ішемії міокарда, так само як і контроль серцевого ритму в па-цієнтів з МА. У двох маломасштабних дослідженнях (< 30 пацієнтів у кожному) показано, що антагоніст кальцію верапаміл, який сповільнює серцевий ритм, може підвищувати здатність до фізичної активності і зменшувати вираженість симптомів у таких хворих.
• У дослідженні CHARM, до якого було залучено 3023 пацієнтів, не виявлено суттєвого зниження ри-зику первинної комбінованої кінцевої точки (смерть унаслідок серцево-судинних подій або госпіталізація з приводу СН), але продемонстровано значне зниження ризику госпіталізації з приводу СН. У досліджен-ні PEP-CHF за участю 850 пацієнтів не було виявлено змінщодокомбінованоїпервинноїкінцевоїточкипро-тягом усього періоду спостереження, проте засвідче-но суттєве зниження смертності внаслідок серцево-судинної патології та госпіталізації з приводу СН упро-довж 1 року.










Комментировать