Механизм действия тромболитических средств. Тромболитическая терапия. Фибринолизин. Стрептокиназа (стрептаза). Урокиназа (аббокиназа). Проурокиназа (саруплаза). АПСАК (анистреплаза). Стафилокиназа. Противопоказания к тромболитической терапии. Журнал «Медицина неотложных состояний»
3(28) 2010 / Практические рекомендации
В отличие от антитромбоцитарных препаратов, прямых и непрямых антикоагулянтов, действие которых направлено на предотвращение тромбообразования, механизм действия тромболитических средств заключается в растворении фибринового тромба. Этот тромб может как образоваться, например, в пораженной атеросклерозом артерии, так и явиться результатом эмболии. Различают тромбозы артериальные и венозные, а тромбоэмболии — системные, легочные и парадоксальные. Локализация и происхождение тромба, как, впрочем, и общее состояние больного, имеют важное значение при решении вопроса о целесообразности тромболитической терапии в каждом конкретном случае, учитывая высокую стоимость тромболитических препаратов и связанный с их применением риск развития серьезных геморрагических осложнений. Тромболитическая терапия показана в остром периоде инфаркта миокарда (ИМ), при массивной или субмассивной тромбоэмболии легочной артерии (ТЭЛА), тромбозе крупных артерий (бедренных, подколенных, подключичных и др.), а также, возможно, в первые часы после возникновения инсульта тромбоэмболического происхождения. Не рекомендуется применение тромболитических препаратов для лечения тромбоза глубоких вен нижних конечностей, так как частичный лизис венозного тромба может повысить риск развития ТЭЛА.
Венозные тромбы, как правило, легче лизируются, чем артериальные, поэтому, например, при лечении ТЭЛА требуются гораздо меньшие дозы тромболитических препаратов, чем при лечении острого ИМ, что неудивительно, учитывая, что в первом случае причиной заболевания служит венозный по происхождению тромб, в то время как во втором случае фибриновый тромб образуется в месте пораженной атеросклерозом коронарной артерии.
Тромболитическая терапия направлена на то, чтобы по возможности быстро растворить фибриновый тромб и восстановить антероградный кровоток в соответствующем органе или части его. Для этого необходимо повысить фибринолитическую активность крови больного, чего теоретически можно достигнуть двумя путями:
- введением активированного in vitro плазмина, увеличивая тем самым его содержание в крови;
- введением активаторов плазминогена, которые усиливают образование плазмина из эндогенного плазминогена.
Фибринолизин
Фибринолизин (или плазмин) — это выделенный из плазмы человека и активированный in vitro трипсином плазминоген (профибринолизин).
Клинические исследования показали, что экзогенный плазмин (препарат фибринолизин) действует медленно и недостаточно эффективен в растворении артериальных тромбов. Кроме того, он часто вызывает пирогенную и аллергическую реакцию, а также серьезные кровотечения. Тем не менее фибринолизин продолжает производиться в Украине и разрешен к клиническому применению в России, поэтому при отсутствии других, более эффективных тромболитических препаратов едва ли следует отказываться от использования фибринолизина, например, при массивной или субмассивной ТЭЛА и периферических тромбозах.
За исключением фибринолизина, применяемые в настоящее время тромболитические препараты по механизму действия являются активаторами эндогенного плазминогена.
Современные тромболитические средства можно условно разделить на 3 основные группы:
1) препараты первого поколения, которые приблизительно в одинаковой мере активируют и связанный с фибрином, и циркулирующий в крови плазминоген и имеют короткие Т1/2 (стрепто-и урокиназа);
2) препараты второго поколения, обладающие относительной специфичностью к связанному с фибрином плазминогену и более продолжительными Т1/2 (рекомбинантная проурокиназа, АПСАК — анизоилированный плазминогенстрептокиназный активаторный комплекс, рекомбинантный тканевый активатор плазминогена — ТАП, рекомбинантная стафилокиназа);
3) препараты третьего поколения, обладающие более высокой тромболитической активностью благодаря изменениям в их молекулах, которые были внесены с помощью метода генной инженерии негликозилированный рекомбинантный ТАП, химерные молекулы, содержащие различные участки ТАП и урокиназы, и др.).
Стрептокиназа (стрептаза)
Стрептокиназа — прямой активатор плазминогена. Это одноцепочечный полипептид, не содержащий углеводов, с молекулярной массой 47 000 Да, который вырабатывается из культуры бета-гемолитического стрептококка группы С (по классификации Лансфильда).
Стрептокиназа — неферментный белок, образующий стехеометрический 1 : 1 комплекс с плазмином, молекула которого при этом претерпевает конформационные изменения, приводящие к обнажению его активного центра. Комплекс «стрептокиназа — плазминоген» играет роль фермента в превращении эндогенного плазминогена в плазмин, причем он приблизительно в одинаковой степени активирует как связанные с фибриновым тромбом, так и свободные, циркулирующие в крови молекулы плазминогена. Т1/2 стрептокиназы 15–25 мин. Стрептокиназу получают из культуры бактерий, вследствие чего она обладает антигенными свойствами. В крови человека всегда обнаруживаются антитела против стрептокиназы, что связано с большой распространенностью стрептококковых инфекций в общей популяции. Титры антистрептокиназных антител быстро нарастают в течение нескольких дней после ее введения и через несколько недель достигают пика. Этот пик может в 1000 раз превышать исходные титры антител против стрептокиназы. У части больных титры антистрептокиназных антител возвращаются к исходному уровню (до ее введения) через 6 мес., однако во многих случаях титры этих антител остаются повышенными у больных, получавших стрептокиназу 2–4 года назад, обусловливая резистентность к повторному введению препарата, а также аллергические реакции.
Учитывая динамику антистрептокиназных антител, обычно не рекомендуют повторное введение стрептокиназы после проведенного лечения, а также сразу после перенесенной стрептококковой инфекции. В то же время недавно показано (М. Buchalter и соавт., 1992 г.), что в течение 72 ч после лечения стрептокиназой повторное ее введение (при необходимости) может быть эффективным и безопасным у большинства больных.
Для профилактики аллергических реакций (включая анафилактический шок) некоторые авторы рекомендуют перед введением стрептокиназы внутривенно ввести кортикостероиды (до 180–240 мг преднизолона) и/или антигистаминные препараты.
Как показывают исследования, эффективность стрептокиназы может значительно варьировать, что, по-видимому, связано с различиями в титрах антистрептокиназных антител у некоторых больных. Неудивительно поэтому, что данные литературы относительно оптимальной дозы стрептокиназы у больных острым инфарктом миокарда разноречивы. По наблюдениям J. Col и соавт. (1989 г.), эффективность 500 000 и 1 500 000 ЕД стрептокиназы примерно одинаковая. В то же время A. Six и соавт. (1990 г.) показали, что 3 000 000 ЕД стрептокиназы значительно превосходят по эффективности дозу препарата 1 500 000 ЕД, которая в настоящее время считается общепринятой.
Данные J. Col и соавт. о достаточно высокой эффективности более низких, чем обычно рекомендуемых, доз стрептокиназы представляют интерес, особенно в связи с довольно высокой стоимостью этого самого дешевого из тромболитических препаратов. Но, поскольку нельзя исключить того, что под наблюдением авторов случайно оказались больные с низкими исходными титрами антистрептокиназных антител, вопрос о наименьшей эффективной дозе стрептокиназы при остром ИМ остается открытым до проведения крупных сравнительных исследований.
В настоящее время при лечении острого ИМ стрептокиназа обычно назначается в дозе 1 500 000 ЕД, которая разводится в 100 мл изотонического раствора хлорида натрия или 5% раствора глюкозы и вводится в течение 60 мин. При более быстром введении 1 500 000 ЕД препарата (за 30 мин) эффективность тромболитической терапии, оцениваемая по проходимости инфаркт-связанной коронарной артерии, увеличивается, но при этом значительно возрастает риск развития гипотонии.
Стрептокиназа выпускается во многих странах мира под различными коммерческими названиями: «стрептаза», «кабикиназа», «авелизин», «целиаза» и др.
Урокиназа (аббокиназа)
Урокиназа является ферментом, который непосредственно превращает плазминоген в плазмин. Впервые обнаруженный в моче человека и ошибочно принятый за киназу, этот фермент был назван урокиназой. Однако, поскольку он обнаруживается также в крови, его правильнее называть активатором плазминогена урокиназного типа. Как было сказано при рассмотрении физиологических основ гемостаза, эндотелиальные клетки в норме секретируют в кровь и субэндотелиальное пространство два активатора плазминогена — тканевого и урокиназного типов.
Недавно установлено, что активатор плазминогена урокиназного типа секретируется в форме профермента, названного «проурокиназа». Это одноцепочечный гликопротеин с молекулярной массой 54 000 Да, который слабо активирует циркулирующий плазминоген, но проявляет умеренную активность в отношении плазминогена, связанного с фибриновым тромбом. Под действием плазмина и других сериновых протеаз проурокиназа легко превращается в двухцепочечную форму (урокиназу), цепи которой соединены одной дисульфидной связью. Существуют две молекулярные формы активатора плазминогена урокиназного типа: низкомолекулярная (молекулярная масса 33 000 Да) и высокомолекулярная (54 000 Да).
Обычный препарат урокиназы представляет собой низкомолекулярную форму двухцепочечного активатора плазминогена урокиназного типа, которая является результатом расщепления ее высокомолекулярной формы, вероятно, за счет аутокаталитического механизма в процессе очистки. Т1/2 урокиназы 15–20 мин. Основной путь элиминации урокиназы — ее разрушение и быстрое выведение печенью. В отличие от стрептокиназы урокиназа не вызывает образования специфических антител. Аллергические реакции при лечении урокиназой встречаются гораздо реже, чем при введении стрептокиназы.
Урокиназа выпускается под различными коммерческими названиями: «аббокиназа», «урокидан» и др.
Проурокиназа (саруплаза)
Проурокиназа, или одноцепочечный активатор плазминогена урокиназного типа, обладает высокой специфичностью в отношении связанного с фибрином плазминогена (по сравнению со стрепто-и урокиназой), а также более продолжительным T1/2.
Проурокиназу можно выделить из мочи и культуры клеток почек эмбриона человека, однако для клинического применения препарат обычно получают ДНК-рекомбинантным методом. В настоящее время выпускают две различные формы рекомбинантной проурокиназы. Негликозилированная форма рекомбинантной проурокиназы, известная под названием «саруплаза» (saruplase), с успехом используется в странах Западной Европы для лечения острого ИМ. Эффективность и безопасность саруплазы недавно была продемонстрирована в крупном исследовании PASS (Practical Applicability of Saruplase Study). В этом открытом исследовании, включавшем 1698 больных, которым саруплазу вводили в первые 6 ч после начала заболевания, отмечена низкая внутрибольничная смертность (5,4 %) и низкая частота повторного ИМ (3,8 %), геморрагического инсульта (0,5 %) и серьезных кровотечений, требующих переливания крови (1,2 %) (F. Vermeer и соавт., 1993 г.).
В США проводятся клинические испытания гликозилированной формы рекомбинантной проурокиназы (А74187) с более быстрым началом действия, чем у негликозилированной проурокиназы. По предварительным данным, 90минутная проходимость инфаркт-связанной коронарной артерии при лечении этим препаратом составляет в среднем 73 %, что выше соответствующего показателя для стрепто-и урокиназы (W. Weaver и соавт., 1994 г.).
При лечении острого ИМ рекомбинантные формы проурокиназы назначают в дозе 40–80 мг в течение 60–120 мин.
АПСАК (анистреплаза)
Анизоилированный (ацетилированный) плазминоген-стрептокиназный комплекс представляет собой неактивный эквимолярный комплекс стрептокиназы и плазминогена человека, в котором к активному центру молекулы плазминогена ковалентно присоединена ацетильная группа. Ацетилирование не влияет на способность АПСАК связываться с фибриновым тромбом, так как фибринсвязывающий центр плазминогена функционально отличается от его активного центра. АПСАК не взаимодействует с плазминогеном до тех пор, пока в результате спонтанного деацетилирования в крови не будет восстановлена его ферментативная активность. T1/2 АПСАК составляет 70–120 мин, что значительно больше, чем у стрепто или урокиназы. Благодаря более длительному T1/2 АПСАК можно назначать в виде однократного болюса. В большинстве сравнительных исследований частота 90-минутной проходимости инфарктсвязанной коронарной артерии при лечении АПСАК была выше, чем при применении стрептокиназы.
Pекомендуемая доза АПСАК для лечения острого ИМ составляет 30 мг (или 30 ЕД), которые вводят в виде внутривенного болюса в течение 2– 5 мин.
В литературе АПСАК часто называют также «анистреплаза» (anistreplase), одно из патентованных названий АПСАК — «эминаза» (eminase).
Тканевый активатор плазминогена (альтеплаза)
Тканевый активатор плазминогена представляет собой сериновую протеазу с молекулярной массой 72 000 Да, которая синтезируется преимущественно эндотелиальными клетками сосудов. В кровяное русло ТАП секретируется в виде одноцепочечной молекулы (молекулярная масса 70 000 Да), которая превращается в двухцепочечную под действием плазмина, трипсина, калликреина или фактора Ха свертывающей системы крови.
Уникальным свойством ТАП является его очень высокая избирательность в отношении связанного с фибрином плазминогена, что обеспечивает его преимущественную активацию на поверхности фибринового тромба. Правда, эта избирательность в значительной мере утрачивается, когда ТАП используется в терапевтических дозах.
ТАП не обладает антигенными свойствами и не оказывает существенного влияния на гемодинамику; пирогенные и аллергические реакции в ответ на введение ТАП встречаются редко.
ТАП выделяют из ткани матки человека и культуры клеток человеческой меланомы. В последние годы для клинического применения ТАП получают ДНК-рекомбинантным методом. В литературе препарат одноцепочечного ТАП, полученного рекомбинантным методом, получил название «альтеплаза» (alteplase), а двухцепочечный ТАП — «дутеплаза» (duteplase).
Альтеплаза выпускается под патентованными названиями «активаза» (activase) и «актилиза» (actilyse).
Экспериментальные исследования свидетельствуют о более высокой тромболитической активности ТАП по сравнению со стрепто-и урокиназой. В остром периоде ИМ комбинантный ТАП быстрее и чаще вызывает лизис окклюзирующего тромба в инфаркт-связанной коронарной артерии. ТАП более эффективно снижает раннюю смертность у больных ИМ, чем стрептокиназа, однако чаще вызывает внутричерепные кровоизлияния.
В клинической практике используется главным образом одноцепочечный рекомбинантный ТАП, или альтеплаза, T1/2 которой составляет 4–8 мин.
Для лечения острого ИМ альтеплазу обычно назначают в общей дозе 100–150 мг в течение 3 ч, причем первые 6–10 мг препарата вводят в виде болюса в течение 2 мин. В связи с тем что альтеплаза в общей дозе 150 мг часто вызывала геморрагические осложнения, а 3-часовая инфузия слишком поздно приводила к реканализации инфаркт-связанной коронарной артерии, в последние годы были предложены две новые схемы введения рекомбинантного ТАП.
К. Neuhaus и соавт. (1989 г.) предложили схему «ускоренного» введения рекомбинантного ТАП: 100 мг в течение 90 мин, причем первые 15 мг препарата вводят в виде болюса, затем начинают инфузию (50 мг за 30 мин и 35 мг за остальные 60 мин).
Схема ускоренного введения альтеплазы была успешно апробирована в одном из самых крупных из исследований по изучению эффективной тромболитической терапии при остром ИМ
GUSTOI (Global Utilization of Streptokinase and Tissue Plasminogen Activator for Occluded Coronary Arteries, 1993 г.). В исследовании GUSTO-I было показано, что при ускоренном введении рекомбинантного ТАП 30-дневная смертность на 15 % ниже, чем при лечении стрептокиназой. На 90-й минуте после начала тромболитической терапии инфаркт-связанная коронарная артерия была проходимой у 81 % больных, леченных ТАП, но лишь у 57 % больных, получавших стрептокиназу, причем полная проходимость наблюдалась в 54 и 31 % случаев соответственно. Учитывая, что при обычной схеме введения альтеплазы частота 90минутной проводимости инфаркт-связанной коронарной артерии составляет в среднем 70 %, результаты исследования GUSTO-I можно рассматривать как доказательства большей эффективности ускоренной схемы введения препарата.
Другая схема введения альтеплазы в остром периоде ИМ предложена J. Puruis и соавт. (1994 г.): препарат вводится в виде двух болюсов по 50 мг с интервалом между болюсами в 30 мин. При двухболюсной схеме назначения рекомбинантного ТАП 90минутная проходимость инфарктсвязанной коронарной артерии отмечалась у 78 из 84 (93 %) больных, причем полная проходимость в 88 % случаев.
Таким образом, новые схемы применения рекомбинантного ТАП при остром ИМ оказались значительно более эффективными, чем рекомендовавшаяся ранее схема 3-часового введения препарата.
Сравнительная характеристика основных применяемых в настоящее время тромболитических препаратов представлена в табл. 1.
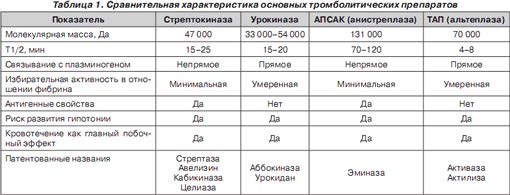
Недостатки существующих тромболитических препаратов (короткий Т1/2, недостаточная фибринолитическая активность, нередкое развитие реокклюзии и т.д.) способствовали разработке новых препаратов на основе использования ДНКрекомбинантного метода. Так была создана модифицированная (негликозилированная) форма рекомбинантного ТАП — препарат ретеплаза (reteplase) с более длительным Т1/2, чем у альтеплазы. Ретеплаза вводится в виде двух болюсов по 10 000 000 ЕД с интервалом 30 мин. В сравнительном исследовании обнаружена более высокая эффективность ретеплазы у больных острым ИМ по сравнению со стандартной схемой применения альтеплазы (100 мг за 3 ч) (W. Weaver и соавт., 1995 г.). Завершено контролируемое исследование по сравнению эффективности и безопасности ретеплазы и ускоренной схемы введения альтеплазы (100 мг за 90 мин). Смертность на 35-й день острого ИМ при лечении ретеплазой была недостоверно ниже, чем при лечении альтеплазой (4,1 и 8,4 %). Частота 90-минутной проходимости инфаркт-связанной коронарной артерии в группе больных, леченных ретеплазой, составила 83 %, что значительно больше, чем в группе больных, получавших альтеплазу (C. Bode и соавт., 1995 г.). Не было различий между ретеплазой и альтеплазой в частоте серьезных кровотечений или геморрагических инсультов. Таким образом, по предварительным данным, ретеплаза является самым эффективным тромболитическим средством из применяемых в настоящее время для лечения острого ИМ.
Стафилокиназа
Стафилокиназа представляет собой одноцепочечный белок без дисульфидных связей, состоящий из 136 аминокислот. Она секретируется некоторыми штаммами золотистого стафилококка, однако для клинического применения в настоящее время стафилокиназу получают ДНКрекомбинантным методом. От стрептокиназы стафилокиназа отличается большей фибринолитической активностью и меньшей аллергенностью.
Недавно продемонстрирована высокая эффективность стафилокиназы в отношении восстановления проходимости инфаркт-связанной коронарной артерии в остром периоде ИМ, а также при недавно возникшей тромботической окклюзии периферической артерии. Общепринятых схем введения стафилокиназы для лечения острого ИМ нет. При сравнении эффективности и безопасности стафилокиназы и рекомбинантного ТАП (альтеплазы) S. Vanderschueren и соавт. (1995 г.) использовали две схемы внутривенного введения стафилокиназы: 1) 1 мг в виде болюса, затем 9 мг в виде инфузии за 30 мин; 2) 2 мг в виде болюса, затем 18 мг в виде инфузии за 30 мин. Внутрибольничная смертность оказалась достоверно ниже в группе больных острым ИМ, получавших стафилокиназу, чем в группе больных, получавших рекомбинантный ТАП (ни одного случая смерти среди 48 больных против 5 случаев среди 52 больных; р < 0,05). Частота кровотечений, реинфарктов или повторных эпизодов ишемии миокарда была недостоверно ниже среди больных, леченных стафилокиназой. Эти данные указывают на то, что рекомбинантная стафилокиназа, повидимому, превосходит по своей эффективности рекомбинантный ТАП, а значит, и стрептокиназу, и урокиназу.
Основными показаниями к применению тромболитических препаратов являются:
1) острый ИМ (обычно в первые 4–6 ч после развития ангинозного приступа;
2) массивная или субмассивная ТЭЛА (в течение 5–14 дней);
3) периферические артериальные тромбозы;
4) тромбоз центральной вены сетчатки;
5) тромбозы других вен (тромбозы печеночных, почечных и других вен, кроме вен нижних конечностей);
6) тромбозы дополнительных сосудистых шунтов (аортокоронарных, артериовенозных шунтов для проведения гемодиализа и др.);
7) тромбоз протеза трехстворчатого клапана сердца.
Среди побочных эффектов тромболитических препаратов наибольшее значение имеют геморрагические осложнения и особенно внутричерепные кровоизлияния, которые встречаются в 0,1–1,0 % случаев. Частота внутричерепных кровоизлияний у больных острым ИМ при лечении альтеплазой выше, чем при лечении стрептокиназой, и приблизительно такая же, как при применении АПСАК.
В то же время аллергические реакции (в частности, анафилактический шок) чаще развиваются при лечении стрептокиназой или АПСАК, чем урокиназой или рекомбинантным ТАП.
По данным исследования GUSTO-I, стойкая гипотония чаще встречается при лечении стрептокиназой, чем альтеплазой.
Реокклюзия (ретромбоз) инфарктсвязанной коронарной артерии после успешной тромболитической терапии острого ИМ наблюдается приблизительно в 15–20 % случаев, хотя далеко не всегда она сопровождается развитием повторного ИМ (или рецидива). Тем не менее, как показывают данные контролируемых исследований, которые проводились до начала широкого использования тромболитических препаратов при лечении острого ИМ, частота раннего повторного ИМ после лечения стрептокиназой в 1,5–2 раза выше, чем среди больных, не получавших тромболитической терапии.
Данные литературы о частоте реокклюзии при лечении острого ИМ различными тромболитическими препаратами противоречивы. Это объясняется тем, что по этическим соображениям невозможно у многих больных проводить повторные ангиографические исследования. Лишь в 5 исследованиях оценивалась частота реокклюзии инфарктсвязанной коронарной артерии, которая была проходимой на 90й минуте после начала тромболитической терапии. Повторная коронароангиография проводилась в разные сроки острого ИМ (от 24 ч до времени выписки больного из стационара). По сводным данным, частота реокклюзии была наибольшей после лечения рекомбинантным ТАП (от 11 до 20 %, в среднем 13 %) и наименьшей после применения АПСАК (2,4 %). После применения стрептокиназы она составляла в среднем 9 %, урокиназы — 10 %. Низкую частоту реокклюзии инфаркт-связанной коронарной артерии после применения АПСАК объясняют как длительным Т1/2 , так и отсутствием избирательности к связанному с фибрином плазминогену, что приводит к снижению содержания фибриногена в крови.
В исследовании GUSTO-I не обнаружено различий в частоте реокклюзии после лечения стрептокиназой и рекомбинантным ТАП (по 5,9 %), но отмечена несколько более высокая частота реокклюзии у больных, которым одновременно подкожно вводили гепарин не менее 7 дней (6,4 %), по сравнению с больными, которым гепарин назначали в виде внутривенной инфузии в течение не менее 48 ч (5,5 %). Проходимость инфаркт-связанной коронарной артерии на 5–7й день острого ИМ составляла 72 % в группе больных, получавших гепарин в виде подкожных инъекций, и 84 % в группе больных, получавших гепарин в виде внутривенных инфузий. Эти данные указывают на то, что внутривенная гепаринотерапия улучшает позднюю проходимость инфаркт-связанной коронарной артерии после успешной тромболитической терапии.
Менее ясным представляется клиническое значение гепаринотерапии после тромболитической терапии. В исследовании GUSTOI частота повторного ИМ была значительно ниже при подкожном введении гепарина, частота серьезных кровотечений, напротив, недостоверно выше при внутривенном введении гепарина. Следовательно, после тромболитической терапии острого ИМ гепарин лучше назначать подкожно, а не внутривенно.
По сводным данным двух крупных исследований — GISSI2 (Gruppo Italiano per lo Studio della soprawivenza nell’ Infarto Miocardico, 1993 г.), добавление гепарина в виде подкожных инъекций к тромболитической терапии не улучшает клинических исходов ИМ (смертность, частота повторного ИМ), но значительно увеличивает риск развития серьезных кровотечений.
Таким образом, вопрос о целесообразности применения гепарина вместе с тромболитической терапией и аспирином в остром периоде ИМ остается открытым.
Важнейшие абсолютные и относительные противопоказания к тромболитической терапии приведены ниже.
Противопоказания к тромболитической терапии
Абсолютные противопоказания:
- острое внутреннее кровотечение;
- недавнее (до 10 дней) серьезное кровотечение из желудочно-кишечного тракта или мочеполовых путей;
- недавняя (в течение 10 дней) обширная операция, травма с возможным повреждением внутренних органов (например, после сердечнолегочной реанимации) или биопсия внутренних органов;
- недавняя (в течение 2 мес.) травма или операция на головном или спинном мозге;
- неконтролируемая артериальная гипертензия (АД выше 200/120 мм рт.ст.);
- геморрагический диатез, включая тромбоцитопению (число тромбоцитов меньше 100 000 в 1 мм3);
- геморрагический инсульт в анамнезе, остаточные явления после перенесенного инсульта;
- подозрение на расслаивающую аневризму аорты или острый панкреатит;
- аллергическая реакция на тромболитический препарат (при необходимости повторного введения стрептокиназы или АПСАК).
Относительные противопоказания:
- тяжелая артериальная гипертензия (АД 180/110 мм рт.ст. или выше);
- заболевания, сочетающиеся с повышенным риском развития кровотечения, включая тяжелые заболевания печени или почек;
- сосудистое заболевание головного мозга;
- травма головного мозга, операция на головном или спинном мозге, кровотечение из желудочно-кишечного тракта или мочеполовых путей в анамнезе;
- тромбоз глубоких вен нижних конечностей;
- наличие тромба в полостях сердца;
- острый перикардит или инфекционный эндокардит;
- диабетическая геморрагическая ретинопатия;
- обширные ожоги;
- беременность;
- переломы костей;
- предшествующая терапия стрептокиназой или АПСАК (особенно в первые 4–9 мес.), если предполагается повторное введение этих препаратов (другие тромболитические препараты не противопоказаны).
Существуют ингибиторы фибринолиза, которые являются специфическими антагонистами тромболитических препаратов. К ним относятся аминокапроновая кислота (e-аминокапроновая кислота — ЭАКК), аминометилбензойная кислота (парааминометилбензойная кислота — ПАМБК), транексамовая кислота и апротинин.
Однако ингибиторы фибринолиза следует с большой осторожностью использовать для лечения геморрагических осложнений тромболитической терапии, учитывая повышенный риск развития повторного тромбоза, особенно у больных острым ИМ. Применение ингибиторов фибринолиза оправданно лишь при кровотечениях, угрожающих жизни больного.
ЭАКК (патентованное название «амикар») быстро тормозит фибринолиз. Препарат обычно водится внутривенно капельно (100 мл 5% раствора в течение 30 мин, затем по 1 г/ч до остановки кровотечения).
ПАМБК (патентованные названия: ПАМБА (РАМВА), «гумбикс», «стриптосолют») обладает малой токсичностью и по антифибринолитической активности примерно в 3 раза превосходит ЭАКК. ПАМБК вводят внутривенно капельно по 1–3 г 3–4 раза в день.
Транексамовая кислота (патентованные названия: «циклокапрон», «френолиз», «экзацил» и др.) в 10 раз активнее, чем ЭАКК. Применяется внутривенно капельно по 1–1,5 г 3 раза в день.
Апротинин (трасилол, контрикал) является природным ингибитором протеолитических ферментов. Из-за высокой стоимости он редко используется в качестве ингибитора фибринолиза. Назначается по 300 000 ME внутривенно капельно.
Контролируемые исследования по изучению эффективности и безопасности ингибиторов фибринолиза при лечении кровотечений у больных острым ИМ, получавших тромболитическую терапию, не проводились. Однако результаты двух многоцентровых исследований, посвященных лечению субарахноидального кровоизлияния, вызванного разрывом аневризмы мозговой артерии, свидетельствуют, что антифибринолитические препараты, снижая смертность от повторного кровотечения, одновременно повышают риск развития ишемического тромботического инсульта.
Ингибиторы фибринолиза иногда сочетают с инфузиями свежезамороженной плазмы. При необходимости переливания крови предпочтительнее использовать свежую кровь.
Таким образом, тромболитические средства являются высокоэффективными средствами для лечения сердечнососудистых заболеваний, обусловленных полной или частичной окклюзией крупного сосуда фибриновым тромбом, однако необходимы строгий учет противопоказаний к назначению этих препаратов и тщательное наблюдение за местами возможного кровотечения, особенно в местах повреждения сосуда, например при его пункции или катетеризации.







Комментировать