Цукровий діабет 1 типу Цукровий діабет типу 2. Загальная описательна інформація. Клінічні прояви ЦД 1 типу. Класифікація. Приклади формування діагнозу, діагностика та терапія.
Общая информация
ЦД 1 типу (інсулінзалежний ЦД) – хронічне ендокринно-обмінне захворювання, зумовлене абсолютною недостатністю інсуліну внаслідок поєднаного впливу різних ендогенних (генетичних) та екзогенних чинників, які призводять до порушення практично всіх видів обміну речовин, функцій органів та систем організму.
Етіологія
Розвиток ЦД 1 типу пов’язують із наявністю деяких антигенів системи гістосумісності (гаплотипи HLA-В8, В15, В35, DR3, DR4, DR3/DR4 та інші). Систему HLA-генів, розміщених на 6 хромосомі, визначають як генетичну детермінанту, яка визначає чутливість β-клітин підшлункової залози до вірусних антигенів та послаблює здатність до противірусного імунітету. При спадковому характері захворювання є ураження генів, відповідальних за синтез інсуліну (11 хромосома), а також пов’язаних з імуноглобулінами та групами крові тощо. Деякі чинники навколишнього середовища можуть сприяти розвитку ЦД 1 типу: віруси (кору, епідпаротиту, краснухи, гепатиту, цитомегаловірусу, Коксакі та ін.), хімічні речовини, токсини, цитотоксичні речовини. У осіб-носіїв зазначених гаплотипів HLA ці чинники можуть прискорювати загибель β-клітин підшлункової залози. У випадках, зумовлених вірусною агресією, спостерігається безпосередня руйнівна дія вірусу на клітини внаслідок зниження толерантності до аутоантигенів. ЦД розвивається гостро, спостерігається сезонність, зумовлена вірусними епідеміями. Також відбувається індукція аутоімунної реакції, сенсибілізація моноцитів, Т-хелперів.
Патогенез
При ЦД 1 типу відбувається інфільтрація β-клітин підшлункової залози імунокомпетентними клітинами (макрофаги, Т-хелпери, цитотоксичні Т-лімфоцити). β-клітини знаходяться на різному ступені ураження, їх поверхня містить велику кількість білків HLA класу І та ІІ. Крім морфологічних змін тканин підшлункової залози, спостерігаються зміни гуморального імунітету у вигляді появи щонайменше 4 груп аутоантитіл (АТ до інсуліну, АТ до глутаматдекарбоксилази, АТ до острівцевих клітин, АТ до тирозинфосфатази підшлункової залози).
Умовно виділяють 6 стадій розвитку ЦД 1 типу.
• Генетична схильність до розвитку ЦД 1 типу за наявності гаплотипів HLA-системи, а також генів, що кодують синтез інсуліну.
• Ініціація аутоімунних процесів різними агентами, що спричиняють лізис, руйнування β-клітин або сприяють вивільненню власних цитоплазматичних білків, які стають аутоантигенами і викликають аутоімунну реакцію.
• Стадія активних аутоімунних процесів, в яких беруть участь макрофаги, лімфоцити. Продуковані ними цитокіни безпосередньо ушкоджують β-клітини або активують клітинні реакції проти них. Утворюються аутоантитіла до антигенів β-клітин, інсуліну, розвивається аутоімунний інсуліт.
• Прогресивне зниження 1 фази секреції інсуліну, стимульованої внутрішньовенним введенням глюкози.
• Клінічна маніфестація ЦД. 80-90% β-клітин підшлункової залози загинуло.
• Повна деструкція β-клітин із відсутньою секрецією інсуліну.
Абсолютний дефіцит інсуліну призводить до зниження проникнення глюкози до цитомембран, погіршення засвоєння глюкози інсулінчутливими тканинами, зниження ліпогенезу, посилення ліполізу, зменшення синтезу білка та посилення протеолізу, зменшення проникнення амінокислот та іонів калію в клітини. В той же час, спостерігається надлишок контрінсулярних гормонів (глюкагону, глюко¬кортикостероїдів, АКТГ, СТГ та ін.), що призводить до мікроциркуляторних та імунних порушень, посилення глікогенолізу, протеолізу, ліполізу та глюконеогенезу, порушення функції органів кровообігу.
Клиническая картина
Клінічні прояви ЦД 1 типу зумовлені ступенем метаболічної компенсації процесів, характером перебігу захворювання, його тривалістю, наявністю ускладнень.
Симптоми, зумовлені декомпенсацією вуглеводного обміну: полідипсія (спрага), поліурія (добовий діурез понад 1,5-2 л), ніктурія (у дітей може розвиватися енурез), сухість у роті, втрата ваги, не зважаючи на поліфагію, слабкість, сонливість після їжі, біль та слабкість у нижніх кінцівках, інколи – біль у животі та підвищення температури тіла.
Клінічні симптоми при вперше виявленому діабеті у дітей наростають дуже швидко, часто – з розвитком діабетичного кетоацидозу. При діабетичному кетоацидозі дефіцит інсуліну призводить до гіперглікемії з осмотичним діурезом, внаслідок чого розвивається дегідратація з втратою електролітів плазми. Активується ліполіз і кетогенез. Накопичення кетонових тіл призводить до зменшення лужного резерву і, як наслідок, розвивається ацидоз. Клінічно це проявляється у вигляді переривчастого, глибокого дихання Куссмауля, анорексії, нудоти, блювоти, болей в животі, які можуть імітувати гострий живіт. Зниження тургору шкіри обумовлене ступенем дегідратації. Дуже важкий кетоацидоз супроводжується артеріальною гіпотонією, ступором, сопором, комою, хаотичним рухом очних яблук, розширеними нерухомими зірницями. У випадку несвоєчасної діагностики та лікування можлива смерть.
При діабеті порушуються функції всіх органів і систем. Зміни шкіри та слизових оболонок проявляються схильністю до фурункульозу, який може виникати за кілька місяців до маніфестації захворювання, діабетичною дерматопатією, сверблячим дерматозом, ліпоїдним некробіозом, інсуліновими ліподистрофіями, у дівчаток – вульвовагінітом та свербежем зовнішніх геніталій.
Ураження травної системи проявляється, насамперед, діабетичною ентеропатією і гепатопатією. Гепатомегалія, у поєднанні з відставанням у фізичному й статевому розвитку, є невід’ємним проявом синдромів Моріака та Нобекура. За наявності синдрому Моріака у дитини спостерігається ще затримка статевого розвитку, зросту, надмірне відкладення жиру в області грудей, живота, стегон, обличчя стає округлим з яскравими щоками. Синдром Нобекура також супроводжується жировою інфільтрацією печінки, відставанням у зрості та статевому розвитку, зниженням маси тіла.
Серед уражень сечових органів, окрім специфічної діабетичної нефропатії, – пієлонефрит, папілярний некроз.
Ураження органа зору виявляється діабетичною ретинопатією, атрофією зорових нервів і катарактою.
Ураження серця у хворих на ЦД може виявлятися у вигляді кардіоміопатії, а ураження судин – у вигляді діабетичної макрота мікроангіопатії. У 1/3 хворих дітей мікроангіопатії виявляються при маніфестації захворювання.
Классификая и примеры формулировки диагноза
Класифікація цукрового діабету (ВООЗ, 1999)
І. Цукровий діабет типу 1 (деструкція β-клітин, що зазвичай призводить до абсолютної інсулінової недостатності):
А. Аутоімунний. Б. Ідіопатичний.
ІІ. Цукровий діабет типу 2 (з переважною резистентністю до інсуліну та відносною інсуліновою недостатністю або з переважно секреторним дефектом та резистентністю до інсуліну чи без неї).
ІІІ. Інші специфічні типи цукрового діабету:
А. Генетичні дефекти функції β-клітин: МОDY-3 (хромосома 12, ген НNF-1а), МОDY-2 (хромосома 7, ген глюкокінази), МОDY-1 (хромосома 20, ген НNF-4а), мітохондріальна мутація ДНК, інші.
Б. Генетичні дефекти в дії інсуліну: резистентність до інсуліну типу А, лепречаунізм, синдром РобсонаМенденхолла, ліпоатрофічний діабет, інші.
В. Хвороби екзокринної частини підшлункової залози: панкреатит, травма / панкреатектомія, неоплазія, кістозний фіброз, гемохроматоз, фіброкалькульозна панкреатопатія.
Г. Ендокринопатії: акромегалія, синдром Кушинга, глюкагонома, феохромоцитома, тиреотоксикоз, соматостатинома, альдостерома, інші.
Д. Цукровий діабет, індукований лікарськими засобами або хімічними речовинами (пентамідин, нікотинова кислота, глюкокортикоїди, тиреоїдні гормони, діазоксид, агоністи β-адренорецепторів, тіазиди, ділантин, β-інтерферон, інші).
Е. Інфекції: вроджена кірева краснуха, цитомегаловірус, інші.
Є. Незвичайні форми імуноопосередкованого ЦД:
«Stiff-man»-синдром, аутоантитіла до рецептора інсуліну, інші.
Ж. Інші генетичні синдроми, які інколи поєднуються з ЦД: синдром Дауна, синдром Клайнфельтера, синдром Тернера, синдром Вольфрама, атаксія Фрідрейха, хорея Гентінгтона, синдром Лоренса-Муна-Бідля, міотонічна дистрофія, порфірія, синдром Прадера-Віллі.
ІV. Гестаційний ЦД.
Клінічна класифікація цукрового діабету
І. Клінічні форми ЦД:
1. Первинний ЦД: а) генетичний; б) есенціальний (з ожирінням або без нього).
2. Вторинний (симптоматичний): а) гіпофізарний; б) стероїдний; в) тирогенний; г) адреналовий; д) панкреатичний (запалення підшлункової залози, пухлини або видалення); е) бронзовий (при гемахроматозі).
3. Діабет вагітних (гестаційний). ІІ. Ступінь тяжкості ЦД:
1. Легка форма (І).
2. Середньої важкості (ІІ).
3. Тяжка форма (ІІІ).
ІІІ. Типи діабету за перебігом:
І тип – інсулінозалежний (лабільний зі схильністю до кетоацидозу та гіпоглікемій, переважно юнацький).
ІІ тип – інсулінонезалежний (стабільний, ЦД людей переважно похилого віку).
ІV. Стан компенсації: Компенсований. Субкомпенсований. Декомпенсований.
V. Наявність ангіопатій (І-ІІІ стадії) та нейропатії:
1. Мікроангіопатія – ретино-, нефро-, капіляропатія нижніх кінцівок або іншої локалізації.
2. Макроангіопатія з переважним ураженням судин серця, головного мозку, нижніх кінцівок, іншої локалізації.
3. Універсальна мікро-, макроангіопатія.
4. Поліневропатія (периферична, автономна або вісцеральна).
5. Енцефалопатія.
VІ. Ураження інших органів і систем: Гепатопатія.
Дерматопатія. Ентеропатія. Катаракта. Остеоартропатія. Інші.
VІІ. Гострі ускладнення діабету: Кетонемічна (кетоацидотична) кома. Гіперосмолярна кома. Гіперлактацидемічна кома. Гіпоглікемічна кома.
Статистична класифікація за МКХ-10
Код МКХ-10: Е10-Е14 Цукровий діабет.
Приклад формулювання діагнозу
Цукровий діабет типу 1, середньої тяжкості, стадія субкомпенсації. Діабетична мікроангіопатія нижніх кінцівок ІІ ступеня. Діабетична дистальна поліневропатія, сенсорна форма. Ліподистрофії гіпертрофічні обох плечей.
Цукровий діабет типу 1, тяжка форма, стадія декомпенсації. Кетонурія. Діабетичний гепатоз. Діабетична проліферативна ретинопатія. Діабетична нефропатія ІІ ст. Діабетична автономна невропатія серця й кишечника. Хайропатія ІІІ ст. Синдром Моріака.
Диагностика
Критерії діагнозу цукрового діабету
У нормі вміст глюкози в капілярній крові складає 3,3-5,5 ммоль/л. За відсутності симптомів ЦД у дитини чи підлітка з групи ризику (обтяжена спадковість, ожиріння тощо) вважають за необхідне проведення орального глюкозотолерантного тесту (ОГТТ). Проводити тест рекомендується зранку, після 3 днів перебування обстежуваного на звичайному харчуванні й на тлі звичайної фізичної активності. Тест повинен проводитися за допомогою глюкози, розчиненої в 250-300 мл води. Розчин варто випити протягом 5 хвилин. Дітям до 14 років кількість глюкози для проведення ОГТТ дають з розрахунку 1,25 г глюкози на 1 кг ваги дитини (загалом не більше 75 г.). Забір крові для дослідження проводиться натще і через 2 години після навантаження (таблиця 1).
Варто пам’ятати, що деякі фактори можуть вплинути на показники тесту, в першу чергу – деякі лікарські препарати, наявність інфекційного або вірусного захворювання у дитини та ін.
При глікемії натще < 6,1 ммоль/л проводиться стандартний оральний тест толерантності до глюкози (див. вище). При отриманні двічі рівня глікемії натще в капілярній крові > 6,1 ммоль/л або у венозній крові > 7,0 ммоль/л, або ж вибірково > 11,1 ммоль/л, діагноз ЦД не викликає сумнівів й тест не проводиться. Якщо наявні симптоми ЦД (поліурія, полідипсія, немотивована втрата у вазі), проводять визначення глікемії натще або вибірково, протягом дня, на тлі звичайного харчування обстежуваного. При глікемії натще 6,1 ммоль/л і більше, а при вибірковому визначенні 11,1 ммоль/л і більше, ставиться діагноз ЦД.
Для встановлення діагнозу ЦД та оцінки стану компенсації захворювання найінформативнішими лабораторними дослідженнями, окрім визначення рівня глюкози крові (одноразове натще і повторні впродовж доби), є визначення рівня глюкози у сечі (добової та фракційної в окремих порціях), а також вмісту кетонових тіл у сечі та крові. Діагностичні критерії ЦД, згідно критеріїв ВООЗ (1985) та Міжнародного комітету експертів при Американській діабетичній асоціації (1998) наведені у таблиці 2.
З метою визначення ступеня порушення інших обмінних процесів проводять дослідження рівня ліпідів крові, білка і його фракцій, електролітів, показників коагулограми і функціонального стану печінки та нирок. Якість довготривалого контролю порушення вуглеводного обміну визначають за допомогою таких показників глікозилювання білків, як глікозильований гемоглобін А1 та А1с, а також фруктозамін.
За сукупністю типових для ЦД І типу симптомів у дітей та підлітків установити діагноз не складно. Такі ознаки, як полідипсія, поліурія, ніктурія, зміна маси тіла, загальна слабкість, свербіж, сухість шкіри, гіперглікемія і глюкозурія, ацетонурія патогномонічні для явного (маніфестного) ЦД.
Диференційна діагностика
Гіперглікемія при ЦД є сталою, на відміну від аліментарної гіперглікемії, частіше супроводжується глюкозурією і поєднується з іншими симптомами захворювання. Гіперглікемія може виникати при вторинному симптоматичному діабеті, який розвивається на тлі таких ендокринних захворювань, як гіперпітуїтаризм, акромегалія, хвороба Іценка-Кушинга, має епізодичний характер, поєднана з іншими симптомами основного захворювання. Гіперглікемія може бути проявом гіперкортицизму, зумовленого аденомою чи гіперплазією коркового шару надниркових залоз, у разі виникнення феохромоцитоми. У хворих із феохромоцитомою гіперглікемія може спостерігатися епізодично, під час кризів. Проте у разі тяжкого, тривалого перебігу хвороби розвивається стійкий вторинний ЦД. Нормалізація вуглеводного обміну спостерігається в більшості випадків ремісії основного захворювання.
Гіперглікемія, зумовлена ураженням нервової системи, не перевищує 10-11 ммоль/л, з усуненням основного неврологічного захворювання нормалізується і глікемія. У деяких випадках ураження нервової системи може провокувати прихований перебіг ЦД.
Глюкозурія є другим симптомом, який потребує дифереціальної діагностики. Розрізняють гіперта нормоглікемічну глюкозурію.
Гіперглікемічна глюкозурія спостерігається при захворюваннях, для яких властива гіперглікемія (ЦД, акромегалія, хвороба Іценка-Кушинга та ін.), при органічному ураженні ЦНС (захворювання, ушкодження, новоутворення), інтоксикації (отруєння чадним газом, солями ртуті, хромовими кислотами, солями урану, кураре, кофеїном, морфіном, та ін.), кисневій недостатності (наркоз, асфіксія), при тяжких загальних ураженнях (обмороження, гарячка, тяжкі фізичні травми, диспепсія і токсикоз новонароджених, інфекційні захворювання в дитячому віці), при внутрішніх хворобах (панкреатит, пневмонія, гепатолентикулярна дегенерація або хвороба Вільсона, цироз печінки), при особливих формах глюкозурії (аліментарна, голодна, емоційна, новонароджених, вагітних, зумовлена введенням стероїдних гормонів, демпінг-синдромом), при конгенітальній тубулопатії (синдром Фанконі, глікофосфатний і глікоамінокислотний діабет) та нефропатії (хронічний пієлонефрит, гломерулонефрит, гострий некроз ниркових канальців, гідронефроз, синдром Фанконі).
Також інколи виникає потреба в диференційній діагностиці між діабетом І та ІІ типу (див. таблиця 3.)
Консультації спеціалістів
Обов’язковим є огляд окуліста, невропатолога та нефролога з метою виявлення доклінічних стадій діабетичних ускладнень. За наявності показань рекомендовано огляд хірурга, стоматолога, гастроентеролога та дерматолога.
Лечение
Лікування хворого на ЦД І типу включає в себе такі основні складові: інсулінотерапія, дієта та фізичне навантаження. Навчання самоконтролю і проведення його у домашніх умовах, консультації психолога та психологічна допомога в адаптації до свого захворювання є важливою ланкою у ланцюзі терапевтичних заходів.
Критеріями ефективності лікування є:
• відсутність клінічних проявів декомпенсації ЦД;
• лабораторна компенсація ЦД (див. табл. 2);
• відсутність тяжких гіпоглікемій. Допускається наявність окремих легких гіпоглікемій;
• нормальний фізичний та статевий розвиток;
• нормальний психосоціальний стан.
Одразу після встановлення діагнозу ЦД призначається інсулін короткої дії підшкірно перед основними прийомами їжі (4-6 разів на день), іноді можлива комбінація швидкодіючого і тривалої дії інсулінів два рази на день.
Доза інсуліну при першій ін’єкції залежить від віку дитини і ступеня гіперглікемії: у дітей перших років життя – 0,5-1 ОД; у школярів – 2-4 ОД; у підлітків – 4-6 ОД.
Подальша доза інсуліну змінюється залежно від динаміки рівня глікемії:
• якщо вона не зменшується, дозу інсуліну підвищують на 50%;
• глікемія наростає – дозу підвищують на 100%;
• глікемія знижується до гіпоглікемії – дозу зменшують на 25-50%. Крім того, за необхідності додатково роблять ін’єкції в 24 і 6 годин.
Через кілька днів переходять на комбіноване введення інсулінів або аналогів тривалої дії (перед сніданком і на ніч) та короткої дії (перед основними прийомами їжі). Потреба в інсуліні при вперше виявленому діабеті – 0,3-0,5 Од/кг, при декомпенсації може перевищувати 1,5-2 ОД/кг маси тіла на добу. Після досягнення компенсації вуглеводного обміну доза інсуліну, як правило, знижується.
Добова потреба в інсуліні: дебют діабету – 0,3-0,6 ОД/кг; період ремісії – < 0,5 ОД/кг; тривалий діабет –0,7-1 ОД/кг; декомпенсація (кетоацидоз) – 1,0-1,5 ОД/ кг; період препубертату – 0,7-1,0 ОД/кг; період пубертату – 1,0-2,0 ОД/кг. Корекція дози інсуліну проводиться у стаціонарі під наглядом лікаря. При корекції враховувати чутливість до інсуліну. Введення 1 ОД інсуліну короткої дії знижує глікемію: у дітей старших 15 років – на 2-3 ммоль/л; у дітей з масою тіла більше 25 кг – на 3-7 ммоль/л; у дітей з масою тіла менше 25 кг – на 5-10 ммоль/л.
Інтенсифікована інсулінотерапія передбачає підшкірне введення інсуліну короткої дії за 30 хв до трьох основних прийомів їжі та інсуліну середньої тривалості або тривалого на ніч. Підбір дози інсуліну для кожного хворого індивідуальний і визначається параметрами вихідної глікемії та чутливістю до інсуліну. Для максимального відтворення фізіологічної секреції інсуліну (базальної та прандіальної секреції) доцільне використання аналогів інсуліну ультракороткої дії. На відміну від інсулінів короткої дії, аналоги ультракороткого інсуліну вводяться безпосередньо перед їжею, краще забезпечують контроль постпрандіальної глікемії та знижують ризик розвитку гіпоглікемічних реакцій. Добова доза інсуліну може змінюватися залежно від режиму харчування та фізичних навантажень протягом дня. Базальну концентрацію інсуліну забезпечують інсулінами подовженої дії або дії середньої тривалості.
У разі виникнення діабетичного кетоацидозу потрібна госпіталізація у відділення інтенсивної терапії, де в листі спостереження за хворими відмічають всі лабораторні показники і лікарські заходи. Якщо хворий в стані шоку, сопору чи коми – вводять назогастральний зонд і сечовий катетер. З метою відновлення внутрішньота позаклітинної рідини розпочинають інфузійну терапію 0,9% розчином хлориду натрію, при низькому тиску застосовують колоїдний розчин, а при низькому рівні калію – хлорид калію. Не потрібно швидко знижувати осмолярність плазми, щоб запобігти розвитку набряку мозку. Останній може розвинутися при використанні бікарбонату натрію. При зменшенні глікемії < 11,0 ммоль/л підключають 5% розчин глюкози.
Інсулінотерапія проводиться безперервно зі швидкістю 0,1 ОД/кг/год. Якщо не вдається швидко підключити інфузійну систему (спадання вен, поява судом), тоді інсулін короткої дії вводять внутрішньом’язово; дітям вводять по 0,25-1,0 ОД/кг кожні 2-4 год, а при легкому кетоацидозі дозу зменшують вдвічі. Якщо через 2 год після введення інсуліну глікемія не зменшується, то дозу інсуліну необхідно подвоїти.
Можливі ускладнення інсулінотерапії: алергія на інсулін, гіпоглікемічний стан, а для хворих з кетоацидозом і комою – передозування калійних препаратів із зупинкою серця, приєднання інфекцій дихальної системи (пневмонії), сечовидільної системи (пієлонефрит, папілярний некроз), шок, набряк легенів та мозку.
Внаслідок передозування інсуліну може розвинутися гіпоглікемічний стан. Це може статися також при недостатньому вживанні вуглеводів, пропусканні прийому їжі, при збільшенні фізичного навантаження, гормональних порушеннях тощо.
Клінічні прояви при гіпоглікемії у разі відсутності допомоги наростають досить швидко: слабкість, пітливість, тахікардія, тремор рук, підвищена збудливість, дратівливість, оніміння губ і пальців, відчуття голоду. Згодом – нудота, блювота, головний біль, гіпотермія, порушення зору, психічна загальмованість, погіршення слуху, амнезія, судоми, кома.
На початку розвитку гіпоглікемії для її усунення достатньо вжити рафіновані вуглеводи (печиво, булочка, цукор, мед, цукерки). При порушенні свідомості необхідно негайне внутрішньовенне введення глюкози. Найнадійнішим засобом виведення хворого з гіпоглікемічного стану є введення гормону глюкагон, який активує викид глюкози з печінки, що підвищує рівень цукру в крові. Перевагою препарату гормону глюкагон є його фізіологічна дія і можливість уводити препарат внутрішньом’язово. Це дає змогу родичам та оточуючим надавати швидку допомогу хворому в стані тяжкої гіпоглікемії в будь-якому місці.
Поряд з інсулінотерапією, дієтичне харчування у хворих на ЦД є одним з основних методів лікування, це важливий фактор у досягненні стійкої компенсації захворювання.
Дієта повинна повністю задовольняти енергетичні затрати хворого, підтримувати на нормальному рівні обмін речовин, повинна задовольняти потреби дитячого організму у вітамінах, мінералах, біологічно активних речовинах. Харчування дитини, хворої на ЦД, повинно мати відповідне співвідношення: білків – 15-20%, жирів – 25-30%, вуглеводів – 50-60%. Добова потреба хворого у калоріях та основних харчових інгредієнтах повинна відповідати віку, масі тіла, рівню фізичної активності, способу життя, особливостям процесів обміну хворого.
При виборі оптимального варіанту дієти для кожного хворого на ЦД стандартна дієта максимально індивідуалізується відповідно до схеми інсулінотерапії, звичок пацієнта та режиму харчування сім’ї.
При харчуванні хворих дітей на ЦД повинні враховуватися наступні принципи:
• контроль глікемії, попередження гіпота гіперглікемій;
• вид, кількість та розподіл вуглеводів повинні бути підібрані так, щоб запобігти різким коливанням глікемії, постпрандіальна гіперглікемія залежить не тільки від кількості, а й від виду вуглеводів;
• необхідність частих дрібних перекусів – при інтенсифікованій схемі інсулінотерапії та їх відсутність – при лікуванні аналогами інсуліну ультракороткої дії;
• по можливості потрібно адаптувати харчування хворого до харчування сім’ї, не готувати їжу окремо;
• додавати у їжу певну кількість харчових волокон та використовувати невелику кількість жиру;
• необхідно прагнути до регулярності харчування, оскільки при відсутності режиму складніше регулювати глікемію;
• через швидкий підйом цукру крові після їжі ін’єкція короткого інсуліну повинна робитися завчасно: за 15-30 хв до їжі та безпосередньо перед їжею при застосуванні аналогів інсуліну ультракороткої дії;
• постійний контроль харчування;
• контроль маси тіла, росту;
• відхилення від нормальних темпів фізичного розвитку вимагає перегляду дієти та корекції інсулінотерапії.
Дотримання цих умов суттєво підвищує якість життя хворого, не виділяє його від інших здорових дітей в родині.
Харчування хворого на ЦД повністю залежить від схеми інсулінотерапії. При інтенсифікованій інсулінотерапії з використанням інсулінів короткої дії рекомендовано три основних прийоми їжі (сніданок, обід, вечеря) та 3-4 додаткових, тобто прийом їжі повинен відбуватися кожні 3 год, а у маленьких дітей – кожні 2-2,5 год. При застосуванні аналогів інсуліну ультракороткої дії потреба в додаткових прийомах їжі відпадає, якщо дитина не може обійтися без їжі на час перекусу, то потрібно вводити додаткову ін’єкцію інсуліну, або ж їжа на цей час повинна містити мало вуглеводів. Крім того, бажано приймати їжу кожен день в однаковий час, оскільки це запобігає виникненню небажаних гіпоглікемічних станів та сприяє виникненню здорового апетиту.
Добовий калораж стандартної фізіологічної дієти розраховується за формулою:
1000+(n•100), де n – вік дитини у роках.
Ця формула повністю відповідає положенню: у 1 рік дитині на покриття енергетичних затрат потрібно, в середньому, 1000 калорій, кожний наступний рік ця потреба збільшується на 100. Якщо маса тіла хворого не відповідає нормативам, то розрахунок добового калоражу проводять на 1 кг ідеальної маси тіла на добу. Потреба в калоріях на 1 кг маси тіла у дітей та підлітків, залежно від віку, змінюється: від 1 року до 1,5 років – 115, від 2 до 3 років – 110, від 4 до 5 – 101, від 6 до 7 – 90, від 8 до 9 – 76, від 10 до 11 – 64, від 12 до 13 – 63, від 14 до 15 – 51 ккал/кг на добу.
Для визначення добового набору продуктів необхідно враховувати вимоги, які висувають до збалансованої фізіологічної дієти, та врахувати особливості харчування хворого на діабет. Різні види харчових продуктів, які містять вуглеводи, можуть по різному впливати на рівень постпрандіальної глікемії, оскільки кожному продукту властивий свій глікемічний індекс. За 100% прийнятий індекс цукру. Продукти, які мають 100-90% глікемічний індекс: кондитерські вироби з цукру, кока-кола, пепсікола, картопляне пюре, мед, кукурудзяні пластівці; від 70 до 90% – білий хліб, сухе печиво, рис, пиво, випічка; від 50 до 70% – банани, кукурудза, вівсяні пластівці, картопля, житній хліб, соки без цукру; від 30 до 50% – молоко, кефір, йогурт, фрукти; менше 30% – овочі, боби, зелень, горіхи. Рекомендовано максимально обмежити вживання продуктів з високим глікемічним індексом, перевага надається продуктам, які містять крохмаль та клітковину.
Крім того, хворому на діабет не рекомендується вживати продукти, які містять тугоплавкі жири та велику кількість холестерину. Потреба в білках покривається за рахунок нежирних сортів м’яса, риби, сиру. Необхідно пам’ятати про співвідношення поліненасичених та насичених жирних кислот і додавати у раціон достатню кількість соняшникової, оливкової, кукурудзяної олії.
Раціональне харчування при цукровому діабеті передбачає чіткий розподіл калорійності та вуглеводного насичення за кількістю та годинами прийому їжі: сніданок –25%, другий сніданок – 10-15%, обід – 25-30%, полуденок – 6-10%, вечеря – 20-25%, друга вечеря – 5-10% добового калоражу та добової кількості вуглеводів (таблиця 4).
Якщо хворий отримує аналоги інсуліну ультракороткої дії, то розподіл калоражу має дещо інакший вигляд: сніданок – 30%, другий сніданок – 0-5%, обід – 35%, полуденок – 0-5%, вечеря – 20-25%, друга вечеря – 0-5% добового калоражу та добової кількості вуглеводів. На другий сніданок, полуденок та другу вечерю бажано давати продукти, які містять менше вуглеводів (наприклад: на другий сніданок – яйце, полуденок – сир, друга вечеря – тушкована морква).
Іншим, проте не менш розповсюдженим, є розрахунок дієти за хлібними одиницями (ХО). Одна хлібна одиниця – це 12 г чистих вуглеводів. Всі харчові продукти за вмістом вуглеводів можна перерахувати на вміст ХО.
20 г білого хліба містять одну ХО. При такому розрахунку враховується тільки кількість вуглеводів, які містяться у продуктах і вживаються на сніданок, обід, вечерю та перекуси. Не потребують перерахунку на ХО всі білкові продукти (м’ясо, риба, яйця, сир та інше), листовий салат, огірки, цибуля, всі види капусти, морква, редис, шпинат, гриби, помідори, кабачки, гарбуз, баклажани, червоний та зелений солодкий перець. Такими розрахунками дієти зручно користуватися при щоденному плануванні харчового раціону.
Різні види харчових продуктів, які містять вуглеводи, неоднаково впливають на рівень цукру в крові, оскільки глюкоза з них всмоктується з різною швидкістю. Здатність харчового продукту підвищувати концентрацію глюкози крові визначається як глікемічний індекс.
Вживання продуктів з глікемічним індексом 90-100% (цукор, цукерки, картопляне пюре, солодкі напої з цукром, кукурудзяні пластівці) треба максимально обмежити, оскільки це призв одить до значного підвищення рівня цукру в крові. У більшості продуктів глюкоза міститься в зв’язаному стані, тому її всмоктування сповільнене, а рівень її у крові після прийому їжі зростає відносно повільно. До таких продуктів належать овочі, крупи, картопля, рис, хліб грубого помолу. Велика кількість клітковини, що міститься в овочах, сповільнює всмоктування і практично не впливає на рівень глікемії. Перевагу у харчуванні слід надавати овочам з глікемічним індексом менше 30% (капуста, салат, кабачки, морква, баклажани, солодкий перець та інше).
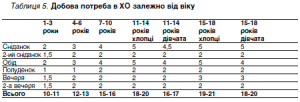
Кількість вуглеводів (ХО), необхідних людині залежно від віку наведені в таблиці 5.
Інтенсифікована інсулінотерапія дає можливість вільно розподіляти ХО та комбінувати різні продукти (таблиця 6).
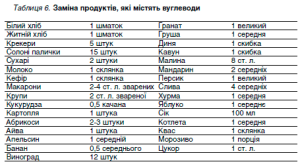
Слід зазначити відмінності в дієті, які виникають у хворих, переведених на аналоги інсуліну тривалої та ультракороткої дії: потреба в додаткових перекусах відпадає, а час основних прийомів їжі можна переносити, залежно від режиму дня, на зручний для хворої дитини або підлітка час. Кількість ХО на основні прийоми їжі при цьому зростає, а на 2-ий сніданок, полуденок та 2-у вечерю зменшується до 0,5-1 ХО. Особливо це зручно для студентів і старшокласників. Проте необхідне дотримання жорсткої умови: кількість хлібних одиниць, що поглинаються на сніданок, обід, вечерю щодня залишається незмінною і не повинно перевищувати 7-8 XО.
Поряд з дієтою, фізичне навантаження сприяє покращенню вуглеводного, білкового та жирового обміну в організмі людини.
Інтенсивне фізичне навантаження підвищує чутливість інсулінових рецепторів до інсуліну, що сприяє зниженню рівня глюкози в крові. По відношенню до цукрового діабету всі види фізичних навантажень можна розмежувати на короткочасні й тривалі.
При різних видах фізичного навантаження поведінка хворого з цукровим діабетом буде різною: існує велика вірогідність виникнення гіпоглікемії під час фізичного навантаження, через що потрібно ретельно контролювати рівень цукру в крові, за необхідності робити додаткові прийоми їжі.
Диспансерне спостереження, діагностичні дослідження і консультації
Обстеження в умовах стаціонарного дитячого відділення – 1 раз на рік, якщо немає ускладнень; за наявності ускладнень – 1 раз на 6 міс. Огляд педіатра-ендокринолога – 1 разів на місяць. Клінічний (розгорнутий) аналіз крові й сечі – за показаннями, але не рідше 2 раз на рік; ацетон сечі – за показаннями; глюкоза крові – 5 разів на день (при маніфестації захворювання та при декомпенсації) – щоденно; глюкоза сечі – 4-5 разів на день (при маніфестації захворювання та при декомпенсації); біохімічний аналіз крові – 1 раз на рік; НвАІc –1 раз на 3 міс; МАУ трикратно – 1 раз на рік через 5 років від початку діабету; оцінка фізичного й статевого розвитку – 2 рази на рік; ЕКГ, РВГ ніг, ФГОГК – 1 раз на рік; огляд окуліста – 1 раз на рік, при раптовому погіршенні зору – терміново. Диспансерний нагляд – протягом усього життя.
Цукровий діабет типу 2
МкХ—10: е11
Общая информация
Цукровий діабет типу 2 – порушення вуглеводного обміну, яке обумовлено інсулінорезистентністю та відносною інсуліновою недостатністю або з переважно секреторним дефектом та резистентністю до інсуліну.
Сьогодні у спеціалістів не викликає сумніву той факт, що ЦД 2 типу може спостерігатися у дітей та підлітків. За останні роки значно збільшилася розповсюдженість цього захворювання серед дітей, особливо у Північній Америці та країнах Африки, що пов’язують з ростом захворюваності на ожиріння серед дітей і підлітків та з їх гіподинамічним станом життя. Показники захворюваності та поширеності ожиріння серед дитячого населення України також мають тенденцію до зростання. Щорічно фіксується біля 14 тисяч нових випадків ожиріння серед дітей у віці 0-14 років, серед дорослого населення цей показник сягає 50 тисяч.
Частота захворюваності на ЦД 2 типу серед дітей та підлітків від загальної захворюваності на ЦД становить 0,14% у країнах Європи та 6-7% – у державах Африки й Америки.
На сьогодні в Україні теж збільшується кількість дітей та, особливо, підлітків 15-18 років, яким встановлюють діагноз ЦД 2 типу.
Патогенез
В основі патогенезу виникнення ЦД 2 типу знаходяться 2 чинники, спричинені генетичними дефектами, – інсулінорезистентність та відносний дефіцит інсуліну. Внаслідок цього розвивається ожиріння, яке призводить до інсулінорезистентності, та падає активність β-клітин підшлункової залози або вони стають нечутливими до гіперглікемії.
Виявляють різновид діабету дорослого типу у молодих: MODY (Maturity-onset diabetes of the young). Характеризується захворювання тим, що починається у молодому віці (до 25 років), відсутністю ожиріння, кетонемії, інсулінорезистентністю та помірною дисфункцією β-клітин.
Диагностика
Критерії діагностики ЦД типу 2
До основних клінічних ознак ЦД 2 типу відносяться: спадковість з боку одного чи обох батьків або близьких родичів, скарги на незначні та транзиторні гіперглікемії, які вперше можуть виявлятися випадково, підвищений індекс маси тіла (ІМТ) та відсутність кетоацидозу. Самі хворі, як правило, ніяких скарг не висловлюють. Тільки інколи можуть скаржитися на поліурію та полідипсію. Зазвичай перші прояви ЦД 2 типу починаються непомітно, мають легкий перебіг і тривалий час можуть залишатися нерозпізнаними.
Для встановлення остаточного діагнозу ЦД 2 типу використовують показники рівня глікемії в плазмі венозної та капілярної крові, а також рівень Hb A1с, фруктозаміну (FA) та рівні інсуліну і С-пептиду крові згідно з рекомендаціями Європейського товариства страхової медицини (1999) та Американської асоціації клінічної ендокринології (ААСЕ, 2001).
Лабораторні показники:
а) обов’язкові (таблиця 6):
• помірна гіперглікемія натще (до 10 ммоль/л);
• постпрандіальна гіперглікемія до 10-14 ммоль/л;
• можливі сліди глюкози у сечі.
б) додаткові лабораторні показники:
• рівень глікованого гемоглобіну на момент виявлення захворювання > 6,4%;
• відсутність маркерів автоімунної реакції до β-клітин підшлункової залози (ІСА-512) та глютаматдекарбоксилази (GAD) є основними лабораторними критеріями для проведення диференційної діагностики та підтвердження ЦД 2 типу у дітей і підлітків.
Лечение
• нормалізація маси тіла;
• низькокалорійна дієта (дієта № 9) з обмеженням вуглеводів, що легко засвоюються, вживанням продуктів, збагачених клітковиною, помірне використання замінників цукру;
• дозоване фізичне навантаження;
• за відсутності компенсації при немедикаментозному лікуванні – метформін (Метфогама) 500-2000 мг/добу (єдиний цукрознижувальний препарат, дозволений для застосування у дитячому віці);
• за відсутності компенсації при лікуванні метформіном – комбінація його з інсуліном;
• за відсутності компенсації при комбінованому лікуванні – інсулінотерапія.
Показання для госпіталізації в ендокринологічне відділення:
• вперше виявлений ЦД – для корекції лікування, навчання в «Школі самоконтролю хворого на ЦД»;
• декомпенсація ЦД, в т.ч. при супутніх захворюваннях, що не коригується в амбулаторних умовах;
• швидке прогресування хронічних ускладнень ЦД.
Критерії ефективності лікування — компенсація цукрового діабету та довготривале її утримання. Тривалість амбулаторного лікування – протягом всього життя з обов’язковим досягненням та утриманням компенсації, періодичного навчання та самоконтролю.
Санаторно-курортне лікування та реабілітація
У комплексі лікувально-оздоровчих і профілактичних заходів для хворих на ЦД істотне значення має санаторно-курортне лікування. Різноманітні природні фактори (бальнеологічні, кліматичні, лікувальні грязі, тощо) стимулюють захисно-пристосувальні сили організму, підвищують функціональну ефективність нейрогуморальних систем, сприяючи оптимізації методів лікування. Лікування та реабілітація хворих на ЦД проводиться у спеціалізованих санаторіях та відділеннях бальнеологічного профілю на різних курортах України (Березовські мінеральні води під Харковом, Миргород, Трускавець та ін.). Мінеральні води поліпшують процеси обміну в печінці, посилюючи її бар’єрну функцію, активізують репаративні процеси, сприяють нормалізації ліпідного обміну. Позитивний вплив справляє бальнеотерапія на функцію травного каналу, сечових органів. Важливим принципом санаторно-курортного лікування є комплексність, яка передбачає не тільки використання різних природних лікувальних чинників у поєднанні з дієтотерапією і фізіотерапевтичними методами, а й терапію, спрямовану на нормалізацію маси тіла, корекцію різних проявів діабетичної ангіопатії та діабетичної нефропатії, супутніх захворювань.
Для визначення доцільності курортного лікування потрібно враховувати тяжкість захворювання, характер його перебігу, стан компенсації, наявність і ступінь прояву діабетичної ангіо-, нейропатії, супутніх захворювань і функціональних порушень, зумовлених ними.
Профілактика
Первинна профілактика ЦД полягає у виявленні схильності до ЦД у родичів хворих шляхом HLA-типування. Можливе використання таких маркерів: титр антитіл до β-клітин острівців, інсуліну, GAD, глікованого гемоглобіну, С-пептиду.
Вторинна профілактика – виявлення маніфестації діабету та стійке утримання захворювання у межах компенсації. Третинна профілактика – виявлення ускладнень діабету на доклінічному рівні та запобігання їх появі.
Юридичні аспекти
Інформована згода батьків на ведення протоколу обстеження і лікування є обов’язковою умовою початку обстеження та медичного втручання. Якщо стан пацієнта критичний, медичне втручання невідкладне, питання вирішує консиліум, у разі неможливості його зібрати – черговий лікар.
План обстеження і лікування обговорюють і погоджують з батьками.
До 6 років пацієнт має право знаходитися з одним з батьків у стаціонарі. З батьками та пацієнтом обговорюють: мету проведення лікарських заходів, можливі ускладнення, наслідки ігнорування лікування. Треба ознайомити хворого та батьків з технікою введення інсуліну, підрахунку ХО, технікою самоконтролю.
Діабетична ангіопатія
МкХ—10: е10.5, е11.5, і79.2
Общая информация
Діабетична ангіопатія – це генералізоване ураження судин, як дрібного калібру (мікроангіопатія), так і судин середнього та великого калібру (макроангіопатія). Діабетична мікроангіопатія має типову патоморфологічну картину: потовщення базальної мембрани капілярів, проліферація ендотелію та відкладення в судині глікопротеїдних комплексів. Патогномонічним для мікроангіопатії є зменшення або повна відсутність перицитів (клітин мезангіуму або муральних клітин), які регулюють тонус судин та товщину базальної мембрани. Таким чином, порушення їх функції веде до розширення просвіту капілярів, гемостазу та підвищення проникливості судин.
Діабетична макроангіопатія не має специфічної відмінності від атеросклеротичних змін у людей без діабету.
Патогенез
Хронічна гіперглікемія є причиною гліколізу багатьох білків та субстратів в організмі, в т.ч. ліпопротеїдів низької щільності, які стають чутливішими до впливу на них вільних радикалів, які утворюються в результаті окислювального стресу при ЦД. Окрім того, ішемія, гіпоксія та псевдогіпоксія є додатковими факторами, які сприяють утворенню реактивних оксидантів у різних органах і тканинах при ЦД. В розвитку судинних ускладнень діабету приймають участь різні генетичні фактори. Прогресування судинних ускладнень обумовлено порушенням нейрогуморальної, гормональної регуляції, гемореологічних властивостей, оксигенації, гіперпродукції контрінсулярних гормонів та аутоімунними змінами.
Клиническая картина
Найбільш значні порушення мікроциркуляції зустрічаються у підлітків з декомпенсацією метаболічних процесів та тривалістю ЦД більше 6-10 років, а також у хворих з вперше виявленим ЦД у стані кетоацидозу. ДМ характеризуються підвищенням тонусу судин, спазмом артеріальної частини, нерівномірністю калібру мікросудин, зменшенням артеріовенозного співвідношення та числа функціонуючих судин. Гіпотонічний тип мікроциркуляторних порушень супроводжується деформацією венозної частини судин, множинними мікроаневризмами, зменшенням кровообігу. В дитячому та підлітковому віці ураження судин нижніх кінцівок найчастіше проявляються мікросимптоматикою. В деяких випадках пацієнти скаржаться на втомлюваність, судоми у м’язах гомілки, мерзлякуватість нижніх кінцівок, трофічні зміни шкіри у вигляді ліпоїдного некробіозу.
Диагностика
Рання діагностика ДМ утруднена. Для виявлення мікроангіопатій кінцівок проводиться капіляроскопія (КПС) нігтьового ложа 4-го пальця руки і 1-го пальця стопи за допомогою капіляроскопа, оцінюються як судинні показники (структура капілярних петель), так і позасудинні (перикапілярний набряк, крововиливи) і внутрішньосудинні (перфузія капілярів); всім хворим проводиться реовазографія (РВГ) та оклюзійна венозна плетизмографія (ОКВП). Додатковим методом дослідження периферичного кровообігу є дистанційна інфрачервона термографія кінцівок.
Рання діагностика судинних уражень з обрахуванням характеру та ступеня мікроциркуляторних порушень, рівня глікованого гемоглобіну, тривалості, тяжкості ЦД дозволяє вибрати правильну тактику лікування і прогнозувати подальше лікування судинних уражень.
Лечение
Враховуючи, що гіперглікемія є основним фактором патогенезу ангіопатій, профілактика та лікування останніх складається в ідеальній компенсації ЦД, тобто підтримання нормоглікемії та глюкозурії протягом довгого часу. Пильну увагу слід приділяти нормалізації постпрандіальної гіперглікемії, яка обумовлює швидкість прогресування судинних ускладнень.
Консервативна терапія:
1. Застосування антиоксидантів (нікотинамід, аскорбінова кислота, селен,
a-токоферол, a-ліпоєва (тіоктова) кислота в таблетках по 300 та 600 мг, для в/в введення – ампули по 300 та 600 мг крапельно на 200 мл фізіологічного розчину NaCl 1 раз на день протягом 10 днів).
2. Препарати вітамінів групи В (водорозчинних – октотіамін), жиророзчинних (бенфотіамін), комбінованих вітамінів В1, В6, В12 – Мільгама).
3. Антигіпоксанти.
4. Вазоактивні препарати: пентоксифілін (Трентал) в дозі 500-1000 мг/добу, троксерутин.
Лікування проводиться курсами по 3-4 тижні, застосовуються не більше 2-3 препаратів одночасно.
Фізіотерапевтичне лікування:
мікрохвильова резонансна терапія;
низькоінтенсивна лазерна терапія на біологічно активні точки.
Профілактика
Відповідний контроль та компенсація діабету, своєчасне та адекватне лікування ускладнень.
Юридичні аспекти
Інформування та узгодження з пацієнтом та його близькими плану обстеження та лікування. Пояснення пацієнту та його родичам мети проведення відповідних лікувальних заходів, можливих ускладнень та побічних дій, необхідності виконання всієї програми обстеження та лікування.
Тривалість сеансів – 20 хвилин, курс лікування – 10 днів, частота курсів – 2-3 на рік.
Діабетична нейропатія
МкХ—10: е10.4, е11.4
Общая информация
Діабетична нейропатія (ДНП) – ураження периферичної нервової системи у хворих на ЦД. У дітей, залежно від методу дослідження, виявляється у 5-50% хворих.
Патогенез
Патогенез ДНП ще до кінця не вивчений. Вважають, що основним чинником в розвитку ДНП виступає підвищення рівня неферментативного глікованого білку на тлі гіперглікемії, що призводить до порушення функціонального стану багатьох морфологічних структур. У патогенезі розвитку діабетичної нейропатії беруть участь також метаболічні, судинні, імунні чинники, недостатність нейрогормонального чинника зростання, оксидативний стрес та інше. Навіть досягши задовільної метаболічної компенсації захворювання, не вдається припинити розвиток нейропатії, у зв’язку з чим проводиться активний пошук патогенетичних методів її профілактики і лікування.
Клиническая картина
Частота розвитку синдромів ураження нервової системи підвищується з віком та довгою тривалістю ЦД. Однією з частих проявів ДНП у дітей та підлітків є гостра енцефалопатія (може бути на тлі кетоацидозу, гіпоглікемії) або первинно-церебральна.
Неврологічні симптоми у дітей та підлітків зустрічаються, залежно від тривалості ЦД, з різною частотою: головний біль, запаморочення, диплопія (подвоєння в очах), м’язова слабкість, астенія, утруднення при ходьбі, парестезії, гіпоестезії, гіперальгезії, гіперпатії, неврозоподібні стани, психічні розлади.
Діагностика
Велике значення для діагностики ДНП має правильний збір скарг та анамнезу, що дозволяє не тільки виявити ознаки ДНП, а й визначити характер порушень.
Неврологічний огляд хворого:
визначення пропріоцептивної чутливості (пасивне згинання п’ястково-фалангових та гомілковостопних суглобів, оцінка ахілового рефлексу);
дослідження вібраційної чутливості (з допомогою камертону за 8-бальною шкалою);
визначення тактильної чутливості (за допомогою монофіламентів);
оцінка температурної чутливості (прикладання до шкіри по черзі предметів з високою та низькою температурою);
електронейроміографія (застосовується для діагностики складніших випадків ДНП).
Классификая и примеры формулировки диагноза
Класифікація діабетичної нейропатії (М. І. Балаболкін, 2000)
І. Субклінічна стадія нейропатії.
1. Електродіагностичні тести: зниження провідності нервового імпульсу чутливих та рухових периферичних нервів; зниження амплітуди нервовом’язових індукованих потенціалів.
2. Тести на перевірку чутливості: вібраційний, тактильний тест, теплова та холодова проби.
3. Функціональні тести автономної нервової системи: порушення функції синусового вузла і порушення ритму серцевої діяльності, зміна потовиділення та зіничного рефлексу.
II. Клінічна стадія нейропатії.
1. Центральна: енцефалопатія, мієлопатія.
2. Периферична дифузна нейропатія.
2.1. Дистальна симетрична сенсорно-рухова полінейропатія.
2.1.1. Первинна нейропатія дрібних волокон.
2.1.2. Первинна нейропатія великих нервових стовбурів.
2.1.3. Змішана.
2.1.4. Проксимальна аміотрофія.
3. Дифузна автономна нейропатія.
3.1. Порушений зіничний рефлекс.
3.2. Порушення потовиділення.
3.3. Автономна нейропатія сечостатевої системи – «нейрогенний сечовий міхур» (дисфункція сечового міхура).
3.4. Автономна нейропатія шлунково-кишкового тракту – атонія шлунка, атонія жовчного міхура, діарея.
3.5. Автономна нейропатія серцево-судинної системи.
3.6. Безсимптомна гіпоглікемія.
4. Локальна нейропатія.
4.1. Мононейропатія.
4.2. Множинна нейропатія.
4.3. Плексопатія.
4.4. Радикулопатія.
4.5. Нейропатія черепних (краніальних) нервів.
Диагностика
Велике значення для діагностики ДНП має правильний збір скарг та анамнезу, що дозволяє не тільки виявити ознаки ДНП, а й визначити характер порушень.
Неврологічний огляд хворого:
визначення пропріоцептивної чутливості (пасивне згинання п’ястково-фалангових та гомілковостопних суглобів, оцінка ахілового рефлексу);
дослідження вібраційної чутливості (з допомогою камертону за 8-бальною шкалою);
визначення тактильної чутливості (за допомогою монофіламентів);
оцінка температурної чутливості (прикладання до шкіри по черзі предметів з високою та низькою температурою);
електронейроміографія (застосовується для діагностики складніших випадків ДНП).
Лечение
1. Дотримання дієти.
2. Адекватна інсулінотерапія.
3. Сірковмісні препарати (альфа-ліпоєва кислота по 600 мг в/в крапельно 1 раз на добу, курс – 10 днів; унітіол 5% в/м 1 раз на добу, № 10).
4. Нейротропні препарати групи В: В6, В12, В1 (мільгама по 100 мг 1-2 рази на день протягом 4-6 тижнів.
5. Ноотропні препарати (прамірацетам по 1 таблетці 2-3 рази на добу, 4-6 тижнів).
6. Седативні препарати (сухий екстракт трави звіробою по 1-2 таблетці на добу) та інші препарати рослинного походження.
7. Симптоматична терапія ДН з урахуванням локалізації процесу.
Санаторно-курортне лікування в спеціальних відділеннях санаторіїв для хворих на ЦД: «Березовий гай» (м. Миргород), «Янтар» (м. Трускавець).
Профілактика
Рання діагностика ЦД, адекватна інсулінотерапія, ретельний самоконтроль.
Юридические аспекты
Попереднє узгодження з пацієнтом та його батьками методів обстеження та плану лікувальних заходів.
Діабетична нейропатія
МкХ—10: е10.4, е11.4
Общая информация
Діабетична нефропатія (ДН) – специфічне ураження судин нирок при цукровому діабеті (ЦД), що супроводжується формуванням вузликового або дифузного гломерулосклерозу, термінальна стадія якого характеризується розвитком ХНН.
Ризик розвитку нефропатії вищий у хворих з початком цукрового діабету в прета пубертатному віці, порівняно з хворими, у яких дебют захворювання припав на вік до 10 років.
Етіологія
У розвитку і прогресуванні ДН основну роль відіграють декомпенсація ЦД, тривалість перебігу захворювання, підвищення АТ. ДН прогресує поступово, минаючи в своєму розвитку низку патогенетичних стадій, причому ранні прояви ушкодження нирок при ЦД протікають безсимптомно, субклінічно і вимагають спеціальних підходів для виявлення. Клінічні ознаки проявляються при загибелі великої кількості нефронів та склерозі 50-75% клубочків.
Патогенез
Метаболічна теорія розвитку ДН пов’язана з довготривалою гіперглікемією і біохімічними порушеннями, які спричиняють виникнення структурних та функціональних змін у нирках. Гемодинамічна теорія пояснює формування склеротичних змін у нирках розвитком внутрішньоклубочкової гіпертензії та гіперфільтрації. Генетична теорія ґрунтується на деяких генетичних чинниках. Всі три механізми тісно пов’язані між собою.
Клиническая картина
Перші три стадії ДН протікають безсимптомно. Починаючи з ІV стадії ДН в аналізах сечі з’являється транзиторна, а потім – постійна протеїнурія. У 30% хворих розвивається нефротичний синдром з масивною протеїнурією, набряками, прогресує підвищення АТ та спостерігаються інші ускладнення ЦД.
Обов’язкові методи дослідження:
дослідження мікроальбумінурії (МАУ) трикратно;
дослідження протеїнурії (у загальному аналізі сечі або у сечі, що зібрана за добу);
дослідження осаду сечі (еритроцити, лейкоцити);
дослідження креатиніну та сечовини сироватки крові;
дослідження ШКФ.
Диагностика
Найбільш раннім маркером в діагностиці ДН є мікроальбумінурія (МАУ).
Скринінг на наявність МАУ необхідно проводити:
при дебюті ЦД типу 1 після пубертату – 1 раз на рік через 5 років від моменту діагностики хвороби;
при дебюті ЦД типу 1 в період пубертату – 1 раз на рік з моменту діагностики хвороби;
при дебюті ЦД у ранньому дитячому віці – щорічно з 10-12 років;
у хворих на ЦД типу 2 – 1 раз на рік з моменту його діагностики.
Наявність МАУ свідчить про наявність у хворого III стадії ДН, яка є єдиною зворотною стадією розвитку ДН, за умови вчасно призначеної терапії.
Діагностичне значення має тільки постійна альбумінурія, тобто визначена тричі протягом 2-3 місяців. МАУ може визначатися при фізичних навантаженнях, інфекції сечовивідних шляхів, при декомпенсації ЦД, фебрильній температурі, при вадах серця, в підлітків у період інтенсивного росту.
Раннім маркером ушкодження нирок є внутрішньоклубочкова гіпертензія, що вважається основною причиною розвитку й прогресування ДН. Вона діагностується на основі підвищення швидкості клубочкової фільтрації більше 140 мл/хв (проба Реберга – кліренс ендогенного креатиніну за добу (норма – 80-120 мл/хв)). Проба Реберга може бути неінформативною в дебюті діабету, при його декомпенсації, вживанні високобілкової дієти.
Лечение
При нормальній екскреції альбуміну із сечею
Ретельна корекція вуглеводного обміну:
глікований гемоглобін не вище 7-7,5%;
артеріальний тиск не вище 110/70 мм рт.ст.;
холестерин нижче 4,5 ммоль/л;
тригліцериди нижче 1,7 ммоль/л.
При мікроальбумінурії
1) Корекція вуглеводного обміну (див. вище).
2) Дієта з обмеженням тваринного білка (до 0,9-1,2 г/кг на добу) і солі.
3) Корекція АТ при підвищеному АТ у середньотерапевтичних дозах призначають інгібітори АПФ (ІАПФ) тривалої дії 1 раз на день увечері, які мають нефропротекторну дію і на стадії мікроальбумінурії дозволяють попередити протеїнурію майже у 55% хворих на ЦД, а при нормальному АТ – у мінімальних дозах. Слід уникати призначення тіазидних діуретиків і неселективних b-адреноблокаторів (підвищують інсулінорезистентність та рівні тригліцеридів, більшість b-блокаторів знижують серцевий викид, чим погіршують ниркову гемодинаміку).
4) Поряд з інгібіторами АПФ, нефропротективну дію має і селективний агоніст імідазолінових рецепторів моксонідин (фізіотенз) – препарат центральної дії, добре переноситься при тривалому прийомі.
5) Корекція внутрішньониркової гемодинаміки:
ІАПФ, навіть при нормальному АТ – у невеликих дозах;
агоніст імідазолінових рецепторів моксонідин (фізіотенз).
6) Ацетилсаліцилова кислота щодня, постійно, на ніч (дітям старше 12 років – 325 мг 1 раз на 3 дні).
7) Сулодексид (група глікозаміногліканів) не впливає на згортальну систему крові, але підвищує вміст гепарансульфату в мембранах ниркових клубочків, відновлює селективну проникність ниркового фільтру й запобігає розвитку склеротичних процесів у тканині нирок. Він є найефективнішим на стадії мікроальбумінурії: внутрішньом’язово 1 раз протягом 5 днів, 2 дні перерви, курс лікування:
З тижні;
або 10 днів в/м, потім 2 тижні у капсулах (курс по 2 капсули 2 рази на день);
або по 2 капсули 2 рази на день 1 місяць (під контролем рівня альбумінурії), через 1 місяць дозу можна збільшити до 3 капсул 2 рази на день.
За наявності протеїнурії:
1) корекція вуглеводного обміну;
2) корекція АТ у постійному режимі. Препарати вибору – ІАПФ. На цій стадії попереджають розвиток хронічної ниркової недостатності (ХНН) у 50-55% хворих на ЦД;
3) за необхідності – комбінація з препаратами інших груп: петльові діуретики (фуросемід, індапамід), блокатори кальцієвих каналів (недигідропіридинові), препарати центральної дії (моксонідин);
4) низькобілкова дієта (тваринний білок – до 0,8-0,9 г/кг маси тіла на добу, бажано замінити тваринний жир рослинним). Дозволено розширення вуглеводного раціону для покриття енерговитрат;
5) корекція ліпідного обміну. При підвищенні холестерину > 6,5 ммоль/л і тригліцеридів > 2,2 ммоль/л – приєднання гіполіпідемічних засобів (перевага – нікотиновій кислоті);
6) сулодексид (див. вище) – внутрішньом’язово 1 раз на добу 10 днів, після чого – по 2-3 капсули 2 рази на добу 14 днів;
7) індобуфен (інгібітор синтезу тромбоксану Н2) збільшує ШКФ, знижує добову протеїнурію; 1 таблетка 2 рази (400 мг/добу), 3 місяці.
На стадії ХНН:
добова потреба в інсуліні різко знижується;
обмеження білка до 0,6 г/кг/добу;
для лікування гіпертензії перевага надається препаратам із подвійним шляхом елімінації (печінка і нирки) й нетривалої дії (для запобігання кумуляції препарату). Призначення ІАПФ на стадії ХНН продовжує додіалізний період життя хворих на ЦД на 4-5 років. Якщо рівень креатиніну > 300 мкмоль/л, слід бути обережним з прийомом ІАПФ, рекомендується комбінована терапія гіпертензії (ІАПФ + петльові діуретики + антагоністи кальцію + препарати центральної дії);
лікування ниркової анемії (еритропоетин);
корекція фосфорно-кальцієвого обміну;
корекція гіперкаліємії;
ентеросорбція;
L-форми амінокислот;
симптоматичне лікування;
корекція Са-Р обміну;
при підвищенні рівня креатиніну крові > 500 мкмоль/л, зниженні ШКФ < 15 мл/хв – екстракорпоральні (гемодіаліз, перитонеальний діаліз) або хірургічні методи лікування (трансплантація нирки).
Профілактика
Первинна профілактика – ідеальна компенсація ЦД. Вторинна профілактика – дотримання основних принципів лікування ДН.
Юридические аспекты
План обстеження та лікування необхідно обговорити та узгодити як з самим пацієнтом, так і з його близькими. Інформація, надана пацієнту та його рідним, повинна містити мету проведення лікувальних заходів, можливі ускладнення та побічні дії цих заходів, необхідність виконання всієї програми лікування, наслідки невиконання програми лікування.
Діабетична нейропатія
МкХ—10: е10.4, е11.4
Общая информация
Діабетична ретинопатія (ДР) – мікроангіопатія судин сітківки ока при цукровому діабеті, що призводить до зниження зору, а в термінальній стадії – до повної втрати зору. Часто спостерігається у дітей підліткового віку. Провідним фактором патогенезу є спадкова схильність, яка на тлі гіперглікемії призводить до ураження сітківки. Гіперглікемія сприяє підвищенню рівня соматотропіну, що в умовах недостатності інсуліну змінює синтез гепатоцитами білків, які зумовлюють диспротеїнемію. Підвищені рівні фібриногену та a2-глобуліну посилюють агрегацію еритроцитів. Гіперглікемія гальмує продукцію простацикліну ендотеліальними клітинами, а підвищення рівня фактора Віллєбранда та зниження рівня простацикліну, в свою чергу, посилюють агрегацію тромбоцитів. Посилення агрегації еритроцитів і тромбоцитів погіршує гемодинаміку в системі мікроциркуляції, що призводить до розвитку гіпоксії та ішемії сітківки.
Клиническая картина
Проявами ДР є:
1. Мікроаневризми – мішкоподібні випинання стінки капілярів розміром 20-200 мкм.
2. Інтраретинальні геморагії у вигляді плям. Збільшення мікроаневризм передбачає прогресування проліферативної форми ДР.
3. Інтраретинальні мікросудинні аномалії – дрібні, повнокровні, звивисті судини всередині сітківки. Інтраренальна неоваскуляризація свідчить про швидкий початок проліферативного процесу.
4. М’які, нечітко окреслені ексудати білого кольору виникають унаслідок оклюзії капілярних секторів дрібних ретинальних судин, що призводить до гострого порушення кровообігу. Тверді ексудативні вогнища – результат просочування плазми, ліпопротеїнів крізь стінки змінених капілярів.
5. Ретинальні венулярні аномалії, подвоєння венул є індикаторами тяжкої гіпоксії сітківки й виявляються при проліферуючій стадії ДР.
Диагностика
1. Обов’язкова:
зовнішній огляд очного яблука, дослідження гостроти зору й полів зору один раз на шість місяців;
визначення рівня внутрішньоочного тиску один раз на 12 місяців у пацієнтів зі стажем ЦД 10 і більше років;
біомікроскопія кришталика і скловидного тіла за допомогою щілинної лампи;
пряма або зворотня офтальмоскопія із широкою зіницею один раз на 12 місяців, при виявленні ускладнень – кожні 3-6 місяців.
2. Додаткова:
фотографування судин очного дна за допомогою фундус-камери;
флуоресцентна ангіографія;
електрофізіологічні методи дослідження для визначення функціонального стану зорового нерва та сітківки;
УЗД за наявності значних помутнінь у скловидному тілі та кришталику. При раптовому зниженні гостроти зору або появі яких-небудь інших скарг на зір обстеження окулістом повинно проводитися негайно.
Лечение
Повинно здійснюватися спільно ендокринологом і окулістом.
1. Компенсація вуглеводного обміну (НвАІс < 7,0-7,5%). Між ступенем компенсації глікемії і розвитком ДР існує чітка залежність.
2. Використання в лікувальних і профілактичних цілях ангіопротекторів визнано малоефективним, особливо на тлі незадовільної компенсації вуглеводного обміну.
3. Найефективнішим для лікування ДР і профілактики сліпоти в даний час є лазерна фотокоагуляція.
Використовують 3 основні методи лазерної фотокоагуляції: фокальна лазерна фотокоагуляція, бар’єрна лазерна фотокоагуляція, панретинальна лазерна фотокоагуляція.
Терміновість проведення лазерної фотокоагуляції залежить від форми і стадії патології (визначає офтальмолог):
1) набряк макули або макулопатія:
при гострій формі – терміново;
при хронічній формі – протягом декількох тижнів;
2) проліферативна ДР:
при центральній формі (новостворені судини на диску зорового нерва) – терміново;
при периферичній формі (новостворені судини в інших місцях сітківки) – не відкладаючи, протягом 1-2 тижнів;
3) передпроліферативна ДР:
за наявності додаткових факторів ризику – не відкладаючи, протягом декількох тижнів;
за відсутності факторів ризику – протягом 2-3 місяців.
Лікування ДР повинно здійснюватись у трьох на прямках: консервативне, лазерне та хірургічне.
1. Консервативне лікування:
а) дотримання дієтотерапії;
б) адекватна цуркознижувальна терапія;
в) корекція артеріального тиску до цільових значень 130/80 мм рт. ст.;
г) корекція гіперліпідемії;
д) корекція гемодинаміки сітківки (антиагрегатні препарати, ангіопротектори, антипротеолітичні препарати).
2. Лазерна коагуляція:
а) фокальна лазерна фотокоагуляція (нанесення коагулянтів у місцях просочування флуоресцеїну при проведенні флуоресцентної ангіографії);
б) бар’єрна лазерна коагуляція (нанесення дрібних коагулянтів парамакулярно, в декілька рядів, при непроліферативній ДР із набряком макулярної області);
в) панретинальна лазерна фотокоагуляція (нанесення коагулянтів по всій площі сітківки, обминаючи макулярну зону, використовують при проліферативній ДР).
Протипоказання до лазерної коагуляції: катаракта, більмо рогівки, гемофтальм, фіброз скловидного тіла, відшарування сітківки, виражений фіброз, ригідна зіниця.
3. Хірургічне лікування:
а) кріокоагуляція (транскон’юнктивальна, транссклеральна);
б) вітректомія.
Критерії ефективності лікування
Стабілізація прогресування ретинопатії.
Профілактика
Первинна профілактика ДР спрямована на попередження розвитку патології очного дна, яка базується на ідеальній компенсації ЦД. Вторинна профілактика спрямована на лікування хворих з нета препроліферативною стадіями ДР, для попередження розвитку проліферації новоутворених судин сітківки.
Юридические аспекты
План обстеження та лікування хворої дитини необхідно обговорити та узгодити з батьками, або, за їх відсутності, з легальними опікунами дитини у письмовому вигляді. Пацієнта інформують про мету відповідних лікувальних заходів, можливі ускладнення, необхідність виконання всієї програми лікування, наслідки невиконання програми лікування, зокрема зниження якості зору, сліпоти.
Діабетична Хайропатія
МкХ—10: е10.6¬е14.6
Общая информация
Діабетична хайропатія (ДХ), або синдром діабетичної руки чи синдром обмеженої рухомості суглобів є одним з найчастіших ускладнень ЦД у дітей та підлітків. ДХ характеризується безболісними контрактурами, які розвиваються переважно в кистях рук.
Етіологія
ДХ виявляється приблизно у 25-40% дітей та підлітків з тривалістю ЦД більше 5 років. При досягненні пубертатного віку ризик розвитку ДХ значно підвищується. Вплив статі на розповсюдженість ДХ не виявлено.
Патологічна фізіологія
При ДХ зміни виникають в периартикулярних тканинах. Обмежена рухливість суглобів є результатом взаємодії метаболічних, генетичних та середовищних факторів. Провідним фактором в механізмах розвитку ДХ є довготривалий вплив гіперглікемії на органи та тканини. Ключові процеси ураження сполучної тканини поєднані з хімічною модифікацією структури колагену внаслідок глікування та окислення. Інші фактори, які сприяють розвитку ДХ, – це активація сорбітолового шляху та мікроангіопатії.
Клиническая картина
В першу чергу, виявляється обмеженість рухомості метакарпальнофалангових та проксимальних суглобів п’ятих пальців кистей рук. В подальшому ці зміни можуть виявлятись в інших пальцях. Процес, як правило, носить двосторонній характер та розповсюджується від п’ятого пальця радіально. В деяких випадках виявляється порушення рухомості в променезап’ясткових суглобах, шийному і навіть грудному відділах хребта, а також у суглобах стопи. Хворі скаржаться на відчуття скутості зранку або напруження в кистях рук. У деяких пацієнтів виражені контрактури ускладнюють проведення тонких ручних маніпуляцій. При здавленні серединного нерва розвивається компресійна нейропатія, яка клінічно проявляється парестезіями, болями з іррадіацією в область плеча та шиї. Пізніше приєднуються слабкість та атрофія м’язів долонь.
Классификая и примеры формулировки диагноза
ДХ має три ступені (A. L. Rosenbloom, 1982):
1 ступінь (легкий) – порушення об’єму в одному або двох проксимальних міжфалангових, одному великому суглобі або тільки двостороннє обмеження рухомості метакарпальнофалангових суглобів.
2 ступінь (помірний) – порушення об’єму руху трьох та більше проксимальних міжфалангових суглобів або двостороннє обмеження рухливості метакарпальнофалангових та будь-якого великого суглоба.
3 ступінь (тяжкий) – явна деформація кисті або поєднання обмеженої рухливості суглобів кистей рук з ураженням шийного відділу хребта.
Диагностика
• детальний збір анамнезу;
• фізикальний огляд хворого (наявність больового синдрому, деформації, набряк, згинальні, розгинальні контрактури, обмеження рухливості суглобів, підвищення температури, можливість виконувати дрібні різноманітні дії);
• лабораторні дослідження (підвищення ШОЕ, позитивна реакція на С-реактивний білок);
• інструментальні методи (рентгенологічний, ультразвукова денситометрія);
• консультація спеціалістів (невропатолог, окуліст).
Лечение
• ідеальна компенсація ЦД;
• ретельний контроль метаболізму;
• дієта (обмеження їжі з великим вмістом жирів, особливо тваринного походження, розширений вміст продуктів, які містять вітаміни, кальцій та фосфор);
• фізичні вправи та фізіотерапевтичні процедури (УВЧ-терапія, магнітота лазеротерапія, масаж, електрофорез);
• препарати кальцію, тривалість лікування 30-60 діб 2-3 рази на рік;
• нестероїдні протизапальні препарати, курс лікування до 7-10 діб.
Юридичні аспекти
План обстеження та лікування обов’язково треба обговорювати з пацієнтом та його рідними або опікунами. Надавати необхідну інформацію про мету проведення відповідних лікувальних заходів, можливі ускладнення, побічні дії, їх попередження й усунення, необхідність виконання всієї програми лікування.
Діабетична Хайропатія
МкХ—10: е10.6¬е14.6
Общая информация
Ліпоїдний некробіоз (ЛН) – рідкісне ураження шкіри з утворенням бляшки неправильної форми, з фестончастими краями, приграничною інфільтрацією шкіри по периферії та центральною атрофічною ділянкою на передній поверхні гомілки.
Етіологія
Серед хворих на ЦД розповсюдженість ЛН складає 0,3%. Процес може маніфестувати вже на початку ЦД, а в деяких випадках – навіть попереджати його типові клінічні прояви.
Патогенез
Патогенез ЛН до кінця не вивчений. Хоча вважається, що в розвитку ЛН глікемічний контроль не має великого значення, але в більшості випадків це ускладнення частіше зустрічається у дітей та підлітків з тяжким перебігом ЦД, які мають високий рівень глікованого гемоглобіну та інші ускладнення ЦД. Ключовим моментом у виникненні ЛН вважається судинний компонент, а порушення вуглеводного обміну та генетичні фактори суттєвої ролі у виникненні процесу не мають. Знайдена при гістологічному дослідженні патологія колагену дає привід зауважити пряме етіологічне значення стану колагену: прискорення його старіння при ЦД або гіпергідратація продуктів його обміну.
Клиническая картина
На передній поверхні гомілки утворюються бляшки неправильної форми з центральною атрофічною ділянкою жовтого кольору та інфільтрацією шкіри на периферії. Процес може починатися з маленької твердої червонокоричневої папули, яка поступово збільшується.
В деяких випадках на поверхні можуть бути телеангіектазії та гіперкератозні лусочки. Ураження зазвичай множинне, частіше – двостороннє, з вогнищами різної величини. У 1/3 хворих спостерігаються виразки на шкірі, які провокуються травмою. В деяких випадках пацієнти скаржаться на свербіж, парестезії, біль у ділянці ураження, але в більшості випадків процес протікає безсимптомно. Окрім нижніх кінцівок, зустрічається інша локалізація ураження – руки, пальці, обличчя, волосиста частина голови.
• Рентгенотерапія ураженої ділянки.
• Хірургічне лікування при виразці ділянки.
Профілактика
Лечение
• Максимальна метаболічна та клінічна компенсація ЦД.
• Препарати нікотинової кислоти (нікотинамід – по 1 таблетці 3 рази на добу, курс – 1 місяць).
• Вазоактивні препарати (трентал – 500-1000 мг/добу, курантил – 25-150 мкг/добу, курс – 1 місяць).
• Фізіотерапевтичне лікування (магнітно-резонансна терапія або лазеротерапія, 10 сеансів на курс лікування).
Стійкий контроль та самоконтроль ЦД, виконання гігієнічних процедур.
Юридичні аспекти
Узгодження плану обстеження та лікування з пацієнтом та батьками (опікунами) хворої дитини.









Комментировать