Успех лечения методами вспомогательной репродукции. лимиты для лечения возрастных пациентов. Лимиты для лечения возрастных пациентов. Обзор литературы по мировым исследованиям.
О.Л. Тишкевич, А.Б. Жабинская, Е.В. Алексеева, С.М. Волоханович, Ю.В. Черноморец
Центр вспомогательной репродукции «Эмбрио», Минск, Республика Беларусь
Доступность современных методов контрацепции, стремление к получению образования и карьерные соображения побуждают современных женщин откладывать рождение детей «на потом». А поскольку с возрастом фертильность снижается, все большему количеству женщин старшего возраста проводится лечение при помощи вспомогательных репродуктивных технологий (ВРТ) после множества неудачных попыток забеременеть самостоятельно.
Успех лечения методами вспомогательной репродукции определяется множеством факторов, основные из которых:
- состояние овариального резерва;
- эффективная стимуляция яичников и получение достаточного количества зрелых ооцитов;
- гормональная подготовка эндометрия к имплантации эмбриона;
- количество и качество переносимых в матку эмбрионов;
- техника переноса эмбрионов в матку;
- адекватная поддержка лютеиновой фазы.
Количество и функциональная компетентность примордиальных фолликулов и герминативных клеток в яичнике составляет его резерв, который, безусловно, имеет значительное влияние на фертильный потенциал.
К снижению овариального резерва приводят возрастные изменения в яичниках, оперативные вмешательства на них, перенесенные воспалительные заболевания органов малого таза, генитальный эн дометриоз, другие факторы (аутоиммунная, эндокринная патология, химио и лучевая терапия).
Возраст женщины один из ведущих факторов снижения овариального резерва и бесплодия. Старение женщины сопровождается истощением пула примордиальных фолликулов, уменьшением количества ооцитов и снижением их качества изза дезорганизации мейотического веретена ооцита, что в дальнейшем ведет к анеуплоидии.
Снижение с возрастом количества ооцитов непреодолимый процесс. Женщины обладают ограниченным запасом герминативных клеток, который не пополняется. При рождении у девочки имеется около 1 млн оогоний, а к началу полового созревания это число снижается до 300 000. С возрастом истощение запаса ускоряется, и у женщины в возрасте 3738 лет количество фолликулов достигает 25 000.
Известно, что хромосомная анеуплоидия чаще встречается у женщин старшего возраста. Еще в 30х годах прошлого века была доказана связь между возрастом матери и риском синдрома Дауна у плода. Встречаемость трисомий среди всех клинических беременностей составляет менее 0,2 % у женщин моложе 25 лет и более 3,5 % у женщин старше 40 лет [6]. Многочисленные многоцентровые исследования, проведенные с помощью методов преимплантационной генетической диагностики при проведении лечения бесплодия методами ВРТ показали, что частота анеуплоидии даже в морфологически нормальных и хорошо развивающихся эмбрионах значительно возрастает с возрастом женщины. Кроме того, FISHанализ ооцитов и эмбрионов, полученных в программах ВРТ у пациенток старшего возраста, выявляет анеуплоидию более чем в 50 % случаев [8].
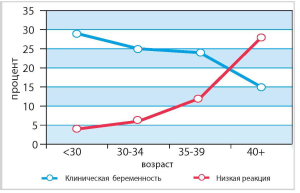
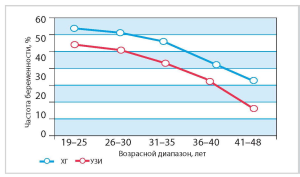
Все это обусловливает, что с возрастом эффективность программ ВРТ драматически снижается, увеличивается доля «слабого ответа» (рис. 1).
Это особенно заметно при анализе результатов лечения бесплодия методами ВРТ у женщин старше 40 лет.
По данным CentersforDiseaseControl (CDC) в США в 2005 г. частота родов одним живым плодом (singletonlivebirthrate) составила 29 % у женщин 24 лет и лишь 3 % у женщин 44 лет (рис. 2).
Рис. 1. Связь возраста, частоты наступления беременности и доли «слабого ответа» в программах VF [4] 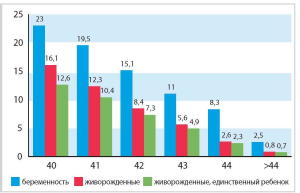
Рис. 2. Эффективность свежих недонорских ВРТ циклов у женщин 40 лет и старше (% – pregnancies, live births, singleton live births) в США в 2005 г. [2]
ПодобныеданныеприводитHuman Fertilization and Embryology Authority (HEFA). Великобритания. За период 19922005 гг. частота родов живым плодом (livebirthrate) на начатый цикл IVFсоставила 7,6 % у пациенток 4044 лет и лишь 0,9 % у женщин 4549 лет. В 2008 г. на конференции EuropeanSocietyofHumanReproductionandEmbryology (ESHRE) Dr. Sullivanпредставила статистику результатов экстракорпорального оплодотворения (IVF) в Австралии у женщин 45 лет и старше за 20022005 гг. Из 1101 начатого цикла IVF639 (58 %) завершились переносом эмбрионов, 21 женщина забеременела, и только 6 беременностей завершились родами живым плодом. Частота родов живым плодом на цикл составила 0,5 %, на ЕТ 0,9 % [2].
С возрастом достоверно увеличивается риск прерывания беременности. Так, по данным HEFA, частота прерывания беременностей после IVFсоставляет:
- в возрасте 30 лет 10,5 %;
- в возрасте 35 лет 13,1 %;
- в возрасте 40 лет 22,7 %;
- в возрасте 43 лет 40,7 %.
Беременность после 40 лет это беременность высокого риска. Течение беременности у женщин старшего возраста сопряжено с риском спонтанных абортов, хромосомных аномалий плода, преждевременных родов, недоношенностью и низким весом плодов, а также с высокой частотой осложнений беременности и родов. Кроме того, высок риск перинатальной и материнской смертности [7].
Возможности повышения эффективности лечения бесплодия после 40 лет весьма ограничены. Это: адекватная оценка овариального резерва, совершенствование протоколов стимуляции, преимплан тационная генетическая диагностика ооцитов и эмбрионов, донорство ооцитов.
Проведение ВРТ у женщин старше 40 лет продолжает оставаться актуальной темой этических дебатов и научных дискуссий. Главные вопросы этих дискуссий:
- Проводить ли лечение, если эффективность близка к нулю?
- Приемлемо ли этически проводить лечение только тем, у кого хороший шанс на успех?
В странах Евросоюза существуют определенные лимиты для лечения возрастных пациентов.
Britain’sNationalInstituteforHealthandClinicalExcellence (NICE) рекомендует проводить IVF, только если эффективность лечения составляет более 10 %. В Бельгии установлен возрастной лимит для проведения IVF 43 го да. Во многих федеральных землях Германии страховые компании не оплачивают лечение пациенткам старше 40 лет.
Демографические тенденции современного развитого общества в полной мере проецируются и на ситуацию в Беларуси. В настоящее время Республика Беларусь характеризуется целым рядом негативных демографических тенденций, одной из которых является изменение возрастной структуры рожающих женщин. По рангу значимости когорта женщин, рожающих в возрасте 2024 лет, занимает первое место, обеспечивая около 43 % всех родившихся. Наблюдается снижение рождаемости в возрасте до 20 лет, что, в основном, связано с более поздним вступлением как в первый, так и в повторные браки в ряду ранжирования эта группа женщин занимает третье место (11,8 % рождений). Второе место в ранге занимают женщины в возрасте 2529 лет, рожающие около 29 % всех детей. Затем идет когорта женщин 3034 лет (11 % рождений). Возрастные группы 3539, 4044, 4549 лет занимают низкие ранговые места в возрастной структуре рождаемости и в совокупности обеспечивают 5,2 % рождений. Однако суммарно число детей, рожденных от матерей в возрасте после 30 лет, возросло и достигло 17 %. Есть основания предполагать, что данная тенденция будет сохраняться.
По данным нашего Центра, доля пациенток старше 36 лет в программах ВРТ составляет 31 %, а доля пациенток старше 40 лет 7,2 % без тенденции к снижению.
Целью нашего исследования явилась оценка эффективности программ ВРТ у пациенток разных возрастных групп, в особенности у женщин старше 40 лет.
Мы провели два последовательных ретроспективных исследования.
В первое исследование включены 403 полных цикла IVFи IVF+ инъекция сперматозоида в клетку (ICSI). Возраст пациенток составил 1948 лет. Они были распределены по группам: 1925, 2630, 3135, 3640, 4148 лет. Стимуляция яичников проводилась по «длинному» протоколу (аГнРГ диферелин, Ipsen; рекФСГ ГоналФ, Serono; фоллико стимулирующий гормон (ХГЧ) Прегнил, Organon). Оплодотворение in vitroпроводилось по стандартной методике. Перенос эмбрионов в матку проводили на 3й день после получения ооцитов. С целью поддержки лютеиновой фазы использовали пероральные и интравагинальные гестагены (Ду фастон, Solvay Pharma; Утрожестан, Besins Int.) и хорионический гонадотропин человека (ХГЧ) (Прегнил, Organon).
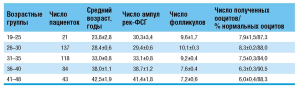
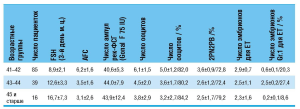
По данным проведенного исследования эффективность овариальной стимуляции напрямую зависит от возраста женщины. С возрастом требуется применение больших дозировок гонадотропинов для достижения адекватного ответа яичников в программах ВРТ. При этом количество зрелых фолликулов и получаемых нормальных ооцитов снижается (табл. 1).
Таблица 1
Клинико-эмбриологическая оценка результатов IVF в зависимости от возраста пациенток.
Результаты овариальной стимуляции
С возрастом снижается частота нормального оплодотворения и нормального развития эмбрионов invitro(рис. 3).
Частота наступления беременности напрямую зависит от возраста пациенток и снижается в 3,3 раза с увеличением возраста от 19 до 48 лет (с 46,6 до 14,0 %) (рис. 4).
Наиболее актуальной и интересной нам показалась оценка результатов ВРТ у женщин старше 40 лет.
С этой целью нами проведено дополнительное исследование в данной возрастной группе.
В исследование включено 140 свежих недонорских циклов IVFи IVF+ICSIи 41 цикл IVFс донорскими ооцитами. Возраст женщин составил 4150 лет. Пациенток распределили по группам 4142, 4344, 45 лет и старше. В исследование включены женщины с базальным уровнем ФСГ < 25 IU/L(недонорские циклы). На 3й день менструального цикла в протоколе стимуляции оценивалось количество антральных фолликулов (AntralFollicleCount AFC). Протоколы стимуляции яичников длинный (аГнРГ Диферелин + рекФСГ ГоналФ + ХГЧ Прегнил). Протокол подготовки эндометрия к переносу эмбрионов (в циклах с донорскими ооцитами) — Прогинова, Schering + Дуфастон + Утрожестан. Оплодотворение in vitro осуществляли по стандартной методике. Перенос эмбрионов в матку проводили на 3й день после получения ооцитов. Поддержка лютеиновой фазы проводилась с использованием гестагенов (Дуфастон + Утрожестан) и ХГЧ (Прегнил).
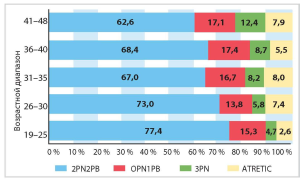
Клиникоэмбриологические результаты недонорских циклов IVF представлены в таблице 2 и на рис. 5.
В группах пациенток не получено достоверных различий в оцениваемых параметрах (базальный ФСГ, доза рекФСГ, число ооцитов и число нормальных ооцитов, показатели нормального оплодотворения). Выявлена тенденция снижения с возрастом количества и доли эмбрионов высокого качества Grade1.
Рис. 3. Сравнительная оценка оплодотворения у пациенток разного возраста
Рис. 4. Частота наступления беременности у пациенток разных возрастных групп
Таблица 2
Клинико-эмбриологическая оценка результатов ЭКО у пациенток старше 40 лет
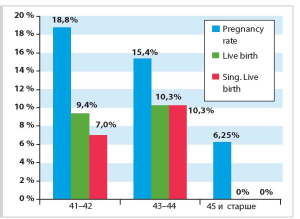
Частота наступления беременности с возрастом драматически снижалась, и составила 18,8 % в возрастной группе 4142 лет, 15,4 % в группе 4344 лет, 6,5 % в группе 45 лет и старше. При этом частота родов живым плодом составила 9,4 % в первой группе, 10,3 % во второй и, что важно, 0 % — у женщин 45 лет и старше.
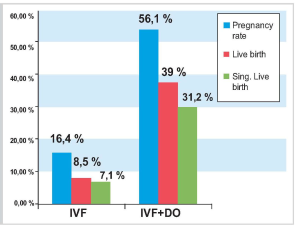
Наиболее интересны и красноречивы результаты ^ с донорскими ооцитами по сравнению с недонорскими циклами ^ у женщин старше 40 лет. Частота наступления беременности в группе ^ с донорскими ооцитами составила 56,1 %, частота родов живым плодом 39,0 %, в то время как в группе недонорского ^ 16,4 и 8,5 % соответственно (рис. 6).
Оценка овариального резерва один из ключевых факторов успеха лечения бесплодия методами ВРТ.
В качестве маркеров овариального резерва мы использовали: базальный уровень ФСГ (на 3й день менструального цикла), число антральных фолликулов на 3й день цикла (AntralFollicleCountAFC). Наши наблюдения совпадают с выводами ряда западных коллег.
Одного ФСГ недостаточно для оценки овариального резерва у женщин старше 40 лет. По образному выражению R. Scott, три женщины 29, 39 и 49 лет с идентичными нормальными базальными уровнями ФСГ имеют далеко не одинаковый репродуктивный потенциал [11]. Подобные выводы на основании своих данных делает I. VanRooij: пациентка в возрасте >41 года с нормальным ФСГ гораздо хуже пациентки <41 года с повышенным уровнем ФСГ [10].
AFCкоррелирует с числом получаемых ооцитов и является хорошим прогностичеким маркером ответа яичников на стимуляцию. Этот показатель достоверно более лучший маркер «слабого ответа», чем возраст, ФСГ и другие эндокринные маркеры [1, 3]. AFC лучший прогностический критерий ответа яичников на стимуляцию, чем базальный ФСГ у женщин >38 лет в программах ВРТ [8].
Рис. 5. Результаты IVF у женщин старше 40 лет
Рис. 6. Результаты IVF у пациенток старше 40 лет. Недонорские и донорские циклы
Вывод
Возраст женщины главный прогностический критерий эффективности лечения методами ВРТ. Проведение лечения бесплодия у пациенток старшего возраста со сниженным овариальным резервом требует:
- адекватной оценки величины овариального резерва;
- уменьшения длительности консервативно голечения при бесплодии,учитывая возраст пациенток и фактор величины овариального резерва;
- выбора оптимальной тактики при применении ВРТ для лечения бесплодия и расширение применения ВРТ с донорскими ооцита ми.
Лечение бесплодия после 40 лет продолжает оставаться серьезной проблемой для специалистов и актуальной темой этических дебатов и научных дискуссий.
Литература
- Bancsi L. et al. Performance of basal folliclestimu lating hormone in the prediction of poor ovarian response and failure to become pregnant after in vitro fertilization: a metaanalysis // Fertil. Steril.
- V.79. P. 10911100.
- Brown S. Fertility in the overforties // Focus Reprod. 2008. V.47. P. 3034.
- Chang M. et al. Use of the antral follicle count to predict the outcome of assisted reproductive technologies //Fertil. Steril. 1998. V.69. P. 505510.
- Copperman A. Antagonists in poorresponder patients //Fertil. Steril. 2003. V.80. P. S16 S24.
- ESHRE Task Force on Ethics and Law 14: Equity of access to assisted reproductive technology //Hum. Reprod. 2008. V.23. P. 772774.
- ESHRE Capri Workshop Group: Fertility and Aging //Hum. Reprod. Update. 2005. V.11. P. 261276.
- Jacobsson B. et al. Advance maternal age and adverse perinatal outcome //Obstet. Gynecol.
- V.104. P. 727733.
- Klinkert R. The antral follicle count is a better marker than basal folliclestimulated hormone for the selection of older patients with acceptable pregnancy prospects after in vitro fertilization //Fertil. Steril. 2005. V.83. P. 811814.
- Kuliev A., Verlinsky Y. The role of preimplantation genetic diagnosis in women of advanced reproductive age //Curr. Opin. Obstet. Gynecol. 2003. V.15. P. 233238.
- Van Rooj I. et al. Women older 40 years of age and those with elevated folliclestimulating hormone levels differ in poor response rate and embryo quality in vitro fertilization //Fertil. Steril. 2003. V.79. P. 482488.
- Scott R. Diminished ovarian reserve and access to care //Fertil. Steril. 2004. V.81. P. 14891491.
Данная статья взята из журнала «Гендерна медицина», № 3(09), 2009.









Комментировать