Ингибиторы нейраминидазы, такие как осельтамивир (Tamiflu®) и занамивир (Relenza®) рекомендованы для раннего лечения гриппа Центрами по контролю и профилактике заболеваний США, Обществом вирусологии Германии и Национальным институтом здоровья и клинического совершенствования Великобритании (NICE). Доказано, что данные вещества способны сокращать длительность и облегчать течение болезни, особенно при раннем начале приёма.
Согласно результатам исследования, которое приводится далее, горячий напиток на основе экстракта эхинацеи оказывает равнозначный терапевтический эффект, имея при этом меньше противопоказаний и нежелательных реакций.
Отмечается, что успех терапии ингибиторами нейраминидазы зависит от чувствительности вирусов к этим препаратам. Например, на протяжении зимы 2008-2009 годов большинство сезонных подтипов гриппа H1N1 выработало резистентность к осельтамивиру. [16] И хотя в последующие годы появились новые подтипы гриппа, которые оказались чувствительны к терапии НП, при назначении лекарственных средств данной группы нельзя исключать вероятность развития резистентности штамма.
В то же время, на данный момент нет информации о развитии резистентности штаммов и подтипов гриппа к препаратам на основе эхинацеи (Echinacea purpurea). Вытяжки из данного растения показали эффективность в отношении вирусов гриппа H1N1, H3N2, H5N1, H7N7 и H1N1pdm2009, включая подтипы H1N1, которые имели резистентность к осельтамивиру. [17,18]
Кроме того, сообщается, что экстракт эхинацеи вызывает значительно меньше побочных эффектов, в то время как осельтамивир может провоцировать тошноту, рвоту, неврологические расстройства и прочие нежелательные реакции. [16]
Дизайн исследования
Оба препарата прошли параллельное многоцентровое двойное слепое рандомизированное плацебоконтролируемое клиническое исследование эффективности на базе 29 заведений общей практики в Среднечешском крае Чехии.
473 пациента европеоидной расы с ранними симптомами острого гриппа (≤48 часов) были отобраны в период с 22 ноября 2011 года по 29 апреля 2013 года и после обследования распределены в 2 группы численностью 237 и 236 пациентов. В ходе испытания часть пациентов была исключена из исследования в связи с несоблюдением протоколов или приемом несовместимых лекарственных препаратов. В конечном итоге, число пациентов составило 203 человека в группе, получавшей экстракт эхинацеи, и 217 пациентов в группе, получавшей осельтамивир.
Первая группа пациентов получала эхинацею в виде горячего напитка Echinaforce ® Hotdrink на протяжении 10 дней. Вторая группа пациентов получала осельтамивир на протяжении первых 5 дней и плацебо на протяжении последующих 5 дней. Для купирования тяжелых симптомов гриппа пациентам также выдали «спасательные препараты» — парацетамол и декстрометорфан.
Участники исследования получили дневники для ежедневной записи симптомов гриппа в течение всего периода лечения. По завершении лечения было проанализировано количество возвращенных лекарственных средств и оценено использование «спасательных препаратов». Образцы крови брали для анализа гематологических и метаболических параметров до и после лечения.
Доля выздоровевших пациентов (симптомы гриппа, оцененные как отсутствующие или умеренные в вечернее время суток) была проанализирована на предмет неравномерности с использованием обобщенного теста Уилкоксона с уровнем значимости α = 0,05 (2-сторонний) и использованием подхода Continuous Integration.
Дозировка
Echinaforce® Hotdrink содержит водноспиртовой экстракт (65% об.) травы (коэффициент экстракции 1:12) и корней (коэффициент экстракции 1:11) эхинацеи (Echinacea purpurea) в соотношении 95% к 5%. 240 мг вышеуказанного активного ингредиента сконцентрировали до густого экстракта и дополнили 276,5 мг экстракта бузины (Sambucus fructus), после чего добавили наполнители, достаточные для получения 1 мл готового препарата. Плацебо-сироп содержал те же наполнители, что и верум, плюс красители и ароматизаторы. Экстракт верум и соответствующее плацебо были разлиты в стеклянные бутылки объемом 200 мл из темно-коричневого стекла.
Компаратор был изготовлен путем рекапсуляции оригинальных капсул осельтамивира (Tamiflu® 75 мг, Hoffmann-La Roche AG) с использованием оптически плотных, темно-зеленых твердых желатиновых капсул. Соответствующее плацебо представляло собой твердые желатиновые капсулы, заполненных микрокристаллической целлюлозой и неотличимые от капсул верум.
Парацетамол и декстрометорфан были предоставлены в качестве «спасательных препаратов» в виде таблеток Paralen® 500 мг и таблеток Stopex® 30 мг, которые использовались в соответствии с инструкциями соответствующих производителей.
Участникам группы Echinaforce® Hotdrink было поручено принять в первые 3 дня 5×5 мл сиропа верум, растворенного в приблизительно 150 мл горячей воды, и 3×5 мл сиропа в течение последующих 7 дней. Точное дозирование обеспечивалось с помощью измерительной ложки, калиброванной в 5 мл. Параллельно пациентам было поручено принимать осельтамивир плацебо два раза в день в течение 10 дней.
Группе осельтамивира верум было дано указание придерживаться того же режима в приеме плацебо-сиропа плюс 5 дней принимать верум-капсулы осельтамивира, а затем еще 5 дней — капсулы-плацебо по два раза в день.
Результаты
В таблице показана количество пациентов, которые выздоравливали в ходе лечения. Показатели восстановления оказались практически идентичными для обеих групп. Ослабление симптомов заболевания по прошествии 1, 5 и 10 дней от начала лечения составило 1,5%, 50,2% и 90,1% для пациентов, получавших сироп эхинацеи, и 4,1%, 48,8% и 84,8% для пациентов, получавших осельтамивир.
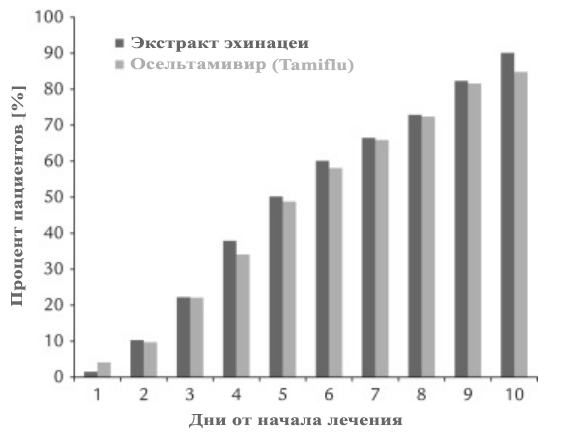
Процент неудачного лечения по прошествии 10 дней показал статистически незначительный перевес в пользу эхинацеи (P> 0,05). В общей сложности на терапию эхинацеей до истечения 10 дня не ответили 9,9% пациентов и осельтамивиром — 15,2%. Данная статистика касается пациентов с клинически диагностированным гриппом.
Ни в один из дней лечения не было продемонстрировано статистически значимое преимущество осельтамивира перед эхинацеей, в то время как оба препарата показали эффективность в сравнении с плацебо в исследованиях, проведенных ранее.
Симптомы заболевания ослабевали и проходили примерно с одинаковой скоростью в обеих группах. Уменьшение таких симптомов как головная боль, кашель и мышечная боль было незначительно более выражено в группе терапии с использованием эхинацеи, но не достигло статистической значимости (P > 0.05). Температура тела нормализовалась в обеих группах в течение первых 2 дней терапии (P = 0.193). Никаких различий между группами с точки зрения возврата к нормальной повседневной активности и нарушений сна не наблюдалось.
Одной из проблем в терапии гриппа является развитие тяжелых осложнений, которые возникают при отсутствии терапии, согласно предыдущим исследованиям, с частотой порядка 10,3%. [23] Число осложнений, возникших в ходе данного клинического испытания, составило 6,5% в группе осельтамивира и 4% в группе эхинацеи. Эта разница приближается к статистической значимости (тест χ2 P = 0,079).
Что касается побочных эффектов, об их возникновении сообщили 11,4% пациентов в группе эхинацеи и 13,9% в группе осельтамивира. При этом из-за нежелательных реакций терапию прекратили, соответственно, 2,2% и 5,2% пациентов. Большинство случаев отказа от приема осельтамивира было связано с тошнотой и рвотой, которые возникали в данной группе в 5 раз чаще, чем в группе терапии эхинацеей, и в 9 случаях привели к прекращению лечения. Сообщалось также о таких серьезных побочных эффектах, как энцефалит, миелит, миокардит или септический шок.
Никаких клинически значимых изменений в биохимических или гематологических лабораторных показателях (эритроциты, лейкоциты, тромбоциты, гемоглобин, гематокрит, MCV, MCH, MCHC, креатинин, холестерин, общий билирубин, АСТ и ГГТ) до и после прохождения терапии не наблюдались.
219 пациентов (95,6%) из группы эхинацеи и 214 пациентов (93%) из группы осельтамивира оценили переносимость лечения как «хорошую» или «очень хорошую». Статистически значимой разницы между группами не было.
По материалам: Effect of an Echinacea-Based Hot Drink Versus Oseltamivir in Influenza Treatment: A Randomized, Double-Blind, Double-Dummy, Multicenter, Noninferiority Clinical Trial, Karel Rauš (Canadian Medical Care, Prague, Czech Republic), Stephan Pleschka (Institute of Medical Virology, Justus-Liebig-University Giessen, Giessen, Germany), Peter Klein MSc (D.S.H. Statistical Services GmbH, Rohrbach, Germany), Roland Schoop MSc (A. Vogel Bioforce AG, Roggwil, Switzerland), Peter Fisher (Royal London Hospital for Integrated Medicine, London, United Kingdom), 20 April 2015, Eudra-CT: 2010-021571-88 https://www.sciencedirect.com/science/article/pii/S0011393X15000053
Литература:
- D.M. Fleming, A.J. Elliot, J.S. Nguyen-van Tam, et al. A winter’s tale: Coming to terms with winter respiratory illnesses, Health Protection Agency, London (2005)
- O. Weber The role of viruses in the etiology and pathogenesis of common cold R.W.O. Eccles (Ed.), Common Cold, Birkhäuser Verlag, Basel, Switzerland (2009), pp. 132-133
- S.A. Call, M.A. Vollenweider, C.A. Hornung, et al.Does this patient has influenza? JAMA, 293 (2005), pp. 987-997
- K.G. NicholsonClinical features of influenza Semin Respir Infect, 7 (1992), pp. 26-37
- A.S. Monto, S. Gravenstein, M. Elliott, et al.Clinical signs and symptoms predicting influenza infectionArch Intern Med, 160 (2000), pp. 3243-3247
- G. Boivin, I. Hardy, G. Tellier, et al. Predicting influenza infections during epidemics with use of a clinical case definition Clin Infect Dis, 31 (2000), pp. 1166-1169
- J. Guarner, C.D. Paddock, W.H. Shieh, et al.Histopathologic and immunohistochemical features of fatal influenza virus infection in children during the 2003-2004 season Clin Infect Dis, 43 (2006), pp. 132-140
- M. StudahlInfluenza virus and CNS manifestations J Clin Virol, 28 (2003), pp. 225-232
- D.G. Jaimovich, A. Kumar, C.L. Shabino, R. FormoliInfluenza B virus infections associated with non-bacterial septic shock-like illness J Infect, 25 (1992), pp. 311-315
- T.R. CateClinical manifestations and consequences of influenza Am J Medicine, 82 (1987), pp. 15-19
- T.A. Reichert, L. Simonsen, A. Sharma, et al.Influenza and the winter increase in mortality in the United States, 1959-1999 Am J Epidemiol, 160 (2004), pp. 492-502
- K.G. Nicholson, J. Kent, V. Hammersley, E. CancioRisk factors for lower respiratory complications of rhinovirus infections in elderly people living in the community: prospective cohort study BMJ, 313 (1996), pp. 1119-1123
- J.J. Treanor, F.G. Hayden, P.S. Vrooman, et al.Efficacy and safety of the oral neuraminidase inhibitor oseltamivir in treating acute influenza: a randomized controlled trial. US oral Neuraminidase Study Group JAMA, 283 (2000), pp. 1016-1024
- F.Y. Aoki, M.D. Macleod, P. Paggiaro, et al., IMPACT Study GroupEarly administration of oral oseltamivir increases the benefits of influenza treatment J Antimicrob Chemother, 51 (2003), pp. 123-129
- R.J. Whitley, C.A. Boucher, B. Lina, et al.Global assessment of resistance to neuraminidase inhibitors, 2008-2011: the Influenza Resistance Information Study (IRIS) Clin Infect Dis, 56 (2013), pp. 1197-1205
- T. Jefferson, M.A. Jones, P. Doshi, et al.Neuraminidase inhibitors for preventing and treating influenza in healthy adults and children Cochrane Database Syst Rev (2014), p. 4 CD008965
- S. Pleschka, M. Stein, R. Schoop, J.B. HundsonAnti-viral properties and mode of action of standardized Echinacea purpurea extract against highly pathogenic avian influenza virus (H5N1, H7N7) and swine-origin H1N1 (S-OIV) Virol J, 6 (2009), p. 197
- M. Sharma, S.A. Anderson, R. Schoop, J.B. HudsonInduction of multiple pro-inflammatory cytokines by respiratory viruses and reversal by standardized Echinacea, a potent antiviral herbal extract Antiviral Res, 83 (2009), pp. 165-170
- M. Sharma, R. Schoop, J.B. HudsonEchinacea as an anti-inflammatory agent: the influence of physiologically relevant parameters Phytother Res, 23 (2009), pp. 863-867
- M.R. Ritchie, J. Gertsch, P. Klein, R. SchoopEffects of Echinaforce® treatment on ex vivo-stimulated blood cellsPhytomedicine, 18 (2011), pp. 826-831
- G.A. Colditz, J.N. Miller, F. MostellerMeasuring gain in the evaluation of medical technology: the probability of a better outcome Int J Technol Assess Health Care, 4 (1988), pp. 637-642
- R.G. NewcombeInterval estimation for the difference between independent proportions: comparison of eleven methods Stat Med, 17 (1988), pp. 873-890
- L. Kaiser, C. Wat, T. MillsImpact of oseltamivir treatment on influenza-related lower respiratory tract complications and hospitalizations Arch Internal Med, 163 (2003), pp. 1667-1672
- D.L. Schanzer, M.J. Garner, T.F. Hatchette, et al.Estimating Sensitivity of Laboratory Testing for Influenza in Canada through Modelling PLoS ONE, 4 (2009), pp. 1-7
- M. Jawad, R. Schoop, A. Suter, et al.Safety and efficacy profile of echinacea purpurea to prevent common cold episodes: a randomized, double-blind, placebo-controlled trial Evid Based Complement Alternat Med (2012), p. 841315 2012
- D.Y. Oh, A.C. HurtA review of the antiviral susceptibility of human and avian influenza viruses over the last decade Scientifica (Cairo) (2014), p. 430629 2014













Комментировать