Стадии хронических нарушений мозгового кровообращения. Хроническая ишемия головного мозга. Оценка эффективности и безопасности применения препарата Кортексин у пациентов с хроническими формами недостаточности кровоснабжения мозга.
Бархатов Д.Ю., Коновалов Р.Н., Федин П.А., Гурьев М.Н., Глотова Н.А., Танашян М.М.
Научный центр неврологии РАМН, г. Москва, Россия
В настоящее время цереброваскулярные заболевания представляют одну из наиболее актуальных проблем современной неврологии, учитывая высокую распространенность этой патологии в популяции.
Одним из наиболее часто встречающихся проявлений хронической ишемии мозга являются нарушения когнитивных функций. При этом в последние десятилетия хроническая недостаточность мозгового кровообращения стала омолаживаться и выявляется уже среди лиц 30–40 летнего возраста [Батышева Т.Т., Бойко А.Н., Скоромец А.А. с соавт., 2007].
Не рассматривая детально этиологию этого заболевания (атеросклероз, гипертоническая болезнь, сахарный диабет, васкулиты, вегето–сосудистая дистония и даже новомодное состояние (предболезнь) – синдром хронической усталости), можно отметить, что существуют две стадии хронических нарушений мозгового кровообращения (ХНМК). Это стадия начальных проявлений и основная стадия – дисциркуляторная энцефалопатия (ДЭ), которые объединены общими признаками, свидетельствующими о расстройстве кровообращения в головном мозге. Начальные стадии проявления ХНМК – головные боли, шум в ушах, головокружения, нарушения сна, метеотропность, утомляемость, ухудшение настроения, переходящее в депрессию, затруднения в выполнении тонких локомоций – практически не изменяют социального статуса пациента. Однако дальнейшее развитие ДЭ проявляется в виде когнитивных расстройств у пациента. Это прежде всего снижение интеллектуальных функций – памяти, внимания, восприятия, воображения, понимания, разумения и планирования, рассуждения, а также мышления, что в целом совершенно конкретно сказывается на трудоспособности пациента и его статусе.
Хроническая ишемия головного мозга, или ДЭ, занимает ведущее место в структуре цереброваскулярных заболеваний по показателям заболеваемости и смертности. Ее распространенность составляет 70–100 человек на 1000 населения [Шахпаронова Н.В., Кадыков А.С., 2008]. Легкие и умеренные когнитивные нарушения относятся к недементным формам когнитивных нарушений в пожилом возрасте. Умеренными когнитивными нарушениями считаются приобретенные нарушения в одной или нескольких когнитивных сферах по сравнению с предшествующим более высоким уровнем в результате органического заболевания головного мозга, выходящие за рамки возрастной нормы, но не приводящие к утрате независимости и самостоятельности в повседневной жизни. Распространенность умеренных когнитивных нарушений в старших возрастных группах велика и достигает 11– 17% среди лиц старше 65 лет [Яхно Н.Н. с соавт., 2005]. В значительном проценте случаев умеренные когнитивные нарушения имеют прогрессирующий характер и со временем трансформируются в деменцию. Так, заболеваемость болезнью Альцгеймера среди пожилых лиц с умеренными когнитивными нарушениями достигает 10–15% в год. Все это свидетельствует о необходимости проведения своевременной и правильно подобранной терапии.
Клинически и инструментально–морфологически у рассматриваемой категории больных выявляются изменения гемодинамики с развитием неврологических, нейропсихологических симптомов, свидетельствующих о нарушениях функционирования нейронов в различных отделах головного мозга. Патоморфологической основой неврологических проявлений при хронических цереброваскулярных заболеваниях (ХЦВЗ) являются диффузные и множественные лакунарные очаговые изменения в семиовальных центрах и подкорковом белом веществе головного мозга, связанные с атеросклеротическим поражением или липогиалинозом мелких пенетрирующих артерий, кровоснабжающих глубинные отделы мозга. Показано, что основную опасность для ткани мозга при его ишемическом поражении представляет образование активных форм кислорода, накапливающихся в промежуточных звеньях дыхательной цепи. Нарушения метаболических процессов приводят к изменению проницаемости мембран и накоплению кальция внутри нейронов. Одновременно запускается реакция свободнорадикального окисления белков, нуклеиновых кислот и липидов. Активация процессов перекисного окисления липидов, истощение эндогенных антиоксидантов и нарушение регуляторных защитных механизмов рассматриваются, как ключевые звенья повреждения нейронов при недостаточности кровоснабжения мозга.
Первичным при ишемических и гипоксических поражениях мозга являются комплексные функционально–метаболические нарушения, где главную роль играет снижение уровня макроэргов – АТФ и креатинфосфата. Изменение функций дыхательной цепи митохондрий приводит к нарушению процесса окислительного фосфорилирования. Параллельно происходит активация гликолиза, который является альтернативным компенсаторным процессом. Наряду с угнетением синтеза АТФ при ишемии нарушаются его транспорт и утилизация.
Проблема совершенствования фармакотерапии у больных с ДЭ актуальна в современной неврологии. Среди препаратов, оказывающих нейрометаболическое, антиоксидантное и антигипоксическое действие, следует выделить препарат пептидной структуры – Кортексин, обладающий универсальным нейрометаболическим действием. Он представляет комплекс низкомолекулярных полипептидных фракций, получаемый из коры головного мозга телят и поросят не старше 12 месяцев. Обоснованность применения Кортексина при ДЭ подтверждается его ноотропным, нейропротекторным и антиоксидантным действием. Кортексин обладает целым рядом потенциально полезных свойств, необходимых при коррекции хронической ишемии мозга. Прежде всего это активация пептидов нейронов и нейротрофических факторов мозга. Кроме того, под действием Кортексина происходит оптимизация баланса метаболизма возбуждающих и тормозных аминокислот, допамина, серотонина; GABA–ергическое воздействие, что в целом проявляется снижением уровня пароксизмальной готовности мозга. Кортексин препятствует также образованию свободных радикалов.
Столь обширный спектр действия препарата, несомненно, оправдан при лечении больных с ДЭ, особенно на ранних стадиях, что в известной степени и определило направление данной работы.
Целью исследования явилась оценка эффективности и безопасности применения препарата Кортексин у пациентов с хроническими формами недостаточности кровоснабжения мозга.
Материалы и методы
В исследование был включен 31 пациент с хроническими цереброваскулярными заболеваниями с легкой либо умеренно выраженной неврологической симптоматикой.
Всем пациентам до и после всего курса лечения проводились неврологическое, нейропсихологическое исследование, функциональная магнитно– резонансная томография, исследование когнитивных вызванных потенциалов.
Ранее отечественными исследователями было многократно показано, что применение Кортексина у больных с хроническими цереброваскулярными заболеваниями приводит к улучшению состояния пациентов и уменьшению выраженности наиболее часто встречающихся объективных и субъективных клинических проявлений данной патологии – астенического синдрома, вегетативных и вестибулярно– мозжечковых нарушений. На этом фоне, естественно, имелось желание оценить терапевтические свойства препарата с помощью современной методики.
Функциональная магнитно–резонансная томография (фМРТ) – современная неинвазивная методика измерения и локализации специфичных функций человеческого мозга без воздействия ионизирующей радиации. Оценка функции мозга осуществляется непрямым путем через определение местных гемодинамических изменений и капиллярах и дренирующих венах так называемых «функциональных зон» мозга в ответ на стимуляцию соответствующих нейрофункциональных систем. Новые мощные градиентные системы и ультрабыстрые МР– последовательности позволяют проводить исследование всего мозга в клинически разумных рамках времени. Большая функциональность обработки данных и немедленный их анализ (так называемая real time fMRI) делают фМРТ все более привлекательной для клиницистов; ведь предоставляются не только множество новейших опций для клинической диагностики и исследований, но также возможен переход от чисто морфологических изображений к визуализации мозговых функций. Использование фМРТ необходимо также и для адекватного подбора и оценки проводимой консервативной терапии и реабилитационных мероприятий. При этом необходимо отметить один из наиболее перспективных аспектов применения фМРТ в исследовании действия фармакологических препаратов, или «фармМРТ» [Танашян М.М. с соавт., 2009]. Зависимость BOLD–сигнала от изменений кровотока ставит перед «фармМРТ» 2 проблемы. Во–первых, назначение фармпрепарата потенциально может изменять взаимоотношение между уровнем регионарного мозгового кровотока и нейрональной активностью, или лекарственные препараты могут напрямую влиять на сосуд, приводя к изменению мозгового кровотока или объема крови в мозге. Во– вторых, при комбинации BOLD фМРТ и фармпрепаратов последний может вызвать общие изменения тонуса сердечно–сосудистой системы, что, в свою очередь, может отразиться на уровне мозгового кровотока и объеме крови в мозге независимо от нейрональной активности, меняя таким образом BOLD–сигнал без изменения активности нервных клеток.
Использование комплексного обследования, одновременно включающего количественное и качественное нейропсихологическое исследование сопряженное с одновременной нейровизуализацией, в т.ч. с проведением фМРТ–исследования, позволяет не только более точно установить характер неврологического дефекта и состояние высших мозговых функций пациентов с хронической цереброваскулярной недостаточностью, но и своевременно назначать адекватную терапию и оценивать ее эффективность.
В процессе данного этапа исследования решались следующие задачи:
Оценка влияния Кортексина на когнитивные функции по результатам:
психометрических тестов (психометрических параметров), включающих общую оценку динамики психической деятельности, исследование слухо–речевой памяти, интеллектуальной деятельности и внимания;
нейрофункциональных методов, вызванные потенциалы (ВП Р300);
фМРТ – на аппарате «Magnetom» Siemens с напряженностью магнитного поля 1,5 Тл по стандартной BOLD–последовательности с использованием 3 когнитивных парадигм по собственной методике: узнавание лица, узнавание лиц по полу, решение арифметических примеров. Больному предлагалось выполнить следующие задания:
идентифицировать по полу (муж/жен) предъявляемые лица – 24 карточки;
узнать из 24 карточек 12, которые ранее были ему предъявленны.
Исследование проводилось до начала введения препарата и по окончании курса лечения (на 14–й день от начала исследования).
Оценка влияния препарата на основные субъективные проявления ДЭ.
Оценка переносимости препарата, с обращением особого внимания на возможные побочные явления, в т.ч. анализ влияния терапии Кортексином на общее состояние больных с ДЭ (артериальное давление, частоту сердечных сокращений) и основные показатели гомеостаза.
Оценка динамики объективных неврологических симптомов ДЭ в результате лечения Кортексином (через 30 дней от начала исследования).
Критерии включения:
Больные (мужчины и женщины) с клинической картиной ДЭ I–II стадии с легкими когнитивными нарушениями по шкале психического статуса (ММSE 24–27) на фоне артериальной гипертонии (уровень АД до 170/100 мм рт. ст.) и/или атеросклероза, подтвержденных с помощью компьютерной рентгеновской (КТ) или магнитно–резонансной (МРТ) томографии головного мозга.
Возраст больных 50–75 лет.
Получение письменного информированного согласия больного на проведение исследования.
В исследовании участвовал 31 пациент (9 женщин и 12 мужчин), от 51 года до 75 лет (средний возраст 64,9±9,6 лет), страдающих ХЦВЗ с легкой либо умеренно выраженной неврологической симптоматикой. Основными сосудистыми заболеваниями, обусловившими развитие неврологических расстройств у обследованных больных, были артериальная гипертония и атеросклероз (в том числе в сочетании друг с другом). Включение пациентов в исследование проводилось вне острого периода ишемического инсульта (не менее 3 месяцев после
перенесенного НМК), при этом критериями исключения являлись грубые двигательные и речевые нарушения, которые могли затруднить проведение нейропсихологического исследования, а также нестабильная соматическая патология. У 8 больных (25,8%) в анамнезе был перенесенный ишемический инсульт; у 28 больных (90,3%) были признаки ДЭ 1–2 ст. Из сосудистых заболеваний: у 12 пациентов (38,7%) была артериальная гипертензия, у 17 (54,8%) – артериальная гипертензия сочеталась с атеросклерозом, у 2 пациентов (6,5%) отмечался распространенный атеросклероз на фоне нормального АД.
В неврологическом статусе у многих больных превалировала негрубая вестибулярно–мозжечковая симптоматика – в 90,3% случаев; также определялась пирамидная симптоматика (в виде оживления и асимметрии сухожильных рефлексов, появления односторонних пирамидных знаков, легкие парезы конечностей) – у 22,6% пациентов, нарушение чувствительности – у 29% пациентов; вегетативные симптомы (тремор рук, гипергидроз ладоней и стоп, вазомоторные реакции, эмоциональная лабильность) – в 74,2% случаев (табл.1).
Можно сделать заключение, что участники данного исследования составляли объективный, типичный «срез», характеризующий данную возрастную группу московской популяции.

При МРТ головного мозга у 28 пациентов (90,3%) отмечались множественные мелкие лакунарные инфаркты в глубоких отделах обоих полушарий головного мозга, легкое или умеренное расширение боковых желудочков и субарахноидальных пространств полушарий большого мозга.
Все пациенты получали Кортексин в суточной дозе 20 мг (внутримышечно по 10 мг – 2 раза в сутки, в течение 14 дней). При необходимости (по медицинским показаниям) больным назначались базововая гипотензивная и кардиальная терапия, антиагрегантные препараты, статины. На протяжении всего курса лечения пациентами не использовались вазоактивные, ноотропные препараты. До и после курса лечения проводились исследования: соматического и неврологического статуса; контроль АД, ЧСС и ЭКГ по стандартной методике; общий анализ крови; изучались также биохимические константы (глюкоза, мочевина, креатинин, общий белок, АЛТ, АСТ, билирубин, холестерин, ЛПВП, ЛПНП, триглицериды).
Эффективность терапии определяли по выраженности основных субъективных проявлений заболевания (головной боли, головокружения, шума в голове, нарушений сна, утомляемости, снижения памяти), а также показателей неврологического статуса (вестибуло–мозжечковых, двигательных, экстрапирамидных, чувствительных и псевдобульбарных расстройств) с помощью балльной рейтинговой шкалы со стандартизированными критериями оценки выраженности каждого симптома (0 – симптом отсутствует, 1 – легкие проявления, 2 – умеренные проявления, 3 – значительные проявления,4 – грубые проявления).
Общая эффективность лечения оценивалась как исследователем, так и пациентами по 5– ступенчатой шкале: 0 – ухудшение, 1 – без динамики, 2 – удовлетворительно (небольшое улучшение), 3 – хорошо (заметное улучшение), 4 – отлично (исчезновение симптомов).
Оценку влияния Кортексина на когнитивные функции проводили путем исследования:
психометрических параметров;
исследования когнитивных вызванных потенциалов;
фМРТ.
Динамика показателей когнитивных функций определялась с использованием следующих нейропсихологических методик:
MMSE – не менее 27 – 24 балла;
заучивание и воспроизведение 10 слов (часть нейропсихологической батареи тестов Лурии);
тест слухо–речевой памяти (Арнольда– Кольмана, по сумме баллов после выполнения 3 заданий);
литеральные и категориальные ассоциации (часть методики деменции Матисса);
таблицы Шульте;
исследование кратковременной памяти (повторение цифр «вперед» и «назад», часть шкалы Векслера).
Также пациентам предлагалось выполнить ряд мнестических заданий, адресованных к зрительной памяти одновременно с проведением фМРТ – с целью выявления очагов максимальной активности определенных зон головного мозга в зависимости от характера предъявляемого материала.
При этом выполнялись следующие задания:
идентифицировать по полу (муж/жен) предъявляемые лица – 24 карточки;
узнать из 24 карточек 12 ранее предъявленных;
определить правильность решения арифметических примеров (действия + и –).
Исследование проводилось до начала введения препарата и в конце курса лечения.
При исследовании фМРТ и для обработки данных использовался следующий протокол (до и после) курса терапии Кортексином:
Техническое оснащение: исследования проводились на аппаратах фирмы SIEMENS с напряженностью магнитного поля 1,5 Тл (Magnetom Avanto и Magnetom Symphony); изображения выводились на прозрачный экран, установленный на столе томографа в ногах пациента, через проектор, смонтированный в пультовой. На головной катушке пациента устанавливалось зеркало, в которое испытуемый видел выводимые изображения. Перед исследованием пациент был подробно проинструктирован о ходе исследования; настраивались размер, высота и резкость выводимого изображения для наибольшего комфорта пациента.
Режимы МРТ:
получены 3D анатомические данные головного мозга в режиме Т1 градиентное эхо;
для каждой парадигмы получены пакеты функциональных данных из 64 аксиальных срезов в режиме Т2 эхопланарное градиентное эхо (TR = 3.75 с, TE = 47).
Парадигма: блоковая парадигма из 4 блоков, каждый блок состоял из двух состояний: периода покоя (8 измерений) и периода активации (8 измерений), всего 64 измерения общей продолжительностью 4,05 мин. Проведено 2 исследования: в первом исследовании пациенту во время периода активации были показаны фотографии людей и предлагалось определить, мужчина или женщина изображены на фотографии; в случае, когда пациент считал, что это мужчина – он приподнимал правую ладонь, если женщина – левую; период активации чередовался с периодом отдыха (черный экран с крестом). Во втором исследовании во время периода активации пациенту показывались как фотографии людей из предыдущего исследования, так и новые лица, и пациенту предлагалось определить, видел он уже данное лицо (приподнимание правой кисти) или это новая фотография (левая кисть); описанные выше периоды активации также чередовались с периодами покоя (черный экран с крестом).
Аналитической обработке подверглись данные пациентов, удовлетворявшие следующим критериям:
Артефакты от движения – минимальные.
Качество изображений – хорошее.
Кооперация со стороны пациента – полная (не затруднена).
4. Обработка данных: пакет статистических программ SPM5.
Результаты исследований
При общей оценке эффекта лечения в целом по группе было выявлено четкое превалирование положительных результатов при использовании Кортексина.
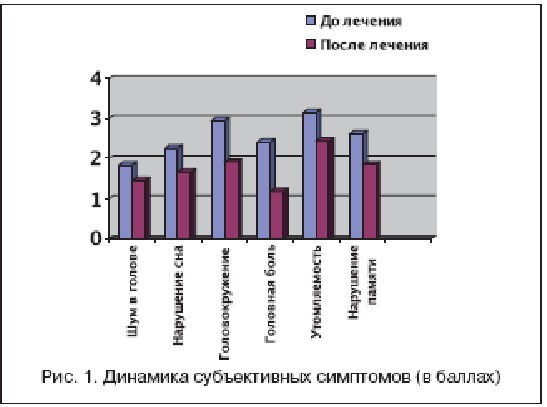
В целом на фоне терапии Кортексином в подавляющем большинстве случаев отмечено улучшение как субъективных симптомов, так и объективных данных. При этом у 90,3% больных отмечалось уменьшение выраженности субъективных симптомов: эмоциональной лабильности, тревоги и депрессивных реакций, утомляемости, головной боли, головокружения (рис. 1).
На фоне лечения Кортексином (рис. 2) происходила положительная динамика в неврологическом статусе, с регрессом преимущественно вестибулярно– мозжечковых и вегетативных симптомов. Ни у одного из пациентов, включенных в исследование, осложнений не отмечено.
Примечательно, что через 30 дней после курса лечения Кортексином (3 визит) неврологическая симптоматика была практически полностью идентична таковой при 2 визите (сразу по окончании курса лечения). Значимых изменений со стороны органической неврологической (пирамидной, экстрапирамидной, чувствительной) симптоматики не получено.
При рассмотрении основных параметров общеклинического состояния (АД, ЧСС, ЭКГ) можно отметить, что несмотря на наличие у большинства пациентов кардиальной патологии (артериальной гипертензии, ИБС), применение Кортексина ни в одном случае не вызвало побочных реакций кардиального характера (аритмии, тахикардии). В общем и биохимическом анализах крови на фоне лечения не было выявлено значимого влияния препарата Кортексин на основные параметры гомеостаза.
Таким образом, на фоне лечения Кортексином в подавляющем большинстве случаев (90,3%) отмечена явная эффективность терапии у пациентов с ДЭ, улучшение как субъективных симптомов, так и объективных данных.
Результаты нейропсихологического обследования
В ходе анализа результатов комплексного нейропсихологического исследования выявлено, что после лечения Кортексином выявлена четкая тенденция к увеличению объема слухоречевой памяти (как непосредственной, так и отсроченной), а также увеличение продуктивности ассоциативно– вербальной деятельности при подборе слов по категориальному признаку. Необходимо отметить, что при обследовании пациентов через 30 дней после окончания курса лечения Кортексином вышеуказанная положительная динамика сохранялась.
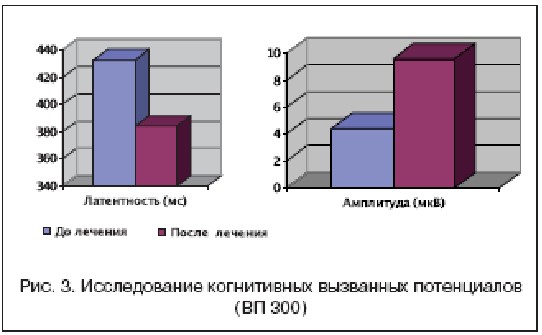
Исследование когнитивных вызванных потенциалов (ВП 300)
Анализировали такие параметры пика Р300, как латентность и его амплитуду (рис. 3).
Из 31 больного у большинства отмечено улучшение параметров Р300 (у 21 пациента – 67,7%), без динамики – у 9 больных (29%) и ухудшение только у 1 больного (3,2%).
Улучшение параметров Р300 заключалось в уменьшении латентности и/или увеличении амплитуды, а также – в появлении пика Р300 у больных, не имевших его до курса лечения препаратом.
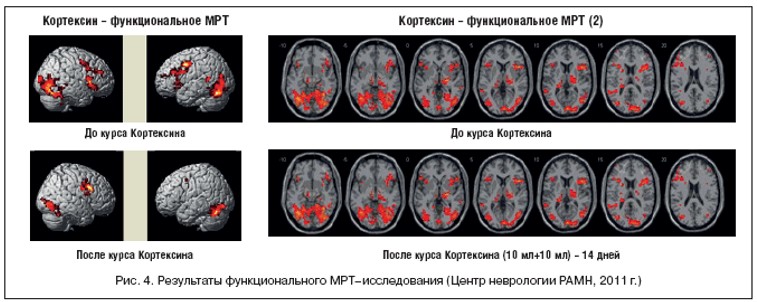
Результаты функционального МРТ– исследования
Как видно из рисунка 4, при проведении фМРТ выявлено достоверное уменьшение зон активации после лечения препаратом Кортексин, особенно в височных и лобных долях, что свидетельствует об уменьшении энергетических затрат мозга на выполнение тех же стандартных психологических нагрузок.
Эти результаты наглядно, впервые на клиническом примере подтверждают ранее проведенные исследования на молекулярном уровне [О.К. Гранстрем с соавт, 2010], где было показано, что Кортексин способен восстанавливать содержание АТФ в молодых и старых нейронах.
Таким образом, применение Кортексина у больных хроническими цереброваскулярными заболеваниями приводит к улучшению состояния пациентов и уменьшению выраженности наиболее часто встречающихся объективных и субъективных клинических проявлений данной патологии – астенического синдрома, вегетативных и вестибулярно– мозжечковых нарушений. Кортексин не влияет на основные параметры сердечной деятельности (АД и ЧСС) и не мешает достижению оптимального гипотензивного эффекта на фоне адекватно подобранной гипотензивной терапии. Отсутствие влияния на кардиальную составляющую сердечно– сосудистых заболеваний позволяет рекомендовать применение Кортексина в качестве церебропротективного средства у пациентов, которым выполнялись ангио– и кардиохирургические операции (аорто–коронарное шунтирование, протезирование клапанов сердца). Исследование показало, что Кортексин обладает широким спектром фармакологического действия, позволяющим применять его при всех формах ишемических цереброваскулярных заболеваний.
Выводы
Кортексин обладает универсальным нейроцитопротективным и ноотропным действием, улучшая тем самым у пациентов когнитивные функции (мнестические функции, функции внимания).
У подавляющего числа пациентов с дисциркуляторной энцефалопатией (в 90,3 % случаев) при лечении Кортексином отмечается уменьшение выраженности субъективных симптомов: эмоциональной лабильности, тревоги и депрессивных реакций, утомляемости, головной боли, головокружения.
- На фоне лечения Кортексином отмечается положительная динамика в неврологическом статусе, с регрессом преимущественно вестибулярно–мозжечковых и вегетативных симптомов. Говоря о динамике объективных неврологических симптомов, следует отметить, что через 30 дней после окончания курса лечения Кортексином неврологическая симптоматика практически полностью идентична таковой сразу по окончании курса лечения.
Кортексин оказывает модулирующее действие на когнитивную деятельность путем уменьшения энергетических затрат мозга для выполнения когнитивных функций. Данный факт энергетически сберегающего действия Кортексина впервые достоверно доказан в клинических условиях.
При лечении Кортексином у пациентов не возникает побочных реакций, препарат не оказывает значимого влияния на основные параметры гомеостаза.
Кортексин может быть рекомендован как нейропротектор не только при цереброваскулярных заболеваниях, но и при целом ряде патологических состояний, сопровождающихся ухудшением когнитивных функций мозга.
Литература
Батышева Т.Т., Бойко А.Н., Скоромец А.А. и др. Нейропротекция в терапии хронической недостаточности мозгового кровообращения. Вестн. Рос. Воен–мед. акад., 2007, №1(17). – С. 11–18.
Бархатов Д.Ю., Танашян М.М. Ишемия в вертебрально–базилярной системе: терапевтические подходы. М., 2010.
Гранстрем О.К. и др. Кортексин: нейропротекция на молекулярном уровне/ Нейроиммунология, 2010 – Т.8,–№1–2.– с.34–40.
Захаров В.В., Яхно Н.Н. Нарушения памяти. М., ГеотарМед, 2003. –
Кадыков А.С., Манвелов Л.С., Шахпаронова Н.В. Хронические сосудистые заболевания головного мозга (дисциркуляторная энцефалопатия). М., ГеотарМед, 2006. –
Танашян М.М., Бархатов Д.Ю., Родионова Ю.В., Коновалов Р.Н. Новые подходы к коррекции когнитивных нарушений у больных с хроническими цереброваскулярными заболеваниями / Неотложные состояния в неврологии // Труды национального конгресса, 2009. – с. 168–171.
Шахпаронова Н.В., Кадыков А.С. Нейрометаболическая терапия больных с заболеваниями нервной системы. Возможности применения актовегина. / Рус. мед. журн., 2008, т. 16, № 26, с 1722–1725.
Яхно Н.Н. Когнитивные нарушения в неврологической практике./ Неврологический журн., 2006, т.11, прил. 1, с. 4–12.
Яхно Н.Н., Захаров В.В., Локшина А.Б. и др. Синдром умеренных когнитивных расстройств при дисцикуляторной энцефалопатии./ Журн. неврологии и психиатрии, 2005, №2, с. 13–17.
Hoyer S., Betz K. Elimination of the delayed postischemic energy deficit in cerebral cortex and hippocampus of aged rats with a dried, deproteinized blood extract (Actovegin). Arch. Gerontol. Geriatr., 9 (1989), 181– 192.
Ihl R., The impact of drugs against dementia on cognition in aging and mild cognitive impairment. Pharma- copsychiatry. 2003, vol.36, suppl.1, 38–43.










Комментировать