Этиология и патогенез диабетической невропатии. Клинические формы и диагностика диабетической невропатии. Лечение и профилактика диабетической невропатии.
Медицинский центр «Хема», Москва
Сахарный диабет (СД) — острейшая медико-социальная проблема современности. В большинстве стран распространенность СД превысила эпидемический уровень 10% и продолжает увеличиваться. При этом более 90% диабетической популяции составляют больные СД 2-го типа. Крайне негативное влияние диабета на здоровье населения и экономику в значительной мере связано с его осложнениями (имеются в виду функциональная дезорганизация и разрушительное влияние на ткани, органы и системы). С диабетом ассоциируются артериальная гипертония (АГ), ишемическая болезнь сердца (ИБС), цереброваскулярная болезнь (ЦВБ), ожирение, ретинопатия, нефропатия, гангрена нижних конечностей и другая патология. Традиционно считается, что в основе осложнений СД лежит повреждение сосудов. Однако есть мнение, что наиболее частым и самым ранним последствием диабета, по крайней мере СД 2-го типа, является поражение нервной системы в виде диабетической энцефаломиелопатии (ДЭМ), диабетической автономной невропатии (ДАН) и диабетической периферической сенсорно-моторной полиневропатии (ДПСМП), которые, будучи самостоятельными клиническими синдромами, одновременно служат предикторами и факторами риска развития другой, ассоциированной с СД 2-го типа, патологии (схема 1).
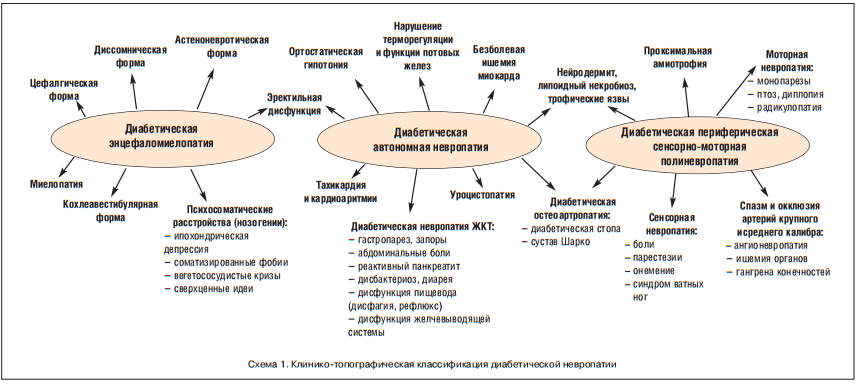
Приведены данные о том, что субклиническая невропатия появляется уже через 1 год после манифестации СД 2-го типа, а у некоторых больных обнаруживается до манифестации [1, 5, 8].
Этиология и патогенез диабетической невропатии
Высказывается мнение, что с точки зрения этиологии и патогенеза такие постоянные спутники СД 2-го типа, как АГ, ИБС, ЦВБ, полиневропатия и ряд других синдромов следует считать не осложнениями диабета, а самостоятельной, но коморбидной патологией, близкой диабету по причинам и механизмам развития. Для такого вывода имеются определенные основания.
Известно, что СД 2-го типа и большинство болезней связаны с наследственной предрасположенностью, — имеется в виду совокупность условно патологических генов, экспрессируемых экзогенными или эндогенными факторами в процессе онтогенеза. Впрочем, такие полигенные болезни и синдромы, особенно СД 2-го типа, нередко возникают без очевидного наследственно-генетического отягощения, а как функциональная энтропия, обусловленная возрастом, неблагоприятными средовыми и социальными условиями, вредными привычками, морбидным фоном и т. д. [3, 5]. Именно возраст считается вторым по значимости фактором риска, точнее, вторым важнейшим этиологическим фактором СД 2-го типа и так называемых коморбидных синдромов. Еще одна этиологическая особенность СД 2-го типа и коморбидных синдромов в том, что они амбивалентны, поскольку могут становиться друг для друга и причиной, и следствием.
В патогенезе СД 2-го типа и коморбидных синдромов первичными патогенетическими факторами являются инсулинорезистентность (ИР) и гиперинсулинемия. Эти патогены не только запускают и поддерживают нарушение углеводного, жиролипоидного, белкового и водно-электролитного обмена, но и оказывают прямое повреждающее действие на ткани, органы и системы [1, 4, 5, 8].
Метаболические нарушения являются вторичными, но не второстепенными факторами патогенеза СД 2-го типа и коморбидных синдромов. Главными метаболическими патогенами служат гипергликемия с усиленным полиольным гликолизом и гликозилированием структур, гиперлипидемия и дислипидемия с оксидативным стрессом, нарушения белкового обмена, особенно гипергомоцистинемия и гиперурикемия (схема 2).
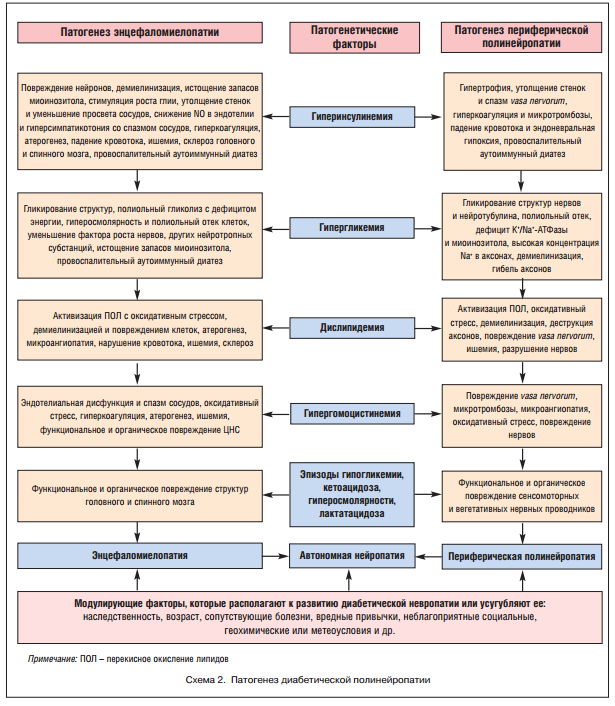
В результате взаимодействия этих и других патогенетических и модулирующих факторов при СД 2-го типа быстро наступает функциональная дезорганизация ЦНС, автономной (АНС) и соматической нервной системы, и одновременно в этих структурах развиваются структурные повреждения: гибель нейронов, глиальных и шванновских клеток, демиелинизация нервных стволов и разрушение аксонов. Основные патогенетические факторы и механизмы развития ДЭМ, ДАН и ДПСМП представлены на схеме 2.
Некоторые из приведенных на схеме 2 патогенетических факторов и механизмов не бесспорны. Однако вполне доказанным и даже ключевым причинным фактором СД и коморбидных синдромов является наследственная предрасположенность, т. е. совокупность условно патологических генов, которые активируются многочисленными эндогенными и экзогенными факторами-триггерами. Эндогенными триггерами экспрессии «диабетических» генов служат эндокринно-метаболические, иммунопатологические, нейропатологические и другие нарушения, не обязательно связанные с СД 2-го типа. Экзогенными пусковыми факторами и модуляторами могут быть такие агенты и условия, как возраст, определенные онтогенетические периоды, неблагополучная экология, геохимические и климатические особенности, курение и прочие вредные привычки, несбалансированная высокоуглеводная и атерогенная диета, гиподинамия, психоэмоциональные перегрузки и стрессы, многое другое.
В заключение анализа этиологии и патогенеза СД 2-го типа и его синдромных ассоциаций можно сделать 3 вывода. Во-первых, СД 2-го типа и сопутствующие синдромы имеют отчетливую мультифакториальную природу. Во-вторых, АГ, ИБС, ЦВБ, невропатия и другая патология — это, как правило, не осложнения СД 2-го типа, а коморбидные синдромы, поскольку имеют с диабетом общий или близкий этиологический и патогенетический базис. В-третьих, между СД 2-го типа и коморбидными синдромами имеются амбивалентные этиологические и патогенетические связи, в результате которых они могут быть и причиной, и следствием друг для друга.
Клинические формы и диагностика диабетической невропатии
Типология клинических форм и проявлений диабетической невропатии (ДН) отражена в многочисленных классификациях, в которых используют традиционный для неврологии синдромно-топографический принцип [1, 2, 5, 8]. В соответствии с ним различают центральную и периферическую невропатию.
Центральную невропатию, т. е. повреждение головного и спинного мозга при СД 2-го типа, обозначают термином «диабетическая энцефаломиелопатия». Следует заметить, что некоторые авторы считают этот термин несостоятельным, а нарушения ЦНС у больных диабетом расценивают как полиморфные психоэмоциональные реакции по типу нозогений [6]. Впрочем, большинство исследователей признают, что при СД 2-го типа имеет место специфическое, присущее именно диабету, функциональное и морфологическое повреждение ЦНС.
Определить ДЭМ можно как прогрессирующее диффузное мелкоочаговое поражение головного и спинного мозга, сопровождаемое нарушением корковых, подкорковых и спинномозговых, надсегментарных и сегментарных, соматических и вегетативных функций и центров и проявляющееся неврозоподобными, психастеническими, мнестическими, вегетоневротическими и соматоневротическими реакциями и дефектами. Клинические формы ДЭМ приведены на схеме 1.
Важно подчеркнуть, что синдром ДЭМ включает повреждение центральных, так называемых надсегментарных образований АНС. В общих чертах патофизиология центральной автономной невропатии характеризуется перевозбуждением симпатических, но торможением парасимпатических отделов ствола мозга, с развитием «центральной гиперсимпатикотонии» [2].
Функциональное, затем и структурное повреждение центральных образований АНС связывают прежде всего с гиперинсулинемией, которая усиливает транспорт глюкозы и ускоряет ее метаболизм в инсулиночувствительных нейронах вентромедиального гипоталамуса [2, 8]. В результате запускаются патогенетические механизмы, отраженные на схеме 1. Кроме того, гиперинсулинемия тормозит обмен норадреналина в периферических структурах симпатоадреналовой системы, поэтому при СД 2-го типа возникает не только центральная, но и периферическая «тканевая гиперсимпатикотония».
Если центральная ДАН — это составная часть ДЭМ, то периферическая ДАН является такой же неотъемлемой частью ДПСМП. Очевидно, что деление ДН на ДЭМ, ДАН и ДПСМП в значительной степени условно. Вместе с тем в патогенезе ряда неврологических и соматических симптомов и синдромов, сопровождающих СД 2-го типа, именно ДАН играет решающую роль, что дает основание рассматривать центральную и периферическую ДАН как отдельные и специфичные разновидности ДН и базовые причины для некоторых нозологических форм (схема 1).
Таким образом, в патогенезе СД 2-го типа и комор-бидных синдромов в числе многих патогенетических факторов и механизмов участвуют дисфункция и деструкция центральных и периферических отделов АНС, т. е. ДАН.
В клиническом, т. е. симптоматическом отношении центральная и периферическая ДАН проявляются лабильной АГ и ортостатической гипотонией, кардиальными нарушениями (аритмия, безболевая ишемия миокарда), расстройством терморегуляции и потоотделения (гипергидроз или сухость кожи), дисфункцией пищеварительного тракта (гастропарез, нарушения перистальтики кишечника, диарея после приема пищи, чередующаяся со спастическими запорами), уроцистопатией в виде атонии мочевого пузыря с затрудненным мочеиспусканием и большим количеством остаточной мочи. ДАН в большой степени определяет эректильную дисфункцию и снижение либидо, трофические расстройства в виде нейродермита и кожных язв, причастна к развитию отеков ног, артропатий и системного остеопороза (схема 1).
Избыточный симпатический тонус проявляется прежде всего АГ. Одновременно гиперсимпатикотония напрямую повреждает сердце, сосуды и почки посредством так называемого патологического ремоделирования. Этот процесс усугубляется чрезмерной активизацией ренин-ангиотензин-альдостероновой системы, которая сопровождается увеличением объема циркулирующей крови, дополнительным спазмом сосудов, тахикардией. В итоге возникают и прогрессируют АГ, ИБС, ЦВБ и другие синдромы, сопровождающие СД 2-го типа.
Несомненно, самым частым и опасным проявлением ДАН является диабетическая сердечно-сосудистая автономная невропатия (ДССАН). Ее ранний симптом — тахикардия покоя. Другим характерным признаком служит так называемый феномен «non-dipper», когда нет урежения частоты сердечных сокращений и понижения кровяного давления в ночные часы. В клинической практике ДССАН реализуется безболевым инфарктом миокарда и пароксизмами вентрикулярной аритмии. Эти синдромы ассоциируются с 5-кратным риском летального исхода [1, 5, 8].
Повреждение соматической нервной системы, т. е. ДПСМП, тоже проявляется множеством ярких симптомов и синдромов. Типичны жалобы на мышечную слабость, онемение и парестезии конечностей, боли в ногах, преимущественно в стопах. Боли постоянные, усиливаются в покое, особенно ночью. Фиксируется асимметричная или симметричная гипорефлексия, вплоть до полного отсутствия сухожильных и кожно-мышечных рефлексов и развития локальных параличей. Характерно нарушение тактильно-вибрационной, болевой и температурной чувствительности по типу носков. Часто имеются признаки атрофии кожи, деформация ногтей, выпадение волос, явления нейродермита, трофические язвы и знаки гангрены. Основные клинические варианты ДПСМП представлены на схеме 1.
Диагностика ДН основана главным образом на субъективной оценке клинических симптомов. При этом, как уже сказано, ДН обусловлена множеством факторов, имеет тесные амбивалентные причинно-следственные связи с другими коморбидными диабетическими синдромами. В этой связи клиническая диагностика ДЭМ, ДАН и ДПСМП крайне трудна и требует экспертного подхода. Эту задачу могут выполнить только квалифицированные специалисты: психоневролог, невропатолог, нейрохирург, вегетоневролог. Очевидно, лишь опытные специалисты могут эффективно использовать традиционные для психологии и неврологии опросники и тесты, правильно оценить результаты специальных диагностических проб (Шелонга, Вальсальвы и др.) и расшифровать данные инструментальных исследований: рефлексометрии, сенсометрии, электронейромиографии.
К сожалению, в силу названных причин данные клинического и инструментального обследования применительно к диагностике ДН неспецифичны, поэтому на их основе даже специалисту трудно сформулировать точный этиологический и синдромный диагноз. Исключением является диагностика ДССАН, для которой есть довольно чувствительные, но неспецифичные методы: кардиоинтервалография (КИГ) и суточное мониторирование артериального давления (СМАД).
С учетом этих обстоятельств диагностику ДН осуществляют методом исключения. Сначала с помощью современных интроскопических, цитологических, иммунологических и других методов диагностики исключают острые нарушения мозгового кровообращения, дегенеративные заболевания, опухоли нервной системы, нейроинфекцию и т. д. Затем на основе данных семейного и личного, в т. ч. морбидного, анамнеза, с учетом длительности СД, его тяжести и клинического течения, делается заключение о наличии ДН, ее клинико-топографической форме (схема 3).

Лечение и профилактика диабетической невропатии
В комплексном лечении ДН при СД 2-го типа нужно исходить из того, что она вызвана не только эндокринно-метаболическими нарушениями. Поэтому профилактику и лечение СД 2-го типа и коморбидных синдромов нужно решать как междисциплинарную проблему, применяя комплексные, но в то же время индивидуальные меры, осуществляемые медицинскими, социальными и другими специалистами и службами (табл. 1).

С учетом того, что роль ИР и гиперинсулинемии в патогенезе СД 2-го типа и ассоциированных синдромов является инициальной и ключевой, эти патогены следует устранять или минимизировать прежде всего. Вместе с диетотерапией средствами выбора являются метформин и глитазоны, которые при необходимости комбинируют с инкретиномиметиками или глиптинами либо сахароснижающими препаратами других групп.
В клинической практике эффективность лечения СД 2-го типа контролируют мониторингом гликемии и эпизодическим исследованием уровня гликированного гемоглобина. Однако данные тесты не отражают динамику гиперинсулинемии и ИР, а эти патогены, как правило, нарастают под влиянием большинства пероральных сахароснижающих средств и, разумеется, при инсулинотерапии, которую при СД 2-го типа назначают неоправданно часто. Очевидно, что лабораторный контроль при лечении ДН нужно расширить за счет определения уровней инсулина, С-пептида, индексов ИР. Впрочем, информативность этих тестов, в особенности индексов ИР, проблематична [6].
Две другие задачи профилактики и лечения ДН — это коррекция гиперлипидемии и устранение оксидативного стресса. Первую задачу решают с помощью гиполипидемических средств. Известно около 10 фармакологических групп липостатиков и десятки конкретных средств и препаратов такого рода. Считается, что для коррекции липидного обмена при СД 2-го типа лучше всего подходят статины или их комбинация с фибратами, но вопрос решается эмпирически.
В качестве антиоксидантов наиболее эффективны соединения α-липоевой (тиоктовой) кислоты. Альфа-липоевая кислота является мощным липофильным антиоксидантом, что определяет возможность ее терапевтического использования; это естественный коэнзим митохондриального комплекса ферментов, который ускоряет окислительное декарбоксилирование α-кетокислот, активирует пируватдегидрогеназу и подавляет пируват, карбоксилазу, а также снижает гликозилирование белков. Вводимая в организм α-липоевая кислота, представляющая собой рацемическую смесь R(+) и S(-) изомеров, восстанавливается в основном из R(+) изоформы до дигидролипоевой, которая и обеспечивает основные терапевтические эффекты, в частности за счет действия в качестве ловушки основного свободного радикала — супероксида. Механизм действия α-липоевой (тиоктовой) кислоты как антиоксиданта основан на способности «улавливать» свободные радикалы, восстанавливать синтез аденозинтрифосфата (АТФ), уменьшая дефицит энергии в тканях. Доказано, что тиоктовая кислота улучшает усвоение глюкозы и восстановление энергетического баланса в нерве.
На фармацевтическом рынке России одним из представителей тиоктовой кислоты является препарат Нейролипон (компания «Фармак»). Препарат обладает антитоксическими и антиоксидантными свойствами. У больных СД Нейролипон снижает ИР и тормозит развитие периферической нейропатии, способствует снижению содержания глюкозы в крови и накоплению гликогена в печени. Препарат вводится в/в медленно в дозе 600 мг смешанной с 0,9% раствором хлорида натрия, 1 р./сут. (600 мг препарата смешивают с 50-250 мл 0,9% раствора натрия хлорида). В тяжелых случаях можно вводить до 1200 мг. Инфузионные растворы следует защищать от света, прикрывая их светозащитными экранами.
Курс лечения — от 2 до 4 нед. После этого переходят на поддерживающую терапию лекарственными формами тиоктовой кислоты для перорального приема в дозе 300-600 мг/сут на протяжении 1-3 мес. Для закрепления эффекта лечения курс терапии препаратом Нейролипон рекомендуется проводить 2 р./год. α-липоевая кислота обеспечивает пролонгированное действие и повышает эффективность препаратов.
Витамины группы В, токоферол и аскорбиновая кислота тоже эффективно устраняют оксидативный стресс и положительно влияют на морфологию и функцию нейронов и нервных проводников, благоприятно действуют на различные дегенеративные и воспалительные процессы, происходящие в нервной ткани и мышцах. Они оказывают дополнительное обезболивающее действие, способствуют улучшению кровообращения и улучшают процесс кроветворения и работу нервной системы.
В то же время возможны ситуации нерационального применения витаминов, в частности группы В. Так, например, витамин В1 не следует вводить парентерально с витаминами РР, С, В12, В6, салицилатами, тетрациклином, симпатомиметиками, гидрокортизоном, т. к. он образует неактивные комплексы с фуросемидом, пенициллинами, стрептомицином, аминогликозидами, АТФ. Однако в сбалансированных поливитаминных комплексах (Витаксон) учитываются рациональные взаимодействия витаминов. При совместном введении витамина В1 и витамина В6 наилучшее их усвоение происходит при избыточном по сравнению с пиридоксином введении тиамина.
Витамин В1 — значимое вещество в метаболизме человека. В процессе метаболизма происходит фосфорилирование с синтезом тиаминдифосфата и тиаминтрифосфата, являющихся биологически активными веществами. Тиаминдифосфат в качестве кофермента участвует в углеводном обмене, а также в метаболизме нервной ткани, влияя на скорость проведения электрического импульса в нервной ткани. При нехватке этого витамина происходит избыточное накопление в тканях продуктов метаболизма, в первую очередь пировиноградной и молочной кислот. Это неизбежно приводит к расстройствам деятельности как центральной, так и периферической нервной системы.
Витамин В6 в форме пиридоксаль-5′-фосфата является ферментом, участвующим в неокислительном метаболизме аминокислот. Этот витамин принимает непосредственное участие в химическом синтезе аминов (таких как серотонин, тирамин, дофамин и гистамин), которые играют важную роль как в анаболических, так и в катаболических реакциях обмена веществ, а также в реакциях синтеза и расщепления аминокислот. Витамин В6 также участвует в 4-х различных реакциях триптофанового метаболизма. Также этот витамин является катализатором при синтезе амино-b-кетоадениновой кислоты.
Витамин В12 жизненно важен для протекания реакций метаболизма в клетках. Он воздействует на процесс кроветворения, участвует в синтезе холина, креатинина, метионина, нуклеиновых кислот, а таже в высоких дозах имеет противоболевой эффект. Поэтому препараты тиоктовой кислоты и витаминотерапию обычно сочетают [1, 5, 6, 8]. Эффективной комбинацией витаминов группы В является препарат Витаксон.
Препарат выпускается в инъекционной форме (раствор для в/м инъекций в ампулах по 2 мл, в упаковках по 5 или 10 штук) и в таблетках (в блистерах 30 или 60 штук). Каждая ампула раствора для инъекций Витаксон содержит 50 мг/мл тиамина гидрохлорида, 50 мг/мл пиридоксина гидрохлорида и 0,5 мг/мл цианкобаламина. Одна таблетка Витаксон содержит 100 мг бенфотиамина и 100 мг гидрохлорида пиридоксина.
Раствор Витаксона вводят, соблюдая стандартные рекомендации для в/м инъекций. При острых болях и в тяжелых клинических случаях рекомендованная доза составляет 2 мл раствора, инъецируемых в/м 1 р./сут. При легких формах патологии или после уменьшения болевого синдрома прием препарата можно сократить до 2 мл, инъецируемых в/м с перерывом в 1 день. Стандартный курс инъекционной терапии составляет 1 мес. Таблетки принимают перорально, запивая достаточно большим количеством воды. Рекомендуется принимать по 1 таблетке до 3 р./сут. В случае лечения острых болей или при необходимости быстрого повышения концентрации Витаксона в крови перорально принимают инъекционную форму препарата в виде раствора. Далее переходят на прием таблетированной формы. Средняя продолжительность курса терапии составляет 1 мес.
Метаболизм гомоцистеина корректируют пиридоксином и фолиевой кислотой, однако нужно иметь в виду, что последняя у пожилых может усиливать парестезии и боль в конечностях.
Перечисленные средства и методы патогенетической терапии дополняют симптоматическим лечением, включающим анестетики, противовоспалительные и противосудорожные средства, антикоагулянты, вазотропные, гипотензивные, кардиотропные и психотропные препараты, средства регуляции и поддержки функций ЖКТ и мочеполовой системы, гели и мази обезболивающего и трофического действия, устройства и приемы ортопедической поддержки. Ориентировочный алгоритм лечения и профилактики ДН приведен в таблице 1. Важно понимать, что из множества препаратов, приведенных в таблице 1, врач должен выбрать наиболее приемлемые с точки зрения нюансов их фармакологического действия и особенностей ДН у конкретного больного.
В заключение отметим, что диагностика, профилактика и лечение ДН стоят в ряду самых актуальных и сложных вопросов, связанных с СД. С сожалением надо признать, что сегодня лечение любой из 3-х основных форм ДН недостаточно эффективно, а ее предупреждение с учетом многофакторного и трудноуточняемого генеза — проблематично. Дополнительная сложность состоит в том, что при лечении СД 2-го типа и коморбидных синдромов врач вынужден назначать много лекарственных средств. Между тем хорошо известны отрицательные последствия полипрагмазии, когда при назначении 5-ти и больше препаратов в 1 день на 50% уменьшается их искомый эффект и резко возрастает частота аллергических реакций [7].
Очевидно, что главным условием эффективной профилактики и лечения СД 2-го типа и коморбидных синдромов является объединение усилий медиков разных специальностей, т. е. междисциплинарный подход, а также активное участие социальных служб, родственников, друзей диабетиков и, конечно, самих больных СД. Второе непременное условие — персонификация. Имеется в виду то, что в программе профилактики и лечения СД 2-го типа и ДН нужно учитывать наследственно-генетические, возрастные, социальные и прочие факторы, а также клинико-топографические и другие особенности течения болезни у конкретного пациента. С соблюдением этих условий профилактика и терапия ДН будут целенаправленными, рациональными и, очевидно, более эффективными.
Литература
- Алгоритмы специализированной медицинской помощи больным сахарным диабетом. 6-е изд. / под ред. И.И. Дедова и др. М.: Медицина, 2013. 215 c.
- Вейн АМ. Вегетативные расстройства: клиника, диагностика, лечение. Мединформ-агенство, 2003. 752 с.
- Возрастные болезни / под ред. М. Дрангой и др. М.: Эксмо, 2007. 734 с.
- Кленова Н.А. Биохимия патологических состояний. Самара: изд-во СГУ, 2006. 213 с.
- Колуэл Г. Сахарный диабет. Новое в профилактике и лечении/пер. с анг. М.: Бином, 2007.288 с.
- Мельниченко Г.А, Удовиченко О.В, Шведова А.Е. Эндокринология. Типичные ошибки практического врача. М.: Медицина, 2014. 188 с.
- Руководство по рациональному использованию лекарственных средств (формуляр) / под ред. А.Г. Чучалина и др. М.: ГЭОТАР-Медиа, 2006. 729 с.
- Ткачева О.Н., Верткин А.Л. Диабетическая автономная нейропатия. М.: ГЭОТАР-Медиа, 2009. 176 с.














Комментировать