Чинники ризику порушень формування мікробіоценозу у новонароджених. Обгрунтування застосування мультипробіотиків. Профілактично-лікувальний ефект пробіотиків.
Проф.Шунько Є.Є., доц. Костюк О.О., доц. Краснова Ю.Ю.
Розвиток медицини пробіотиків, що містять живі клітини фізіологічно корисних мікроорганізмів, – перспектива мікроекологічного здоров’я людей ХХІ-ого століття.
Мікрофлора матері є найбільш спорідненою до організму дитини в антигенному відношенні.
Cучасний стан екології довкілля, несприятливий вплив соціально-економічних чинників на стан здоров’я людини гостро ставлять перед суспільством питання щодо подальшого збереження здоров’я, передусім внутрішньоутробного плода та новонародженої дитини. Стан дитини під час народження визначається багатьма чинниками, серед яких важливе значення мають репродуктивне здоров’я матері та батька, перебіг вагітності, ведення пологів, фізіологічна адаптація новонародженого за умов необмеженого контакту з матір’ю, раннього початку грудного вигодовування, підтримки винятково грудного вигодовування до 6 місяців. Формування біоценозу новонародженої дитини починається під час проходження через пологові шляхи, коли відбувається заселення організму плода та новонародженого фізіологічною мікрофлорою матері. Мікрофлора матері найбільш споріднена до організму дитини в антигенному відношенні, контролюється імунною системою і забезпечує колонізаційну резистентність проти патогенної мікрофлори.
Несприятливий вплив на розвиток внутрішньоутробного плода, стан здоров’я новонародженої дитини та на формування її імунобіологічного захисту мають урогенітальні інфекції у вагітної, безсимптомна бактеріурія, хронічний та гострий пієлонефрит, бактеріальний вагіноз, ендометрит у пологах тощо. За відсутності контакту матері та дитини, грудного вигодовування, перебування дитини у відділенні інтенсивної терапії у новонароджених порушуються фізіологічні процеси бактеріальної колонізації організму немовляти, підвищується ризик колонізації організму дитини госпітальними штамами бактерій, грибів, вірусів із розвитком захворювань, зокрема сепсису, некротичного ентероколіту.
Чинники ризику порушень формування мікробіоценозу у новонароджених
Пренатальні чинники ризику: обтяжений акушерсько-гінекологічний анамнез, ускладнений перебіг вагітності;
Інтранатальні чинники ризику: материнська інфекція в пологах, хоріонамніоніт, ендометрит), інфекції пологових шляхів (носійство стрептокока гр. В, кандидоз, генітальный герпес тощо.), акушерські втручання в пологах: часті дослідження піхви, накладання акушерських щипців, кесарів розтин, медикаментозні пологи
Постнатальні фактори ризику: Вигодовування молочними сумішами, в т.ч. долактаційне годування, перебування дитини окремо від матері, передчасне народження
Інтенсивний неонатальный догляд: інтенсивна терапія, штучна вентиляція легень, парентеральне харчування, катетеризація судин, внутрішньоутробні інфекції, перинатальні інфекції, сепсис
За достатньої кількості нормальної лактота біфідофлори, навіть у разі колонізації дитини умовно-патогенною мікрофлорою, патологічна колонізація не трапляється
ПАТОЛОГІЧНА БАКТЕРІАЛЬНА КОЛОНІЗАЦІЯ
Перенести Графік
термін „патологічна колонізація” включає виділення з біологічного матеріалу в значній кількості (>106 КУО в 1 мл фекалій) факультативних або не властивих для даного біотопу мікроорганізмів на фоні зменшення чисельності представників нормальної мікрофлори
Перенести Графік
• Грудне молоко – основне джерело формування нормальної мікрофлори кишківника новонародженої дитини
Дослідження
Низка досліджень із високим рівнем доказовості («Культивація мікроорганізмів та незалежна оцінка бактеріальної різноманітності грудного молока серед здорових жінок» (Martin R. Res Microbiol. 2007; 158:31-7);
1. «Різноманітність груп Lactobacillus у грудному молоці та піхві здорових жінок, їх потенційна роль у колонізації кишечника новонародженого» (Martin R. J. ApplMicrobiol. 2007; 103:2638-44);
2. «Природні бактерії грудного молока як посередник рецепторів розчинного CD14» (MO Labeta. J. Exp. Med. 2000; 191:1807-12) підтвердили надзвичайно важливе імунобіологічне значення грудного молока в процесі формування нормальної мікрофлори кишківника новонародженого.
Наступна група проведених наукових досліджень спрямована на дослідження ролі деяких пробіотиків, а також застосування одночасно різних груп пробіотиків для запобігання розвитку некротичного ентероколіту (НЕК) у новонароджених, сепсису та інших інфекційних ускладнень у новонароджених з перинатальною патологією:
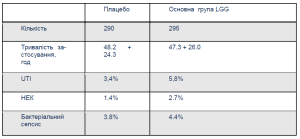
1. «Застосування пероральних пробіотиків для запобігання інфекціям сечовивідного тракту, бактеріального сепсису та некротичного ентероколіту у передчасно народжених немовлят. Проспективне подвійне сліпе дослідження». (Dani C. Biol. Neonate. 2002;82:103-8).Дослідження проводили в Італії у 12 ВІТН у 585 немовлят з ГВ <33—34 тижнів та масою тіла <1500,0 г. Використовували стандартну суміш для новонароджених, збагачену Lactobacillus GG (Dicoflor, Dicofarm, Rome, Italy).
Доза: 6×109 КУО/добу до виписування.
Висновок: порівняно з групою плацебо достовірно знизилася частота розвитку НЕК та сепсису у новонароджених, які отримували Lactobacillus GG.
«Пероральні пробіотики запобігають випадкам та важкості перебігу НЕК у немовлят з дуже малою масою тіла». Lin HC. Pediatrics 2005; 115:1-4.
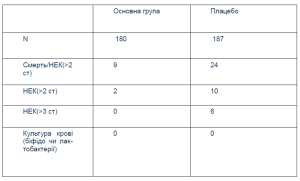
DBPCR у немовлят з ДММТ (<1500,0 г) (ентеральне годування > 7-го дня) грудне молоко +/Infloran (Lactobacillus acidophilus and Bifidobacterium infantis) primary outcome був летальний наслідок або розвиток НЕК (> чи = 2 стадії).
Висновок: НЕК 2 ст. діагностовано значно рідше та НЕК 3 ст. не зустрічався в новонароджених порівняно з групою плацебо.
«Пероральні пробіотики запобігають НЕК у немовлят з ДММТ». Bin-Nun A. J. Pediatr. 2005;147:192-6
Немовлята з масою тіла <1500,0 г отримували грудне молоко +/– суміш пробіотиків (Bifido infantis, Strepto thermo, Bifido bifidus; Solgar, Israel) 109 КУО/д.
Висновок: НЕК розвинувся лише у чверті немовлят, які отримували пробіотики.
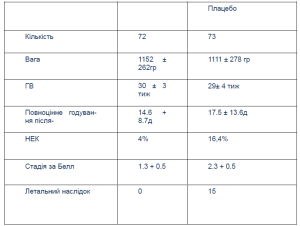
«Ентеральне годування передчасно народжених немовлят із Saccharomyces boulardii (SB)». Costalos C. Early Hum. Dev. 2003; 74:89-96.
Рандомізовані контрольовані дослідження проведено у 87 новонароджених з ГВ 28—32 тижнів. Використовували суміш для недоношених +/– S. boulardii (50 мг/кг кожні 12 годин протягом 30 днів). Визначено здатність Saccharomyces boulardii SB до модифікації оптимальної мікробної екології та функції кишечнику. Виявлено достовірне збільшення колонізації біфідофлорою та достовірне зменшення колонізації патогенними стафілококами, кишковою паличкою, ентерококами, у жодного з новонароджених дітей з НЕК або сепсисом S. boulardii не виділено з крові чи випорожнень.
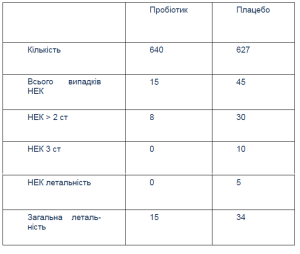
5«Пробіотики та НЕК: систематичний огляд». Barclay AR. J. Pediatr Gastroenterol Nutr.2007; 45:569-76.
5 попередніх досліжень: (Dani / Lin / Bin Nun / Manzoni / Costalos)
Сумарний висновок: значна перевага використання пробіотиків
Профілактично-лікувальний ефект пробіотиків:
• Пробіотик Lactobacillus GG може підвищувати захисні властивості, які регулюють апоптоз та сприяють цитопротекторній відповіді в кишечнику. (Lin PW. Pediatr Res. 2008; 64:511-6).
• LGG регулює гени з цитопротекторними ефектами, які стимулюють антиапоптичні і цитопротекторні відповіді (апоптоз — попередник НЕК).
Обґрунтування застосування мультипробіотиків:
• Безпечність та пробіотична активність.
• Лактобактерії, біфідобактерії, пропіоновокислі бактерії.
• Симбіоз із синергізмом пробіотичної активності штамів.
• Профілактичний і терапевтичний потенціал мультипробіотика.
• Мікроорганізми у високоактивній формі починають діяти відразу після введення в організм.
Обгрунтування застосування мультипробіотиків
• Безпечність та пробіотична активність
• Лактобактерії, біфідобактерії, пропіоновокислі бактерії
• Симбіоз із синергізмом пробіотичної активності штамів
• Профілактичний і терапевтичний потенціал мультипробіотика
• Мікроорганізми у високоактивній формі, починають діяти відразу після введення в організм
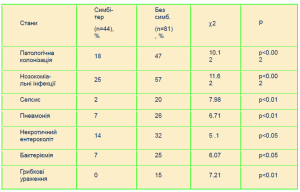
• КІЛЬКІСТЬ ВИДІЛЕНИХ МІКРООРГАНІЗМІВ У НОВОНАРОДЖЕНИХ З КЛІНІКОЮ НОЗОКОМІАЛЬНИХ ІНФЕКЦІЙ В ЛІКАРНІ (повторне обстеження)
КІЛЬКІСТЬ ВИДІЛЕНИХ МІКРООРГАНІЗМІВ У НОВОНАРОДЖЕНИХ З КЛІНІКОЮ НОЗОКОМІАЛЬНИХ ІНФЕКЦІЙ В ЛІКАРНІ (повторне обстеження)
Ефективність профілактичного застосування симбітеру з перших днів життя у новонароджених з перинатальною патологією.
З метою профілактики мультипробіотик «Симбітер» було застосовано у новонароджених з перинатальною патологією, які отримували лікування у відділенні інтенсивної терапії новонароджених. «Симбітер» було обрано з огляду на різноманітний склад мікроорганізмів. Це 14 штамів чотирьох таксономічних груп мікрофлори, які є фізіологічними для людини: біфідобактерії, лактобактерії, пропіоновокислі бактерії.
За результатами проведених досліджень у новонароджених, яким було застосовано «Симбітер», достовірно рідше діагностовано розвиток некротичного ентероколіту, сепсису, пневмонії. У недоношених новонароджених застосування «Симбітеру» сприяло підвищенню ефективності ентерального вигодовування.
Сумарний висновок: значна перевага використання пробіотиків у новонароджених дітей з дуже малою масою тіла, доведений вплив на зниження захворюваності та летальності.
1. Застосування мультипробіотиків «Симбітер» доцільно рекомендувати жінкам на етапі планування сім’ї, виношування вагітності та грудного вигодовування, що дає можливість поліпшити біоценоз організму матері та новонародженої дитини. Застосування мультипробіотика «Симбітер» у новонароджених з перинатальною патологією, новонароджених груп ризику та здорових новонароджених за відсутності грудного вигодовування позитивно впливає на стан здоров’я та розвитку немовлят.
2. Застосування пробіотиків достовірно знижує частоту і важкість НЕК.
3. Подальші дослідження щодо застосування пробіотиків у немовлят із дуже малою масою тіла є актуальними.
4. Існують різні рекомендації щодо початку застосування пробіотиків: (у перші 24 години або додавання в перше годування протягом 1-го тижня ентерального годування) та тривалості курсів пробіотиків (14—28—30 днів — до виписування).
5. Більша кількість штамів у складі пробіотика забезпечує ефективніший профілактичний та терапевтичний результат.
Ентеральне годування сумішшю та материнським молоком в пологовому будинку
Висновки:
профілактична спрямованість застосування пробіотиків у вагітних та новонароджених –забезпечення фізіологічної мікроекології організму
• застосування пробіотиків достовірно (ймовірно) знижує частоту розвитку НЕК та неонатального сепсису
• потребує подальшого дослідження застосування пробіотиків немовлят з ДММТ
• різноманітні рецептури/ дозування
• різні рекомендації щодо початку та тривалоств застосування
Література: Матеріали
«Застосування пероральних пробіотиків в попередженні інфекцій сечовивідного тракту, бактеріального сепсису та некротичного ентероколіту у передчасно народжених немовлят». Проспективне подвійне сліпе дослідження.
(Dani C. Biol Neonate. 2002;82:103-8). Проводилося в Італії у 12 ВІТН у 585 немовлят з ГВ <33-34 тижнів з вагою < 1500,0 г
«Стандартна суміш для новонароджених, збагачена supplemented Lactobacillus GG. (Dicoflor, Dicofarm, Rome, Italy)
(Costalos C. Early Hum Dev 2003;74:89-96).Рандомізовані контрольовані дослідження у 87 новонароджених з ГВ 28 – 32 тижнів
• Здатність Saccharomyces boulardii SB до модифікації оптимальної мікробної екології та функції кишковика
• Суміш для недоношених +/S. boulardii (50 мг/кг кожні 12 годин протягом 30 днів) (680 нмоль поліамінів/кг/д) – достовірне збільшення колонізаціїї біфідофлорою та достовірне зменшення колонізації патогенними стафілококами, кишковою паличкою, ентерококами
• S. boulardii supplemented formula is well tolerated
• IN NONE of the babies with NEC or sepsis was
• S. boulardii isolated from blood or stools








Комментировать