Аменорея: общая характеристика и варианты классификаций. Пороки развития гонад. Лечение дисгенезии гонад. Описание клинического примера.
И.Б. Манухин, М.А. Геворкян, Лечебный факультет МГМСУ, г. Москва, Россия; Л.Г. Тумилович, ОАО «Моситалмед», г. Москва, Россия Газета «Новости медицины и фармации»
Акушерство, гинекология, репродуктология (275) 2009 (тематический номер) / Лекция
Аменорея — отсутствие менструаций у женщин репродуктивного возраста. Нарушение менструального цикла по типу аменореи в популяции среди женщин репродуктивного возраста составляет примерно 3,5 %, а в структуре нарушений менструальной и генеративной функции 10-15 %. Аменорея — не самостоятельное заболевание, а симптом не только патологии различных уровней репродуктивной системы, но и других нейроэндокринных заболеваний, доброкачественных и злокачественных новообразований. Благодаря значительному прогрессу в области гинекологической эндокринологии в настоящее время имеется возможность своевременного выявления уровня поражения при аменорее и проведения патогенетической терапии. Восстановление генеративной функции у больных с аменореей является сложной задачей. Однако совершенствование методов вспомогательной репродукции позволяет решить и эту проблему.
До настоящего времени отсутствует единая общепринятая классификация аменореи, что связано с многообразием этиологических и патогенетических механизмов ее развития. Это создает значительные трудности для практических врачей, так как успех терапии прежде всего основан на выявлении причин аменореи.
Аменорею традиционно делят на первичную — месячных никогда не было и вторичную — отсутствие месячных в течение 3 месяцев регулярного цикла и 6 месяцев нерегулярного цикла. Авторы считают целесообразным выделять первичную аменорею с задержкой полового развития (нарушением развития вторичных половых признаков) и первичную аменорею без задержки полового развития (без нарушения развития вторичных половых признаков).
- Первичная аменорея
В первую очередь необходимо иметь четкие представления о том, когда нужно начинать обследовать девушек при отсутствии менструации, для чего нужно знать критерии первичной аменореи:
- отсутствие менархе в возрасте 16 лет и старше;
- отсутствие признаков полового созревания (молочных желез, полового оволосения) в возрасте 14 лет и старше;
- отсутствие менархе в течение 3 лет и более от начала появления и развития вторичных половых признаков;
- несоответствие показателей роста и массы тела хронологическому возрасту или несоответствие биологического возраста календарному, что можно определить по характеру окостенения костей кисти и запястья. Так, сесамовидная кость у основания первой фаланги большого пальца на рентгенограмме появляется за 2-3 месяца до менархе и, следовательно, соответствует возрасту 12-13 лет [1-3].
- Первичная аменорея с задержкой полового развития (зпр)
А) Пороки развития гонад:
- дисгенезия гонад;
- синдром тестикулярной феминизации.
Б) Нарушения гипоталамо-гипофизарной системы (ГГС):
- конституциональная форма ЗПР;
- функциональные нарушения ГГС;
- органические нарушения ГГС.
Пороки развития гонад
Дисгенезия гонад (ДГ) — наиболее частая причина первичной аменореи на фоне отсутствия вторичных половых признаков. ДГ относится к врожденной патологии, при которой отсутствует функционально активная гормонопродуцирующая ткань яичников. В результате дефицита эстрогенов по принципу обратной связи увеличивается синтез и выделение гонадотропинов, поэтому такую форму аменореи относят к гипергонадотроп- ным. Частота ДГ составляет 1 на 12 тыс. новорожденных.
Патогенез. Как известно, для развития яичников необходимо наличие двух половых Х-хромосом; женский кариотип обозначается как 46-ХХ, а мужской — 46-ХУ
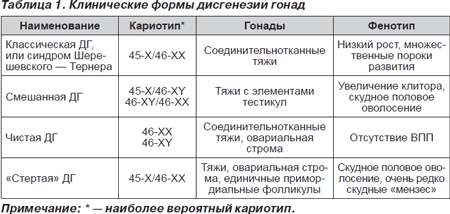
В ходе мейотического деления половых клеток возможно появление аномального набора половых хромосом. При слиянии таких половых клеток в оплодотворенную яйцеклетку попадает патологический набор хромосом. Хромосомные дефекты могут быть количественными: отсутствие одной хромосомы (моно- сомия — 45-Х), удвоение или утроение числа хромосом (47-ХХХ или 47-XXY — полисомия). Возможно образование мозаичных наборов хромосом, когда различные клоны клеток имеют разный набор хромосом. Может быть структурный дефект хромосом, например потеря части хромосомы — делеция, перенос части хромосомы на другую — транслокация и т.д. (табл. 1).
В результате различных аномалий половых хромосом нормального развития гонады не происходит. Кроме того, в Х-хромосоме находятся гены, детерминирующие развитие не только яичников, но и роста тела в длину. Выпадение этих фрагментов Х-хромосомы приводит к низкорослости. Поэтому возможны различные клинические формы дисгенезии гонад.
Типичная форма дисгенезии гонад, или синдром Шерешевского — тернера. Для этой формы характерен кариотип 45-Х. Клиническая картина характеризуется специфическим внешним видом («фенотип Шерешевского — Тернера»), низким ростом — не более 150 см. Диспластичное телосложение: короткая шея с
низкой линией роста волос, кожные складки от сосцевидных отростков до акромиальных, микрогнатия и высокое небо, низко расположенные ушные раковины, вальгусная деформация локтевых и коленных суставов. Кроме того, могут быть аномалия прикуса, косоглазие, щитовидная грудная клетка. У 38 % больных встречаются аномалии почек и мочеточников, у 16 % — пороки развития сердечно-сосудистой системы. Половое оволосение отсутствует, молочные железы не развиты, матка резко гипопластична, т.е. имеется выраженный генитальный инфантилизм. По данным УЗИ размеры гонад в виде соединительнотканных тяжей составляют 1-1,5 см в длину и 0,3-0,5 см в ширину. При гистологическом исследовании — элементы стромы, хилусные клетки, примордиальные фолликулы и ооциты отсутствуют.
Диагностика не представляет трудности в связи с типичным внешним видом пациенток. Диагноз подтверждается данными УЗИ, гормональными исследованиями, для которых характерно резкое повышение уровня гонадотропинов, особенно фолликулостимулирующего гормона (ФСГ), уровень которого соответствует ранней постменопаузе. Генетическое обследование включает определение полового хроматина в буккальных мазках и кариотипа, при котором выявляется соответственно отсутствие полового хроматина и типичный кариотип — 45-Х.
«Стертая форма» дисгенезии гонад. Эта форма характеризуется вариабельностью клинических проявлений.
Кариотип имеет мозаичный характер, чаще 45-Х/46- ХХ. Помимо мозаичного кариотипа, могут быть другие варианты хромосомных аберраций, такие как делеция длинного или короткого плеча Х-хромосомы (Хс-, Хр-), изохромосомы по длинному плечу X (Хс), по короткому плечу X (Хр), сбалансированные транслокации между Х-хромосомой и аутосомой. Клиническая картина зависит от процентного соотношения нормального и аберрантного клона клеток. Чем выше процент клона клеток с кариотипом 45-Х, тем больше больные по внешнему виду и клинической картине похожи на пациенток с синдромом Шерешевского — Тернера. Соответственно при превалировании нормального клона с кариотипом 46-ХХ клиническая картина может характеризоваться нормальным морфотипом, спонтанным развитием вторичных половых признаков и даже спорадическими самостоятельными менструациями. Но всегда имеет место генитальный инфантилизм, повышенный уровень гонадотропинов и на УЗИ признаки дисгенетичных гонад.
Чистая форма дисгенезии гонад. Характерен кариотип 46-ХХ или 46^ (синдром Свайера). Эта форма ДГ наиболее редкая, ее частота — 1 на 100 тыс. новорожденных. Клиническая картина имеет особенности: внешний вид характеризуется нормальным ростом, соматические дисплазии отсутствуют, морфотип может быть евнухоидным или интерсексуальным, с умеренно выраженным гирсутизмом (при синдроме Свайера), вторичные половые признаки не развиты на фоне выраженного генитального инфантилизма. Гонады — в виде соединительнотканных тяжей, а при синдроме Свайера — с элементами тестикул, которые могут приобретать злокачественный характер. Интерес представляют больные с чистой формой дисгенезии гонад при кариотипе 46-ХХ. Причины возникновения этой формы до конца не известны. Описание семейных случаев заболевания свидетельствует о наследственной природе чистой формы дисгенезии гонад.
Диагностика основывается: на данных клинической картины, в которой основным выступает выраженный половой инфантилизм; эхоскопических признаках дисгенетичных гонад; высоких уровнях гонадотропинов; определении кариотипа и отсутствия полового хроматина. Лапароскопия с биопсией гонад подтверждает диагноз.
Смешанная форма дисгенезии гонад. Для этой формы характерен мозаичный кариотип с обязательным присутствием Y-хромосомы или ее участка. Наиболее часто встречается кариотип 45-Х/46-ХУ Клиническая картина характеризуется вариабельностью в зависимости от превалирования того или иного клона клеток. Морфотип, как правило, интерсексуальный, с умеренно выраженным гирсутизмом, могут быть соматические дисплазии и внешнее сходство с синдромом Шерешевского — Тернера. Для наружных половых признаков характерны элементы вирилизации, гипертрофия клитора, редко — с персистенцией урогенитального синуса, что обусловлено наличием Y-хромосомы. Вторичные половые признаки не развиты, матка резко гипопластична. При лапароскопии с биопсией гонад всегда выявляются элементы тестикулярной ткани типа клеток Лейдига и Сертоли, а также недифференцированные половые клетки — гоноциты. В пубертатном возрасте часто развиваются опухоли гонад комбинированного строения с элементами стромы полового тяжа и половых клеток типа гонадобластомы, эмбриональной карциномы. Опухоли такого строения выявляются у 75 % больных в возрасте до 25 лет. При этом в клинической картине прогрессируют признаки вирилизации, что обусловлено гормонально-активной андрогенсе- кретирующей опухолью.
Диагностика основывается на особенностях клинической картины, характеризующейся элементами вирилизации на фоне генитального инфантилизма, УЗИ признаков дисгенетичных яичников, лапароскопии с биопсией гонад. Обязательным является определение кариотипа, при котором выявляется наличие Y-хромосомы.
Таким образом, различные формы дисгенезии гонад обусловлены мозаичным кариотипом и отличаются особенностями клинической картины. Но для всех форм данной патологии имеются общие диагностические критерии:
- первичная аменорея;
- отсутствие или резкое недоразвитие вторичных половых признаков, генитальный инфантилизм;
- УЗИ-признаки дисгенетичных гонад;
- высокий уровень гонадотропинов, особенно ФСГ, соответствующий постменопаузальному возрасту;
- кариотип с аномальным набором половых хромосом, отсутствие или значительное снижение полового хроматина;
- отрицательная проба с гестагенами, но положительная — с эстрогенами и гестагенами;
- гонады представляют собой соединительнотканные тяжи, иногда с элементами яичников (примордиальные фолликулы) или тестикул.
Лечение дисгенезии гонад
Терапия дисгенезии гонад зависит от наличия в ка- риотипе Y-хромосомы. В связи с высоким риском малиг- низации гонад при наличии Y-хромосомы необходимо их оперативное удаление [4, 5]. В настоящее время это производится с минимальным инвазивным вмешательством при лапароскопии. При отсутствии в кариотипе Y-хромосомы или после оперативного удаления гонад при ее наличии проводится заместительная гормональная терапия (ЗГТ), которая направлена:
- на феминизацию фигуры, развитие полового оволосения, молочных желез, матки;
- подавление уровня гонадотропинов;
- циклические изменения в эндометрии с менструальноподобной реакцией;
- профилактику эстроген-дефицитных состояний (остеопороза, метаболических нарушений, сердечнососудистых заболеваний);
- социальную адаптацию.
Заместительная гормональная терапия обычно начинается с применения эстрогенов: этинилэстрадиол (микрофоллин) по 0,05 мг в день или натуральные эстрогены (прогинова, эстрофем) по 2 мг в день в течение 21 дня. Такая терапия проводится 2-3 циклами, в дальнейшем переходят к терапии эстрогенами и гестагенами. Из гестагенов применяют дюфастон по 20 мг (2 таблетки), микронизированный прогестерон 100 мг 2 раза в день, утрожестан 200 мг в день в день с 16-го по 25-й день условного менструального цикла. После 20 лет можно назначать комбинированные оральные контрацептивы (КОК), предпочтительнее трехфазные, имитирующие физиологические колебания гормонов яичников в организме (трирегол, тризистон, триквилар). После 35 лет целесообразнее назначать натуральные эстрогены в сочетании с гестагенами, т.е. препараты, применяемые для заместительной гормональной терапии в постменопаузе (фемостон, климен, климонорм и др.). Гормональная терапия проводится длительное время, практически пожизненно, поэтому каждые полгода желательно делать перерыв на 1-2 месяца с назначением гепатопро- текторов и витаминов.
Прогноз для жизни и здоровья при проведении заместительной гормональной терапии благоприятный. Восстановление генеративной функции весьма сложно, но возможно с использованием методов вспомогательной репродукции путем экстракорпорального оплодотворения донорской яйцеклетки и переноса эмбриона в матку после подготовки эндометрия к имплантации [6].
Клинический пример
Пациентка А. (Москва). В возрасте 18 лет обратилась по поводу первичной аменореи и отсутствия вторичных половых признаков. При осмотре: рост 170 см, вес 58 кг, ИМТ 20, телосложение интерсексуальное, кожа чистая, полового оволосения нет, молочные железы не развиты, наружные половые органы соответствуют 8-летнему возрасту. При УЗИ выявлена резко гипопластичная матка (2,1 х 1,4 х 2,1 см). Яичники не визуализируются. При исследовании кариотипа 46-ХХ, ФСГ — 112 ME, эстрадиол — 20 п/моль. С диагнозом «чистая дисгенезия гонад» начата терапия эстрогенами (эстрофем по 2 мг в день в течение 3 мес., затем к гормонотерапии присоединен дюфастон по 20 мг с 16-го по 25-й день цикла; через 6 мес. начато применение трехфазного контрацептива трисеквенс, который пациентка получала в течение 3 лет). Под влиянием лечения молочные железы развились до 3-й стадии по Таннеру, появилось половое и скудное подмышечное оволосение. Размеры матки увеличились до 4 х 3,5 х 5 см. Женщина вела нормальную половую жизнь, в связи с настойчивым желанием иметь ребенка ей было предложено ЭКО с до- нацией ооцитов, которые были взяты у ее родной сестры и оплодотворены спермой мужа. После соответствующей подготовки эндометрия была произведена подсадка эмбриона. С первой же попытки наступила беременность двойней. До 16 недель проводилась поддерживающая терапия гестагенами и эстрогенами, и в 38 недель путем кесарева сечения извлечены два здоровых разнополых новорожденных весом 2800 и 2400 г. Послеоперационный период протекал гладко. Особо отметим, что с 5-го дня началась обильная лактация и пациентка кормила детей до 1,5 года. Для подавления лактации был назначен парлодел.
Синдром тестикулярной феминизации (СТФ). С известным допущением к дисгенезии гонад можно отнести СТФ, поскольку термин «дисгенез» означает «нарушение развития». Правда, при СТФ нарушается развитие не яичников, а тестикул. Кроме того, эта патология, как и ДГ, имеет генетические причины.
Патогенез
Данная патология характеризуется мужским набором половых хромосом XY при женском фенотипе. СТФ обусловлен генетически запрограммированной нечувствительностью тканей-мишеней к андрогенам — отсутствуют рецепторы андрогенов. Дефектный ген, определяющий нечувствительность рецепторов к андрогенам, расположен в Х-хромосоме. СТФ наследуется по сцепленному с X рецессивному типу [7]. В результате в ходе эмбрионального развития формируются тестикулы, с 8-й недели эмбрионального развития секретирующие тестостерон, к которому ткани не чувствительны, и АМГ (анти- мюллеровский гормон), вызывающий регрессию пара- мезонефральных (мюллеровых) протоков, из которых формируются трубы, матка, шейка матки, верхняя треть влагалища. Наружные половые органы формируются по нейтральному, женскому фенотипу: неполноценное укороченное влагалище, заканчивающееся слепо. Гона- ды-тестикулы расположены у стенок таза или чаще — в паховых каналах и толще больших половых губ. При этой патологии имеется также дефект гена SRY, локализованного в Y-хромосоме, вследствие чего сперматогенез в гонадах отсутствует. Тестостерон образуется в количествах, соответствующих мужскому уровню, а поскольку продукция ароматазы не нарушена, синтез половых гормонов также в норме и тестостерон превращается в эстрадиол в количестве, достаточном для того, чтобы в пубертатном возрасте развились молочные железы. Правда, околосо- сковые поля и соски остаются не пигментированными, половое и подмышечное оволосение отсутствует.
СТФ относится к редким формам ложного мужского гермафродитизма с неполноценными (нет сперматогенеза) тестикулами, отсутствием матки и верхней трети влагалища при мужском наборе хромосом 46-ХУ
Частота этого нарушения развития составляет 1 на 15 тыс. новорожденных.
Клиническая картина
Клиника характеризуется описанными выше нарушениями развития наружных и внутренних половых органов, а также отсутствием полового и подмышечного оволосения. Молочные железы развиты правильно или гипопластичны.
Диагностика
Трудности в диагностике возникают только в том случае, если врач не знает о существовании такой патологии.
Для подтверждения диагноза определяют кариотип (46^), половой хроматин, который отсутствует или резко снижен (менее 6 %).
Определяется локализация гонад (паховые каналы, большие половые губы или полость таза).
Гормональные исследования не информативны: ЛГ, ФСГ, Э2 и Т в пределах нормы.
Лечение
Обязательным этапом лечения является удаление неполноценных тестикул, поскольку более чем в 30 % случаев в них развиваются злокачественные опухоли [5]. Гонадэктомия рекомендуется в возрасте старше 16 лет, после пубертатного скачка роста и развития молочных желез. Как правило, необходимо формирование искусственного влагалища (кольпопоэз) из тазовой брюшины или сигмовидной кишки.
Пациентки с СТФ имеют чисто женскую психосоциальную ориентацию. После удаления гонад обязательно проводится длительная заместительная гормональная терапия для профилактики атрофических изменений в урогенитальной, костной, сердечно-сосудистой системах. Можно использовать КОК или препараты натуральных эстрогенов, применяемые для лечения постменопаузальных нарушений.
Клинический пример
Больная С., 24 года (Москва). Обратилась с жалобами на сухость, жжение в области влагалища, невозможность половой жизни, учащенное мочеиспускание.
Из анамнеза: в возрасте 6 лет в детской больнице оперирована по поводу паховой грыжи справа. В паховом канале обнаружено образование округлой формы, которое при гистологическом исследовании оказалось яичком. При обследовании во втором паховом канале (слева) также обнаружено яичко. Оба яичка были удалены. При генетическом обследовании установлен кариотип 46^ и диагностирован синдром тестикулярной феминизации. В возрасте 6 лет была произведена операция кольпопоэза из сигмовидной кишки. Операция прошла без осложнений. В дальнейшем девочка наблюдалась в той же больнице. В 16 лет была начата циклическая гормонотерапия в связи с отсутствием развития мо- лочныхжелез (микрофоллин по 0,05 мг в день — 15 дней и норколут по 10 мг в день — 10 последующих дней). К 18 годам отмечалось увеличение молочных желез, полового оволосения не наблюдалось. С 20 лет — начало половой жизни, которая сопровождалась болями и жжением во влагалище. В 22 года назначены трехфазные КОК. Улучшения состояния не отмечала. Беспокоило также учащенное болезненное мочеиспускание, по поводу чего она упорно и без эффекта лечилась с диагнозом «хронический цистит» у уролога. В последние месяцы стала раздражительна, мнительна, склонна к депрессии.
Перенесенные заболевания: детские инфекции без осложнений, частые ангины, хронический бронхит.
При объективном исследовании: рост 166 см, вес 54 кг, ИМТ 21. Кожа сухая и чистая. Полового и подмышечного оволосения нет. Молочные железы гипопластич- ны, отделяемого из сосков нет. При гинекологическом исследовании: малые половые губы гипопластичны, влагалище по зонду 6 см, слизистая ярко-розовая, складчатость не выражена, при дотрагивании слегка кровоточит.
Диагноз СТФ был известен самой пациентке и подтвержден данными генетического обследования.
Определение гормонов крови не проводилось, так как пациентка принимала гормональные препараты. Состояние и жалобы были проявлением выраженной ги- поэстрогении. Местно во влагалище назначены свечи с овестином, перорально — эстрофем по 2 мг в день. Через 30 дней отмечено улучшение состояния, явления цистита исчезли, сухость во влагалище значительно уменьшилась, диспареуния не отмечалась. Молочные железы при пальпации чувствительные, заметно увеличились. При гинекологическом исследовании отмечено уменьшение гиперемии слизистой влагалища, кровоточивости нет.
Рекомендовано продолжить прием эстрофема в течение месяца, после чего использовать гестагенсо- держащие препараты (фемостон 1/5). При необходимости — местно свечи с овестином.
Через 3 месяца состояние пациентки удовлетворительное, жалоб не предъявляет, мочеиспускание не нарушено, половая жизнь без боли. Самочувствие и настроение хорошее, имеет желание усыновить ребенка.
Была ли правильной тактика врачей? Понятно, что обнаруженные в паховых каналах тестикулы при женском фенотипе следовало удалить — не только по хирургическим, но и по онкологическим показаниям. Как уже упоминалось, злокачественные опухоли в подобных тестикулах развиваются более чем в 30 % случаев. Однако кольпопоэз следовало бы отсрочить до 16-18 лет и провести его после предварительной гормонотерапии, что значительно облегчило бы проведение этой сложной и травматичной операции. Правда, среди детских хирургов есть мнение, что эти операции следует делать в раннем детском возрасте во избежание психической травмы. Гормонотерапию не следовало прекращать в 18 лет, чтобы избежать симптомов эстро- гендефицита. Назначенная в 20 лет заместительная терапия трехфазными КОК была явно недостаточной и привела к типичным постменопаузальным урогенитальным нарушениям: учащенное мочеиспускание, сухость влагалища, кожи, гипопластические изменения молочных желез.
В дальнейшем пациентке показана заместительная гормональная терапия под контролем УЗИ, рентгенографии молочных желез и состояния слизистой влагалища.
Нарушения функции гипоталамо-гипофизарной системы
Эта группа ЗПР объединяет нарушения гипоталамо- гипофизарной системы функционального и/или органического характера. Все эти формы аменореи характеризуются низким содержанием гонадотропинов (менее 5 МЕ/л) для ЛГ и ФСГ и отсутствием их циклической секреции.
Функциональные нарушения ггс. Данная форма аменореи может быть следствием недостаточного питания, хронических инфекций, интоксикаций, заболеваний почек, печени, анемии и другой патологии.
Около 10 % функциональных причин ЗПР составляет так называемая конституциональная форма ЗПР, часто наследственно обусловленная. Это форма первичной аменореи, при которой пубертатный период как бы сдвинут во времени на более поздние сроки. Развитие молочных желез, полового оволосения и менархе наступает в возрасте старше 16 лет. Такое отсроченное половое созревание характерно для народов, населяющих северные регионы, имеет конституциональный характер, что связано, очевидно, с климатическими, алиментарными факторами и имеет наследственную природу.
Конституциональная форма лечения не требует. Следует исключить и другие причины аменореи. Наиболее информативно определение гонадотропинов (ЛГ и ФСГ) крови, уровень которых соответствует пубертатному возрасту. Диагностическое значение имеет также определение костного возраста по рентгенографической картине костей кистей, запястья и нижней трети предплечья. Костный возраст при этой форме ЗПР на 2-4 года отстает от календарного.
К функциональным нарушениям ГГС относят также особую форму ЗПР, при которой обнаруживают только изолированную гонадотропную недостаточность. Патогенез ее до конца не изучен, возможна генетическая обусловленность данной патологии [8]. Клиническая картина описана достаточно подробно и характеризуется евнухоидным телосложением, недоразвитием наружных и внутренних половых органов. При гормональном исследовании обнаруживают низкий уровень гонадотропинов — менее 5 МЕ. При УЗИ — яичники уменьшены в размерах, с мелкими фолликулами. При гистологическом исследовании — фолликулы на стадии примордиальных и преантральных.
органические нарушения ггс. К органическим причинам относятся опухоли гипоталамо-гипофизар- ной области. Например, краниофарингиома — опухоль, развивающаяся из ткани ножки гипофиза. Опухоль доброкачественная, часто подвергается кальцинозу, что облегчает ее диагностику на рентгенограмме черепа; располагается супраселлярно. Клиническая картина, помимо первичной аменореи и ЗПР, характеризуется неврологической симптоматикой, зависящей от локализации опухоли, которая приводит пациенток к невропатологам, а не к гинекологам.
К редким формам органической патологии ГГС относится синдром Каллмана — первичная аменорея в сочетании с аносмией, т.е. неспособностью воспринимать запахи. Эта патология обусловлена врожденным дефектом строения гипофизотропной зоны гипоталамуса, в структурах которой секретируется гонадотро- пин-рилизинг-гормон (ГнРГ) [9]. Следовательно, гонадотропная недостаточность гипофиза имеет вторичный характер. На аутопсии при исследовании мозга обнаруживают полную или частичную агенезию обонятельной луковицы. Синдром аносмии — аменореи был описан Каллманом в 1944 году и назван ольфакто-генитальной дисплазией. Исследования эмбриогенеза мозга показали, что нейроны гонадотропных рилизингов развиваются в обонятельной доле и оттуда мигрируют в передние отделы гипоталамуса в ходе роста и развития подкорковых структур мозга. Поэтому становится понятным странное на первый взгляд сочетание аменореи и аносмии. Следует отметить, что аносмия встречается, как правило, у мужчин, у женщин — чрезвычайно редко.
Патология эта генетически обусловлена. Дефектный ген локализуется в Х-хромосоме и наследуется аутосом- но рецессивно.
Клиническая картина
Характеризуется инфантилизмом наружных и внутренних половых органов, отсутствием вторичных половых признаков и, как было отмечено, аносмией. Последнее облегчает диагностику.
лечение — заместительная гормональная терапия. Хотя диагностика таких форм первичной аменореи и ЗПР не представляет трудности, выявление причин нарушения функции ГГС достаточно сложно. Все описанные формы клинически однотипны и характеризуются ев- нухоидным телосложением, резким недоразвитием наружных и внутренних половых органов, отсутствием или резким недоразвитием вторичных половых признаков. При гормональных исследованиях определяют низкие уровни гонадотропинов. Поэтому все эти формы первичной аменореи и ЗПР называют гипогонадотропными — в отличие от описанных выше пороков развития гонад, для которых характерен гипергонадотропизм. Содержание эстрогенов в крови резко снижено. При УЗИ размеры яичников уменьшены за счет отсутствия полостных фолликулов, в строме содержатся в основном примордиальные и преантральные фолликулы. В выяснении причин аменореи помогает наличие таких особых симптомов, как неврологические нарушения и аносмия.
Гормональные пробы позволяют уточнить степень заинтересованности гипофиза. Так, например, увеличение уровня гонадотропинов после введения препаратов-агонистов ГнРГ свидетельствует о его резервных возможностях. Проба с аГнРГ: однократно вводится трипторелин в дозе 100 мкг внутривенно, через 30-45 мин определяют уровень ФСГ и ЛГ в крови. Повышение уровня гонадотропинов не менее чем в 3 раза указывает на способность гипофиза секретировать гонадотропины и на гипоталамический уровень нарушения. Проба отрицательная, если повышения уровня гонадотропинов не отмечается, что свидетельствует о гипофизарном уровне нарушения. Повышение содержания эстрадио- ла после введения гонадотропных препаратов — свидетельство потенциальной активности яичников.
Лечение функциональных нарушений ГГС — заместительная гормональная терапия препаратами половых стероидов. Восстановление репродуктивной функции возможно только с применением вспомогательных репродуктивных технологий (ЭКО). ЗГТ необходима для развития вторичных половых признаков и менструальных выделений, которые положительно влияют на психику женщины, подтверждая ее полноценность. Кроме того, ЗГТ ликвидирует проявления дефицита эстрогенов в сердечно-сосудистой и костной системе.
Первичная аменорея без задержки развития вторичных половых признаков
Пороки развития половых органов:
А) гинатрезии;
Б) аплазия матки.
Атрезия гимена или части влагалища
Патогенез
Данный порок развития возникает в результате нарушения канализации нижнего отдела урогенитального синуса в период внутриутробного развития. Причины изучены недостаточно.
Клиническая картина
При атрезии гимена или части влагалища пациентки жалуются на циклические боли внизу живота, что связано с нарушением оттока менструальной крови и формированием гематокольпоса, скоплением крови в матке и трубах. При несвоевременной коррекции данного порока имеется риск развития наружного эндометриоза в результате ретроградной менструации. Других жалоб пациентки не предъявляют.
Диагностика
Диагностика сложности не представляет. Данный порок развития легко устанавливается при гинекологическом исследовании и эхографии малого таза.
Лечение
Хирургическое лечение сводится к рассечению гимена или поперечной перегородки, что нормализует менструальную и, в дальнейшем, генеративную функцию. Более сложными являются операции при восстановлении частично атрезированного влагалища.
Аплазия матки (синдром майера — рокитанского — кюстнера)
Аплазия матки часто сочетается с аплазией влагалища. Точно установлено, что в яичниках происходит нормальный фолликулогенез, овуляция и образование желтых тел. Это было доказано хирургами во время ла- паротомии этим пациенткам, которую производили при операции кольпопоэза.
Клиническая картина
Женщину ничего не беспокоит, кроме отсутствия менструации. Важно помнить, что у 40 % пациенток имеются пороки мочевыделительной системы: аплазия почки, подковообразная почка, удвоение мочеточников.
Диагностика
При гинекологическом исследовании диагноз сложности не представляет в случае аплазии влагалища и матки. При аплазии только матки имеется нижняя треть слепо заканчивающегося влагалища, что подтверждается при гинекологическом исследовании.
УЗИ окончательно подтверждает диагноз, при этом определяются нормальных размеров яичники и отсутствие матки.
Гормональные исследования дают мало информации, уровни гонадотропинов и половых стероидов в пределах возрастных нормативов и циклически изменяются.
Лапароскопия проводится не только с целью подтверждения диагноза, но и на этапах проведения хирургического лечения — кольпопоэза из тазовой брюшины или сигмовидной кишки. После пластической операции возможна половая жизнь. Генеративная функция может быть выполнена с помощью вспомогательных репродуктивных технологий с использованием суррогатной матки.
Практическим врачам необходимо помнить, что отсутствие матки при первичной аменорее бывает только в двух случаях: при синдроме Майера — Ро- китанского — Кюстнера (кариотип женский 46-ХХ) и синдроме тестикулярной феминизации (кариотип мужской 46-XY). Основным дифференциально-диагностическим критерием является определение ка- риотипа, который в последнем случае носит мужской характер (46-XY).
Заканчивая раздел, посвященный первичной аменорее без ЗПР, еще раз подчеркнем, что она является результатом пороков развития, формирующихся на ранних этапах эмбриогенеза. Диагностика причин аменореи основана на знании основ эмбриогенеза. Терапия имеет паллиативный характер — не устраняя причины аменореи, пациентку адаптируют к условиям жизни в соответствии с ее женским фенотипом.
- Вторичная аменорея
2.1. Внутриматочная патология:
- травматические повреждения;
- синехии эндометрия.
2.2. Функциональные нарушения гипоталамо-гипофизарной системы:
- аменорея на фоне потери массы тела;
- психогенная аменорея (стресс-аменорея);
- синдром гиперторможения яичников.
2.3. Органические нарушения гипоталамо-гипофизарной системы:
- послеродовой гипопитуитаризм (синдром Шихана);
- синдром «пустого» турецкого седла.
2.4. Яичниковые формы:
- синдром резистентных яичников;
- синдром истощения яичников.
При вторичной аменорее нарушения развития вторичных половых признаков не наблюдается, поскольку пубертатный период протекает в соответствующих возрастных пределах (12-16 лет).
В отличие от первичной вторичная аменорея встречается часто, составляет до 80 % в структуре аменореи и является едва ли не постоянным симптомом гормональных нарушений функции яичников, надпочечников, щитовидной железы, гиперпролактинемии. На долю вторичной аменореи при патологии названных эндокринных желез приходится более 50 %.
Ниже разбираются вторичные аменореи, являющиеся симптомами травматических заболеваний матки, нарушений гипоталамо-гипофизарной системы.
2.1.Внутриматочная патология
Травматические повреждения шейки и тела матки
Атрезия цервикального канала
Отсутствие менструаций является следствием травматичных внутриматочных манипуляций, выскабливания, при которых повреждается базальная мембрана эндоцервикса.
Клиническая картина
Клиническими признаками этой патологии являются прекращение менструаций после аборта, диагностического выскабливания, удаления полипов цервикального канала и других манипуляций.
Важным клиническим симптомом являются циклические боли вследствие нарушения оттока менструальной крови.
Диагностика
Диагноз устанавливается на основании анамнеза, клинической картины и данных УЗИ, произведенного при болях: расширенная полость матки и скопление в ней жидкости.
Лечение
Восстановление проходимости цервикального канала при зондировании, которое можно проводить амбулаторно.
Внутриматочные синехии (синдром Ашермана)
Внутриматочные синехии (синдром Ашермана) — следствие частых грубых выскабливаний или эндометритов. Заподозрить эту патологию можно при изучении анамнеза.
Клиническая картина
В отличие от атрезии цервикального канала циклических болей при внутриматочных синехиях пациентки не отмечают. Частой ошибкой практических врачей является поиск эндокринных нарушений при аменорее после аборта.
Диагностика
Уровень половых и гонадотропных гормонов в пределах нормы, поэтому эту форму аменореи называют нормогонадотропной.
По данным трансвагинальной эхографии можно заподозрить внутриматочные синехии.
Важное диагностическое значение имеет отрицательная проба с эстрогенами и гестагенами. При гистероскопии и гистеросальпингографии выявляется типичная картина внутриматочныхсинехий.
Лечение
Лечение хирургическое и заключается в рассечении спаек при гистерорезектоскопии.
При подозрении на инфекционный генез синдрома Ашермана (по данным анамнеза) производится выскабливание с последующим бактериологическим и микробиологическим исследованием. После хирургического рассечения внутриматочных синехий проводится антибактериальная терапия и в течение 3 месяцев — циклическая гормональная терапия: эстрогены с 5-го по 15-й день цикла, гестагены с 16-го по 26-й день цикла. КОК применять не следует, так как они препятствуют пролиферации эндометрия. L. Speroff и др. рекомендуют после разделения спаек вводить в полость матки детский катетер Фолея, заполнять его на 3 мл жидкостью и оставлять на 7 дней, в течение которых пациентке назначают эстрогенсодержащие препараты [10].
2.2. Функциональные нарушения гипоталамо-гипофизарной системы
Аменорея на фоне потери массы тела (косметическая аменорея)
В структуре вторичной аменореи среди подростков эта патология составляет до 25 %. Очень часто эмоционально неустойчивые девушки 14-18 лет соблюдают косметическую низкокалорийную диету для достижения «идеальной фигуры». Помимо диеты, для усиления эффекта многие пациентки используют медикаментозные средства (диуретки, аноректики), очистительные клизмы, прибегая даже к искусственно вызываемой рвоте, а также физические нагрузки. Оценить границу между небольшой потерей массы тела, которая не отражается на состоянии здоровья, и началом заболевания практически невозможно, так как патологические изменения на фоне голодания развиваются постепенно, а хорошее самочувствие сохраняется длительное время. Кроме того, реакция организма на похудание индивидуальна, и даже небольшая потеря массы тела (на 3-10 %) может привести к началу заболевания.
Патогенез
Патогенетические механизмы развития вторичной аменореи на фоне потери массы тела связаны с нарушением нейромедиаторного обмена ЦНС с уменьшением выделения люлиберина. Определенную роль играет уменьшение количества жировой ткани. Установлено, что первая менструация наступает при определенном количестве жировой ткани — 17 % от веса тела, а для нормального становления менструальной функции этот процент еще выше — 22 %. Быстрая потеря 10-15 % жировой ткани не только в период пубертата, но и в пост- пубертатном периоде приводит к резкому прекращению менструации.
В патогенезе этой формы аменореи определенную роль играет лептин-белковый гормон, образующийся в адипоцитах. В регуляции его секреции важную роль играет инсулин, уровень которого повышается после насыщения. Уровень лептина четко коррелирует с количеством жировой ткани. Лептин синергично с ИПФР-1 подавляет секрецию эстрадиола в гранулезных клетках фолликулов [11, 12].
Вторичная аменорея — один из самых заметных признаков начала заболевания при соблюдении косметической диеты, что заставляет девушек обращаться именно к гинекологу. Хотя это только признак общего заболевания, связанного с голоданием. Пациентки тщательно скрывают факт соблюдения косметической диеты и голодание, поэтому часто назначается неправильное лечение, в основном направленное на нормализацию менструального цикла (эстроген-гестагенные препараты, усугубляющие торможение гонадотропной секреции).
Для этих пациенток характерна отличная учеба в школе, сильный волевой характер, лидерство в любом коллективе. Толчками к соблюдению косметической диеты часто служат стресс, нейроинфекции, нетактичное замечание окружающих относительно дефекта фигуры или незначительной полноты. При потере массы тела на 5-18 % резко прекращаются менструации без периода олигоменореи. На фоне продолжающейся потери массы тела нарастают симптомы голодания — брадикардия, гипотония, гипогликемия, гипотермия, гастрит, запоры.
Конфликты в семье, когда родители заставляют молодых девушек нормально питаться, вызывают раздражительность, плаксивость, бессонницу, агрессивные или депрессивные состояния. В дальнейшем развивается кахексия с полной потерей аппетита и отвращением к еде. Эта симптоматика очень сходна с психическим заболеванием — нервной анорексией. Некоторые психиатры полагают, что аменорея на фоне потери массы тела является начальной стадией шизофрении, требующей лечения под наблюдением психоневролога.
При осмотре обращает на себя внимание резкое уменьшение подкожно-жировой ткани, снижение массы тела. Телосложение женского типа. Вторичные половые признаки развиты нормально. При гинекологическом исследовании гипоплазия матки, сухость слизистых вульвы и влагалища.
Диагностика
Диагноз аменореи на фоне потери массы тела может быть поставлен в поликлинических условия на основании следующих критериев:
- соблюдение косметической диеты (выясняется при активном опросе);
- хронологическое совпадение потери массы тела и наступления аменореи.
Гормональные исследования характеризуются снижением ЛГ, ФСГ, эстрадиола. При последовательном проведении гормональных проб выявляются резервные возможности различных уровней репродуктивной системы. Гестагеновая проба может быть положительной или отрицательной, что связано с длительностью аменореи и состоянием эндометрия. Проба с эстрогенами и гестагенами всегда положительная. Кломифеновая проба также может быть положительной или, при длительном голодании, отрицательной. Проба с люлибери- ном свидетельствует о сохраненной функции гипофиза, а проба с гонадотропинами способствует нормальному росту и созреванию фолликулов, т.е. адекватной реакции яичников на стимуляцию.
Лечение
Лечение во многом определяется психоэмоциональным состоянием пациентки. Необходимо убедить девушку в том, что основная причина заболевания — потеря массы тела. Следует помнить, что упорный отказ от пищи может быть первым симптомом юношеской шизофрении. При этом показана консультация психиатра. Из психотропных средств можно рекомендовать настой валерианы, пустырника и другие. При необходимости можно госпитализировать пациентку в стационар, что избавляет ее от конфликтной ситуации в семье, школе. Диета должна быть высококалорийной, с 5-6-разовым питанием, легкоусвояемой, с добавлением соленых и острых продуктов, повышающих аппетит. Обязательно назначение витаминов группы В или поливитаминов, циклической витаминотерапии.
Восстановление менструального цикла возможно только после нормализации массы тела и прекращения приема психотропных препаратов. Следует помнить, что эти препараты подавляют гонадотропную функцию гипофиза.
В результате лечения через 6-8 месяцев нормализуется масса тела, улучшается общее состояние и показатели гормонов крови, у 80 % больных восстанавливается менструальный цикл. При отсутствии эффекта требуется дообследование в специализированном стационаре; можно рекомендовать микродозы циклической терапии натуральными эстрогенами и гестагенами (дивитрен, дивина, фемостон, циклопрогинова и др.) в течение 3-6 месяцев, что оказывает стимулирующий эффект на гипоталамические структуры. После нормализации массы тела можно проводить стимуляцию овуляции кломифеном по общепринятой методике.
Прогноз благоприятный для восстановления менструальной и генеративной функции при своевременной диагностике и лечении.
Профилактика — нормализация режима труда и отдыха, полноценное питание, особенно в период полового развития. Родители и учителя должны быть информированы об основах физиологического развития подростков.
Клинический пример
Больная К., 17лет (Москва). Пришла в сопровождении матери, посещению врача сопротивлялась. Жалоб не предъявляет, контактна, но агрессивна и груба.
Со слов матери, аменорея у девочки в течение 3 лет, отсутствие менструаций девушку не волнует.
Из анамнеза: при опросе установлено, что менструации с 12,5 года. Последовательность развития вторичных половых признаков не нарушалась. До 14 лет менструации регулярные, умеренно болезненные, необильные. С 14,5 года стала ограничивать прием пищи, так как считала свой вес избыточным, кроме того, многие ее сверстницы стремились похудеть. К 15 годам потеряла в весе 12 кг, менструации прекратились. Самочувствие оставалось удовлетворительным, ела очень мало, указывая на отвращение к пище. Мясо и жиры из рациона исключила, ела только вареные овощи в небольшом количестве. Если после длительных уговоров и ссор вместе с семьей съедала обед или ужин — вызывала рвоту. Периодически принимала слабительные, ссылаясь на запоры. По совету гинеколога с целью восстановления менструального цикла без предварительного обследования начала принимать КОК (ригевидон) в циклическом режиме. В течение 3 месяцев приема КОК были скудные менструальноподобные выделения. Затем в 16,5 года категорически отказалась от приема препарата, поскольку «от него толстеют». Училась хорошо, на утомляемость и слабость не жаловалась. Помимо учебы в школе, занималась изучением английского языка и игрой на фортепиано. В школьных мероприятиях участвовала неохотно, друзей не имела, с родителями груба. Соблюдение диеты объясняет желанием «поддерживать форму». Половой жизнью не живет.
При объективном исследовании: рост 167 см, вес 43 кг, ИМТ 15. Кожа бледная, с сероватым оттенком, шелушащаяся на локтях и ладонях. Молочные железы дряблые. При гинекологическом исследовании наружные половые органы гипотрофичны, слизистая вульвы бледная, сухая.
При УЗИ (трансабдоминальным датчиком) матка 30 х 20 х 21 мм — эндометрий линейный. Объем яичников: правого — 4, левого — 3,3 см3. Фолликулярный аппарат не выражен.
Гормональные исследования: ЛГ 1,2, ФСГ 1,8 МЕ/л, ПРЛ 120 мМЕ/л, ТТГ 0,3 мМЕ/л, эстрадиол 80 пмоль/л, кортизол 520 нмоль/л.
В данном случае на фоне потери массы тела было отмечено снижение уровня тропных гормонов гипофиза, имелись указания на гипофункцию яичников и щитовидной железы центрального генеза, выраженные клинические проявления дефицита эстрогенов.
Поведение больной заставило нас обратиться к психиатру. С диагнозом «нервная анорексия» больная госпитализирована в психоневрологическую клинику. Проводилась инфузионная терапия, витаминотерапия, лечение психотропными препаратами. После выписки из стационара прием психотропных препаратов продолжала под контролем психиатра, с постепенным уменьшением дозы по мере улучшения общего состояния.
В данном случае было психическое заболевание, которое в конце концов оказалось расценено как одна из форм шизофрении. Ошибкой в тактике врача было позднее обращение за консультацией к психиатру и, соответственно, позднее начало патогенетической терапии. Вряд ли было целесообразно назначать КОК, так как они могут вызывать нарушения настроения и усугублять депрессию, что следовало учитывать у данной пациентки. Далее — восстановление менструального цикла в подобных случаях представляет значительные трудности, так как психотропные препараты усугубляют нарушения гипоталамо-гипофи- зарной системы и вызывают торможение гормональной функции яичников.
Восстановить менструальный цикл в таких случаях можно только после стойкой ремиссии психического заболевании; при этом происходит самостоятельное восстановление менструального цикла.
Молодые девушки и подростки с аменореей на фоне потери массы тела, как правило, обращаются (сами или их родители) к гинекологу. И поэтому нам нельзя забывать о возможности психического заболевания под маской «косметической диеты», о чем и свидетельствует описанный клинический случай.
Психогенная аменорея (стресс-аменорея)
Вторичная аменорея в репродуктивном возрасте может быть следствием психоэмоциональных нарушений. В качестве примера всегда приводят аменорею военного времени.
Клиника характеризуется внезапным прекращением менструации без предварительного периода олигоменореи. Отсутствуют также вегетососудистые симптомы, характерные для климакса.
Патогенез
Существует две гипотезы возможных механизмов развития психогенной аменореи:
- повышенная активность опиоидергической системы и увеличение синтеза эндорфинов;
- повышение синтеза КТРГ и активизация коры надпочечников.
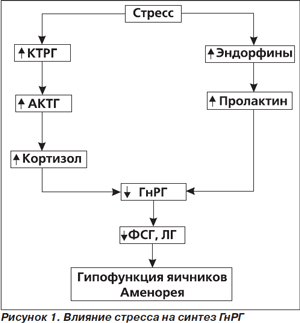
Вследствие этих процессов тормозится синтез ГнРГ, опосредованно — синтез гонадотропинов и половых стероидов яичников (рис. 1).
Диагноз устанавливают на основании анамнеза и клинической картины. При гормональных исследованиях отмечается снижение уровней гонадотропинов и половых стероидов до базальных значений.
Следует отметить, что при длительном течении такой аменореи в возрасте старше 40 лет она может перейти в раннюю менопаузу.
Лечение
Гормональная терапия не требуется. При нормализации ситуации — ликвидации стресса — восстанавливается нормальная функция гипоталамо-гипофизарной системы.
Клинический пример
Женщина 38 лет обратилась с жалобами на отсутствие месячных в течение 5 лет. Месячные прекратились после автомобильной катастрофы, при которой погибли трое ее родственников, ехавших с ней в машине, а пациентка по счастливой случайности не пострадала. После аварии у нее сразу прекратились месячные. До катастрофы месячные были регулярными, а в анамнезе было 2 родов и 2 неосложненных аборта. Кроме того, у женщины совершенно пропал аппетит. При осмотре отмечена выраженная кахексия, вес 42 кг при росте 168 см, ИМТ 15. Кожа сероватого цвета, сухая, шелушащаяся на локтях и коленях. Молочные железы дряблые, железистая ткань при пальпации не определяется. При гинекологическом исследовании отмечается гипоплазия наружных половых органов, сглаженность слизистой влагалища бледно-розового цвета, шейка матки гипо- пластична, матка пальпаторно уменьшена в размерах, но угол между телом и шейкой выражен. При УЗИ яичники размерами: ПЯ — 2 х 2,5 х 1,4 см; ЛЯ — 2,2 х 1,9 х 1,1 см. Визуализируются антральные фолликулы диаметром 2-5 мм, размеры матки: 2,6 х 2,0 х 4,0 см. Отмечено, что особых жалоб на слабость и плохое самочувствие женщина не предъявляла, продолжала работать по специальности (бухгалтер в крупном банке). Периодически обращалась к врачам. При обследовании отмечено снижение уровней ФСГ З-5 МЕ, ЛГ 2-5 МЕ при нормальных (нижние границы нормы) уровнях ТТГ, АКТЕ, пролакти- на. Периодически, по рекомендации врача, принимала гормональные двухфазные малодозированные КОК, менструальноподобной реакции не отмечалось. В данном случае имелось сочетании эмоционально-психического стресса и анорексии.
Больная была направлена к психологу. Несомненно, первым этапом терапии в данном случае должно быть психотерапевтическое воздействие в сочетании с медикаментозным, а также нормализация питания. Терапия половыми яичниковыми гормонами должна быть рекомендована только после нормализации массы тела.
Синдром гиперторможения яичников (ятрогенная аменорея)
Эта форма аменореи имеет ятрогенное происхождение. Она вызвана приемом лекарственных препаратов, а именно длительным приемом КОК, аГнРГ, пролонгированных гестагенов, т.е. препаратов, механизм действия которых состоит в торможении секреции гонадотропинов. Этот синдром чаще наблюдается у женщин, у которых в анамнезе позднее менархе, периодические задержки цикла, длительное ановуляторное бесплодие, т.е. признаки гипофункции яичников.
Клиническая картина
Характеризуется вторичной аменореей, четко наступившей после отмены названных выше препаратов. При этом клинических проявлений гипоэстрогении — вегетососудистых симптомов, гипотрофии молочных желез, наружных и внутренних половых органов — не отмечают. Правда, нельзя забывать, что пациентки — это женщины в возрасте до 35 лет (как правило), и обращаются они к врачу не позднее чем через 2-3 месяца после отсутствия очередных менструаций.
Диагноз устанавливают на основании анамнеза. При определении гонадотропинов — содержание ФСГ и ЛГ в пределах базального уровня. Нередко отмечается повышение уровня пролактина, как правило, не выше 1000 мМЕ. Поэтому необходима КГ или МРТ черепа с определением величины и структуры гипофиза (про- лактинома). При УЗИ — размеры матки не изменены, толщина эндометрия не более 6 мм, размеры яичников соответствуют нормативам. Фолликулярный аппарат визуализируется в виде антральных фолликулов до 8-10 мм в диаметре.
Лечение
Как правило, в течение 3 месяцев менструальный цикл восстанавливается без лечения (в тех случаях, когда уровень пролактина в норме). При отсутствии месячных в течение указанного срока рекомендуется стимуляция кломифеном в обычной дозе, используемой для стимуляции овуляции, т.е. по 50 мг с 3-го по 7-й или с 5-го по 9-й дни формируемого цикла. Контроль за действием препарата с помощью УЗИ — определение динамики роста фолликула и толщины эндометрия, начиная с 7-10-го дня после приема кломифена. Как правило, достаточно 3 циклов стимуляции, причем при положительной динамике во 2-й и 3-й циклы можно уменьшить дозу кломифена до 25 мг. При повышении уровня пролактина назначают парлодел или его аналоги в дозе не более 2,5 мг/сут. Нормализация функции яичников (менструация) наступает через 3-4 нед. лечения. Если аменорея наступила после приема КОК, после восстановления цикла в течение года следует применять негормональные методы контрацепции.
Клиническиий пример
Больная Е., 26 лет. Обратилась с жалобами на отсутствие менструации в течение 7,5 месяца. Других жалоб нет.
Из анамнеза: менструации с 13,5 года, цикл неустойчивый, с тенденцией к олигоменорее, длительность менструального цикла 34-45 дней.
Половая жизнь с 18 лет вне брака, в беременности не заинтересована. До 22 лет половая жизнь без контрацепции, беременность не наступала.
В возрасте 15 лет соблюдала косметическую диету, в течение 6 месяцев масса тела снизилась на 8 кг. С 15,5 года наступила аменорея. По совету врача провела курс витаминотерапии, рационально питалась, прибавила в весе 6 кг. Через 3 месяца менструации возобновились: по 3-4 дня через 32-45 дней.
Гинекологические заболевания: кольпит (хламидиоз, гарднереллез).
Перенесенные заболевания: болезнь Боткина в детстве, частые ОРВИ, аппендэктомия в 14 лет без осложнений. Наследственность не отягощена.
По совету врача в 22 года начала принимать марве- лон с целью контрацепции, в последние 6 месяцев приема препарата отмечала оскудение менструации. Принимала марвелон в течение 3 лет, после отмены КОК развилась вторичная аменорея.
При объективном исследовании: рост 164 см, вес 52 кг, ИМТ 20. Телосложение, оволосение женского типа.
Молочные железы развиты правильно, отделяемого из сосков нет.
При гинекологическом исследовании патологии не выявлено. Компьютерная томография черепа без патологии.
Гормональные исследования на фоне аменореи: Л Г 4,4; ФСГ 6,2 МЕ/л; ПРЛ 502 мМЕ/л; ТТГ 1,5 мМЕ/л; эстрадиол 96 пмоль/л; тестостерон 1,8 нмоль/л.
УЗИ органов малого таза: матка 44 х 29 х 34 мм, объем яичников: правого — 4,2 см3, левого — 3,8 см3, эхо- структура по типу МФЯ.
Проба с гестагенами положительная. После менструальной реакции на гестагены проведена стимуляция овуляции кломифеном в дозе 50 мг с 5-го по 9-й день цикла. На 16-й день по УЗИ выявлен доминантный фолликул в левом яичнике диаметром 16 мм, эндометрий 8 мм. Через 16 дней была скудная менструальная реакция в течение 2-3 дней. Базальная температура гипертер- мическая с 20-го по 26-й день цикла. Проведено еще два цикла стимуляции овуляции кломифеном в дозе 75 мг. По данным базальной температуры третий цикл был овуляторный, с длительностью второй фазы 10 дней, с хорошей менструальной реакцией. Эндометрий по УЗИ на 24-й день цикла был 10 мм.
2.3. Органические нарушения гипоталамо-гипо- физарной системы
Органические нарушения гипоталамо-гипофизар- ной системы как причина вторичной аменореи встречаются достаточно редко. Как правило, речь идет об опухолевых процессах, и неврологические симптомы, которые им сопутствуют, заставляют пациентов обращаться к невропатологам. J. Schillings и Н. McClamrock [13] перечисляют как причину органических нарушений гипоталамуса следующие образования: краниофарин- гиома, герминома, туберкулезная и саркоидная гранулема и дермоидная киста. Опухоли гипофиза — также достаточно редкая причина вторичной аменореи. Исключение составляют пролактиномы, секретирующие пролактин; опухоли, секретирующие соматотропный гормон и вызывающие акромегалию; опухоли, секрети- рующие АКТГ, вызывающие болезнь Иценко — Кушинга; опухоли, вызывающие гипертиреоидизм. Пациенты гинеколога-эндокринолога — это женщины, у которых нарушена гонадотропная функция гипофиза, что изолированно встречается крайне редко. В то же время встречаются так называемые не функционирующие, «молчащие» опухоли гипофиза, при которых нарушений секреции тропных гормонов не находят, клинических проявлений их дефицита не обнаруживают.
Среди органической патологии гипофиза как причины аменореи следует назвать следующие.
Послеродовый гипопитуитаризм (синдром Шихана)
Синдром Шихана развивается вследствие некротических изменений в гипофизе на фоне спазма или кровоизлияния в передней доле гипофиза на фоне массивного послеродового кровотечения. Этому может способствовать особенность кровоснабжения гипофиза, масса которого во время беременности увеличивается в два раза в жестком ложе турецкого седла. Предрасполагают к внутрисосудистому свертыванию крови гестозы в тяжелой форме. Синдром Шихана — патология достаточно редкая, составляет 0,1 % среди вторичных аменорей, тем более что совершенствование акушерской помощи значительно сократило частоту обильных кровотечений в родах.
Клиническая картина
Анализ литературы и собственный опыт А.С. Калиниченко и др. [14] позволили выделить три формы синдрома по степени тяжести. Легкая форма — характеризуется слабостью, утомляемостью, тенденцией к гипотензии, выраженных гормональных нарушений не отмечают. Форма средней тяжести характеризуется олигоменореей и ановуляторным бесплодием (гипогонадотропизм), пастозностью, сухостью кожи, утомляемостью, гипотензией, симптомами гипотиреоза. При тяжелой форме имеет место клиника выраженного гипотиреоза: миксе- дема, сонливость, отеки, облысение, снижение памяти, снижение уровня АКТГ (гипотензия, адинамия, слабость, пигментация кожи). Отмечается также анемия. Первым симптомом после родов является агалактия — полное отсутствие образования молока: резко снижен пролактин. Следует отметить, что легкие формы и формы средней тяжести, как правило, не диагностируются; все симптомы связываются с «усталостью после родов».
Диагноз устанавливают на основании анамнеза (ге- стоз, кровотечение в родах, агалактия), а также на основании снижения уровня гонадотропных, пролактина, АКТГ и снижения уровня ТТГ в крови. Как правило, имеет место аменорея, снижение уровня периферических гормонов — эстрадиола, кортизола, тироксина, трийод- тиронина.
Лечение
В зависимости от тяжести симптомов и уровня периферических гормонов назначают глюкокортикоиды, ти- реоидные гормоны, при аменорее — ЗГТ половыми гормонами (предпочтительны применяемые при лечении климактерического синдрома — климен, климонорм, фемостон 2/10). Следует отметить, что тяжесть симптоматики не всегда соответствует степени поражения передней доли гипофиза.
Синдром «пустого» турецкого седла
Частота этой патологии, по данным аутопсии, составляет до 5 %; в основном у женщин (85 %).
«Пустое» турецкое седло образуется как следствие недостаточности диафрагмы седла, образующейся из твердой мозговой оболочки. В диафрагме имеется отверстие, в которое проходит ножка гипофиза, и в норме спинномозговая жидкость в полость седла не попадает. При недостаточности диафрагмы жидкость, окруженная паутинной оболочкой, через дефект в дифрагме попадает в ложе гипофиза и сдавливает его (рис. 2).
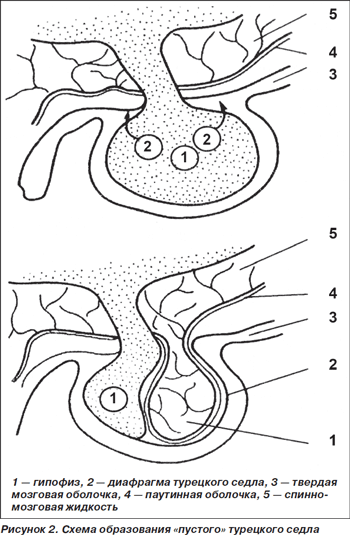
Причиной образования «пустого» седла называют частые беременности, патологические роды, арахноидиты и арахноидальные кисты, некроз гранулем гипофиза, некроз и кровоизлияния в аденомы гипофиза.
Клиническая картина
Зависит от поражения тех или иных тропных функций передней доли гипофиза. Чаще всего наблюдают ги- погонадотропные нарушения, а именно аменорею — до 70 %. Нарушения адренокортикотропной и тиреотроп- ной функции отмечают значительно реже — до 6 %; отмечают также несахарный диабет — до 11 % случаев.
Описаны случаи, когда «пустое» седло было обнаружено на аутопсии; в жизни никаких клинических проявления эта патология может не вызывать.
Лечение
Зависит от клинических проявлений. При аменорее проводится ЗГТ до возраста перименопаузы. Существуют формы аменореи у женщин репродуктивного возраста, причины которых еще недостаточно изучены. Предложенные объяснения патогенеза имеют характер гипотез.
В зарубежной литературе существует термин «преждевременная яичниковая недостаточность», который употребляется для обозначения вторичной аменореи у женщин до 36 лет, с повышенным уровнем гонадотропинов и гипоэстрогенией. В 1990 г. В.П. Сметник [15] предложила выделить из этой группы две клинические формы преждевременной яичниковой недостаточности: синдром резистентных яичников (СРЯ) и синдром истощения яичников. Как показали дальнейшие исследования, эти формы имеют существенное клиническое, морфологическое и отчасти гормональное различие.
Синдром резистентных яичников
Синдром резистентных яичников возникает у женщин в возрасте до 36 лет, характеризуется вторичной аменореей, макро- и микроскопически неизмененными яичниками и повышенным уровнем гонадотропинов. Частота СРЯ составляет примерно 5 % среди всех форм аменореи.
Патогенез
Причины возникновения СРЯ недостаточно изучены. Возможно, его развитие связано с дефектами рецепторного аппарата фолликулов. Возможно, резистентность к гонадотропинам объясняется нарушенной структурой ФСГ или патологией рецепторов гонадотропинов в яичниках [16, 17]. Однако большинство исследователей считают причиной аутоиммунные процессы. Так, обнаружены антиовариальные антитела в крови этих женщин, а также частое сочетание с аутоиммунными заболеваниями [18]. Кроме того, возможное спонтанное восстановление менструаций и овуляции и даже наступление беременностей позволяет рассматривать эту патологию как аутоиммунную преходящую атаку [19].
Клиническая картина
Характерно развитие аменореи в возрасте до 36 лет. В анамнезе больных с СРЯ отмечается наследственная отягощенность по нарушениям менструальной и генеративной функции, большая частота инфекционных и аутоиммунных заболеваний. Начало заболевания пациентки связывают с тяжелыми вирусными инфекциями, стрессовыми ситуациями. Помимо отсутствия менструации, других жалоб у больных нет. Важным информативным признаком является отсутствие приливов и других вегетососудистых нарушений, характерных для физиологической постменопаузы.
Возраст менархе своевременный, менструации постепенно приобретают характер олигоменореи, и до 36 лет развивается аменорея, беременности бывают редко.
Телосложение женского типа, масса ИМТ 20-25, вторичные половые признаки развиты правильно. При гинекологическом исследовании обращает на себя внимание то, что выраженных признаков гипоэстроге- нии — истончения слизистых вульвы и влагалища — не наблюдается.
Диагностика
Решающую роль в диагностике играют гормональные исследования, при которых определяются высокие уровни ЛГ и ФСГ и низкие — эстрадиола, уровень ПРЛ в пределах нормы. При УЗИ определяются нормальных размеров яичники с множеством фолликулов диаметром до 5-6 мм, матка нормальных размеров, эндометрий тонкий. Гестагеновая проба чаще отрицательная, проба с эстрогенами и гестагенами всегда положительная. При гипергонадотропных формах аменореи проведение кломифеновой пробы нецелесообразно, поскольку она направлена на повышение синтеза и выделения гонадотропинов, которые и так повышены. Реакция гонадотропной функции гипофиза на введение люлиберина и эстрогенов имеет адекватный характер: снижение уровня ФСГ на введение эстрогенов и повышение уровня ФСГ и ЛГ на введение люлиберина. Эта проба указывает на сохранность механизмов обратных связей и исключает наличие гонадотропин- секретирующей аденомы гипофиза. Тем не менее КТ и рентгенография черепа и турецкого седла необходимы. Лапароскопия с биопсией гонад и гистологическим исследованием подтверждает диагноз СРЯ.
Критерии диагностики СРЯ следующие:
- аменорея вторичная;
- при УЗИ — яичники нормальных размеров с фолликулярным аппаратом;
- высокие уровни ЛГ и ФСГ (перименопаузальные);
- положительная проба с эстрогенами и гестагенами.
Лечение
Терапия СРЯ представляет большие трудности в плане восстановления генеративной функции. Попытки терапии гонадотропинами и люлиберином не увенчались успехом. Рекомендуется заместительная гормональная терапия эстрогенами и гестагенами, комбинированными оральными контрацептивами или натуральными эстрогенами. Терапия направлена на профилактику эстроген-дефицитных состояний и нормализацию менструального цикла, а также на подавление уровня гонадотропинов. Восстановление генеративной функции возможно с помощью вспомогательных репродуктивных технологий путем эстракорпорального оплодотворения донорской яйцеклетки.
Однако, как было отмечено выше, иногда наблюдается спонтанное восстановление овуляторной и менструальной функции.
Синдром истощения яичников (СИЯ)
СИЯ характеризуется вторичной аменореей с ве- гетососудистыми нарушениями у женщин в возрасте в среднем до 38 лет, имевших в прошлом нормальную менструальную и генеративную функцию. Частота СИЯ в популяции составляет до 2 %, а в структуре вторичной аменореи до 5-6 %. Нельзя отождествлять СИЯ с ранним климаксом, который является возрастным физиологическим процессом. Климакс, как известно, проходит с постепенным угасанием функции репродуктивной системы. Прекращение менструаций не свидетельствует о прекращении гормональной функции яичников, которая продолжается в постменопаузе достаточно длительное время. Поэтому для обозначения этой патологии В.П. Сметник был предложен термин «истощение яичников».
Патогенез
Имеется множество теорий, объясняющих преждевременное истощение фолликулярного аппарата яичников. Одной из причин являются хромосомные аномалии, в частности наличие трех Х-хромосом. Показана семейная концентрация генов, ответственных за проявление данной патологии. Установлено, что различные неблагоприятные факторы как в антенатальном, так и в постнатальном периоде (радиация, химические вещества, тератогенные лекарственные препараты, вирус гриппа, краснухи, паротита) могут привести к повреждению гонад и замещению их соединительной тканью. Возможно, имеет место ускоренный, по сравнению с физиологическим, апоптоз ооцитов в яичниках. Вероятно, на фоне неполноценного генома любые экзогенные воздействия (инфекционные заболевания, интоксикации, стрессы) могут способствовать развитию синдрома истощения яичников [20].
Клиническая картина
В отличие от СРЯ при СИЯ отмечаются типичные для постменопаузы вегетососудистые проявления — приливы, потливость, слабость, головные боли с нарушением трудоспособности.
Возраст менархе своевременный, менструальная и генеративная функции не нарушены длительное время. Заболевание начинается с аменореи, редко ей предшествует период олигоменореи. Для таких женщин ожирение не характерно. На фоне аменореи развиваются прогрессирующие атрофические процессы в молочных железах и половых органах.
Диагностика
Диагностика основывается на данных анамнеза и клинической картины. Решающая роль принадлежит гормональным исследованиям, при которых определяются значительно повышенные уровни гонадотропинов, особенно ФСГ, и резкое снижение уровня эстрадиола.
При трансвагинальной эхографии яичники уменьшены в размерах, фолликулы отсутствуют, матка меньше нормы, эндометрий линейный.
В.П. Сметник предлагает различать раннюю менопаузу и СИЯ по следующим признакам. При СИЯ гестагеновая проба отрицательная, тогда как при раннем климаксе — положительная. Кломифеновая проба при СИЯ всегда отрицательная, а при раннем климаксе может быть положительной. В основе развития физиологического климакса и СИЯ лежат разные механизмы. В пременопаузальном (климактерическом) периоде изменяется чувствительность гипоталамо-гипофизарной системы к половым стероидам, что проявляется повышением уровня гонадотропинов. В яичниках отмечается резистентность оставшихся фолликулов к собственным гонадотропинам, но они еще функционируют в течение 5 и более лет постменопаузы. При СИЯ фолликулярный аппарат яичников атрезирован, поэтому стимуляция овуляции не эффективна. Эти данные важны для практических врачей, поскольку пациентки с СИЯ часто обращаются именно по поводу вторичного бесплодия.
Диагностическими критериями СИЯ являются:
- вторичная аменорея у женщин репродуктивного возраста, имевших в прошлом нормальную менструальную и генеративную функцию;
- приливы и другие вегетососудистые нарушения;
- значительное повышение уровня ФСГ и снижение эстрадиола;
- уменьшение размеров яичников и матки с отсутствием фолликулов по данным трансвагинальной эхографии.
Лечение
Лечение направлено на профилактику и терапию эстрогендефицитных состояний: вегетососудистых нарушений, урогенитальных расстройств, остеопороза и сердечно-сосудистых заболеваний. С этой целью проводится заместительная гормональная терапия препаратами натуральных эстрогенов (фемостон, дивина, климен, анжелик и другие) до возраста естественной менопаузы и далее. На фоне лечения быстро проходят приливы, улучшается общее самочувствие, работоспособность. Восстановление генеративной функции возможно путем экстракорпорального оплодотворения с донорской яйцеклеткой.
СИЯ может развиться после субтотальной их резекции при различных хирургических вмешательствах, особенно по поводу апоплексии яичника. Иногда при операциях по поводу трубной беременности, консервативной миомэктомии и других проводится неоправданная резекция яичников в связи с их так называемой «кистозной дегенерацией» — термин, который должен быть прочно забыт гинекологами! Снижается фолликулярный резерв яичников, быстро развивается апоптоз и атрезия фолликулов и впоследствии развивается их истощение. Об этом следует помнить практическим врачам и производить резекцию яичников строго по показаниям с максимальным сохранением здоровой ткани.
Клинический пример
Больная П., 36 лет. Обратилась с жалобами на аменорею в течение 1,5 года. Периодически отмечает тошноту, сердцебиение, потливость, слабость. К врачу обращается впервые.
Из анамнеза: менархе в 16 лет (родилась и жила на Севере). Менструации установились в 18,5 года, через 30 дней по 3-5 дней. Половая жизнь с 25 лет. Беременность наступила через три года замужества без контрацепции. Беременность протекала с угрозой прерывания во втором триместре. Роды без осложнений в срок. Вес ребенка 3100 г, длина 50 см. Лактация 6 месяцев. Менструации после родов начались через 8 месяцев. В 33 года отмечает оскудение менструаций и задержки до 45 дней. В 34 года наступила аменорея.
Гинекологические заболевания отрицает.
Перенесенные заболевания: аппендэктомия в детстве, перелом нижней трети голени в 32 года и перелом предплечья в 34 года, частые ОРВИ.
Наследственность не отягощена: у младшей сестры и у матери нарушений менструальной и генеративной функции не было.
Объективное обследование: рост 158 см, вес 50 кг, ИМТ 20. Молочные железы мягкие, отделяемого из сосков нет. Телосложение и оволосение женского типа. При гинекологическом исследование сухие и гиперемиро- ванные вульва и влагалище, симптом натяжения цервикальной слизи 0-1 см, матка гипопластична, яичники не определяются.
Дополнительное обследование
УЗИ: матка 45 х 30 х 36 мм, яичники: правый 24 х 14 х 20 мм, левый 18 х 12 х 17 мм, фолликулы не визуализируются.
Гормональные исследования: ФСГ 42 МЕ/л, ЛГ29 МЕ/л, эстрадиол 80 пмоль/л, пролактин 130 мМЕ/л.
Проба с гестагенами отрицательная, проба с эстрогенами и гестагенами положительная.
При исследовании МПКТ(поясничные позвонки и шейка бедра) полученные результаты Т—2,8 и Т — 2,6, что соответствует остеопорозу. На основании данных клиники и обследования установлен диагноз: синдром истощения яичников.
Несмотря на отсутствие приливов, у пациентки были клинические проявления вегетососудистых нарушений, и, кроме того, анамнестические данные свидетельствовали о хрупкости костей (переломы голени и предплечья). В анамнезе имеются указания на гипофункцию яичников: позднее менархе, единственная беременность, наступившая после 3 лет половой жизни без контрацепции.
Назначена ЗГТ трисеквенсом. Терапия рассчитана на длительный период применения с целью профилактики постменопаузальной патологии, которая, по данным анамнеза и обследования, ожидается в ближайшем будущем. К терапии следует добавить препараты кальция, витамин 03 с целью лечения остеопороза.
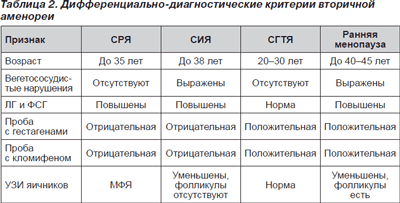
Клинические и гормональные характеристики СРЯ, СИЯ, СГТЯ приведены в табл. 2.
- Рохлин Д.Г. и др. Рентгенология. — М., 1954 —С.104.Frisch R. // Reprod. Endocrinol. — 1985. — Vol. 3. — P. 45-49.
- Богданова A. Гинекология детей и подростков. — М., 2000. — С. 166-180.
- Schillings W., McClamrook H. et al. // Novak’s Gynecology. — 2002. — 13th ed. — S. 5, Ch. 24. — P. 821.
- Conte F., Grumbach M. // — Philadelphia: W.B. Saunders; 1989. — 1810-47.
- Шаваева A. Состояние репродуктивной системы при дисгенезии гонад на фоне гормонотерапии: Авто- реф. дис… канд. мед. наук. — М., 1999.
- Luban D. et al. // — 1989. — Vol. 240. — P. 327-330.
- Чеботникова Т.В. и др. Гормональные и метаболические особенности врожденного гипопитуитаризма // Пробл. репродукции. — 2005. — № 1. — С. 61-68.
- Oliveira L. et al. // Clin. Endocrinol. Metab. — Vol. 86. — P. 1532-1538.
- Speroff L. et al. // Gynecol. Endocrinol. Infertil. — 6th ed. — S. 2, Ch. 11. — P. 440.
- Considine R. et al. // Engl. J. Med. — 1995. — Vol. 334. — P. 292.
- Tataranni P. Et al. // J. Obes. Relat. Metab. Disord. — 1997. — Vol. 21. — P. 818.
- Schillings J., McClamrock H. // Novak’s Gynecol. — 13th ed. — S. 5, Ch. 24. — P. 857.
- Калиниченко С.Ю. Актуальные проблемы нейроэндокринологии / Козлов Г.И. Материалы научно-практической конференции. — М., 2001.— С. 857.
- Сметник В.П. // Акушерство и гинекология. — 1990. — № 6. — С. 29-31.
- Fenichel P. // Gynecol. Endocrinol. — 2000.23. — P. 143-149.
- Марченко Л.А., Тагиева Г.В. // Пробл. репродукции. — 2004. — № 4. — С. 15-21.
- Wheateroft N. et al. // Reprod. — 1997. — Vol. 12. — P. 2617-2622.
- Toledo S. et al. // Clin. Endocrinol. Metab. — 1996. — Vol. 81. — P. 3850.
- Сметник В.П., Тумилович Л.Г. Неоперативная гинекология. — М., 2003. — С. 179-181.








Комментировать