Йододефицитные заболевания. Дефицит йода в питании населения Земли: глобальность смягчилась, проблема остается. Акушерские аспекты йодного дефицита. Акушерские аспекты коррекции дефицита йода. Прегравидарная профилактика дефицита йода. Гестационная профилактика дефицита йода. Лактационная профилактика дефицита йода.
Д.Е.Шилин
Московский государственный медикостоматологический университет
Йододефицитные заболевания так легко предотвратить, что рождение даже одного ребенка с умственной отсталостью вследствие этого недуга является преступлением.
Анри Лабуисс (Labouisse) (ЮНИСЕФ, 1978)
Эпиграф к книге Бэзила С. Хетцела «Повесть о йодной недостаточности. Международныеусилиявобластипитания» (BASIL S. HETZEL. THE STORY OF IODINE DEFICIENCY. An International Challenge in Nutrition.)
Прошло пять лет с начала века с момента, который ранее был объявлен рубежной вехой для реализации всемирной инициативы по глобальной ликвидации йодного дефицита среди современного человечества (Всемирная ассамблея здравоохранения, 42я сессия, 1990 г.). Более пяти лет в России осуществляется государственная программа йодной профилактики («О мерах по профилактике заболеваний, связанных с дефицитом йода», постановление Правительства РФ №5037 от 05.10.1999). Прошло пять лет с того времени, когда впервые на страницах отечественного журнала «Гинекология» был поднят вопрос о коррекции йодной недостаточности у беременной, плода, новорожденного [1]. За эти годы журнал неоднократно публиковал материалы по разным проблемам женского репродуктивного здоровья, связанным с дефицитом йода. Тем не менее чрезвычайная важность этой проблемы как на медицинском, так и на демографическом уровне заставляет постоянно возвращаться к вопросам коррекции йодного статуса у женщин детородного возраста, беременных и кормящих.
Исключительный интерес практических акушеров гинекологов к данной тематике постоянно поддерживается нарастающим потоком научной информации из различных стран мира. И в самом деле, микронутриентная недостаточность перигестаци онного периода будет всегда оставаться актуальным и приоритетным направлением здравоохранения любого государства. Поэтому и настоящая (десятая) публикация нашего журнала посвящена острым и спорным вопросам практической реализации адекватной дотации йода женщинам России как на массовом, так и на групповом и индивидуальном уровне (с учетом наиболее современных представлений, международного опыта и новейших рекомендаций экспертных организаций).
Дефицит йода в питании населения Земли: глобальность смягчилась, проблема остается
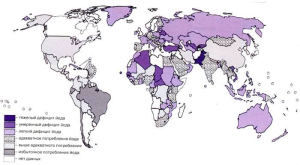
Совсем недавно, в апреле 2005 г., на 58й сессии Всемирной ассамблеи здравоохранения был представлен доклад «Профилактика нарушений, вызываемых недостаточностью йода, и борьба с ними (резолюция WHA52.24)». Знаменательно уже то, что в повестке дня он попрежнему значился первым пунктом. В нем отражены наиболее оперативные официальные сведения ВОЗ о ситуации в мире через 15 лет после объявления на глобальном уровне «тотальной войны» дефициту йода (А58/23 от 18.04.2005). Заявлено о достижении значительных успехов в деле ликвидации недостаточности йода: число стран, в которых эта проблема стала проблемой общественного здравоохранения, сократилось наполовину со 126 в 1993 г. до 54 к 2004 г. Потребление йода стало достаточным или более чем достаточным в 72 государствах (в пяти из них даже чрезмерным). Но употребление йода все еще остается недостаточным в 54 странах, о 66 данные отсутствуют (а в них проживает около 9% населения мира). В целом 2 млрд человек (из 6,5 млрд на 19.12.2005), т.е. треть человечества (!), все еще не получают достаточного количества йода в основном в ЮгоВосточной Азии, Европейском регионе (в том числе в России!) и Западной части Океании (рис. 1).
Акушерские аспекты йодного дефицита
- Пересмотр отношения к вопросу о физиологической потребности в йоде
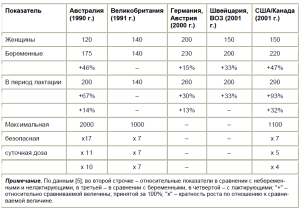
Бурный прогресс в научном понимании проблемы и широкое внедрение йодной профилактики в различных регионах земного шара способствовали уточнению и критической переоценке некоторых базовых представлений о йодном дефиците. В том числе это коснулось вопроса о нормальном потреблении микроэлемента отдельными категориями населения. Но если для основной массы жителей Земли представления о том, какое обеспечение считать достаточным, существенных перемен не претерпели (дети старшего возраста, подростки, мужчины), то в отношении беременных, кормящих и младенцев теперь однозначно рекомендуется повысить порог физиологической потребности со 140175, 140200, 4050 мкг в сутки до 200250, 200300, 90130 мг в сутки соответственно [27]. На переосмысление этого вопроса и принятие решения потребовалось целое десятилетие (табл. 1).
Таблица 1. Динамика представлений об уровне физиологической потребности в йоде в 1990/12000/1 гг.
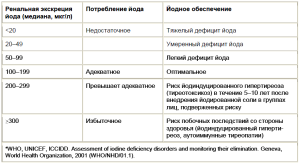
Вместе с тем понимание границы супрафизиологи ческой и фармакологической дозы сместилось в обратную сторону в диапазон значений более низких, чем ранее, и близких к 1 мг. Сразу отметим, что между рекомендуемой минимальной нормой и максимальным уровнем, превышение которого сопряжено с риском передозировки (причем риском крайне низким скорее теоретическим, чем реальным), сохраняется широкий «коридор», гарантирующий высокий уровень безопасности профилактических мероприятий. Так, для новорожденных нежелательно потребление йода больше удвоенной суточной нормы, для беременных и кормящих более чем 35кратное повышение. Также и для остальных слоев населения, нуждающихся в меньшем количестве микроэлемента: ориентиры избыточности потребления переместились согласно указаниям экспертов ВОЗ/Международного совета по контролю йододефицитных заболеваний в сторону менее высоких показателей (табл. 2).
Таблица 2. Эпидемиологические критерии оценки йодного обеспечения, основанные на медиане ре нальной экскреции йода у детей школьного возраста*
- Уточнение главных приоритетов и целей стабильной ликвидации дефицита йода
Важно отметить факт массовой консолидации ведущих специалистов мира по вопросу неотложности ликвидации йодного дефицита на основании относительно новых идеологических позиций, а именно с точки зрения предотвращения минимизации последствий для интеллектуального потенциала населения Земли. Так, если столетие назад негативные эффекты дефицита микроэлемента рассматривались преимущественно через узкую призму эндокринных нарушений (патологии щитовидной железы ЩЖ), а позднее репродуктивного, соматического неблагополучия, то в последние десятилетия в широком спектре йододефицитных состояний максимальное внимание авторитетных экспертов и врачейпрактиков сконцентрировано на вопросах нейротератогенного эффекта нехватки йода в организме беременной с самых ранних сроков гестации в виде повреждения головного мозга ребенка на наиболее критическом этапе его созревания, в I триместре [8].
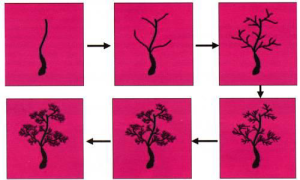
В процессе вынашивания с первых недель после зачатия в развивающемся мозге плода ежесекундно появляется до 50 тыс. новых клеток. Прогрессирование беременности и первые годы после рождения ребенка сопряжены с интенсификацией анатомического и функционального созревания мозга: 90% из общего количества его клеток у взрослого человека (а это 100 млрд, или 1х1011) и 2/3 от его массы формируется в интервале между 3м пренатальным месяцем и 3м постнатальным годом жизни. Более того, между нейроцитами формирующегося мозга устанавливается колоссальное число связей порядка одного квадриллиона (1х1015), что в целом составляет основной «фундамент» будущего интеллекта (рис. 2).
Рис. 2. Уменьшение ветвления отростков клеток головного мозга в результате дефицита йода Ж сни-жение числа межнейрональных связей Ж снижение коэффициента (IQ).
Весь этот длительный период развития является для головного мозга критическим: с точки зрения высокой потребности в защитном эффекте тирео идных гормонов, уязвимости системы в ответ даже на относительный дефицит ее главного продукта тироксина, с точки зрения негативных последствий для психонейроинтеллектуального статуса ребенка, главной причины материнской гипотироксине мии йодного дефицита (даже минимальной степени).
Гормоны ЩЖ, начиная с самых ранних сроков гестации, обеспечивают полноценное развитие центральной нервной системы (ЦНС) эмбриона. Они регулируют экспрессию генов нейрона и синтез ряда специфических белков нейроглии через систему ядерных рецепторов. Они выполняют роль своеобразного «синхронизатора», обеспечивающего строгую последовательность процессов формирования, созревания и функционирования головного мозга. Назовем лишь основной десяток контролируемых ими белков, входящих в состав нейроцитов: микро тубулинассоциированные протеины, изотубулин р 4, основной протеин миелина, миелинсвязанный гликопротеин, калбиндин, инозитол1,3,5 трифосфат рецептор, протеин2 клеток Пуркинье; фактор роста нервов; эпидермальный фактор роста; синапсин I; протеин RC3 (участвует в клеточных механизмах памяти и научения).
Поскольку адекватный синтез тиреоидных гормонов во время беременности возможен лишь при условии полноценного снабжения ЩЖ будущей матери повышенным количеством йода, а сами гормоны в первой половине беременности оказывают мощное влияние на дифференциацию и миелинизацию нейронов, их мультипликацию, миграцию и апоптоз, то на фоне дефицита йода могут возникать разнообразные нарушения формирования головного мозга будущего ребенка [4, 8, 9]. Повышается риск не только самопроизвольных выкидышей, мертво рождений, соматического тератогенеза, но и таких необратимых нарушений, как эндемический неврологический кретинизм (проявляется умственной отсталостью, спастической диплегией по типу церебрального паралича, глухонемотой, косоглазием) или эндемический микседематозный кретинизм (проявляется фетальным и постнатальным гипотиреозом).
- Нейроинтеллектуальные исходы гестацион ной гипотироксинемии: не только кретинизм
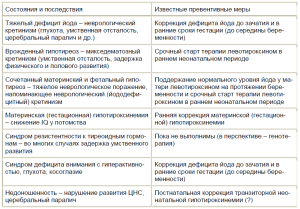
Вместе с тем очевидным достижением последнего времени стало яркое доказательство патологической роли так называемой бессимптомной материнской гипотироксинемии в формировании широкого спектра неврологических нарушений не только грубого анатомического характера (как при кретинизме), но и разнообразных отклонений менее катастрофического порядка на функциональном уровне в виде аномальной задержки психонейро моторного и/или интеллектуального развития по типу «субкретинизма» (табл. 3, 4). Но если в современных реалиях легкой недостаточности и погранично низкого потребления йода беременными первые в действительности встречаются чрезвычайно редко, то случаи умственной отсталости, ментальной дисфункции, когнитивного дефицита, мнестических нарушений меньшей выраженности носят, безусловно, более массовый характер и, по официальным сводкам РФ, выросли на 20%. Это объясняется вполне понятной причиной, поскольку по результатам серии исследований последних лет, которые выполнялись разными авторами в разных этнических группах беременных и разных климатогеографических зонах планеты, стало известно, что распространенность ранней гестацион ной гипотироксинемии в условиях даже невыраженного дефицита йода может достигать десятков процентов [4, 1012].
Таблица 3. Клинические аспекты роли тиреоидных гормонов в созревании головного мозга человека [4, 12]
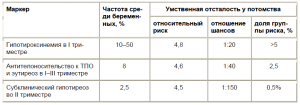
Таблица 4. Маркеры тиреоидной патологии у беременных и интеллектуальный прогноз для потомства [14]
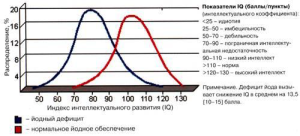
В подтверждение справедливости положения о традиционно цитируются результаты ставшей уже негативном влиянии пренатального дефицита йода хрестоматийной работы Н.Блейчродта и М.Борна и материнского тироксина на интеллект потомства (1994 г.). При выполнении крупного метаанализа двух десятков научных исследований на большом объединенном клиническом материале им впервые удалось с позиций доказательной медицины продемонстрировать существенное снижение интеллектуального потенциала детей жителей ареалов йодного дефицита (рис. 3).
Рис. 3. Интеллектуальное развитие детей, проживающих в регионах с различным обеспечением йодом (по N.Bleichrodt, 1989).
В последние годы, в том числе и в России, появились данные о том, что наиболее подвержены риску интеллектуальной недостаточности в результате внутриутробного дефицита йода новорожденные с легким транзиторным неонатальным гипотиреозом или даже дети, имеющие при рождении еще менее выраженные изменения функции ЩЖ (по типу изолированной неонатальной гипертиреотропинемии, не сопровождающейся явным снижением продукции тироксина у ребенка) [9, 13]. При более выраженном эндемическом дефиците йода снижение интеллекта выражено в большей степени (рис. 4), а сами случаи транзиторного неонатального гипотиреоза до внедрения групповой профилактики среди беременных встречаются существенно чаще [1, 2, 14]. И именно такие случаи в условиях некомпенсированной нехватки йода во время беременности встречаются чаще всего среди потомства матерей, перенесших в первой половине гестации субклини ческую гипотироксинемию [10, 12].
И наконец, важно хотя бы упомянуть сведения, недавно опубликованные итальянскими авторами, которые в результате хорошо спланированного длительного (911 лет!) проспективного психоневрологического и психометрического наблюдения (рандомизированное клиническое исследование РКИ) в йододефицитной зоне за потомством матерей, имевших на 520й неделе гестации низкие значения свободного тироксина при идеально нормальных показателях тиреотропного гомона ТТГ (чаще ниже 2 мЕд/л!), впервые сформулировали концепцию о новом клиническом индикаторе геста ционной гипотироксинемии в регионах йододефицитной эндемии. Таковым, по мнению F.Vermiglio и соавт., можно считать синдром дефицита внимания с гиперактивностью у детей младшего возраста [22].
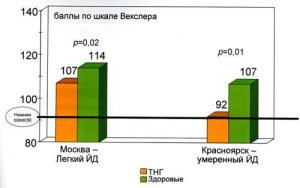
Рис. 4. Показатели IQ у детей 5–7 лет, перенесших транзиторный неонатальный гипотиреоз (ТНГ), и у их ровесников с нормальными результатами неонатального скрининга на гипотиреоз в очагах йододе-фицита – ЙД (ЙД: легкий – Москва [9] и выраженный – Красноярск [15]).
Примечание. Снижение интеллектуального индекса у перенесших ТНГ составляет в среднем 715 баллов по отношению к здоровым при рождении (с нормальным ТТГ).
- Дефицит йода во время беременности: потенцирующий негативный эффект курения
У здоровой беременной, не имеющей патологии ЩЖ и проживающей в условиях адекватного снабжения йодом, повышенная потребность в тиреоид ных гормонах на фоне гестации успешно обеспечивается целым рядом физиологических механизмов (гормональными функциями хориона и плаценты, адаптивными сдвигами со стороны печени и почек). Эти реакции перестройки имеют абсолютно нормальный приспособительный характер, но только в случае, если беременная в течение всего гестаци онного периода получает адекватно высокие количества йода изо дня в день. При достаточном потреблении йодсодержащих продуктов перечисленные факторы определяют возможность физиологической стимуляции ЩЖ, способствуют увеличению продукции ее гормонов, обеспечивают физиологический гипертиреоз беременных, за счет чего и происходит удовлетворение повышенных запросов в тироксине. Но у беременных, проживающих в условиях даже легкой йодной недостаточности и даже в отсутствие патологии ЩЖ, возникают и напряженно реализуются совершенно иные реакции. На фоне скудных запасов интратиреоидного йода способность ЩЖ вырабатывать дополнительные порции гормонов заметно снижена. ЩЖ в условиях «йодного голода» лишена возможности обеспечить организм беременной и плода достаточным количеством требуемых гормонов. При этом в эндемичных по дефициту йода регионах у большинства беременных формируются субклини ческие или явные патологические сдвиги: относительная или очевидная гипотироксинемия; избыточная утечка из фолликулов ЩЖ тиреоглобулина, молекулы которого имеют обедненный гормональный резерв; супрафизиологическая гипертрофия ЩЖ вплоть до формирования диффузного зоба.
Наряду с этим разнообразные химические соединения, поступающие в организм беременной из окружающей среды, способны утяжелять имеющуюся недостаточность йода в природе (как правило, легкую или умеренную) и обострять ее патологические влияния на внутриутробное развитие ребенка. При этом обычно обсуждаются эффекты так называемых пищевых струмогенов (например, крестоцветные растения) или производственных поллю тантов (промышленные и сельскохозяйственные). Но не меньшую пагубную роль на ЩЖ способны оказывать и другие бытовые токсиканты, например курение [16]. По имеющимся данным, компоненты табачного дыма оказывают на тиреоидную систему разносторонние эффекты. Они могут обладать как тиреостимулирующими (протиреоидны ми), так и тиреостатическими (антитиреоидными) свойствами во многом это зависит от исходного состояния ЩЖ. Так, эффекты первого свойства проявятся скорее у здоровых и на фоне нормального поступления йода они будут определяться вкладом никотина, тогда как тиреоблокирующие свойства иных компонентов (тиоцианат, соли кадмия, лития и пр.) реализуются с большей частотой и силой на фоне исходного гипотиреоза (явный или субклинический) и/или дефицита йода. Причем патологические сдвиги и у беременной, и у плода могут формироваться не только в результате активного курения женщины, но и в результате пассивного проникновения элементов табачного дыма в их организм за счет курения мужей/отцов.
В условиях погранично низкого поступления йода на фоне гестации курение является не только достаточно частым (830%), но и клинически значимым фактором, осложняющим течение беременности и созревания плода. В 2000 г. нами при обследовании 384 новорожденных и 382 родильниц из числа их матерей показано, что у потомства курящих беременных, не получающих физиологическую дотацию йода, помимо известных проявлений токсического воздействия табачного дыма на параметры общего развития детей в неонатальном периоде имеет место очевидное ухудшение показателей йодного обмена и снижение активности ЩЖ. У новорожденных от курящих матерей были выявлены: более низкая масса тела, меньшие размеры головы и более тяжелое состояние в первые минуты после рождения (по шкале Апгар), что сопровождалось особенно низким уровнем обеспеченности йодом (25 мкг/сут против 37 мкг/сут при потребности 90110 мкг/сут), особенно большими размерами ЩЖ и наиболее высокой частотой неонатального зоба (19% против 7%), а распространенность гормональной недостаточности достигала у них 52% (против 33% у потомства некурящих) [16]. Таким образом, курение во время беременности негативно отражается на тиреоидном статусе будущей матери и плода и усугубляет йододефицитную патологию перинатального периода. Скорее всего, отрицательное влияние курения на организм будущей матери и ребенка опосредовано ингибирующими эффектами табачных смол и/или солей тяжелых металлов на разные этапы обмена йода в ЩЖ, на активность ключевых ферментов интрати реоидного гормоногенеза и/или на экстратиреоид ный пул йодного метаболизма.
В то же время пренатальная йодная профилактика, по данным того же поперечного исследования в Москве, назначаемая на фоне легкого дефицита йода женщинам с наиболее ранних сроков гестации, надежно устраняет у беременной и плода йодную недостаточность и ее проявления, предотвращая эндемическое увеличение и гипофункцию ЩЖ у новорожденных. Современные препараты йодида калия в дозе до 200 мкг/сут эффективно ликвидируют дефицит йода во время гестации и, по нашим данным, полностью компенсируют в регионе легкой йодной эндемии повышенную потребность беременных женщин в этом микроэлементе, даже у курящих [16].
Акушерские аспекты коррекции дефицита йода
Основная стратегия всеобщей профилактики и борьбы с недостаточностью йода заключается на современном этапе в универсальном йодировании пищевой соли (Доклад ВОЗ А58/23 от 18.04.2005). Сегодня уже более 100 стран имеют программу йодирования соли в сравнении с единичными государствами, которые располагали такой программой в 90е годы. Йодированная соль потребляется в 67% всех домашних хозяйств во всем мире. Но этот показатель является благополучным, превышая 90%, только в 28 странах (в сравнении с 19 странами 5 лет назад). Поскольку использование йодированной соли в продуктах питания не признано обязательным или не стало законодательно регулируемым в большинстве стран (порядка 2/3 государств, по которым имеется информация). Вероятно, именно поэтому все еще сохраняется крайне неблагоприятная ситуация, при которой на некоторых территориях, где йодная профилактика продекларирована даже на государственном уровне, она до сих пор так и не стала действительно массовой.
Согласно современной идеологии ликвидации йодного дефицита с позиций предотвращения дальнейшего падения интеллектуального потенциала населения этих регионов мира экспертами ВОЗ собрана информация и проведено картирование планеты по среднегодовой численности новорожденных, головной мозг у которых остается на этапе внутриутробного развития не защищенным от тератогенных эффектов гипотироксинемии матерей, не получающих массовую йодную профилактику (рис. 5). Наш объединенный регион (Восточная Европа, СНГ, Балтия) занимает в рейтинге по абсолютной численности 4ю позицию из 7 (4,467 млн детей, ежегодно рождающихся с не защищенным от йодного дефицита головным мозгом, т.е. 9 из 49,2%). Но намного важнее и особенно печально, что доля детей с незащищенным мозгом у нас самая высокая и составляет 77,4%. Это означает, что только 1 из 4 новорожденных в России появляется на свет в условиях достаточного йодного обеспечения, в которых он находился на внутриутробном этапе развития и которые обеспечили ему (в отсутствие других неблагоприятных факторов) полноценную закладку и активное функционирование головного мозга и других жизненно важных систем и органов. Тогда как 3/4 детей такую гарантированную пренатальную защиту не получают (а это около 910 тыс. новорожденных в РФ ежегодно) и «вливаются» в группу риска проявления ментальных нарушений в более старшем возрасте, а также школьной и социальной дезадаптации.
Рис. 5. Среднегодовая численность новорожденных, не защищенных от дефицита йода: а – на карте ми-ра, б – в долях и процентах, в – в миллионах/год. Данные ВОЗ на ноябрь 2001 г.
В ныне действующих отечественных методических указаниях определена основная стратегия ликвидации йодного дефицита на территории РФ, которая включает использование йодированной поваренной соли в качестве метода массовой йодной профилактики и использование йодсодержащих фармацевтических препаратов с фиксированной физиологической дозой йода, для проведения групповой и индивидуальной йодной профилактики (МУ 2.3.7. 106401 «Контроль программы профилактики заболеваний, обусловленных дефицитом йода, путем всеобщего йодирования соли», утверждены 27.07.01 и введены в действие Главным государственным санитарным врачом РФ 01.10.01). Поскольку в группах риска особенно высока распространенность эндемического зоба, то прием препаратов с точной дозировкой йода имеет не только профилактическое, но и лечебное значение.
Использование пищевых добавок, биологически активных добавок (БАД), содержащих нестандарти зованную дозу йода, например в соединении с белками и углеводами, не может быть рекомендовано в качестве групповой и индивидуальной йодной профилактики (Н.Ю.Свириденко, 2003), особенно у лиц с повышенным риском развития йододефицитной патологии (беременные, кормящие) [7, 17, 18]. В этой ситуации вопрос о дозировке йода является принципиальным.
Поскольку для практического акушерагинеколога и любого другого врача, принимающего участие в ведении беременных, вопросы йодной профилактики носят особый (специфический) характер, остановимся подробнее на каждом из трех ее последовательных этапах (прегравидарная Ж гестационная Ж лактационная).
Прегравидарная профилактика дефицита йода
Йодная профилактика должна сопровождать жителей всех йододефицитных регионов на протяжении
всей жизни. Главная проблема в реализации этой концепции здорового питания носит на сегодняшний день исключительно технический характер: как это обеспечить организационно для всех? Но наиболее остро переживают «йодный голод» женщины из групп перигестационного риска, а наибольшая моральная ответственность на курирующих их репродуктивное здоровье медицинских работников возлагается в ситуациях осознанного планирования беременности и более широко в отношении всех женщин детородного возраста, которые потенциально готовы к ее наступлению (и будут ее сохранять).
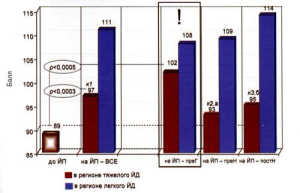
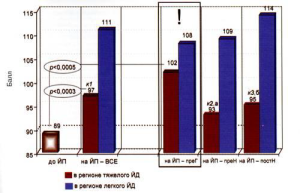
Именно в подобных случаях мы имеем уникальную возможность полностью устранить любые возможные риски йододефицитных нарушений и для будущей беременной, и для ее потомства в плане предупреждения как акушерских, соматических и эндокринных осложнений, так и реально в плане протекции мозга и гарантии благоприятного нейроинтел лектуального прогноза. Практическое подтверждение этой гипотезы, сформулированной в прошлом веке, было получено на конкретном фактическом материале совсем недавно в исследовании N.Salarkia и соавт. [11], которые сравнили параметры умственного развития у детей через 10 лет после внедрения йодной профилактики в одном из очагов тяжелого дефицита йода в Иране (рис. 6). Оказалось, что у детей, поступающих в школу, и у младших школьников ментальные способности на самом деле повышаются (на 79 баллов по шкале Равена) и почти не отличаются от показателей у сверстников контрольной группы только при условии старта профилактических мероприятий за 14 года до зачатия (при пре гравидарной подготовке). Наихудшие значения Ю (на таком же низком уровне, как и до внедрения программы ликвидации дефицита йода) сохранились не только у детей, которые начали получать йод очень поздно после рождения, но и у тех, кто получал его даже пренатально, но без предшествующей подготовки будущей матери к наступлению беременности.
Рис. 6. Оценки коэффициента интеллекта IQ (по тесту Равена) у детей школьного возраста в регионе тяжелого (коричневые столбики) и легкого (синие столбики – контроль) дефицита йода в зависимости от проведения йодной профилактики (ЙП) и сроков ее начала (преГ – прегравидарно, преН – пренатально, постН – постнатально). Достоверность различий с соответствующей группой контроля (к1 – p<0,000001; к2 – p<0,002; к3 – p<0,001) или по отношению к подгруппе преГЙП (а – p<0,03; б – p<0,04) [11].
Исходя из мирового опыта, непозволительно допускать сомнения в безусловной пользе йода для всех остальных функций организма беременной, как бы поздно после зачатия он не стал вводиться в адекватных дозах. Разумеется, чем раньше, тем лучше! Но в отношении ранних стадий нейрогенеза любая попытка исключительно пренатальной/постконцепционной подготовки (ввиду невозможности ее практического осуществления на массовом уровне в сроках до 56 нед) будет, конечно же, неэффективной. Ведь ее старт даже к концу I триместра (с 1012й недели гестации) уже не сможет предотвратить раннюю гестационную гипотирок синемию и по этой причине уже сформировавшиеся к этому времени морфологические изменения в коре и подкорковых центрах головного мозга будущего ребенка (попрежнему признается, что такие отклонения носят необратимый характер). Поэтому в идеале преконцепционная профилактика должна планомерно проводиться на массовой алиментарной основе (йодированная соль), начиная с детства. Но если таковой не было, то для экстренной подготовки каждой здоровой женщине, обратившейся по вопросу подготовки к беременности, и тем более любой пациентке, курируемой на гинекологическом приеме по поводу бесплодия и другой репродуктивной патологии, наряду с фолиевой кислотой надо обязательно назначать препарат йода в дозе 200 мкг (например, 1 таблетка йодомарина 200 ежедневно утром) не менее чем за 3 мес до прекращения контрацепции без перерыва вплоть до зачатия.
Гестационная профилактика дефицита йода
На приеме у акушера
Вы что, женщина, себе позволяете?
Вы почему так вес набираете?
Вы должны забыть слово «соль».
Ни грамма соли в день!..
М. Арбатова
(«Меня зовут женщина», 1999)
Ликвидация нарушений, связанных с недостаточностью йода, является одной из главных целей общественного здравоохранения с учетом ее последствий для социального экономического развития и достижения целей тысячелетия, связанных со здравоохранением, в области развития Организации Объединенных Наций. В уже цитировавшемся Докладе ВОЗ обозначена задача обеспечить усиление программ йодирования соли в остающихся 54 странах, где эта проблема сохраняется, и обеспечить в долгосрочной перспективе устойчивость программ по борьбе в других странах. Но тут же упоминаются основные сдерживающие факторы: затруднения с доставкой йодированной соли, особенно наиболее уязвимым группам населения, обязательства мелких производителей соли, мониторинг программ, а также соответствие и обязательное выполнение соответствующего законодательства (А58/23, 18.04.2005). В контексте йодной профилактики у беременных речь идет о совершенно особой ситуации, когда, несмотря на всю важность дотации йода, могут возникать объективные условия, препятствующие реализации профилактики с помощью йодированной соли [6, 17, 19]. Это: а) наличие осложнений беременности (нефропатия беременных, артериальная гипертензия беременных, многоводие, пиелонефрит и другая почечная патология, ожирение, преэклампсия, гестозы и т.д.), когда ввиду высокого риска перегрузки натрием акушер настойчиво предложит ограничить/исключить соль из рациона; б) индивидуальные особенности пищевого поведения и вкусовые предпочтения не позволят потреблять чрезмерное количество соли ежедневно (ведь если небеременным взрослым для удовлетворения потребности, равной 100 мкг, полагается съедать как минимум 56 г йодированной соли, то во время гестации, когда нужно 200 мкг, придется добавлять в готовую пищу 1012 г, а это 2 чайные ложки).
Первый клинический опыт применения добавок йода для групповой профилактики йодного дефицита был опубликован почти 90 лет назад американским биохимиком Дэвидом Марином: в испытании на 4,5 тыс. школьниц штата Огайо была доказана 100 кратная эффективность и безопасность йода в профилактике эндемического зоба (1917 г.).
Поэтому неслучайно в память об этом событии популярный в России йодистый препарат известен под названием «Йодомарин» («Берлин Хеми»/Менарини групп).
Препарат «Йодомарин 200» содержит фиксированную физиологическую дозу йода, чем принципиально отличается от большого числа биологически активных добавок, которые появляются на российском рынке. Его назначение при дефиците йода способствует восстановлению нарушенного синтеза гормонов ЩЖ. Он служит незаменимым источником физиологических доз йода для коррекции йодной недостаточности у женщин, планирующих беременность, на всех этапах гестации и грудного вскармливания. В заключение важно отметить, что в современную редакцию Международной конвенции о правах ребенка внесено принципиально новое дополнение, которое гласит: «Каждая беременная имеет право на адекватное потребление йода для обеспечения нормального умственного развития ее ребенка. Каждый ребенок имеет право на адекватное снабжение йодом для обеспечения нормального развития» (Всемирная встреча в интересах детей. НьюЙорк, 1990 г.). Безусловное проведение рациональной йодной профилактики в группах риска должно стать своеобразным профессиональным и гражданским «кодексом чести» любого врача, ведущего даже здоровых беременных или наблюдающего детей (особенно младенцев) в регионе йодной недостаточности (это вся территория России).
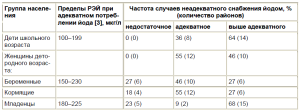
Новейшее многоцентровое исследование, беспрецедентное по масштабу (на почти 15 тыс. населения) и по научнопрактической ценности, было завершено недавно в Китае [19]. С одной стороны, грамотная государственная кампания в этой стране в очередной раз и наиболее ярко продемонстрировала эффективность превентивных мер на фоне рационального внедрения йодированной соли для населения в целом. Но, с другой стороны, колоссальный китайский опыт показал, что данная программа массовой пищевой профилактики не позволяет полностью решить вопрос о надежной и без опасной гестационной профилактике, поскольку даже после явного избыточного перенасыщения населения йодом в первые 7 лет программы и несмотря на снижение дозы йода в соли с 50 до 35 мг/кг в последующие 5 лет у 2/3 детей и почти половины женщин детородного возраста оставались признаки «сверхадекватного» потребления йода, но тем не менее каждая четвертаяпятая беременная и каждый четвертый младенец имели с учетом специфических норм для них четкие признаки лабораторно доказанной йодной недостаточности (табл. 5).
Таблица 5. Йодное обеспечение в группах повышенного риска в сравнении с остальным населением на фоне универсальной профилактики йодированной солью в Китае [19]
Результаты, аналогичные данным китайского проекта, получены также известным исследователем F.Azizi и соавт. в Иране (2003 г.). Низкие показатели экскреции йода с мочой (менее 150 мкг/л) были установлены у беременных (с частотой 28%!) не только в населенных пунктах, где старшие дети имели нормальное потребление йода (йодурия 186190 мкг/л), но и тогда, когда детское население получало йод в количестве, выше адекватного уровня (дефицит йода у 26% беременных при йо дурии 212 мкг/л у школьников) и даже в случаях его явного избытка (соответственно 8% и 338 мкг/л). Иными словами, даже ценой обогащения пищи йодом в количестве, выше рекомендуемого ВОЗ для детей и обычного взрослого населения, при современной технологии так называемой немой профилактики йодированной солью нереально насытить всех лиц в группах критического риска.
Поэтому в соответствии с ранее упомянутым отечественным нормативным документом и учитывая тот факт, что беременность является периодом наибольшего риска развития самых тяжелых йододефицитных заболеваний (в том числе репродуктивных потерь), использование йодированной соли во время беременности и грудного вскармливания целесообразно дополнить групповой йодной профилактикой. Оптимальным методом гестационной йодной профилактики следует признать прием препаратов, содержащих физиологические дозы йодистого калия (200 мкг йода в день) [1, 7, 1417, 19, 20], т.е. продолжить ежедневный прием 1 таблетки йодомарина 200 утром, а в случаях утренней тошноты, рвоты в связи с наличием токсикоза беременных для полного усвоения йода разрешается перенести прием таблетки на вторую половину дня. При назначении беременной адаптированных витаминноминеральных комплексов, даже при условии, что некоторые из них могут содержать 150 мкг йода, важно помнить о целевых значениях нормального потребления микроэлемента в это время 200250 мкг/день. Поэтому к йодированным комплексам следует добавлять 1/41/2 таблетки йодомарина 200 или 1/21 таблетку йодомарина 100 (50100 мкг йода), а к не содержащим йод целую таблетку йодомарина 200.
Лактационная профилактика дефицита йода
Технология йодного обеспечения новорожденных и детей грудного возраста, опираясь на современную доктрину о предпочтительности вскармливания материнским молоком и полностью соответствуя ей, предполагает как наиболее рациональный способ удовлетворения запросов младенца в йоде лактационную профилактику. В молоко женщины (как в молозиво и переходное, так и особенно в зрелое) гормоны ЩЖ матери поступают в столь малом количестве, что с точки зрения нейропротекторного эффекта на головной мозг ребенка им можно пренебречь. В то время как йод, столь необходимый ребенку для поддержания нормальной функции ЩЖ уже с первых дней постнатальной жизни (90 110 мкг в день на 05м месяце и 130 мкг на 612м месяце), принимает прямое участие в физиологическом лактогенезе и лактопоэзе и таким путем беспрепятственно попадает в организм вскармливаемого грудью ребенка. Исходя из столь высокой физиологической потребности младенцев в микроэлементе (практически, как у взрослого человека), при проведении лактационной профилактики рекомендуется для адекватного снабжения и матери, и ребенка назначать женщине 300 мкг йода ежедневно (например, в виде 1,5 таблетки йодомарина 200). Этой рекомендации следует придерживаться (табл. 6) с первых дней после родов (когда она еще не покинула родильный дом) и на весь период лактации (по возможности, не менее 612 мес).
Таблица 6. Место лактационной профилактики в йодном обеспечении новорожденных и младенцев
Литература
- Шилин Д.Е. Профилактика дефицита йода у беременной, плода, новорожденного. Гинекология. 2000; 2 (6): 1736. [Доступ в интернет URL http://www.consiliummedicum.com/media/ gynecology/00_06/173.shtml].
- Шилин Д.Е., Шилина С.Ю., Яковлева И.Н. Проблема дефицита йода глазами неонатолога. Педиатрия (приложение к журналу Consilium medicum). 2004; 3: 1925. Доступ в интернет http://www.consiliummedicum.com/media/consilium/04_03c/19.shtml.
- Delange F. Optimal iodine nutrition during pregnancy, lactation and the neonatal period. Int J Endocrinol Metab 2004; 2: 112.
- Morreale de Escobar G, Escobar del Rey F, Obregon MJ. Maternal hypothyroxinemia and neurodevelopment: to screen or not to screen; to treat or not to treat. HOT THYROIDOLOGY (www.hotthyroidology.com). 2002; 2 [Available via Internet URL http://www. hotthyroidology.com/editorial_71.html].
- Thomson CD. Dietary Recommendations for Iodine Around the World. IDD Newsletter 2002; 18 (3): 3842.
- Zimmermann M, Aeberli I, Torresani T, Burgi H. Increasing the iodine concentration in the Swiss iodized salt program markedly improved iodine status in pregnant women and children: a 5yprospective national study. Am J Clin Nutr 2005; 82 (2): 38892.
- Zimmermann M, Delange F. Iodine supplementation of pregnant women in Europe: a review and recommendations. Eur J Clin Nutr 2005; 58: 97984.
- Hollowell JGJr, Hannon WH. Teratogen update: Iodine deficiency, a community teratogen. Teratology 1997; 55: 389405.
- Киселева Т.В. Врожденный транзиторный гипотиреоз: распространенность, группы риска, прогноз. Автореф. дис. … канд. мед. наук. М., 2004.
- Курмачева Н.А. Профилактика йодного дефицита у детей первого года жизни (медикосоциальные аспекты). Автореф. дис. … дра. мед. наук. М., 2004.
- Salarkia N, Mirmiran P, Azizi F. Timing of the effect of iodine supplementation intelligence quotients of schoolchildren. Int J Endocrinol Metab 2004; 2: 95102.
- Vermiglio F, Lo Presti VP, Moleti M et al. Attention deficit and hyperactivity disorders in the offspring of mothers exposed to mildmoderate iodine deficiency: a possible novel iodine deficiency disorder in developed countries. J Clin Endocrinol Metab 2004; 89: 605460.
- Шилин Д.Е., Пыков М.И., Логачева Т.С., Архипова С.А. Эффективность витаминноминерального комплекса «Матерна» в пренатальной профилактике йоддефицитной патологии. В кн.: Актуальные проблемы современной эндокринологии: материалы IV Всероссийского конгресса эндокринологов. СПб., 2001; с. 415.
- Дедов И.И., Мельниченко Г.А., Трошина Е.А. и др. Профилактика и лечение йододефицитных заболеваний в группах повышенного риска (пособие для врачей). М., 2004.
- Трифонова И.Ю. Йодное обеспечение и последствия дефицита йода у детей в условиях зобной эндемии средней степени тяжести. Автореф. дис. … канд. мед. наук. Красноярск, 2001.
- Шилин Д.Е., Пыков М.И., Логачева Т.С., Байков
- Д. Курение и беременность: влияние на щитовидную железу родильниц и новорожденных в йододефицитной местности. Клин. тиреоидол. 2004; 2 (1): 238. [Доступ в интернет URL: http://www.clinthyroid.ru/current/f_05_03_03.htm].
- Беременность и заболевания щитовидной железы: эндокринологические, акушерские и перинатальные аспекты (пособие для врачей). Под ред.
- И.Краснопольского и др. М.: ИнтелТек, 2005.
- Lee SM, Lewis J, Buss DH et al. Iodine in British foods and diets. Br J Nutr 1994; 72: 43546.
- Yan YQ, Chen ZP, Yang XM et al. Attention to the hiding iodine deficiency in pregnant and lactating women after universal salt iodization: A multicommunity study in China. J Endocrinol Invest 2005; 28: 54753.
- Контроль программы профилактики заболеваний, обусловленных дефицитом йода, путем всеобщего йодирования соли. Методические указания 2.3.7.106401. М.: Минздрав России, 2001.















Комментировать