Неалкогольная жировая болезнь печени: основная характеристика, этиология, особенности течения заболевания, сложности диагностики. Варианты лечения и выбор лекарственных средств.
Е.А. ЧЕРКАШИНА, к.м.н., Ульяновский государственный университет
Неалкогольная жировая болезнь печени является хроническим заболеванием, объединяющим стеатоз, неалкогольный стеатогепатит, цирроз. Неалкогольная жировая болезнь печени ассоциирована с ожирением и является составляющей метаболического синдрома, что повышает кардиометаболический риск, определяет прогноз, продолжительность жизни пациентов. В обзоре изложены механизмы развития, симптомы, диагностика и лечение неалкогольной жировой болезни печени.
Ключевые слова: неалкогольная жировая болезнь печени, метаболический синдром, гепатопротекторы, стеатоз, стеатогепатит, ожирение.
Сегодня в мире количество больных гепатобилиарной патологией превышает 2 млрд человек. Заболевания печени лидируют среди заболеваний желудочно-кишечного тракта; это прежде всего касается метаболических поражений данного органа.
Неалкогольная жировая болезнь печени (НАЖБП) — хроническое заболевание, характеризующееся патологическим накоплением жира в клетках печени, не связанное с употреблением алкоголя. Имеет три формы, отражающие стадии патологического процесса: неалкогольный стеатоз — избыточное накопление жира — жировая дистрофия гепатоцитов, неалкогольный стеатогепатит — воспалительная инфильтрация с очагами некроза, неалкогольный фиброз — цирроз, когда нарушается архитектоника печени вследствие образования узлов соединительной ткани.
В настоящее время заболеваемость НАЖБП достигает эпидемических размеров, 20-30% взрослого населения западных стран страдает этой патологией [14]. По данным большинства авторов, чаще страдают женщины, а в общей популяции детей НАЖБП протекает у 3% и у 53% детей, страдающих ожирением. В России НАЖБП выявлена у 27% обследованных, причем 80,3% из них имели стеатоз, 16,8% — стеатогепатит и 2,9% — цирроз печени [10]. Распространенность дислипидемии среди пациентов с НАЖБП достигает 75%, и эти показатели в два раза выше, чем в популяции [9]. В 2003 г. на I Всемирном конгрессе по инсулинорезистентности в Лос-Анджелесе было выдвинуто предположение, что НАЖБП, наряду с ожирением, СД 2-го типа, дислипидемией, артериальной гипертензией, является компонентом метаболического синдрома. Причины развития НАЖБП разнообразны, но чаще имеется их сочетание [3, 6]. Основные этиологические факторы НАЖБП:
- употребление пищи с высоким содержанием насыщенных жиров;
- низкая физическая активность;
- гормональные нарушения;
- первичная и вторичная инсулинорезистентность (ИР);
- ожирение.
У пациентов с СД 2-го типа и ожирением НАЖБП встречается от 70 до 100%, у данной группы больных стеатогепатит встречается в 50% случаев, а у каждого шестого в сочетании с СД 2-го типа – цирроз печени [2]. Жировая ткань является эндокринным органом, имеющим обширную сеть капилляров, сообщающихся с портальной системой. Жиры сальника легко липолизируются и приводят к выбросу свободных жирных кислот в портальную вену. Избыток свободных жирных кислот (СЖК) перемещается в гепатоциты, образуются триглицериды, липопротеиды низкой плотности. Часть свободных жирных кислот вовлекается в глюконеогенез и способствует избыточной секреции печенью глюкозы в кровоток. ИР поддерживает гиперинсулинемию, увеличивается липолиз с высвобождением свободных жирных кислот, стимулируется липогенез, формируется жировая дистрофия гепатоцитов – стеатоз.
В развитии ИР важная роль отводится адипонектину — гормону жировой ткани, обладающему антиатерогенным действием, уменьшая продукцию свободных жирных кислот жировой тканью, предотвращая апоптоз гепатоцитов. У пациентов с НАЖБП и ожирением уровень адипонектина ниже, чем у обследованных с аналогичным ИМТ без НАЖБП. Существует модель патогенеза НАЖБП — теория двух толчков. При нарастании ожирения на фоне ИР увеличивается поступление в печень СЖК, развивается дисбаланс между усиленным синтезом триглицеридов в печени и снижением их поступления в кровь — первый толчок (результат: стеатоз, печень становится более чувствительной к агрессивным факторам). В процессе реакций окисления СЖК образуются реактивные формы кислорода, продукты перекисного окисления липидов, провоспалительные цитокины, оксидативный стресс — теория второго толчка. Хроническое воспаление, приводящее к апоптозу, некрозу гепатоцитов, трансформирует стеатоз в стеатогепатит с последующим развитием фиброза печеночной ткани. Фиброз выявляется у 20-37% пациентов с НАЖБП. В патогенезе НАЖБП могут принимать участие гены, регулирующие метаболизм глюкозы, липидов, воспаление и развитие фиброза. Длительная гипертриглицеридемия при ИР нарушает эндотелий-зависимую вазодилатацию, вызывает оксидативный стресс и является фактором риска раннего атеросклероза.
Главная особенность НАЖБП — это отсутствие симптомов, болезнь часто выявляется случайно, на основании лабораторных или инструментальных тестов. Симптомы НАСГ неспецифичны, не коррелируют со степенью его тяжести. Астеновегетативный синдром обнаруживается у половины пациентов с НАСГ; реже отмечается дискомфорт в правом подреберье. Появление жалоб на кожный зуд, анорексию, диспептический синдром, наряду с развитием желтухи и симптомов портальной гипертензии, свидетельствует о трансформации НАСГ в цирроз [7]. При обследовании у 50-75% с НАЖБП больных обнаруживают гепатомегалию [2]. Диагностический поиск проводится при выявлении следующих признаков:
- бессимптомном повышении уровней аминотрансфераз;
- необъяснимом существовании постоянной гепатомегалии;
- гепатомегалии при радиологическом исследовании;
- исключении всех других причин, приводящих к гепатомегалии.
В процессе диагностики НАЖБП очень важен сбор анамнеза с оценкой факторов риска. Исключить необходимо алкогольное, хроническое вирусное заболевание печени. Исследование ферритина, насыщение железом трансферрина позволяет дифференцировать гемохроматоз, уровень церулоплазмина; наличие кольца Кайзера-Флейшнера — болезнь Вильсона. Анализ аутоиммунных заболеваний печени проводится по клиническим симптомам и уровню антител — антинуклеарных, антимитохондриальных.
Существуют предикторы высокого риска прогрессирования НАЖБП с развитием стеатогепатита и фиброза:
- возраст старше 45 лет;
- женский пол;
- ИМТ более 28 кг/м2;
- увеличение активности АЛТ в два раза и более;
- уровень ТГ более 1,7 ммоль/л;
- наличие артериальной гипертензии;
- СД 2-го типа; индекс ИР (НОМА-Ш) более 5. Выявление более двух критериев указывает на высокий риск фиброза печени.
Лабораторные и инструментальные методы диагностики НАЖБП:
- повышение активности АЛТ и АСТ не более чем в четыре-пять раз, индекс АСТ/АЛТ — не более 1, чаще повышена активность АЛТ;
- повышение активности ЩФ и ГГТП, не более чем до двух норм;
- гипертриглицеридемия, гиперхолестеринемия;
- гипергликемия (НТГ или СД 2-го типа) — повышение уровня глюкозы натощак более 6,1 ммоль/л, изменение глюкозотолерантного теста, повышение С-пептида;
- гипоальбуминемия;
- повышение уровня билирубина (в пределах 30-35 ммоль/л);
- тромбоцитопения, увеличение протромбинового времени.
В развитии НАЖБП важную роль играют провоспалительные цитокины — интерлейкины 6 и 8 и ФНО-α. ФНО-α является многофункциональным провоспалительным цитокином, секретирующимся в основном макрофагами, преимущественно жировой ткани, обладающим ауто- и паракринными эффектами. Многие исследователи рассматривают ФНО-α как медиатор ИР при ожирении. У пациентов с НАСГ обнаружена гиперэкспрессия мРНК ФНО-α не только в жировой ткани, но и в печени, что проявляется более высокими плазменными концентрациями ФНО-α [15]. ФНО-α активирует ядерный транскрипционный фактор каппа В (NF-kB) в адипоцитах и гепатоцитах, что ведет к усилению фосфорилирования инсулинового рецептора I типа, нарушению связывания инсулина с рецептором, уменьшению активности ГЛЮТ-4 и фосфоинозитол-3-киназы, снижению захвата и утилизации глюкозы клетками, развитию ИР. Под воздействием ФНО-α гладкомышечные и эндотелиальные клетки сосудов усиливают продукцию моноцитарного хемотаксического белка-1 (МСР-1), играющего важную роль в патогенезе атеросклероза. Также ФНО-α способствует повышению экспрессии и синтеза белка BcL-2, активирующего апоптоз гепатоцитов. ИЛ-6, ИЛ-8 — провоспалительные цитокины, продуцируемые жировой тканью, могут индуцировать синтез провоспалительных белков, таких как фибриноген и С-реактивный белок. У пациентов с НАСГ содержание интерлейкинов в плазме крови часто повышено. Маркером НАЖБП может являться содержание в сыворотке крови фрагментов белка — филамента цитокератина-18 (CK18-Asp396), образующихся при его расщеплении активированными каспазами из гепатоцитов при апоптозе. Повышение уровней этого вещества специфично для стеатогепатита.
В диагностике НАЖБП используются фибротесты, оценивающие степень повреждения печени, но в связи с отсутствием достоверных данных по сопоставлению тестов с клинико-морфологическими изменениями в печени при пункционной биопсии фибротесты не являются основным методом диагностики НАЖБП. Так как основные печеночные тесты неспецифичны, не всегда коррелируют с гистологией, биопсия является золотым стандартом диагностики, определения стадии и терапевтической эффективности при НАЖБП. Биопсия печени не показана, когда уровень трансаминаз в норме.
Показания для биопсии:
- возраст старше 45 лет и хронический цитолиз неустановленной этиологии;
- сочетание хронического цитолиза неустановленной этиологии, по крайней мере с двумя проявлениями МС, независимо от возраста.
Морфологическое исследование определяет степень активности НАСГ и стадию фиброза печени (табл. 1,2).
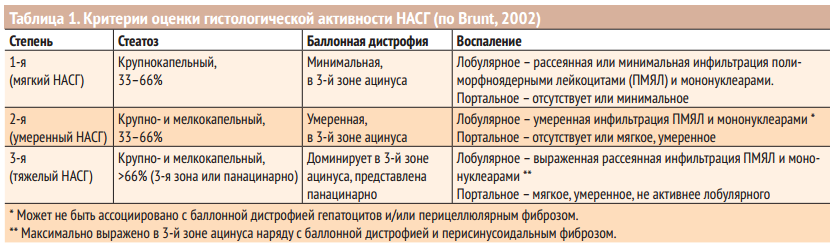

На основе существующей классификации была разработана и предложена Шкала активности НАЖБП (NAFLD activity score — NAS), представляющая комплексную оценку морфологических изменений в баллах, объединяющая такие критерии, как стеатоз (0-3), лобулярное воспаление (0-2) и баллонная дистрофия гепатоцитов (0-2). Сумма баллов менее 3 исключает, более 5 свидетельствует о наличии стеатогепатита.
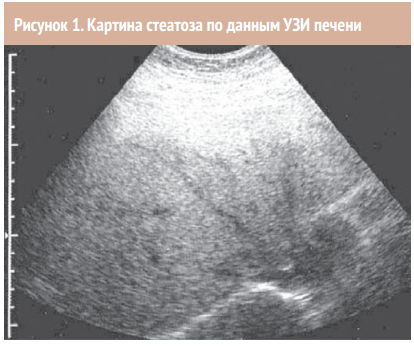
При отсутствии клинической симптоматики, изменений печеночных тестов, невозможности проведения исследования печени УЗИ ОБП (рис. 1) служит объективным методом для распознавания стеато-за, особенно при наличии одного или более факторов риска развития НАСГ, позволяет следить за динамикой патологического процесса. Выявить жировую инфильтрацию печени позволяют и другие методы инструментальной диагностики: компьютерная томография, магнитно-резонансная томография.
Фармакотерапия показана больным с прогрессирующим течением заболевания или высоким риском прогрессии. При отсутствии лечения и диетической коррекции в 12-14% стеатоз трансформируется в стеатогепатит, в 5-10% — в фиброз печени.
Больные с избыточной массой должны соблюдать диету с суточной калорийностью 1 500—1 700 ккал, снижением насыщенных жиров. Сочетание диеты с физической активностью 30 мин в день дает больший эффект, чем только соблюдение диеты.
Официальной классификации гепатопротективных препаратов нет, наиболее близко подошли к решению этого вопроса С. Оковитый с соавт. [11]. В целом гепато-протекторы имеют единую направленность в оказании прямого и опосредованного влияния на патогенез повреждения печеночной ткани. Имея разную природу, химический состав, пути метаболизма, они должны обеспечить антиоксидативную защиту гепатоцитов, сосудов и стромы печени, репарацию и улучшение всех функций, тормозить фибротические изменения в печени, оказывая мембраностабилизирующее, противовоспалительное, антиоксидантное, антиапоптотическое действие [4].
Целью лечения НАЖБП является снижение накопления СЖК, восстановление поврежденных мембран, снижение оксидативного стресса, замедление прогрессирования фиброза печеночной ткани. Этим требованиям и отвечают гепатопротекторы, содержащие эссенциальные фосфолипиды (ЭФЛ). Основу ЭФЛ составляет преимущественно фосфатидилхолин с высокой концентрацией полиненасыщенных жирных кислот. Гепатотропное действие достигается встраиванием молекул ЭФЛ в мембраны клеток, и ингибируются процессы ПОЛ [1, 5, 8, 12]. ЭФЛ защищают поврежденные мембраны, улучшают показатели липидного обмена, а значит, влияют не только на НАЖБП, но и на метаболический синдром в целом. На фармацевтическом рынке появилась и активно используется БАД Гепагард Актив (ООО «НПФ БИОС» по заказу ООО «АнвиЛаб»). БАД к пище Гепагард Актив — современный российский комбинированный гепатопротектор (Евразийский патент №ЕА19268 от 28.02.2014), в состав которого, кроме ЭФЛ, входит липотропное вещество L-карнитин, повышающее мобилизацию жирных кислот из клеток и уменьшающий уровень триглицеридов, и витамин Е — универсальный антиоксидант. Принимать Гепагард Актив рекомендуется курсом: 1 мес. по 1 капсуле три раза в день во время еды. Согласно данным исследований ряда авторов [13], у пациентов с НАЖБП на стадии стеатоза и стеатогепатита доказано, что прием средства Гепагард Актив способствует статистически значимому снижению уровня общего холестерина (ОХ) и липопротеидов низкой плотности (ЛПНП), триглицеридов (ТГ) и коэффициента атерогенности (КА). По данным ФиброМакс-теста, где оценивалась активность патологического процесса, фиброза, метаболических нарушений, отмечалась положительная динамика: выявлено снижение индекса массы тела (ИМТ) в среднем на 10,7% и количества жировой ткани в организме пациентов на 20,6%, отмечен рост активной клеточной массы (АКМ). Продемонстрирована способность Гепагарда Актив улучшать состояние микробиоценоза кишечника, повышать показатели качества жизни пациентов. Кроме этого, в ходе исследования установлено, что у лиц с избыточной массой тела и ожирением применение Гепагарда Актив приводит к достоверному снижению уровня лептина, нормализации углеводного обмена. У пациенток с избыточной массой отмечено улучшение психоэмоционального статуса, характеризующееся снижением уровня реактивной и личностной тревожности и регрессом депрессивных нарушений.
Прием средства Гепагард Актив способствует улучшению функционального состояния нервной системы, проводимости нервных импульсов. Это связано с тем, что лецитин служит субстратом для формирования миелиновых оболочек нервных клеток и аксонов. L-карнитин как составляющая Гепагард Актив способствует катаболическим превращениям жирных кислот, защищая печень от лишнего жира, усиливает синтез антиатерогенных липопротеидов.
Таким образом, Гепагард Актив может использоваться у лиц с НАЖБП, метаболическим синдромом, при наличии лишнего веса, СД и дислипидемии. Кроме самостоятельного действия, Гепагард Актив потенцирует эффекты силимарина, препаратов УДХК, которые используются при лечении НАЖБП. В связи с тесной ассоциацией НАЖБП и ИР пациентам показаны препараты инсулино-сенситайзеров (бигуаниды, тиазолидиндионы).
Для НАЖБП характерно доброкачественное течение. Однако, учитывая, что данная патология часто ассоциирована с наличием СД 2-го типа, ожирением, ИБС, пациенты имеют более высокий риск развития осложнений и летального исхода, поэтому им следует рекомендовать оставаться под врачебным наблюдением и раз в 6 мес. повторять УЗИ ОБП, а также определять уровень сывороточных трансаминаз, липидный спектр, показатели углеводного обмена.
ЛИТЕРАТУРА
- Балукова Е.В. Эссенциальные фосфолипиды в комплексной терапии неалкогольной жировой болезни печени. Русский медицинский журнал. Режим доступа: www.rmj.ru/articles_7995.htm, свободный.
- Богомолов П.О. Неалкогольный стеатогепатит: патофизиология, патоморфология, клиника и подходы к лечению. Фарматека, 2003, 10: 31-39.
- Богомолов П.О. Многофакторный генез жирной болезни печени. Гепатологический форум, 2006, 3: 4-10.
- Голофеевский В. Важнейшие вопросы патоморфогенеза и лечения НАЖБП у больных СД. Врач, 2012, 7: 8-11.
- Драпкина О.Н. Терапия неалкогольного стеатогепатита при метаболическом синдроме: фокус на эссенциальные фосфолипиды. Лечащий врач, 2010, 2: 43-45.
- Драпкина О.В. НАЖБП. Современный взгляд на проблему. Лечащий врач. 2010. 5. 5: 57-61.
- Ивашкин В.Т. Диагностика и лечение неалкогольной жировой болезни печени. Методические рекомендации. Российские медицинские вести, 2009, XIV, 3: 71-72.
- Корнеева О.Н. Неалкогольный стеатогепатит при метаболическом синдроме. Consilium medicum. 2007. 2: 18-21.
- Мехтиев С.Н. Современный взгляд на перспективы терапии неалкогольной болезни печени. Эффективная фармакотерапия. 2011. 2: 50.
- Никитин И.Г. Скрининговая программа по выявлению распространенности неалкогольной жировой болезни печени и определению факторов риска развития заболевания. Российские медицинские вести. 2010. XV(1): 41-46.
- Оковитый С.В. Гепатопротекторы. ГЭОТАР-Медиа, 2010: 56.
- Полунина Т.Е. Неалкогольный стеатоз печени в практике интерниста. Эффективная фармакотерапия в гастроэнтерологии. 2009. 1: 14-19.
- Селиверстов П.В., Радченко В.Г. Оптимизация больных неалкогольной жировой болезнью печени. Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2014. 24. 4: 39-44
- BeLLentani S. Behavior therapy for nonalcoholic fatty Liver disease: the need for a multidisciplinary approach. Hepatology, 2008, 47: 746-754.
- Browning JD, Horton JD. Molecular mediators of hepatic steatosis and liver injury. J. Clin. Invest., 2004, 114: 147-52.







А у нас в державі фахівців немає? Обовязково рекламувати москальський БАД? І коли психологія зміниться, куди нам до європи…